基于教学评一体化视域下的高中化学实验教学
2024-09-29康桐

在现代化的高中化学教学中,教师要注重学生综合能力的培养,将教学评融为一体,落实教学评一体化的教育观念,更全面地了解学生的学习情况,及时调整教学方法和内容,提高教学质量,使教学更贴近学生的需求,从而促进学生的全面发展。
一、做好教材分析,确定教学评目标
做好教材分析需要教师对课程内容做好分析,并结合学生的学习情况明确课程教学的重难点。与此同时,教师确定教学评一体化目标时要结合教材分析的结果,明确教学目标和评价标准,确保目标的合理性和可行性,其中应包括知识、能力、素质等方面的要求,既要考虑学科知识的传授,又要注重学生综合素质的培养。
如在教学“化学反应速率的影响因素”时,教师对教材作了如下分析:
这节课是新课程开发的“实验活动课”,要求学生探究实验的整个过程,通过实验操作、观察,探究影响化学反应速率的各种因素,让学生感受化学反应的快慢,从而初步构建“反应规律的探究实验”模型,激发学生学习化学的兴趣,培养其科学探究能力。
在学情方面,学生对影响化学反应速率的因素已有了初步的感性认识与一定的动手能力,但实验设计能力比较欠缺;学生缺乏使用数字化实验仪器进行实验探究的实践;学生对“变量控制”对比实验的模型建构比较陌生,对自变量和因变量的逻辑关系不清晰,无法完整设计严谨的实验方案。
基于上述分析,教师确定如下目标:
【教学目标】
1.体验外界条件对化学反应速率的影响,理解改变外界条件可以调控化学反应速率。
2.学习用“变量控制法”研究化学反应规律。
3.初步构建“反应规律的探究实验”认识模型。
【评价目标】
1.实验中发现问题、分析问题、解决问题的能力。
2.通过对实验设计方案的交流与点评,诊断并发展学生实验探究设计的水平。
3.通过对实验结果的判断和分析,诊断并发展学生对化学反应速率因素的认识进阶和认识思路的结构化水平。
4.促进学生形成科学的实验思维和严谨的实验态度。
5.引导学生借助化学实验原理分析并解决实际问题。
二、坚持目标引领,落实一体化教学过程
在教学评一体化的落实过程中,教师要坚持目标引领,将评价目标落实到各个教学环节中,对教法、学法进行评价,对教、学情况进行评价,从而用评价结果反馈真实的教、学质量,从而促进教学评一体化的有效落实。
(一)设计问题,引入新课
教师设计问题的目的是导入新课,引导学生认识本次实验学习要解决的问题、要探究的知识,从而激发学生的学习兴趣,让学生做到心中有数,同时为后续教学做好铺垫。为此,教师可以结合学生的生活经验设计易于学生理解的问题,并鼓励学生从化学角度展开思考。
如在“化学反应速率的影响因素”实验教学中,教师可以先为学生设计如下问题:同样是夏季,为什么面包的保质期比蛋糕的时间长?相同的面包,为什么冬季的保质期比夏季的时间长?这些问题在我们的生活中很常见,大家能猜出其背后的原因吗?
基于上述问题,教师引导学生回顾以前的知识:食物的变质是一个化学变化的过程,所以保质期的长短其实就是化学反应的快慢问题,前面我们已经学习了影响化学反应速率的因素,知道化学反应速率主要由反应物的性质决定。
教师:结合面包夏季保质期时间短的问题,化学反应的速率还会受到哪些因素的影响呢?
学生:反应温度。温度高的时候,反应速率就会加快,这就是为什么冬天的时候温度低,C+eNmoBenlJsxcwKHazi3svUaxTt+anMBNUd0K+ug7A=面包保质期会比夏季温度高的时候长一些。
教师:除了反应温度外,在真实的化学反应过程中,你认为还有哪些因素会影响化学反应的速率呢?
学生:反应物浓度、催化剂等外界条件的影响。
教师过渡:今天我们一起来探究外界条件对化学反应速率的影响,验证大家的猜想是否正确。
教师以问题引导的方式将新课知识引入课堂,激发学生的好奇心和求知欲,同时让实验目标更加明确,易于学生理解和接受。在此环节中,教师展开如下评价:
1.评价学生是否能够发现关键问题,并结合自己的生活经验展开分析。
2.评价学生是否能够结合化学学习经验,对教师提出的问题展开大胆猜想。
基于上述评价,教师可以发现学生在化学实验学习中存在的不足,并在后期教学中予以完善和强化,从而促进教学评一体化的有效落实。
(二)引领示范,方法建模
方法建模的过程旨在引导学生认识本实验探究的核心方法,构建实验模型,要求学生能够基于所学知识和方法经验,对要探究的问题提出自己的解决思路,从而确定合理的实验研究方法,以此提高实验教学的有效性。为此,教师要为学生做好引领示范,通过真实的实验情境启发学生思考,促进学生化学思维和实验探究能力的提升。
如在“化学反应速率的影响因素”实验教学中,教师可以按照以下途径引导学生构建实验模型。
教师:双氧水的分解是我们熟悉的反应,该反应常温下分解速率快吗?可以采用什么样的方式促进其分解呢?
学生:可以通过加入催化剂的方式促进其分解。
教师根据学生的回答提供实验所用试剂:10%的H2O2溶液、1mol/L的FeCl3溶液、MnO2粉末、蒸馏水。
教师鼓励学生根据他们的猜想设计实验方案,探究催化剂是否能够影响双氧水的分解。
学生:取一定量的过氧化氢溶液于两支试管中,往其中一支中滴加氯化铁。观察现象。
教师:这样的操作是否能够直接判断出催化剂提升了反应速率呢?
学生:可以取相同量的过氧化氢溶液于两支试管中,往其中一支中滴加氯化铁,另一支什么都不加,观察现象,通过对比来判断催化剂的作用。
教师按照学生陈述的方案进行演示,边实验边提出问题:
1.该取多少H2O2?
2.两支试管的H2O2需要一样多吗?
3.如何确保所加的药品一样多?
4.为什么需要加入一样多的药品?
5.你看到了什么现象?是否可以证明催化剂影响了化学反应速率?
教师在演示实验和问题串的引导中将该实验用到的方法要点进行逐一梳理和归纳,在此基础上很快得出科学方法——变量控制法,并引导学生构建实验模型。具体如下。
实验目标:探究催化剂对化学反应速率的影响。
实验方法:变量控制法,试管①中未加催化剂;试管②③加入相同量的不同催化剂;三支试管中加入H2O2的浓度和体积相同,反应液的温度相同。
实验过程:向三支大小相同的试管中各加入2 mL
10%的H2O2溶液;再向其中的两支试管中分别加入少量MnO2粉末和2滴1mol/L的FeCl3溶液;观察、比较三支试管中气泡出现的快慢;通过对比实验现象,判断催化剂是否能够影响化学反应的速率?区分不同催化剂对化学反应速率的影响大小。
实验现象:加入FeCl3溶液的H2O2溶液出现大量气泡;加入MnO2粉末的H2O2溶液快速出现大量气泡;没有加入任何催化剂的H2O2溶液则出现少量气泡。
实验结论:在其他条件不变时,使用催化剂能加快化学反应的速率,但不同催化剂的催化效果不同。
教师为学生展示化学实验探究的认知模型:基于问题→提出假设→明确研究对象→设计实验方案→实施实验→形成结论,并指导学生认识本实验探究过程中应用了变量控制法,即只改变一种条件,控制其他条件不变,观察实验结果,从而得出该条件对结果的影响。
通过这样的教学过程,教师引导学生学会构建实验模型,让学生能够基于所学知识设计实验方案,从而自主完成整个实验探究过程,以此提高学生的实验探究能力,培养学生的实验思维。在此环节中,教师要针对学生的学习表现展开如下评价:
1.评价学生是否能够通过对实验设计方案的交流与点评,自主完成实验方案的设计。
2.评价学生是否能够通过对实验结果的判断和分析,得出准确的实验结论。
3.评价学生是否形成了科学的实验思维和严谨的实验态度。
基于上述评价,教师考查学生在实验探究方面的水平以及存在的问题,并对教学过程做好评价,反馈教法的合理性以及学法的正确性,并在后期对教法、学法进行纠正,以此促进教学评一体化的有效落实。
(三)应用模型,设计方案
在化学实验教学中,教师展示实验模型,鼓励学生应用教师指导的模型自主设计实验方案,从而培养学生举一反三的应用能力,提高学生的实验水平。
教师可以指导学生回顾变量控制法的原理,并向学生提出驱动性问题:刚才老师为大家展示了催化剂对化学反应速率的影响探究实验,那对其他的影响因素,我们是否也可以通过变量控制法进行探究呢?
教师可以指导学生探究“硫代硫酸钠(Na2S2O3)与硫酸的反应”,并判断反应物浓度对反应速率的影响,从而根据所学知识设计实验方案。具体如下。
实验目标:探究反应物浓度对化学反应速率的影响。
反应体系:硫代硫酸钠(Na2S2O3)与硫酸的反应。
反应方程式:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O可以通过比较黄色浑浊现象出现所需时间的长短判断反应进行的快慢。
实验试剂:0.1mol/L的Na2S2O3溶液、0.1mol/L的 H2SO4溶液、蒸馏水、热水。
实验方法:变量控制法,改变反应物浓度,其他条件保持不变。
实验过程:取两支大小相同的试管,分别加入2 mL和1 mL0.1mol·L-1的Na2S2O3溶液,向盛有1mLNa2S2O3溶液的试管中加入1 mL蒸馏水,摇匀。再同时向上述两支试管中加入2 mL0.1mol·L-1的H2SO4溶液,振荡。观察、比较两支试管中溶液出现浑浊的快慢。
实验现象:两支试管中均出现黄色浑浊,但试管①中的黄色浑浊出现的更早、更快。
实验结论:当其他条件相同时,反应物浓度越大,反应速率越快;反应物浓度越小,反应速率越慢。
基于上述实验方案设计,教师引导学生按照实验步骤完成实验过程,并验证实验猜想,趁热打铁,对“温度对化学反应速率的影响”展开实验方案设计。具体如下。
实验目标:探究温度对化学反应速率的影响。
反应体系:硫代硫酸钠(Na2S2O3)与硫酸的反应。
反应方程式:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O可以通过比较黄色浑浊现象出现所需时间的长短判断反应的快慢。
实验试剂:0.1 mol/L的Na2S2O3溶液、0.1 mol/L的H2SO4溶液、蒸馏水、热水。
实验方法:变量控制法,改变反应温度,其他条件保持不变。
实验过程:取两支大小相同的试管,各加入2 mL
0.1mol·L-1的Na2S2O3溶液,分别放入盛有冷水和热水的两个烧杯中。再同时向上述两支试管中加入
2 mL0.1mol·L-1H2SO4的溶液,振荡。观察、比较两支试管中溶液出现浑浊的快慢。
实验现象:两支试管中均出现黄色浑浊,但试管②中的黄色浑浊出现的更早、更快。
实验结论:当其他条件相同时,温度越高,反应速率越快;温度越低,反应速率越慢。
通过这样的教学过程,教师不仅可以培养学生用所学知识设计实验方案的能力,发展学生的化学思维,还能提升学生的实验操作能力与实验探究素养,促进学生养成良好的观察习惯。与此同时,教师要对学生的学习表现展开如下评价:
1.是否能通过自主学习完成实验方案的设计。
2.是否能通过对实验结果的判断和分析,得出准确的实验结论。
3.是否具有科学的实验思维和严谨的实验态度。
基于评价结果,教师可以更全面地掌握实验探究教学的真实情况,以便发现教学中存在的问题以及学生的弱点区域,从而在后期教学中予以必要的指导和帮助,充分发挥教学评价的作用,促进教学评一体化的有效落实。
(四)归纳总结,解决问题
在实验教学中,教师要组织学生对所学实验原理、实验方法、实验过程等进行汇总和梳理,引导学生用实验知识解决实际问题,从而进行课堂延伸,促进实验教学效果的提升。
教师提出启发式问题:通过今天的实验探究,大家小结下影响化学反应速率的因素有哪些?它们是如何影响化学反应速率的?基于此问题,学生汇总本实验课程的核心知识。具体如下。
1.影响化学反应速率的因素包括催化剂、反应物的浓度和温度。
2.使用催化剂,反应速率增大;增大反应物的浓度,反应速率增大;升高温度,反应速率增大。
教师:冬天和夏天面包的保质期为什么不一样?
学生:冬天温度低,食物氧化速度慢,不易变质。
教师:可以采用哪些方式延缓面包或者其他食物的变质速度呢?
学生:低温冷藏,如放在冰箱中;隔绝氧气,如保存食物的时候,尽量将袋子里的空气排空,或者使用专门的真空机抽干或者尽可能和外界阻隔,如在没吃完的食物上覆盖一层保鲜膜等。
教师:在通常情况下,铁与冷水或热水都不发生反应,但红热的铁与水蒸气则可发生反应,生成Fe3O4和H2。试从反应条件的角度思考并解释这一事实。
基于此问题,教师指导学生从影响化学反应速率的角度出发,分析其背后的原因。如温度对铁与水反应的影响至关重要,升高到一定温度可以加快该反应的速率,观察到较为明显的实验现象。
通过这样的教学过程,学生可以加深学习印象,同时对化学知识产生全面的理解。在该过程中,教师可以对学生展开评价:是否能够借助化学实验原理分析并解决实际问题。
基于此评价,教师针对学生解决实际问题的能力进行判断,并予以必要的指导和帮助,让教学满足学生的发展需求,促进教学评一体化的有效落实。
(五)牛刀小试,习题巩固
教师为学生展示实验对应的练习题,巩固学生对实验原理、实验方法的理解和掌握。形如:
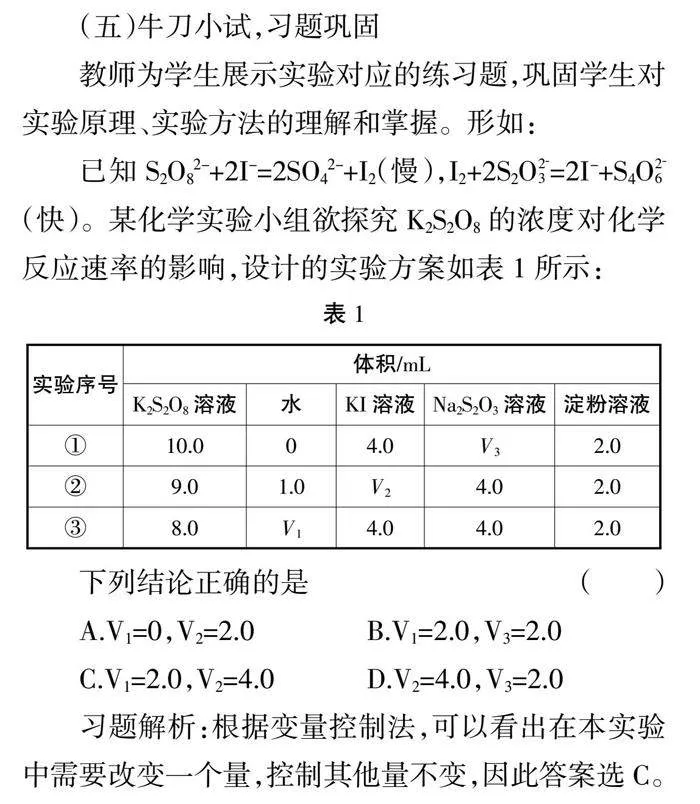
已知S2O82-+2I-=2SO42-+I2(慢),I2+2S2O2-3=2I-+S4O2-6(快)。某化学实验小组欲探究K2S2O8的浓度对化学反应速率的影响,设计的实验方案如表1所示:
下列结论正确的是( )
A.V1=0,V2=2.0 B.V1=2.0,V3=2.0
C.V1=2.0,V2=4.0 D.V2=4.0,V3=2.0
习题解析:根据变量控制法,可以看出在本实验中需要改变一个量,控制其他量不变,因此答案选C。
三、结语
综上所述,在高中化学实验教学中,教学评一体化的有效落实具有非常突出的实践意义。教师要根据课程知识的特点,设计合理的化学实验学习环节,同时将评价目标落实到教学过程中,以此反馈真实的教学情况,并针对教学中出现的问题进行优化和完善,从而让教学满足学生的发展需求,促进教、学质量的双提升,以此促进教学评一体化的有效实践。
(作者单位:甘肃省兰州新区舟曲中学)
编辑:赵文静
