抗生素联合宫腔灌注对反复种植失败合并慢性子宫内膜炎患者的作用及机制分析
2024-05-30刘荣娜包莉莉魏蕊霞
刘荣娜,王 恺,包莉莉,魏蕊霞
目前对于反复种植失败(repeated implantation failure, RIF)仍然没有统一的标准,临床上常将接受3次及以上周期的胚胎移植,并且每次植入1或2枚的优质胚胎仍未获临床妊娠者称为RIF,母体、胚胎因素以及二者相作用的微环境为RIF的主要原因[1]。慢性子宫内膜炎(chronic endometritis, CE)症状不明显,且在临床中的发病率较低。但是越来越多的研究表明CE可以引起不孕,并导致胚胎移植失败。目前CE的病因不明,多考虑是由细菌感染所致,盆腔炎、多次流产史等因素均可诱发该病,患者通常无典型临床症状或症状轻微,易被忽略[2]。研究显示,CE可促使子宫内膜容受性降低进而导致RIF,因此分析CE影响RIF的相关因素会对患者治疗和预后有一定指导作用[3]。目前,临床多针对CE患者进行经验性口服抗生素治疗,可减轻患者炎症反应,但因受药物具体用量及患者实际情况的影响,易出现耐药现象,从而降低治疗效果[4]。宫腔灌注作为一种对子宫局部冲洗治疗的方式,通过在无菌条件下经阴道向宫腔内部灌注药物,使药物能够直接作用于子宫内膜,发挥局部的抗炎作用,且对机体的损伤较小,临床上常将其用于子宫内膜炎、宫腔粘连等疾病的治疗[5]。本研究旨在探讨抗生素联合宫腔灌注在RIF合并CE患者中的应用及其作用机制,现报告如下。
1 资料与方法
1.1 一般资料
选取2021年1月—2022年5月于联勤保障部队第九八〇医院生殖医学中心接受体外受精-胚胎移植助孕的160例RIF作为研究对象,根据是否合并CE分为CE组80例和非CE组80例。另将CE组依据随机数字表法分为A组与B组,均为40例。A组年龄24~39(35.12±3.89)岁;体质量指数(BMI)18~26(22.68±1.22)kg/m2。B组年龄25~38(34.57±4.21)岁;BMI 18~25(22.43±1.73)kg/m2。A组与B组上述一般资料经比较差异无统计学意义(P>0.05),具有可比性。本研究经联勤保障部队第九八〇医院医学伦理委员会批准后实施(2021-KY-75),患者及家属均自愿签署知情同意书。
1.2 诊断标准及病例选择标准
诊断标准:RIF参照《胚胎植入前遗传学诊断/筛查技术专家共识》[6]中相关诊断标准:移植3次及以上或移植高评分卵裂期胚胎数4~6个或高评分囊胚数3个及以上均失败;子宫内膜经CD138免疫组织化学染色,于400倍高倍镜视野下发现典型浆细胞≥5个,即诊断为CE[7]。纳入标准:年龄<40岁;与上述诊断标准均相符合者;无精神障碍,可配合相关研究者;未合并恶性肿瘤者。排除标准:年龄≥40岁;免疫功能障碍或患有强直性脊柱炎、系统性红斑狼疮等免疫相关疾病者;经检查染色体异常者;合并其他对妊娠有严重影响疾病者;生殖道解剖结构异常者。
1.3 方法
1)免疫组织化学染色:所有患者于月经干净3~7 d在无同房史的状态下行宫腔镜检查,术毕轻柔搔刮宫腔,所取内膜组织标本常规送病理科进行CD138免疫组织化学染色。染色结果的判定由2名经验丰富的病理医师分别独立对同一切片进行阅读,有分歧的切片由2位病理医师对所获取的结果进行协商后确定。CD138染色后其特征为浆细胞膜显示强阳性,而细胞质显示弱阳性,视野下可见到核圆但偏于细胞一侧,染色质粗,沿核膜呈辐射状排列。
2)治疗:A组口服抗生素治疗,甲硝唑片(远大医药有限公司,国药准字H42021947,规格:0.2 g)0.4 g口服,2/d;左氧氟沙星片(山东齐都药业有限公司,国药准字H20057913,规格:0.5 g)0.5 g口服,2/d。B组在此基础上联合宫腔灌注治疗,患者保持膀胱截石位,以聚维酮碘进行外阴消毒后,无菌状态下使用人工授精管宫腔灌注10 mg地塞米松磷酸钠注射液(重庆莱美药业股份有限公司,国药准字H20080355,规格:10 mg)进行治疗,每3天灌注1次。2组均持续治疗2周。
3)宫腔液的采集及检测:在患者治疗前、治疗后的月经干净第3~5天采用生理盐水擦净阴道壁及宫颈口,用人工授精管轻轻插入宫腔内缓慢注入生理盐水3 mL,反复轻柔抽吸3次,收集宫腔冲洗液,然后放置于离心机进行离心,离心转速:3 000 r/min,离心时间:15 min,离心半径:13.5 cm,离心结束后取上清液在-80 ℃环境保存,以酶联免疫吸附试验检测宫腔液中白细胞介素-6(interleukin, IL-6)、IL-8、肿瘤坏死因子-α(tumor necrosis factor-α, TNF-α)水平,具体操作步骤参考联科生物酶联免疫吸附试验试剂盒说明书。
4)子宫动脉血流参数测评:所有CE患者均于胚胎移植日(排卵后第3天或第5天)的前一天应用GE Voluson E8彩色多普勒超声诊断仪经阴道超声探头检测子宫动脉参数,包括搏动指数、血流分支、子宫内膜-肌层交界区(endometrial-myometrial interface, EMI)低回声区占肌层比例。
1.4 观察指标
1)统计并比较CE组与非CE组的基线资料,主要包括年龄、BMI、宫腔内占位性病变情况、输卵管积水、不孕年限、人工流产次数、是否患有子宫腺肌症、继发性不孕及宫腔镜检查异常(子宫内膜增生样改变、子宫内膜炎性改变、宫腔粘连)情况。2)采用单因素及多因素Logistic回归分析影响RIF患者CE的相关因素。3)A组、B组治疗前后宫腔液炎性因子IL-6、IL-8、TNF-α水平变化。4)比较A组、B组治疗前后的子宫动脉搏动指数、血流分支、EMI低回声区占肌层比例。5)比较A、B组生化妊娠率、临床妊娠率、胚胎着床率、早期流产率,其中胚胎着床率=孕囊数/总移植胚胎数×100%,早期流产率=孕12周内自然流产周期数/临床妊娠周期数×100%;临床妊娠主要是指患者移植术后35 d的超声检查结果显示宫内或宫外有孕囊回声,临床妊娠率=临床妊娠周期数/移植周期例数×100%;生化妊娠主要是指患者移植术后14 d的血β-人绒毛膜促性腺激素高于正常水平,之后逐渐降低,并经超声检查结果显示宫内或宫外无孕囊回声,生化妊娠率=生化妊娠周期数/移植周期例数×100%。6)观察患者治疗过程中不良反应发生情况。
1.5 统计学方法
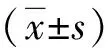
2 结果
2.1 CE组与非CE组基线资料
与非CE组比较,CE组年龄较大,宫腔内占位性病变、输卵管积水、子宫腺肌症、人工流产次数≥2次、继发性不孕、宫腔镜检查异常比例较高,不孕年限较长(P<0.05,P<0.01)。2组BMI比较差异无统计学意义(P>0.05)。见表1。

表1 CE组与非CE组RIF患者基线资料比较
2.2 RIF患者CE的相关影响因素
经多因素Logistic分析显示,年龄较大(≥33岁)、宫腔内占位性病变、输卵管积水、子宫腺肌症、不孕年限较长(≥3.5年)、多次人工流产(≥2次)、继发性不孕、宫腔镜检查异常均为RIF患者CE的相关影响因素(P<0.05,P<0.01)。见表2。
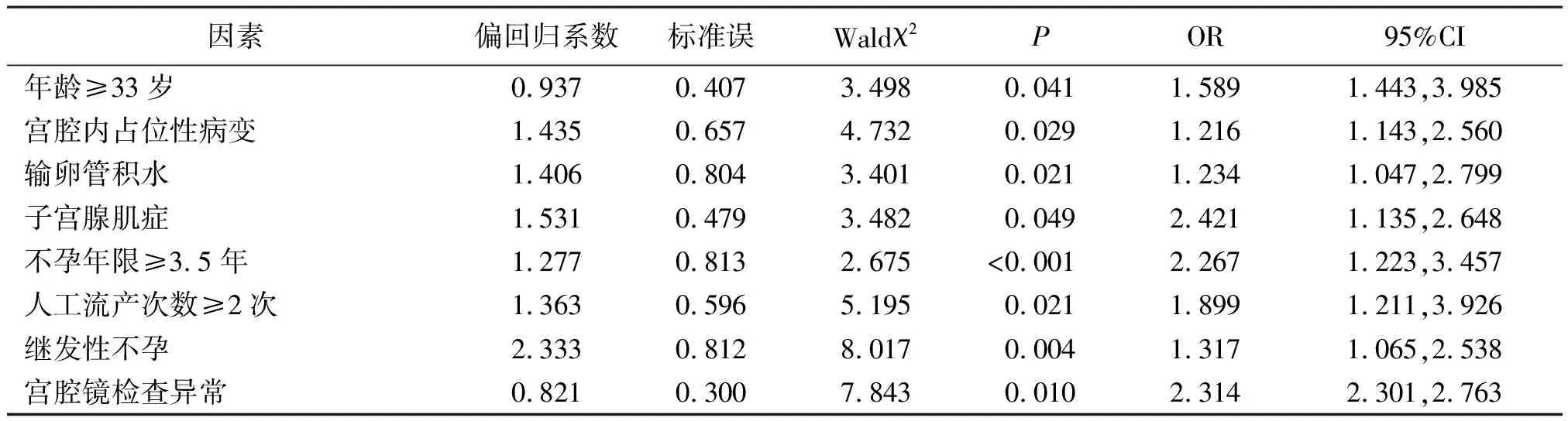
表2 影响RIF患者CE的多因素Logistic回归分析
2.3 A组与B组治疗前后宫腔液中炎性因子水平变化
与治疗前比较,治疗后2组宫腔液中IL-6、IL-8、TNF-α水平均降低,其中B组低于A组,差异有统计学意义(P<0.05)。见表3。

表3 A组与B组RIF合并CE患者治疗前后宫腔液中炎性因子水平比较
2.4 A组与B组子宫动脉血流参数变化
与治疗前比较,治疗后(在胚胎移植前一天进行超声检测)2组子宫动脉搏动指数、EMI低回声区占肌层比例均降低,且B组低于A组;治疗后2组血流分支均增加,且B组多于A组,差异有统计学意义(P<0.05)。见表4。

表4 A组与B组RIF合并CE患者治疗前后子宫动脉血流参数比较
2.5 A组与B组胚胎着床率、临床妊娠率、生化妊娠率、早期流产率比较
A组总移植胚胎数为72个,胚胎着床率为34.72%(25/72);B组总移植胚胎数为69个,胚胎着床率为56.52%(39/69)。与A组比较,B组胚胎着床率、临床妊娠率较高,差异有统计学意义(P<0.05)。2组生化妊娠率、早期流产率比较差异无统计学意义(P>0.05)。见表5。
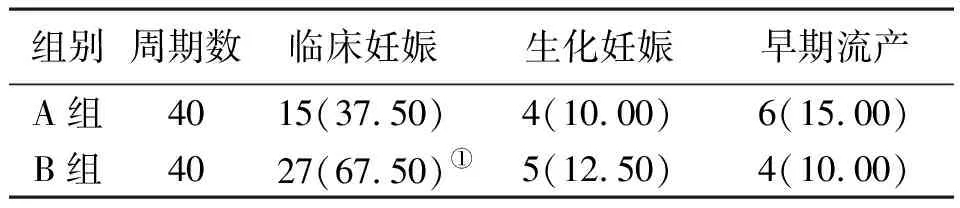
表5 A组与B组RIF合并CE患者临床妊娠率、生化妊娠率、早期流产率比较[例(%)]
2.6 不良反应比较
患者治疗过程中均未出现不良反应情况。
3 讨论
RIF是目前辅助生殖技术中的一大难点,有研究显示其在不孕症中的发生率为15%~20%[8-9]。有效的胚胎植入仍然是提高辅助生殖技术妊娠率的主要方法,特别是涉及体外受精-胚胎移植的妊娠率。胚胎植入是胚胎发育的一个复杂过程,涉及囊胚和子宫内膜接受能力之间的时间协调,研究表明许多RIF的发生与子宫内膜形态、功能的异常有关。
CE是一种以子宫内膜间质异常浆细胞浸润为特征的持续性轻微局部炎症性疾病。通过高通量测序技术及常规细菌培养发现CE最常见的致病菌为粪肠球菌、肠杆菌、链球菌、葡萄球菌、阴道加德纳菌属和支原体属[10-11]。有研究表明,CE在不孕症患者中的患病率约为39%[12],在RIF患者中可高达66%[13]。CE影响胚胎植入的主要机制在于对子宫内膜容受性的改变,导致子宫内膜微环境发生紊乱,免疫系统稳态遭受破坏,进而对胚胎植入造成影响[14]。有研究表明,随着年龄增大,继发性不孕比例有所增加,而且不孕年限越长,精卵结合障碍越严重,进而胚胎着床失败的风险也越高;宫腔内占位性病变、人工流产次数较多,可对患者子宫内膜结构形态产生影响,或可引发宫腔逆行感染,进而破坏受精卵着床;子宫腺肌症可造成子宫形态发生变化,进而影响胚胎植入的整体质量[15]。
目前,临床上针对CE患者的治疗多为抗生素经验性用药,常规给予甲硝唑、盐酸多西环素等药物口服后经机体血液循环到达子宫内膜的治疗效果被大大削弱,临床疗效欠佳[16]。宫腔灌注作为一种局部给药方式能够改善患者子宫内膜血流的异常状态,加快着床部位局部的血管生成及组织重构进程[17]。另外,借助冲洗的方式联合灌洗液能使药物与子宫内膜充分接触,提升药物在子宫内膜局部的有效浓度。子宫动脉的血流动力学参数可有效反映子宫内膜血运状态,与单独应用口服抗生素治疗比较,联合宫腔内灌注能够改善宫腔微环境使其适宜正常的胚胎着床,还可保持良好的子宫内膜容受性,进而提升患者的临床妊娠率[18-19]。本研究结果发现,治疗后B组子宫动脉搏动指数、EMI低回声区占肌层比例均低于A组,血流分支多于A组,胚胎着床率、临床妊娠率与A组比较均处于较高水平。表明抗生素联合宫腔灌注治疗可改善RIF合并CE患者的子宫内膜容受性,提升临床妊娠率与胚胎着床率,效果显著。
由于CE被认为是一种宫腔轻微炎症反应,并且炎症不会扩散到全身,因此血液中炎性因子的表达差异并不明显。然而,针对宫腔微生物群的炎症反应可以局部影响子宫内膜微环境,局部炎症会导致以产生促炎因子为主Th1细胞的过度表达。另有研究显示,胚胎的种植过程主要受到子宫内膜局部抗炎因子与促炎因子动态平衡的影响,CE患者机体炎性细胞的持续性浸润、渗出,导致子宫内膜局部微环境发生改变,进而对其接受胚胎的能力产生负面影响[20-21]。促炎因子TNF-α、IL-6、IL-8等可损伤宫腔微环境进而导致胚胎种植失败或早期流产;TNF-α是由淋巴细胞分泌的一种可溶性多肽细胞因子,而IL-6、IL-8是白细胞介素家族中的重要组成成员,当机体处于感染状态时,这些细胞因子在患者体内可呈现不同程度的高表达,然后进一步激活多形核白细胞和内皮细胞等效应细胞,同时释放大量的自由基、蛋白酶等,加速花生四烯酸代谢,释放血栓素、前列腺素、白三烯和一氧化氮等炎性介质,形成瀑布效应,导致机体发生过度炎症反应。IL-6、IL-8等可对调控正常妊娠的内分泌-细胞因子网络造成不良影响,胚胎植入过程中IL-6、IL-8可参与子宫内膜局部血管生成、滋养层分化、胎盘发育等,促使不利于妊娠维持的免疫功能增强,进而导致不良的临床妊娠结局[22]。因涉及医学伦理问题,本研究未对RIF中无CE患者进行宫腔液提取及检测,但本研究结果显示,治疗后A、B组宫腔液中的炎性因子表达水平均降低,说明CE可能通过增加炎性因子的分泌调控子宫内膜局部微环境。
地塞米松作为一种糖皮质激素,能对巨噬细胞吞噬抗原的过程起到屏障作用,减少溶酶体酶的释放;地塞米松还可以抑制自身抗体及各项促炎因子的产生与聚集,避免因炎症反应激活子宫内膜局部免疫应答进程;地塞米松可调控子宫内膜自然杀伤细胞的基因转录过程,改善外周血Th1/Th2比例的失衡状态,纠正紊乱的子宫形态结构,缓解机体的炎症反应[23]。此外,有研究还显示,应用宫腔灌注治疗并不会对宫腔造成损伤,降低患者胚胎种植率,是一项行之有效且安全的治疗方式[24-25]。通过对本研究结果分析发现,抗生素联合宫腔灌注治疗可减轻RIF合并CE患者子宫内膜局部的炎症反应,改善生殖助孕结局。
本研究发现,年龄偏大、宫腔内占位性病变、输卵管积水、子宫腺肌症、不孕年限较长、多次人工流产、继发性不孕、宫腔镜检查异常可能引起CE进而导致RIF,临床上口服抗生素联合宫腔灌注地塞米松治疗RIF合并CE可有效减轻子宫内膜局部的炎症反应,改善患者的子宫内膜容受性,提升胚胎着床率及临床妊娠率。因胚胎植入是受多因素影响的复杂过程,临床上可进行大样本量、多中心的研究,以指导RIF合并CE患者的综合干预,达到改善预后及临床妊娠结局的目的。
