川崎病患儿血清CaN、NFATc1水平与免疫球蛋白治疗反应的相关性
2024-05-16侯颖莹
侯颖莹
(平顶山市第一人民医院 儿科一病区,河南 平顶山 467000)
川崎病是以全身性血管炎症改变为主要病理特征的急性发热、出疹性疾病,可能会引起冠状动脉病变、后天性心脏病等并发症,对患儿的生命健康、成长发育产生严重影响[1]。静脉注射免疫球蛋白(immunoglobulin’intravenous,IVIG)联合阿司匹林是目前临床上治疗川崎病患儿的首选方式,对改善患儿预后具有重要作用[2]。但有报道显示有10%~20%的患儿在治疗后出现持续性发热、复热等治疗无反应情况[3]。目前普遍认为过度炎症反应及免疫系统异常激活是导致患儿IVIG治疗无反应的病理基础[4-5]。钙调神经磷酸酶(calcineurin,CaN)是控制炎症因子表达的重要调节因子[6]。活化T细胞核因子c1(nuclear factor of activated T cells c1,NFATc1)是具有多种调节功能的转录因子,可参与多种免疫细胞的表达。因此推断上述两种因子或可通过促成过度炎症反应、免疫异常表达来造成患者IVIG治疗无反应。为验证以上推断,本研究采用前瞻性研究方法重点探讨血清CaN、血清NFATc1与患儿IVIG治疗反应的关系,以期为临床提高治疗效果提供理论依据。
1 资料与方法
1.1 研究对象
本研究经医院医学伦理委员会审批。采用前瞻性研究,选取平顶山市第一人民医院2018年1月至2023年1月收治的100例川崎病患儿作为研究对象。(1)纳入标准:①川崎病参照第9版《儿科学》[7]中诊断标准,且处于急性期;②首次发病;③符合接受IVIG联合阿司匹林治疗指征;④患儿监护人同意参与本研究并签署研究知情同意书。(2)排除标准:①入组前即接受相关治疗;②合并渗出性多形性红斑、幼年特发性关节炎全身型等类似症状的疾病;③对IVIG治疗过敏;④合并恶性肿瘤、多器官功能障碍;⑤合并自身免疫系统障碍、血液系统疾病;⑥合并急慢性感染性疾病,例如脓毒血症、败血症等。(3)脱落标准:①未严格遵照医嘱治疗;②未完成后续随访或转出本院继续治疗;③因个人原因申请退出研究。根据上述标准纳入100例患儿,其中男62例、女38例;年龄3~6岁,平均5.00(3.00,6.00)岁;入院时体温39.0~40.0 ℃,平均(39.48±0.32)℃。
1.2 方法
1.2.1治疗方案
患儿入院后均接受对症支持治疗,包括补液、保肝、保心肌等,并采用IVIG(贵州泰邦生物制品有限公司,国药准字H20046260)联合阿司匹林肠溶片(黑龙江鼎恒升药业有限公司,国药准字H2302213)治疗,静脉输注IVIG,每日剂量2 g·kg-1,连续输注1周;口服阿司匹林每日30~50 mg·kg-1,在患儿体温恢复正常3 d后或患儿病程14 d后,其剂量逐渐减少至每日3~5 mg·kg-1,连续治疗6~8周后停止。
1.2.2IVIG反应性的评估标准[8]
在患儿经过IVIG治疗后仍出现持续性发热,且持续时间≥36 h,或者提示患儿在退热后再次发热,满足上述1条即视为治疗无反应,纳入IVIG治疗无反应组,其他纳入IVIG治疗敏感组。
1.2.3实验室指标
(1)血清学指标:在患儿入院时抽取空腹静脉血6 mL放置于2个干净无菌试管中,1管离心(转速3 000 r·min-1,离心时间15 min,离心半径8 cm)后分离上层清液使用酶联免疫吸附法检测患儿血清CaN、NFATc1、白细胞介素-6(interleukin-6,IL-6)水平;使用溴甲酚绿发检测血清白蛋白水平;使用速率散射浊度法检测患儿C反应蛋白(C-reactive protein,CRP),所有试纸均采自广州万孚生物科技有限公司;使用全自动生化分析仪(重庆润康生物科技有限公司,RC-480)检测丙氨酸氨基转移酶(alanine aminotransferase,ALT)、天冬氨酸氨基转移酶(aspartate aminotransferase,AST)。(2)全血指标:另1管使用血细胞分析仪(深圳赛斯鹏芯生物科技有限公司,XPEN 60 CRP SAA)检测患儿的白细胞计数、血小板计数、中性粒细胞计数以及血红蛋白(hemoglobin,Hb)水平,另使用自动化红细胞沉降率分析仪(武汉迪艾斯科技有限公司,型号:VES-TECH 20)检测患儿的红细胞沉降率(erythrocyte sedimentation rate,ESR)水平。
1.2.4一般资料
由研究人员参考相关文献[4,6],结合研究目的自制一般资料收集表,统计患儿的性别(男、女)、年龄、体重指数(body mass index,BMI)(BMI<18.5 kg·m-2视为体重过轻;BMI 18.5~23.9 kg·m-2视为体重正常;BMI 24.0~27.9 kg·m-2视为超重;BMI≥28 kg·m-2视为肥胖)[9]、入院时体温、病程、发热时间、住院时间。
1.2.5统计学方法
2 结果
2.1 川崎病患儿IVIG治疗反应性情况
100例患儿中有20例表现出IVIG治疗无反应,占比为20%(220/100),纳入IVOG治疗无反应组;另80例患儿治疗敏感,占比为80%(80/100),纳入IVIG治疗敏感组。
2.2 两组一般资料
IVIG治疗无反应组患儿入院时血清CaN、NFATc1及CRP水平高于IVIG治疗敏感组(P<0.05);其余一般资料比较,差异无统计学意义(P>0.05)。见表1。

表1 两组患儿一般资料比较
2.3 血清CaN、NFATc1水平与IVIG治疗反应的相关性
经点二列相关性检验显示,血清CaN、NFATc1水平与川崎病患儿IVIG治疗无反应存在正相关关系(r=0.647、0.800,P<0.001)。
2.4 血清CaN、NFATc1水平对IVIG治疗反应影响的logistic回归性分析
将表1中差异有统计学意义的相关因子作为自变量(血清CaN、血清NFATc1、CRP),将患儿IVIG治疗反应作为因变量(治疗无反应=1,治疗敏感=0)。经logistic回归性分析检验显示高水平血清CaN、血清NFATc1是导致患儿IVIG治疗无反应的影响因素(P<0.05)。见表2。
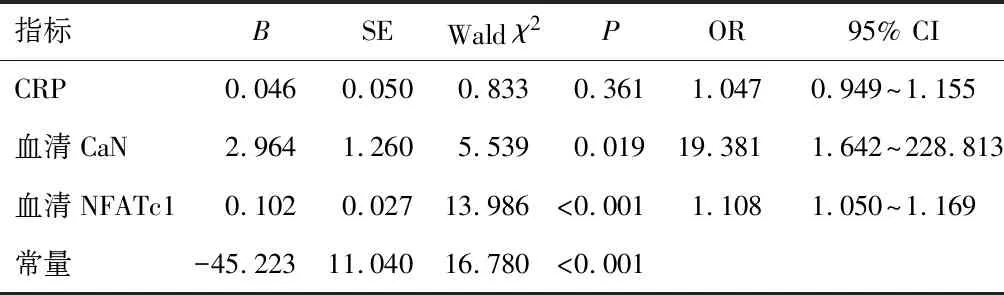
表2 血清CaN、NFATc1水平对IVIG治疗反应影响的logistic回归性分析
3 讨论
虽然多数川崎病患儿在经过IVIG联合阿司匹林治疗后可获得满意预后,但仍有部分患儿表现出IVIG治疗无反应,进而增加冠状动脉损害、血栓栓塞等并发症的发生风险,导致其预后不良。现有研究表明,过度炎症反应、免疫功能异常与IVIG治疗无反应关系密切,而血清CaN、血清NFATc1在机体的炎症反应及免疫表达中发挥重要作用,故分析上述二者可能与IVIG治疗无反应存在关系[10]。本研究100例患儿中有20例出现IVIG治疗无反应,发生率为20%,稍高于张俊民等[11]研究中的15.82%,分析是与纳入患儿年龄范围不同有关。但总体而言,川崎病患儿IVIG治疗无反应的发生率较高,临床应当积极关注患儿IVIG治疗反应情况,以便及时更改治疗方案。
本研究结果显示,IVIG治疗无反应组患儿的血清CaN、血清NFATc1水平均高于IVIG治疗敏感组,初步说明高水平的血清CaN、血清NFATc1与IVIG治疗无反应有关。这是因为血清CaN是广泛存在于神经细胞、淋巴细胞、骨骼肌细胞等不同类型细胞细胞质中的异二聚体蛋白质,能够调节多种离子通路与信号,参与并加剧炎症反应过程,进而加快患儿体内血管炎症发展,故表现出IVIG治疗无反应。血清NFATc1是血清CaN下游调节产物,能够协同血清CaN发挥促炎效用,进一步恶化炎症损害,最终降低患儿IVIG治疗反应性。
为验证以上推断,本研究采用点二列相关性检验显示高水平血清CaN、血清NFATc1与IVIG治疗无反应呈正相关关系,且经logistic回归性检验显示血清CaN、血清NFATc1是导致IVIG治疗无反应的影响因素,说明血清CaN、血清NFATc1水平越高,患儿IVIG治疗无反应的发生风险越高。分析原因在于高水平的血清CaN会激活T细胞,提高IL-1β、肿瘤坏死因子-α等多种炎症因子的表达,诱导患儿出现脉管炎症反应,而该种炎症反应会进一步刺激尾加压素-2的信号传递,从而促进血管内皮细胞凋亡,加重全身血管炎症病变,最终造成IVIG治疗无反应[12-13]。不仅如此,高水平的血清CaN还能促进半胱氨酸天冬氨酸蛋白酶-3表达,直接作用于细胞器引发内皮细胞的凋亡,损伤血管内皮功能,增加患儿发生冠脉损害风险,进一步降低IVIG治疗获益。何雷等[13]研究中也指出,IVIG治疗无效亚组患儿血清CaN高于有效亚组,也能证明血清CaN可影响患儿IVIG治疗反应情况,且在其研究中也指出血清CaN与川崎病患儿发生冠脉损害关系密切。本研究未作此类分析,可在后续补充证明。血清NFATc1是血清CaN的下游产物,高水平的血清CaN会激活血清NFATc1的表达,促使其去磷酸化并转移至细胞核内,调节多种细胞因子转录,提高炎症因子、黏性因子的表达,导致机体免疫功能异常,削弱IVIG治疗获益。不仅如此,现有研究表明血清NFATc1与血清CaN通路能够有效维持血管内皮细胞的正常功能,而高水平的NFATc1能够刺激通路表达,促进川崎病患儿血管内皮功能损害,进而推动患儿病情发展,导致IVIG治疗无反应情况的出现[14]。
侯玉等[15]研究中指出血清CRP是影响患儿IVIG治疗反应的相关因素。在本研究中也显示IVIG治疗无反应组患儿的CRP水平高于IVIG敏感组。这是因为CRP是机体中重要的非特异性炎症标志物,高水平表达说明机体中炎症反应更剧烈,而IVIG治疗无反应的病例基础则为过度的炎症反应,因此CRP表现为升高。但经logistic回归性分析显示CRP并非导致IVIG治疗无反应的独立风险因子,分析是与因子之间相互作用有关。
4 结论
川崎病患儿IVIG治疗无反应发生风险较高,且与血清CaN、血清NFATc1水平有关。
