肺移植术后膈肌移动度与自主呼吸试验期间呼吸功能参数的相关性
2024-05-11姜淑云张佳悦许红阳
王 宋 姜淑云 张佳悦 董 妍 田 静 许红阳
肺移植术已成为大多终末期肺病患者的唯一有效治疗方法,而有创机械通气在肺移植术中和术后的呼吸功能支持中具有重要作用,极大地改善了患者的临床结局。但由于肺移植术操作复杂、创伤性大,导致围手术期病情复杂,肺移植受者术后易出现机械通气时间延长,甚至需要多次接受机械通气以维持呼吸功能。机械通气的撤离是肺移植术成功与否的关键,而肺移植术后机械通气患者常发生膈肌功能障碍,可导致撤机成功率下降、重症加强护理病房(intensive care unit,ICU)监护时间延长、相关并发症发生风险升高,但目前临床因ICU 环境中评估及监测膈肌功能方法受限,尚未能及时监测并做出改善。超声作为一种非侵入性操作,近年来在急危重症领域的应用逐渐开展,可于机械通气及撤机过程中对患者心肺功能进行评估,其所测膈肌功能参数在预测肺移植受者撤机结果中有一定的应用价值。本研究通过分析超声所测膈肌移动度(diaphragm excursion,DE)与自主呼吸试验(spontaneous breathing trail,SBT)期间呼吸功能参数的相关性,旨在准确评估肺移植术后患者呼吸功能,为指导顺利撤机提供参考指标。
资料与方法
一、研究对象
选取2022 年7 月至2023 年2 月于我院心肺诊疗中心行肺移植术患者114例,男83例,女31例,年龄27~68岁,平均(55.4±11.9)岁。纳入标准:①年龄≥18 岁;②肺移植术后机械通气时间≥48 h,全身状况稳定;③病历资料完整。排除标准:①术前已行气管切开,机械通气时间<48 h;②T6 以上胸椎疾病、脊髓损伤等神经系统损伤;③患者依从性差;④超声检查时膈肌图像获取不佳。本研究经我院医学伦理委员会批准,所有患者均签署知情同意书。
二、仪器与方法
1.呼吸功能监测:使用迈瑞BeneVision N22、N19监护仪监测患者生命体征;Dräger Evita4 呼吸机对患者进行机械通气治疗,监测潮气量(VT)、浅快呼吸指数(RSBI),记录呼吸机支持时间;抽取患者桡动脉血5 ml,采用血气分析仪检测动脉血氧饱和度(SaO2)、血氧分压(PaO2)、pH、二氧化碳分压(PaCO2)。
2.SBT 及分组:SBT 前先行撤机筛查,符合条件者[即吸入氧浓度≤40%,呼气终末正压≤5 cmH2O(1 cmH2O=0.098 kPa),血流动力学稳定无需使用血管活性药物,呛咳能力好]进一步行30 min SBT。SBT成功标准[1]:①SaO2≥90%,PaO2≥60 mmHg(1 mmHg=0.133 kPa);②pH 为7.35~7.45,PaCO2增 加<10 mmHg,心 率<140 次/min;③90 mmHg<收缩压<200 mmHg;④呼吸频率<35次/min;⑤意识清醒,无不适感,无辅助呼吸肌肉参与,满足以上任意3 项及以上即可判定。SBT 成功后,患者于24 h 内撤机,若撤机后48 h 内无需再次行机械通气判为撤机成功,若SBT 失败或撤机48 h 内需再次行机械通气判为撤机失败。本研究依据撤机结果分为撤机失败组92例和撤机成功组22例。
3.超声检查:于肺移植术后首次行SBT 15 min 时使用康乃馨床旁彩色多普勒超声诊断仪(深圳华声医疗技术股份有限公司,凸阵探头,频率1~5 MHz)监测膈肌收缩功能,患者取仰卧位,将探头置于右侧锁骨中线肋缘,以肝为声窗,取可同时显示肝、膈肌和下腔静脉的切面,然后切换至M 型模式,调整取样线使其与膈肌垂直,分别测量平静呼吸时膈肌在吸气相、呼气相垂直运动的距离,计算其差值即为DE。以上操作均由同一具有2 年以上工作经验的超声医师完成,所测参数均重复测量3次取平均值。
4.临床资料收集:通过查阅病历获取患者性别、年龄、体质量指数、合并症、原发病、肺移植术术式及时间、术后原发性移植物失功(primary graft dysfunction,PGD)发生情况等。
三、统计学处理
应用SPSS 26.0统计软件,计量资料以x±s表示,组间比较采用t检验;计数资料以例或率表示,采用χ2检验。采用Pearson相关分析法分析DE与呼吸功能参数的相关性。P<0.05为差异有统计学意义。
结果
一、两组临床资料比较
与撤机失败组比较,撤机成功组合并症中糖尿病占比更低,原发病中慢性阻塞性肺炎、矽肺占比更高,肺移植术时间更短,术后PGD 发生率更低,差异均有统计学意义(均P<0.05);两组性别、年龄、体质量指数、肺移植术术式比较差异均无统计学意义。见表1。

表1 两组临床资料比较
二、两组DE及呼吸功能参数比较
与撤机失败组比较,撤机成功组PaO2、VT、DE 均更高,RSBI更低,呼吸机支持时间更短,差异均有统计学意义(均P<0.05)。见表2和图1。
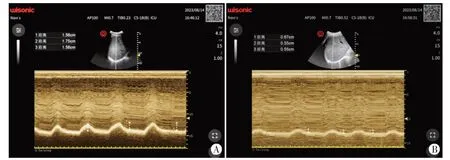
图1 两组膈肌超声图

表2 两组DE及呼吸功能参数比较(x±s)
三、相关性分析结果
DE 与PaO2、VT 均呈正相关(r=0.478、0.734,均P<0.05),与RSBI、呼吸机支持时间均呈负相关(r=-0.593、-0.567,均P<0.05)。见图2。

图2 DE、PaO2、VT、RSBI及呼吸机支持时间的组内相关性分析
讨 论
肺移植是终末期肺病患者最有效的治疗方法,术后患者早期呼吸机撤离被视为肺移植术阶段性成功的标志,故SBT 期间动态监测患者呼吸功能尤为重要[2]。近年来,床旁超声在急危重症领域的应用逐渐开展,膈肌超声、肺部超声等在评估重症患者呼吸功能方面应用广泛,具有实时、操作简便、可重复性佳、安全等优势[3]。膈肌是人体最重要的呼吸肌,占所有呼吸肌功能的60%~80%,并参与咳嗽、遏制消化道反流、排便、分娩等重要生理过程,故膈肌功能也是肺移植术后的重要监测内容[4]。目前国内外围绕膈肌功能预测呼吸机撤机的相关研究[5-6]均取得了积极验证,对确定合适的撤机拔管时机、预测患者转归均有重要的意义。然而,常用的呼吸功能监测参数PaO2、VT、RSBI 仅反映整体呼吸系统功能,并不能代表膈肌所致的呼吸驱动。本研究应用超声测量肺移植术后患者DE,并分析其与SBT 期间呼吸功能参数的相关性,旨在为指导肺移植术后撤机寻找新的可靠参考信息。
研究[7]发现超过2/3 的肺移植患者术后可出现膈肌功能障碍,且功能恢复至正常水平的时间可长达1~2年。膈肌发生失用性萎缩的速度是其他骨骼肌的8倍,可导致患者撤机成功率下降、ICU监护时间延长、相关并发症发生风险升高。有学者[8]于肺移植术前后对所有患者进行监测,发现膈肌功能障碍主要表现为收缩乏力、电活动和运动学方面指标减弱,虽然临床呼吸参数(肺功能、6 min 步行试验)表现良好,但膈肌功能不全从术后至恢复正常水平所需时间平均长达1 年。膈肌功能障碍患者的机械通气持续时间增加,Boscolo 等[9]研究显示肺移植术后膈肌功能障碍发生率高达78%,与撤机困难有关;且撤机困难患者的膈肌功能参数及神经通气效率的平均值较撤机容易患者均更低,上述参数在预测撤机结果方面显示出相似的准确率,与呼吸机支持时间呈负相关。本研究中,肺移植患者术后总体撤机成功率为80.7%,撤机成功组SBT 期间PaO2、VT、DE 均较撤机失败组更高,RSBI更低,呼吸机支持时间更短,差异均有统计学意义(均P<0.05),提示肺移植术后呼吸功能差、低氧、低潮气量患者撤机失败率更高;患者膈肌功能不全可能通过影响呼吸功能延长机械通气时间,最终导致肺移植后预后不佳。Le Neindre 等[6]通过Meta 分析总结发现膈肌超声预测危重患者撤机失败风险的特异度较高(0.80),但灵敏度较低(0.71),分析原因为撤机也受非膈肌相关因素的影响,未发生膈肌功能障碍并不意味着无撤机失败的风险。此外,与撤机失败组比较,本研究撤机成功组合并症中糖尿病占比更低,原发病中慢性阻塞性肺炎、矽肺占比更高,肺移植手术时间更短,术后PGD 发生率更低,差异均有统计学意义(均P<0.05)。分析其原因:PGD为患者肺移植术后早期死亡和长期生存率降低的主要原因,糖尿病、肥胖、慢性肺功能不全等多种危险因素均可增加PGD 的发生风险。PGD 的发展与不良结局有关,早期低氧亦可导致呼吸支持依赖及早期撤机失败。
本研究相关性分析显示,DE与PaO2、VT均呈正相关(r=0.478、0.734,均P<0.05),与RSBI、呼吸机支持时间均负相关(r=-0.593、-0.567,均P<0.05),与既往研究[10]结果一致。提示膈肌功能受损可影响肺移植术后的撤机结果,超声可作为肺移植术后早期危重症患者呼吸功能监测的有效手段。
本研究的局限性:①为单中心、回顾性研究,样本量偏小,超声检查及图像分析均由同一超声医师完成,其操作经验和水平可能影响图像质量及数据,从而直接影响本研究结果与其他研究间的异质性;②未区分单肺(左、右)移植对DE 测值的影响,后续需完善试验设计以排除混杂因素对结果的影响;③未对患者的远期预后进行随访,今后需行多中心、大样本研究进一步探讨。
综上所述,肺移植术后超声所测DE与SBT期间呼吸功能参数均相关,可用于肺移植术后呼吸功能的评估以指导撤机时机的选择。
