基于铜死亡相关的铁死亡基因构建预测肝癌患者预后的模型
2024-05-07谭天华宋京海
谭天华,宋京海
(1. 中国医学科学院/北京协和医学院研究生院,北京 100730;2. 北京医院/国家老年医学中心/中国医学科学院老年医学研究院,北京100730)
肝细胞癌(简称肝癌)是全球范围内最常见的恶性肿瘤之一,根据世界卫生组织(WHO)的数据,每年全球有超过80万人被诊断患有肝癌,而且几乎相同数量的患者因此丧失生命[1]。肝癌的预后评估、个体化治疗策略的制定一直是临床研究的重点之一[2]。目前,临床医生主要依靠临床特征和病理学指标来判断肝癌患者的预后,然而这些传统的预测指标存在一定的局限性,无法做到个体化[3]。因此,寻找新的预测指标和生物标志物来评估肝癌患者的预后风险具有重要意义。铁死亡是铁依赖的新型细胞程序性死亡方式,主要进程包括铁积累、脂质过氧化、修复系统受损,可造成细胞死亡和膜破坏,促进铁死亡可作为诱发肿瘤细胞死亡的治疗手段[4]。铁死亡在肝癌的发生、发展中发挥重要作用,NRF2、Rb、MT1G等多种基因参与肝癌细胞抵抗索拉非尼诱导的铁死亡[5]。铜死亡通过铜离子与三羧酸循环的脂质组分结合,促进铁硫蛋白损伤、脂酰化蛋白聚集,产生毒性应激导致癌细胞死亡[6]。铁、铜离子具有剂量依赖性细胞毒性,能相互作用共同促进肿瘤细胞死亡[7]。本研究通过构建基于铜死亡相关的铁死亡基因的模型,评估了其与肝癌患者生存期、免疫功能的关系,以寻找预测肝癌预后的标志物,为临床研究提供参考。
1 资料和方法
1.1数据来源 使用TCGA(The Cancer Genome Atlas)数据库中的肝癌患者RNA序列转录组数据、相关临床特征数据和突变数据,对转录组数据进行了整理,分离出mRNA和LncRNA,并提取了临床信息和计算肿瘤突变负荷,最终纳入370例肝癌患者,按照1∶1的比例将合并后的数据集随机分为训练组(即训练模型数据,通过训练组的数据确定拟合曲线的参数,185例)和测试组(即测试已经训练好的模型的精确度,185例)。同时下载driver、Suppressor和Marker三类与铁死亡相关的基因,合并为铁死亡相关基因集合。将铜死亡基因和铁死亡基因与mRNA结合,获得这些基因相关的表达矩阵。使用R Studio软件中的limma包,过滤标准为相关系数corFilter=0.3,并设置p值过滤标准为pvalueFilter=0.05,筛选与铜死亡相关基因具有相关性的铁死亡基因。
1.2模型的构建 使用R Studio软件中的limma包将与铜死亡相关的铁死亡基因与肝癌患者的临床数据合并。基于中位风险评分,建立低风险组、高风险组2个亚组。利用Lasso Cox回归方法,在TCGA数据集中寻找与肝癌患者生存期显著相关的铜死亡相关的铁死亡基因。通过多因素Cox回归分析铜死亡相关的铁死亡基因,建立铜死亡相关的铁死亡基因的风险模型。风险评分的计算公式:风险评分=铜死亡相关的铁死亡基因1×coef+铜死亡相关的铁死亡基因2×coef+……+铜死亡相关的铁死亡基因n×coef,其中coef代表铁死亡基因与生存期相关的系数。
1.3模型的验证 绘制风险曲线,观察高风险组和低风险组的差异。采用单因素和多因素的Cox回归分析,验证预后模型是否能够独立于肝癌患者的其他临床特征(如性别、年龄、肿瘤分级和肿瘤分期)来区分预后。绘制ROC曲线和C-index曲线,评估和验证模型预测肝癌患者生存期的准确性。
1.4基因的功能和免疫相关性分析 选取高风险组和低风险组的具有差异表达的基因进行与免疫功能相关性分析,探索2组中表达显著差异的免疫功能指标,绘制瀑布图,比较高风险组和低风险组中基因突变频率的情况。通过将肿瘤突变负荷与肝癌患者的风险评分结合进行分析,获得联合的生存曲线。
1.5统计学方法 运用SPSS 26.0和R 4.0进行数据分析,使用Kaplan-Meier生存曲线和log-rank检验进行高低风险组间的生存期比较,运用单因素和多因素Cox回顾分析预测模型对肝癌患者预后的独立预后价值,绘制ROC曲线评估模型预测肝癌患者生存期的价值,P<0.05为差异有统计学意义。
2 结 果
2.1风险模型的构建 肝癌患者的生存数据和与铜死亡相关的铁死亡基因(见图1)合并后获得13个与铜死亡相关的基因,提取13个基因在肝癌患者中的表达量。运用Lasso回归分析与铜死亡相关的预后基因,并构建Cox模型。在多变量Cox回归数据中选择EIF2S1、G6PD和NRAS这3个与铜死亡相关的铁死亡基因进一步分析,结果显示训练组中EIF2S1、G6PD、NRAS与生存期独立相关(P均<0.05),可构建风险模型以评估肝癌患者的预后风险。根据多变量Cox回归分析得出的预后模型公式如下:风险评分=(0.594 652 370 045 789×EIF2S1表达)+(0.205 764 004 842 305×G6PD表达)+(0.369 015 871 232 048×NRAS表达)。
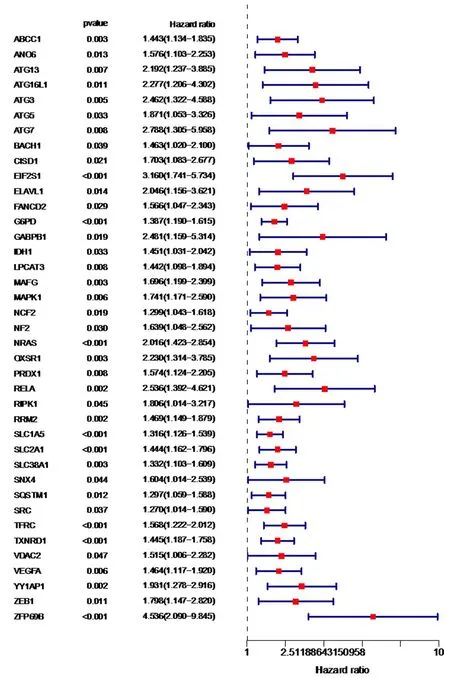
图1 肝癌与铜死亡基因相关的铁死亡基因的表达情况
2.2模型的验证 Kaplan-Meier分析显示,与低风险组比较,高风险组患者的生存期较短(P<0.05),生存率较低(P<0.05),见图2。单因素Cox回归分析显示,铜死亡相关的铁死亡基因构建的风险模型HR为1.734,95% CI为1.494~2.034,P<0.001,见图3。多因素Cox回归分析显示,铜死亡相关的铁死亡基因构建的风险模型HR为1.661,95% CI为1.397~1.976,P<0.001,见图4。ROC曲线分析发现,风险模型预测肝癌患者第1,3,5年生存期的曲线下面积(AUC)分别为0.760,0.663和0.636,AUC均大于0.5,说明该模型对预测肝癌患者的生存期具有较高的准确性,见图5。Kaplan-Meier生存曲线分析显示,与早期肝癌患者相比,晚期肝癌患者生存期更短(P<0.05),生存率更低(P<0.05),见图6。
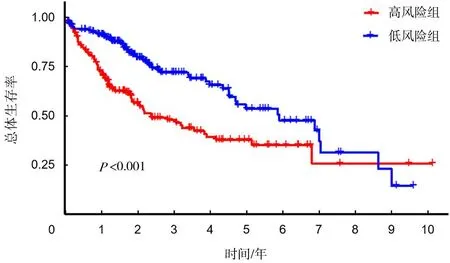
图2 高低风险肝癌患者的Kaplan-Meier 生存曲线
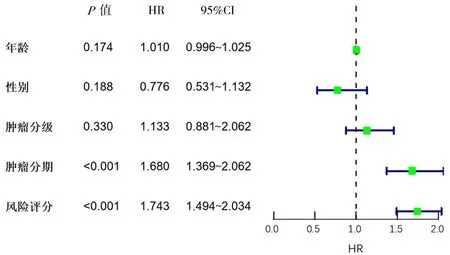
图3 单因素Cox回归分析铜死亡相关的铁死亡基因构建的风险模型对肝癌生存期的预测价值

图4 多因素Cox回归分析铜死亡相关的铁死亡基因构建的风险模型对肝癌生存期的预测价值
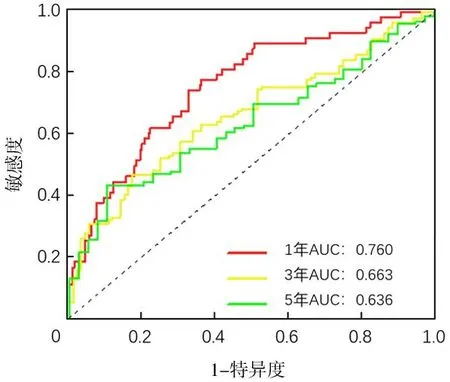
图5 ROC曲线分析铜死亡相关的铁死亡基因构建的风险模型对肝癌生存期的预测价值
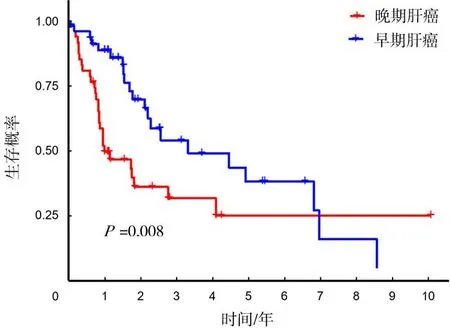
图6 早期和晚期肝癌患者的Kaplan-Meier 生存曲线
2.3基因功能和免疫相关性 在高风险组和低风险组中,Type Ⅱ IFN Response、Parainflammation、APC co-stimulation、CCR、Check-point和MHC class Ⅰ这6个免疫功能的表达存在统计学差异(P均<0.05),见图7。Kaplan-Meier生存曲线分析显示,高肿瘤突变负荷的肝癌患者生存期明显短于低肿瘤突变负荷的患者(P<0.05)。见图8。
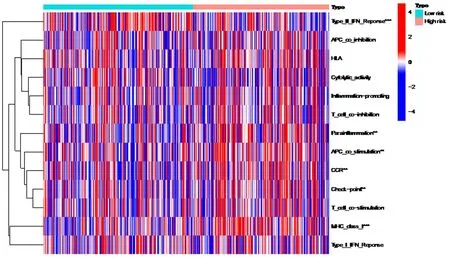
图7 高低风险组患者的免疫功能分析
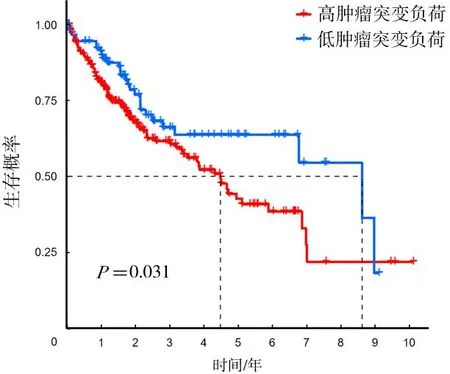
图8 高肿瘤突变负荷与低肿瘤突变负荷肝癌患者的Kaplan-Meier生存曲线
3 讨 论
随着对肝癌细胞学和肿瘤生物学的深入研究,发现铜死亡和铁死亡途径在肿瘤发生发展中具有重要作用,为选择与铜死亡相关的铁死亡基因作为预后模型的关键基因集奠定了理论基础[8]。本研究通过对TCGA数据库中获取的RNA序列转录组数据分析显示,与铜死亡相关的铁死亡基因的表达与肝癌患者的生存期密切相关;通过Lasso回归分析和Cox模型的构建,确定了3个铜死亡相关的铁死亡基因(EIF2S1、G6PD和NRAS)作为预后模型的关键基因,在训练组中被证实与生存期独立相关,其表达水平与风险评分呈正相关。根据多变量Cox回归分析得出的预后模型公式,计算每个患者的风险评分,Kaplan-Meier生存曲线分析显示高风险组和低风险组患者的生存期存在统计学差异,表明构建的模型能对高低风险肝癌患者的生存期具有一定的预测价值;单因素和多因素Cox回归分析验证结果表明铜死亡相关的铁死亡基因构建的风险模型具有肝癌的独立预后特征,可以作为评估患者预后风险的重要指标;ROC曲线分析表明,风险模型能够有效预测肝癌患者的生存期,为临床决策提供了重要的参考依据;Kaplan-Meier生存曲线分析显示晚期肝癌患者生存期明显短于早期肝癌患者,表明风险模型可以准确地预测肝癌患者不同临床阶段的生存期,有助于为不同阶段患者的治疗提供参考。
免疫功能与肝癌患者预后密切相关,其中Type Ⅱ IFN Response反应与抗病毒免疫有关, Parainflammation反应与慢性炎症相关,APC co-stimulation参与T细胞的活化和抗原递呈,CCR与细胞趋化和炎症反应有关,Check-point影响T细胞调节,MHC class Ⅰ在肿瘤免疫监视中起到重要作用[9-14]。本研究结果发现,在高风险组和低风险组中,Type Ⅱ IFN Response、Parainflammation、APC co-stimulation、CCR、Check-point和MHC class Ⅰ这6个免疫功能指标有统计学差异,表明铜死亡相关的铁死亡基因可能参与肝癌的免疫功能调节,与肝癌患者的预后密切相关。
肿瘤突变负荷被认为是一个重要的肿瘤特征,与肿瘤进展和预后密切相关[15]。本研究结果发现,高肿瘤突变负荷患者的生存期明显低于低肿瘤突变负荷的患者,验证了肿瘤突变负荷对肝癌患者生存期的影响,并为评估患者预后提供了重要的补充信息。
综上所述,与铜死亡相关的铁死亡基因在肝癌患者预后、免疫功能和肿瘤突变负荷中有重要作用。本研究为肝癌预后评估提供了一个可靠和准确的模型,该模型基于与铜死亡相关的铁死亡基因能够区分不同预后风险的患者,可以用于指导患者的治疗选择和监测,评估不同预后风险患者对特定治疗方案的反应以及个体化治疗策略的有效性,且为进一步研究铜死亡相关的铁死亡基因与肝癌免疫治疗的关系提供了新的线索,为个体化治疗策略的开发提供了新的方向和目标。
利益冲突:所有作者均声明不存在利益冲突。
