BI-RADS 分级联合超声弹性成像对乳腺癌的诊断价值
2024-04-30陈红燕
陈红燕
(广饶县丁庄中心卫生院广北分院超声科 山东 东营 257347)
乳腺癌是发病率较高的恶性肿瘤之一,前期症状不明显,不易被查出,具有较高的死亡风险,需积极进行早期诊断、治疗,控制病情进展[1]。目前,手术病理学检查是判断乳腺癌发生的有效手段,但检测时间较长,且具有一定创伤性,容易对早期诊断结果产生影响,导致患者错失最佳治疗时机[2]。近年来,乳腺影像报告与数据系统(breast imaging reporting and data system,BIRADS)分级与超声弹性成像(ultrasonic elastography,UE)逐渐得到临床应用,其用于两癌筛查,能够有效对病灶情况进行显示,从而判断疾病进展程度[3]。但两种技术单独使用时容易受到操作者主观因素的影响,导致疾病诊断准确率降低。有研究指出,BI-RADS 分级、UE 检查技术联合使用能够提高疾病诊出率,提高诊断效能[4]。因此,本研究对126 例疑似乳腺癌患者资料进行分析,旨在探讨BI-RADS 分级、UE 检查技术联合使用的诊断价值,详情如下。
1 资料与方法
1.1 一般资料
选取2021 年1 月—2023 年9 月期间在广饶县丁庄中心卫生院广北分院进行两癌筛查的疑似乳腺癌患者126 例,均为女性,患者年龄45 ~65 岁,平均(55.23±3.45)岁,病灶部位:左乳、右乳分别为67 例、59 例。本研究符合《赫尔辛基宣言》中的伦理准则。
纳入标准:(1)所有患者均有明确的症状、手术病理及随访结果;(2)均无肿瘤病史;(3)均符合BIRADS 分级、UE 检查指征;(4)存在乳腺手术史者;(5)患者知情同意。排除标准:(1)病灶直径在1 cm以下;(2)处在妊娠期或哺乳期等特殊时期的女性;(3)检查前1 个月内存在化疗、放疗史者;(4)病灶内部为液化状态者。
1.2 方法
使用彩色多普勒超声诊断仪(迈瑞昆仑Resona 5T)检查,使用高频探头,探头频率设置为(10 ~15)MHz。患者取仰卧位,将双侧乳腺充分暴露,对乳房体积、形态等情况进行观察,判断乳头是否存在内陷问题,将乳头作为中心,对其实施灰阶超声检查,对乳腺肿块的形态、解剖结构进行探查、记录,同时分析患者乳腺肿块的大小、边缘、血流信号、内部微钙化情况,对患者腋窝进行扫描,分析是否存在淋巴结重大问题。使用BI-RADS 分级对患者乳腺肿块进行分级,然后将超声切换至弹性成像模式,实施外力加压检查,并对感兴趣区(ROI)进行重点观察,获得UE,根据UE 显示,对图像硬度进行评价。
1.3 判定标准
1.3.1 BI-RADS 分级标准[5]无法判定类别,需要其他影像学辅助评估为0 级;结果显示阴性,超声检查未发现肿块、微钙化情况及结构紊乱问题为1 级;未发现恶性病灶为2 级;极大可能为良性病灶,需要短期随访为3 级;疑似恶性病灶,风险度在3%~<95%,需进行介入处理为4 级;中等疑似恶性,发生率在95%及以上为5 级;高度提示恶性为6 级。其中0 分:≤3 级,1 分:4 级,2 分:5 级,3 分:6 级。若评分为0 ~1 分,提示患者为良性病变,若评分为2 ~3 分,提示患者为恶性病变。
1.3.2 UE 评分标准[6]1 分:病灶大部分呈绿色;2 分:病灶中间位置呈现蓝色,周围组织呈现绿色;3 分:病灶部位蓝色与绿色所占比例相当;4 分:病灶以蓝色为主,少部分呈现绿色;5 分:病灶及周围组织均呈蓝色。评分在3 分及以下为乳腺增生,评分在4 分及以上为乳腺癌。
1.3.3 联合诊断评价标准 结合UE 对BI-RADS 分级对患者进行调整及矫正,当UE 评分在2 分及以下时,BI-RADS 分级3 ~5 级则下调一级;UE 评分在4 分及以上时,BI-RADS 分级2 ~4 级则上调一级;UE 评分为3 级时,BI-RADS 分级不改变。
1.4 统计学方法
采用SPSS 25.0 统计软件分析数据,符合正态分布的计量资料以均数±标准差(± s)表示,采用t检验;计数资料以频数(n)、百分率(%)表示,采用χ2检验。P<0.05 表示差异有统计学意义。
2 结果
2.1 手术病理结果分析
126 例疑似乳腺癌患者中,116 例为乳腺增生;10 例为恶性肿瘤,其中7 例为导管内原位癌,2 例为浸润性导管癌,1 例为髓样癌。
2.2 两组BI-RADS 分级、UE 评分比较
乳腺癌组BI-RADS 分级、UE 评分均显著高于乳腺增生组(P<0.05)。见表1。
表1 两组BI-RADS 分级、UE 评分比较(± s)

表1 两组BI-RADS 分级、UE 评分比较(± s)
组别例数BI-RADS 分级/级 UE 评分/分乳腺癌组 102.25±0.584.05±0.74乳腺增生组1161.56±0.432.76±0.61 t 4.7306.309 P<0.001 <0.001
2.3 BI-RADS 分级、UE 单独检查及联合检查的诊断结果比较
BI-RADS 分级准确检出乳腺癌6 例,乳腺增生104 例;UE 检查准确检出乳腺癌5 例,乳腺增生102 例;联合检查准确检出乳腺癌10 例,乳腺增生114 例。见表2。
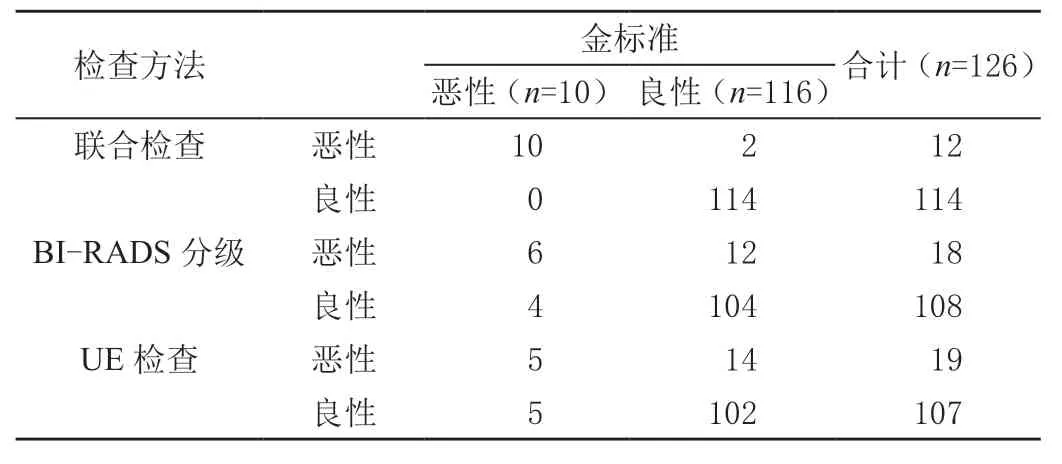
表2 BI-RADS 分级、UE 单独检查及联合检查诊断结果 单位:例
2.4 BI-RADS 分级、UE 单独检查及联合检查的诊断效能比较
联合检查灵敏度、特异度、阳性预测值、阴性预测值、准确率分别为100.00%、98.28%、83.33%、100.00%、98.41%,均高于BI-RADS 检查的60.00%、89.66%、33.33%、96.30%、87.30%及UE 检查的50.00%、87.93%、26.32%、95.33%、84.92%,其中灵敏度、特异度、阳性预测值、准确率差异有统计学意义(P<0.05)。见表3。
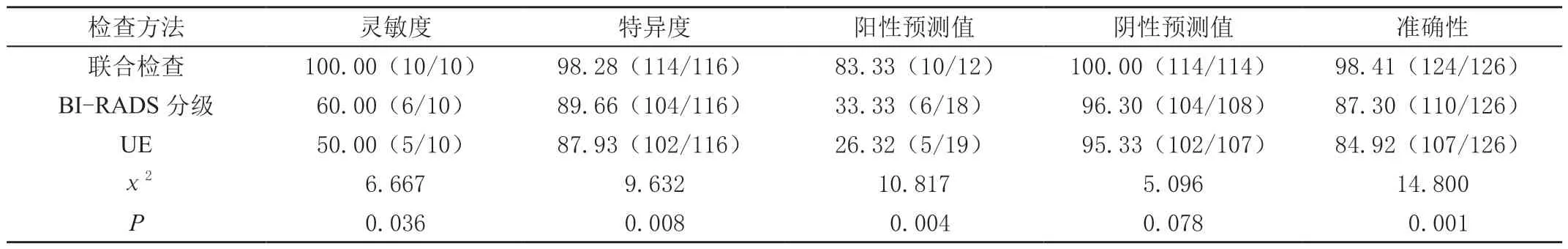
表3 BI-RADS 分级、UE 单独检查、联合检查的诊断效能比较[%(n/m)]
3 讨论
乳腺癌主要发生于乳腺上皮组织,好发于女性,当乳腺细胞生长失去控制后,则会导致乳腺癌发生,患者会出现不同大小的乳腺肿块,多数患者不会出现疼痛问题,不易被发现,随着疾病的发展,患者会逐渐出现乳房皮肤的橘皮样改变,具有较高的死亡风险[7]。因此,早期诊断、治疗对病情的改善至关重要。
目前,穿刺活检、手术病理学组织检查是诊断乳腺癌的“金标准”,具有较高的诊断准确率。本研究结果显示,126 例疑似乳腺癌患者中,116 例为乳腺增生;10 例为恶性肿瘤,其中导管内原位癌、浸润性导管癌、髓样癌分别有7 例、2 例、1 例。但由于穿刺活检、手术病理学组织检查具有一定创伤性,容易对患者身心造成影响,不容易被患者接受,也无法在两癌筛查中应用[8]。近年来,超声技术逐渐得到临床的广泛应用,具有自动扫查、分辨率高的优势,能够准确对乳腺肿块的性质进行判断,可充分显现肿块的性质、边界情况、内部钙化情况等[9]。BI-RADS 分级是临床常用检查技术,能够有效显现患者肿块大小、边界等情况,通过分级对病变情况进行判断[10]。UE 是一种操作简单、可重复的检查技术,可通过不同色彩对患者组织的弹性属性进行判断,还可有效反映病灶组织的软硬程度[11]。本研究中,乳腺癌组BI-RADS 分级、UE 评分与乳腺增生组相比更高,提示BI-RADS 分级、UE 评分均具有一定诊断价值。但BI-RADS 容易受到操作者主观因素的影响,导致分类标准缺乏一定客观性;而UE 由于操作者对图片进行识别时容易存在差异,会导致评分结果的准确性受到影响,尤其评分在3 ~4 分的病灶,具有较高的漏诊、误诊率[12]。
本研究结果中,联合检查灵敏度、特异度、阳性预测值、阴性预测值、准确率分别为100.00%、98.28%、83.33%、100.00%、98.41%,均高于BI-RADS 检查的60.00%、89.66%、33.33%、96.30%、87.30% 及UE 检查的50.00%、87.93%、26.32%、95.33%、84.92%,其中灵敏度、特异度、阳性预测值、准确率差异有统计学意义(P<0.05)。单纯使用BI-RADS 分级技术,虽然能够检出多数患者,但若乳腺癌病灶较小,则会导致其早期生物学特征不明显,多数患者不会显现特征性异常征象,容易影响分级判断的准确性[13]。而UE 技术具有半定量、定性价值,能够对肿块结节的硬度、弹性数据进行评估,从而获得关于肿块的相关数据,对病变组织性质进行全面定位、鉴别,从而减轻操作者主观因素的影响[14]。但单独使用时,若乳腺肿块组织位置较深,施加压力时不容易使其发生改变,导致UE 评分增加,导致假阳性出现;若施加压力高低不适,则会导致UE 评分降低,导致假阴性出现[14]。联合使用则可降低假阴性、假阳性发生率,降低主观因素对结果的影响,对患者乳腺肿块性质进行评估,准确获得肿块结构、形态、回声,根据组织表现的硬度对病变情况进行诊断,从而提高诊断准确性,减少漏诊、误诊的发生。
综上所述,将BI-RADS 分级联合超声弹性成像应用于乳腺癌的检查中,能有效提高疾病诊出率,具有较高的诊断价值。
