淀粉制品中铝残留量的测定
2024-04-10杨晓珺贾添慧
◎ 孙 静,刘 梅,杨晓珺,贾添慧
(太仓市检验检测中心,江苏 太仓 215400)
铝是地壳中含量最高的金属元素,主要以氧化态的三价铝形式广泛存在于自然界中。随着科学技术的进步和发展,人们发现铝是一种对人体健康有危害的元素,体内蓄积过量的铝会对人体骨骼、生殖系统以及生长发育等产生危害[1-4]。铝进入人体的途径有食物、铝制炊具及容器、饮用水等,其中铝摄入的主要来源是食物[5]。普通食物中铝的本底含量通常较低,大部分食物中的铝含量主要来自含铝食品添加剂的使用[6]。粉皮、粉丝等淀粉制品是人们日常消费较多的食品,加入硫酸铝钾、硫酸铝铵等含铝食品添加剂,可以提升淀粉制品的口感和韧性,但若过量则会对消费者健康造成危害。近年来市场监管总局以及各地市场监管局公布的食品安全抽检数据表明,淀粉制品的铝超标情况仍处于较高水平,因此很有必要对淀粉制品中的铝残留量进行检测。《食品安全国家标准 食品中铝的测定》(GB 5009.182—2017)[7]是测定食品中铝的标准方法,国标方法规定了待测样品在消解前需置于85 ℃恒温干燥箱中干燥4 h。笔者在日常试验中发现,国标方法干燥操作耗时较长,且粉皮、凉粉等水分含量较高的淀粉制品在经过4 h 的干燥处理后,样品容易黏结起来,变得比较坚硬,导致后续试验无法均匀取样,影响样品中铝残留量的测定结果。滕布雷等[8]应用红外线水分测定仪对糕点中的水分含量进行测定,并结合电感耦合等离子体质谱法成功测定了糕点中的铝含量,减少了糕点样品烘干4 h 后的变化。红外线水分测定仪操作简单,加热速度快,能够在较短时间内测定出食品、粮食、茶叶等样品的水分含量。电感耦合等离子体质谱法测定铝虽然检测精度较高,但使用的检测设备以及检测成本也很高[9]。而分光光度法使用的分光光度计设备价格低廉、普及率高,操作相对简便,是一般基层实验室都具备的检测手段。
本文尝试将淀粉制品粉碎均匀后直接进行湿法消解,结合分光光度法测定湿样品中铝的质量;同时另取适量粉碎均匀的湿样品置于红外线水分测定仪中快速测定样品的水分含量得到样品干质量,以此计算出样品中的铝残留量。本文对湿法消解温度和消解时间、显色反应时间等试验条件也进行了研究,优化了国标分光光度法的湿法消解条件,明确了显色体系最佳稳定时间。
1 材料与方法
1.1 材料与试剂
随机取样市售的粉皮、凉粉、粉丝等淀粉制品6 批次。
铝溶液标准物质:1 000 mg·L-1,北京坛墨质检科技有限公司;硝酸、硫酸、盐酸、氨水、无水乙醇,以上试剂均为优级纯;对硝基苯酚、铬天青S、乙二胺、聚乙二醇辛基苯醚(Triton X-100)、溴代十六烷基吡啶(CPB)、抗坏血酸,以上试剂均为分析纯。
本试验所用水均为超纯水,试验用的玻璃器皿都在硝酸溶液中(硝酸与水体积比为1 ∶5)浸泡24 h以上,取出后用自来水冲洗干净,最后用超纯水冲洗3 遍后晾干使用。
1.2 仪器与设备
UV2700 紫外-可见分光光度计,岛津仪器(苏州)有限公司;MOC-120H 红外线水分测定仪,日本岛津公司;FA2004 型电子分析天平,上海精科天美科学仪器有限公司;DHG-9240A型电热恒温鼓风干燥箱,上海精宏实验设备有限公司;NH-L 型耐酸耐碱控温电热板,苏州九联科技有限公司;Milli-Q Reference超纯水机,美国Millipore 公司。
1.3 试验方法
1.3.1 试剂及铝标准使用液的配制
1 g·L-1铬天青S溶液:称取0.1 g铬天青S于烧杯中,用乙醇溶液(无水乙醇与水体积比为1 ∶1)溶解并转移至100 mL 容量瓶中定容,混合均匀。
3%Triton X-100 溶液:吸取3 mL Triton X-100 于100 mL 容量瓶中,用水定容,混合均匀。
3 g·L-1CPB 溶液:称取0.3 g CPB 于烧杯中,加入15 mL 无水乙醇使其溶解,用水转移至100 mL 容量瓶中并定容,混合均匀。
乙二胺-盐酸缓冲溶液(pH 值6.7 ~7.0):量取100 mL 乙二胺,缓慢加入盛有200 mL 水的烧杯中,冷却后再往烧杯中缓缓加入190 mL 盐酸,用玻璃棒混匀,用盐酸溶液(盐酸与水体积比为1 ∶1)或乙二胺溶液(乙二胺与水体积比为1 ∶2)调节pH 值至6.7 ~7.0。每次使用前,需重新测定并调节溶液pH 值至6.7 ~7.0。
铝标准中间液(100 mg·L-1):吸取1.00 mL 铝溶液标准物质于10 mL 容量瓶中,用5%硝酸溶液定容,混合均匀。
铝标准使用液(1.00 mg·L-1):吸取1.00 mL 铝标准中间液于100 mL 容量瓶中,用5%硝酸溶液定容,混合均匀。
1.3.2 样品水分含量的测定
称取10 g 左右粉碎好的样品,平铺于红外线水分测定仪的样品盘中,样品层厚应尽量在5 mm 以内,设定设备加热温度为105 ℃,待样品前后两次水分含量变化值为0.01%时设备停止加热,读取设备显示屏上的样品水分含量示值。
1.3.3 样品的消解
称取粉碎好的样品1 ~3 g(精确至0.001 g)置于150 mL 锥形瓶中,依次加入10 mL 硝酸和0.5 mL硫酸,将锥形瓶置于耐酸碱控温电热板上加热消解,消解条件为120 ℃加热0.5 h,升至180 ℃加热2 h,然后升至200 ℃加热,注意若样品消化液变棕色则及时补加适量硝酸,防止消解物炭化,直至锥形瓶内充满白烟且消化液澄清透明或略呈浅黄色。取下锥形瓶并冷却,将消化液用水转移至50 mL 具塞比色管中定容至刻度,混匀。同步做试剂空白试验,空白应与样品加入相同量的酸。
1.3.4 样品中铝残留量的测定
按照国标GB 5009.182—2017第一法分光光度法,分别将1.00 mL 样品消化液、1.00 mL 试剂空白溶液置于25 mL 具塞比色管中,加水至比色管10 mL 刻度。分别取0 mL、0.500 mL、1.00 mL、2.00 mL、3.00 mL、4.00 mL 和5.00 mL 铝标准使用溶液置于25 mL 具塞比色管中,依次向各比色管中加入1 mL 1%硫酸溶液,然后加水至比色管10 mL 刻度。分别向以上比色管中滴加1 滴1 g·L-1对硝基苯酚乙醇溶液,混匀后滴加氨水溶液(1+1)至浅黄色,随后滴加2.5%硝酸溶液,直至浅黄色消失后再多加1 mL 2.5%硝酸溶液,然后加入1 mL 10g·L-1抗坏血酸溶液,混匀后加入3 mL 1g·L-1铬天青S 溶液,再次混匀后加入1 mL 3%Triton-X溶液、3 mL 3g·L-1CPB 溶液和3 mL 乙二胺-盐酸缓冲溶液,最后加水定容至25 mL 刻度,混匀,放置40 min。以空白溶液为参比,用1 cm 比色皿在620 nm波长下测定溶液吸光度值。以标准系列溶液中铝的质量为横坐标,相应的吸光度值为纵坐标,绘制标准曲线,根据样品消化液的吸光度值与标准曲线比较定量。
样品中的铝残留量按式(1)计算。
式中:X为样品中的铝残留量,mg·kg-1;m1为测定用样品消化液中铝的质量,μg;m0为空白溶液中铝的质量,μg;V1为样品消化液总体积,mL;m为样品称样量,g;W为样品水分含量,%;V2为测定用样品消化液体积,mL。
2 结果与分析
2.1 淀粉制品的水分含量测定结果
将市售的粉皮、凉粉、粉丝共3 种6 批次淀粉制品粉碎均匀,用红外线水分测定仪快速测定样品的水分含量,表1 是6 批次样品水分含量的测定结果。由表1可知,粉皮、凉粉的水分含量较高,在75%以上,粉丝的水分含量较低,在15%左右。6 批次样品水分含量平行测定值的相对偏差均小于1%,表明红外线水分测定仪能够快速、准确地测定出淀粉制品的水分含量。
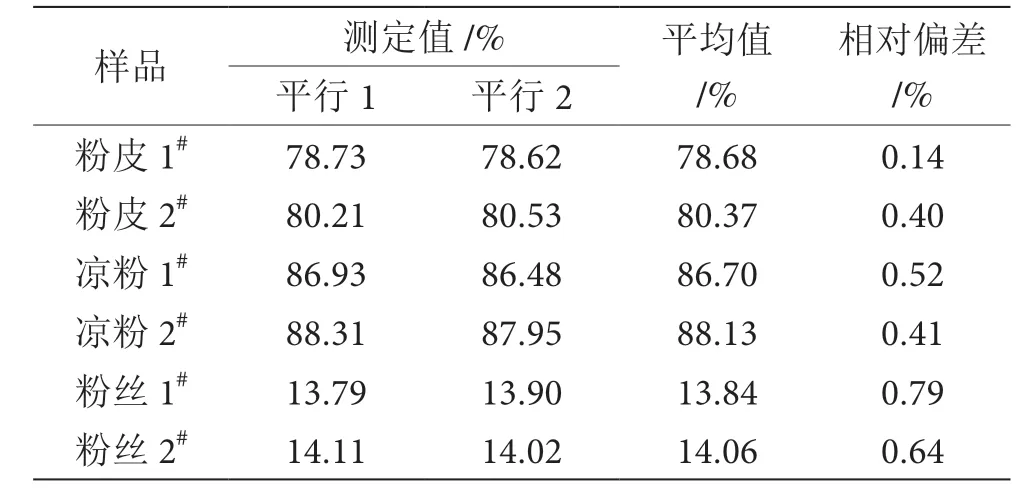
表1 淀粉制品的水分含量测定结果表
2.2 样品消解温度和消解时间的选择
湿法消解操作简便、设备成本低,是一种广泛应用于食品中重金属检测的前处理方法。粉丝、粉皮等淀粉制品油脂含量少,采用湿法消解方法可在较短时间内将其消解完全。称取3 g 左右粉碎均匀且未经干燥处理的粉皮1#样品置于150 mL 锥形瓶中,根据国标方法加入10 mL 硝酸+0.5 mL 硫酸的混合酸体系,将锥形瓶置于耐酸碱控温电热板上加热消解。本文选择了两种样品消解条件进行试验,条件1 为GB 5009.182—2017 第 一法(100 ℃ 1 h →150 ℃ 1 h→180 ℃ 2 h →200 ℃至消化液澄清透明或略呈浅黄色),条件2 为电热板120 ℃加热0.5 h →180 ℃加热2 h →200 ℃至消化液澄清透明或略呈浅黄色。试验结果显示,在两种消解条件下样品均能够消解完全,且消化液澄清透明或略呈浅黄色。条件2 消解用时更短,因此本文选择条件2 为样品消解条件。
2.3 显色时间的研究
以铝空白标准溶液为参比,在620 nm 波长处测定不同显色时间下含量为5 μg 的铝标准溶液的吸光度值。以显色时间为横坐标,以Z值为纵坐标(Z值为各显色时间下铝标准溶液吸光度值与最大吸光度值的比值),绘制曲线图,结果见图1。

图1 不同时间点吸光度比值的变化图
结果表明,在体系显色反应时间为30~50 min时,铝标准溶液的吸光度值较高且相对稳定,在40 min 时体系的吸光度值最高,之后吸光度值随时间逐渐降低,100 min 后体系的吸光度值已降低到40 min 时的89%。表明铝和铬天青S 以及两种表面活性剂形成的蓝绿色四元胶束不能长时间保持稳定状态,应在体系显色反应达到相对稳定阶段后及时测定吸光度值。本文选择在显色反应40 min后立即测定样品的吸光度值。
2.4 标准曲线线性范围
铝标准系列溶液中铝的质量分别为0 μg、0.500 μg、1.000 μg、2.000 μg、3.000 μg、4.000 μg 和5.000 μg,用分光光度计测定其吸光度值并绘制标准曲线。结果显示,在0 ~5.000 μg,标准曲线线性较好,相关系数在0.997 0 ~0.999 7。
2.5 方法精密度试验
分别称取适量粉碎均匀的粉皮1#样品、凉粉1#样品各6 份,进行方法精密度试验。由表2 试验结果可知,粉皮1#样品和凉粉1#样品中铝残留量的相对标准偏差分别为2.5%和1.9%,表明该方法精密度较好。

表2 方法精密度试验结果表
2.6 加标回收率试验
称取适量粉碎均匀的粉皮1#样品,加入铝标准溶液,使铝添加水平分别为25 mg·kg-1、50 mg·kg-1、100 mg·kg-1,进行加标回收率试验。如表3 所示,回收率结果为92.9%~107.2%,符合回收率一般要求。
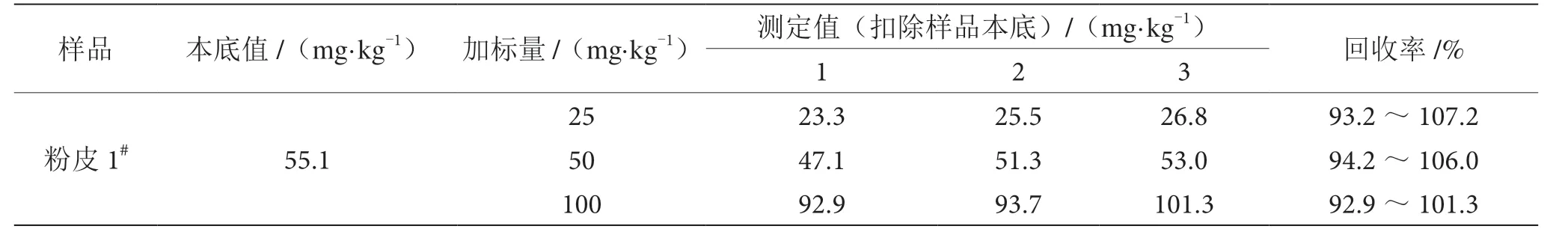
表3 加标回收率试验结果表
2.7 两种方法铝残留量测定结果的比较
随机取6 批次市售粉皮、凉粉、粉丝等淀粉制品,分别采用国标分光光度法和本方法进行样品中铝残留量的测定,结果见表4。国标方法所得样品中铝残留量的平行测定值相对偏差为3.6%~8.5%,水分含量扣除法所得样品中铝残留量的平行测定值相对偏差为1.7%~5.3%。结果表明,采用水分含量扣除法,样品平行测定结果之间的差异性更小。试验结果还显示,水分含量扣除法测定结果比国标方法测定结果略高。这可能是因为红外线水分测定仪是采用红外线加热样品,而红外线具有一定的穿透能力,加热速度快,能够使样品内外部受热均匀,有利于样品中的水分蒸发彻底,使得样品水分含量测定结果较准确;而电热恒温烘箱是采用热空气加热样品,可能使样品内外受热不均,且淀粉制品经加热后表面容易黏结起来,导致样品无法干燥完全。两种方法铝残留量测定值的相对偏差在1.3%~4.7%,在偏差允许范围之内,说明本文建立的铝残留量测定方法可行。综上所述,水分含量扣除法准确率较高,能够应用于淀粉制品中铝残留量的测定。
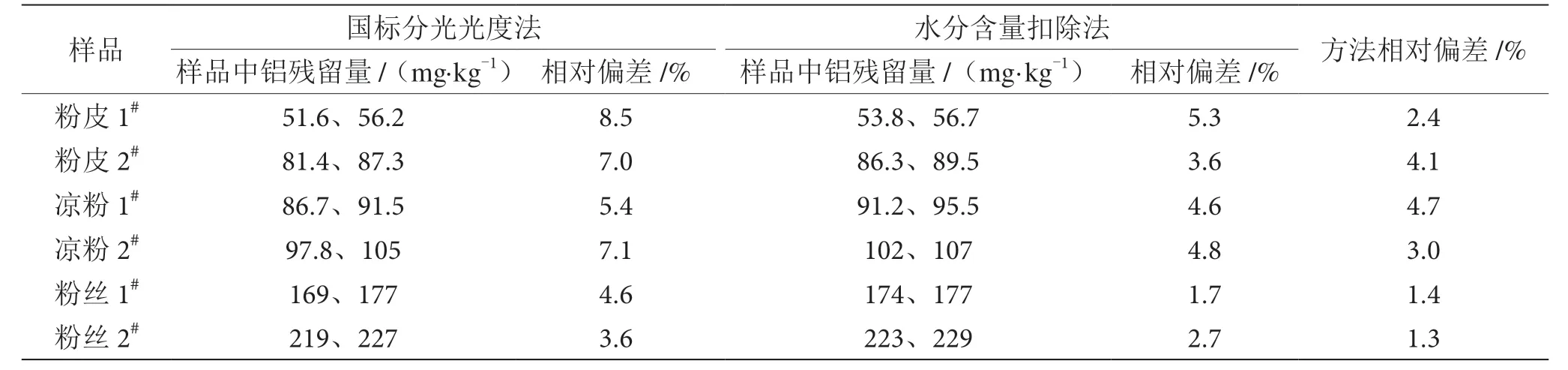
表4 两种方法得到的淀粉制品中铝残留量的测定结果表
依据《食品安全国家标准 食品添加剂使用标准》(GB 2760—2014)[10]和《国家卫生计生委关于批准β-半乳糖苷酶为食品添加剂新品种等的公告》(2015 年第1 号)[11],铝的残留量(干样品,以Al 计)在淀粉制品中的允许残留水平为:粉丝、粉条≤200 mg·kg-1。由此可知,随机检测的6 批次市售淀粉制品中有5 批次样品的铝残留量检测结果合格,粉丝2#样品的铝残留量检测结果超出了限量值,为不合格样品。
3 结论与讨论
本文采用红外线水分测定仪快速测定出淀粉制品的水分含量,扣除水分含量后得到样品干质量,采用优化的湿法消解条件消解样品,结合分光光度法成功测定了淀粉制品中的铝残留量。方法测定结果的相对标准偏差为1.9%~2.5%,加标回收率为92.9%~107.2%,与国标分光光度法测定结果的相对偏差为1.3%~4.7%,方法测定结果可靠。与国标方法相比,本方法不需要对样品进行4 h 烘干操作,有效降低了烘干处理后样品变化引起的试验偏差,并且缩短了检测时间,为淀粉制品中铝残留量的测定提供了一种可行的方法选择。
随机检测了6 批次市售淀粉制品的铝残留量,结果显示1 批次样品的铝残留量超标,表明市售淀粉制品中仍存在个别超限量添加含铝食品添加剂的情况。建议监管部门对铝超标问题加强监管,定期对相关从业人员进行食品安全宣传教育,增强从业人员的主体责任意识,降低食品安全风险,保障消费者食品安全。
