细菌溶解产物胶囊在慢性阻塞性肺疾病稳定期患者中的应用效果
2024-03-23吕艳红
吕艳红
(河南省直第三人民医院 郑州 450006)
慢性阻塞性肺疾病(COPD)属于常见呼吸道感染疾病,是以气道重塑、气流受阻为主要症状的肺部疾病,主要特点为持续性、阶段性病情加重[1]。细菌感染是诱发COPD 的重要因素,患者临床症状表现为气促、咳嗽、咳痰等,若未能及时进行有效的治疗,可加重气流受阻症状、使肺功能进一步恶化,严重者甚至会出现呼吸功能衰竭、多器官功能障碍以及心脏病等并发症,严重威胁患者生命安全[2~3]。目前,临床将COPD 划分为急性期与稳定期,对急性期的治疗方案与技术比较完善,但稳定期的治疗与预防手段尚未成熟,故需予以COPD 稳定期患者更积极的治疗以改善预后效果,减少急性复发[4]。细菌溶解产物胶囊是由多细菌提取的免疫刺激药,主要用于调节机体免疫应答特异性与非特异性,抑制细菌引发的感染,对临床稳定期COPD 的治疗具有较高价值[5]。本研究选择医院收治的82 例COPD 稳定期患者作为研究对象,旨在探究细菌溶解产物胶囊治疗稳定期COPD 的应用效果。现报道如下:
1 资料与方法
1.1 一般资料 选择2021年5月至2022年5月医院收治的82 例COPD 稳定期患者,按照随机数字表法分为观察组和对照组,每组41 例。观察组男18 例,女23 例;年龄52~83 岁,平均(66.93±6.28)岁;病程3~10年,平均(5.86±0.86)年;COPD 稳定期Ⅰ期18 例,Ⅱ期23 例。对照组男20 例,女21 例;年龄52~81 岁,平均(66.98±6.23)岁;病程2~10年,平均(5.72±0.92)年;COPD 稳定期Ⅰ期17 例,Ⅱ期24 例。两组一般资料对比,差异无统计学意义(P>0.05)。本研究经医院医学伦理委员会批准(伦理审批号:PJ2021-0426)。
1.2 入组标准 纳入标准:符合2013年修订《慢性阻塞性肺疾病诊治指南》[6]中COPD 稳定期的诊断标准;为急性加重病情入院,并经医院门诊或住院治疗后转为稳定期;治疗前未接受糖皮质激素药物治疗;支气管扩张检测结果提示为阴性;研究涉及资料齐全,患者及家属均签署知情同意书。排除标准:COPD 重症患者;重度支气管哮喘、支气管扩张患者;高血压、糖尿病患者;合并严重呼吸道感染、呼吸衰竭患者;合并严重心脑血管疾病患者;合并肝、肾等器官功能障碍患者;合并神经系统性疾病患者;对研究涉及药物过敏,抗胆碱药物不耐受患者。
1.3 治疗方法 对照组入院后行常规对症治疗。进行呼吸训练以防止呼吸道重度感染,研究前进行2周洗脱治疗,同时采用噻托溴铵吸入粉雾剂(国药准字H20090279)治疗,1 吸/次,1 次/d。观察组在上述治疗基础上联合细菌溶解产物胶囊(注册证号SJ20150041)治疗,1 粒/ 次,1 次/d,根据病情进展调整具体用药总量,两组均持续治疗2 个月。
1.4 观察指标 (1)临床效果。显效:患者治疗后肺功能有显著改善,临床各项症状消失;有效:患者治疗后肺功能有一定程度改善,临床症状有所缓解;无效:治疗后患者肺部功能无任何改善,临床症状未缓解,或病情加重。总有效率为显效率与有效率之和。(2)症状评分。运用调查问卷对治疗前、治疗2 个月后两组患者临床症状进行评分,0 分:无气促、咳嗽、咳痰,肺部湿啰音消失,恢复日常生活质量;1 分:气促、肺部湿啰音症状轻微,咳嗽咳痰次数约20 次/d,日常生活无明显影响;2 分:气促、肺部湿啰音症状较治疗前有所缓解,咳嗽咳痰次数约50 次/d,日常生活有一定影响;3 分:气促、咳嗽、咳痰症状加重,肺部湿啰音明显,对日常生活影响较大。治疗前及治疗2 个月后所得分数之和为最终得分,总分0~12分,得分越高提示症状越严重。(3)COPD 评分(CAT)。采用问卷调查对治疗前、治疗2 个月后两组患者病情轻重程度进行评估,内容包括8 个项目,每项评分0~5 分,总分0~40 分。其中,0~10 分表示COPD 存在轻微影响;11~20 分表示存在中等影响;21~30 分表示存在严重影响;31~40 分表示存在极度严重影响,得分越高提示病情越重。(4)呼吸困难指数(mMRC)[7]。采用mMRC 评价患者活动时呼吸困难程度,内容包括1 个条目,共计5 个选项,分值为0~4 分,0 分表示仅费力运动时呼吸困难;1 分表示快走或爬坡时呼吸困难;2 分表示平地行走时出现气短;3 分表示平地短时间行走需停下休息;4 分表示日常穿衣、脱衣等受严重影响,出现严重呼吸困难。分数越高提示呼吸困难程度越重。(5)6 min 步行距离(6MWT)[8]。测量两组治疗前、治疗后2 个月6 min 步行距离,选择一条长度距离为30 m 的无障碍直行走廊进行测试,安排患者尽可能地直行至走廊一端,并迅速折返,直行速度由患者自身情况决定,计算患者行走6 min 直线距离,测量3 次,每次测试间隔25 min,取平均值。(6)肺功能指标。采用FGY-200 型肺功能检测仪(合肥健桥医疗电子有限责任公司)检测两组患者用力肺活量(FVC)、第1 秒用力呼气容积(FEV1)、峰值呼气流速(PEF)。(7)免疫功能指标。采用流式细胞仪对两组治疗前后CD3+、CD4+、CD8+指标水平进行检测。(8)不良反应发生情况。包括头晕、口干、咽喉不适等
1.5 统计学方法 采用SPSS22.0 统计学软件处理数据,计量资料以(±s)表示,采用t检验;计数资料用%表示,采用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组临床疗效比较 观察组治疗总有效率高于对照组(P<0.05)。见表1。
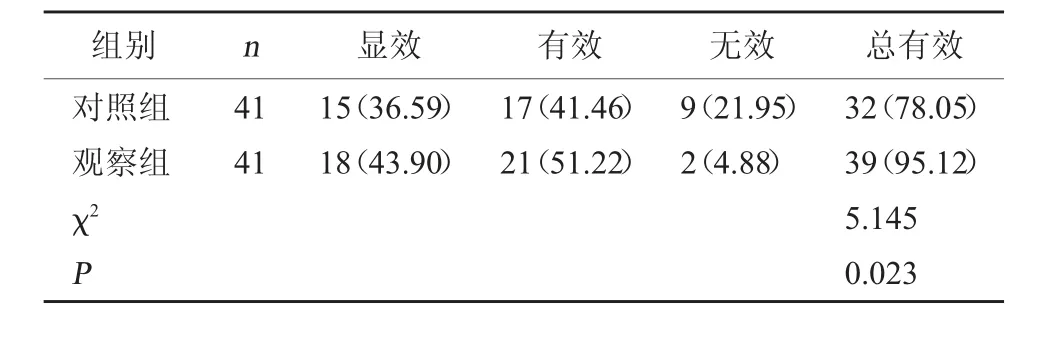
表1 两组临床疗效比较[例(%)]
2.2 两组症状评分、CAT 评分、mMRC、6MWT 比较治疗后,观察组症状评分、CAT 评分及mMRC 评分低于对照组,6MWT 高于对照组(P<0.05)。见表2。
表2 两组症状评分、CAT 评分、mMRC、6MWT 比较(±s)

表2 两组症状评分、CAT 评分、mMRC、6MWT 比较(±s)
6MWT(m)治疗前治疗后对照组观察组组别n症状评分(分)治疗前治疗后CAT 评分(分)治疗前治疗后mMRC 评分(分)治疗前治疗后41 41 t P 5.34±0.46 5.27±0.51 0.653 0.516 5.32±0.45 4.11±0.46 12.040 0.000 38.25±4.13 38.34±4.17 0.098 0.922 30.55±3.24 26.93±3.36 4.966 0.000 2.34±0.64 2.33±0.72 0.067 0.947 2.31±0.78 1.54±0.42 5.565 0.000 308.75±34.67 311.33±33.65 0.342 0.733 437.34±48.52 525.75±51.24 8.022 0.000
2.3 两组肺功能指标比较 治疗后,观察组FVC、 FEV1、PEF 均高于对照组(P<0.05)。见表3。
表3 两组肺功能指标比较(±s)
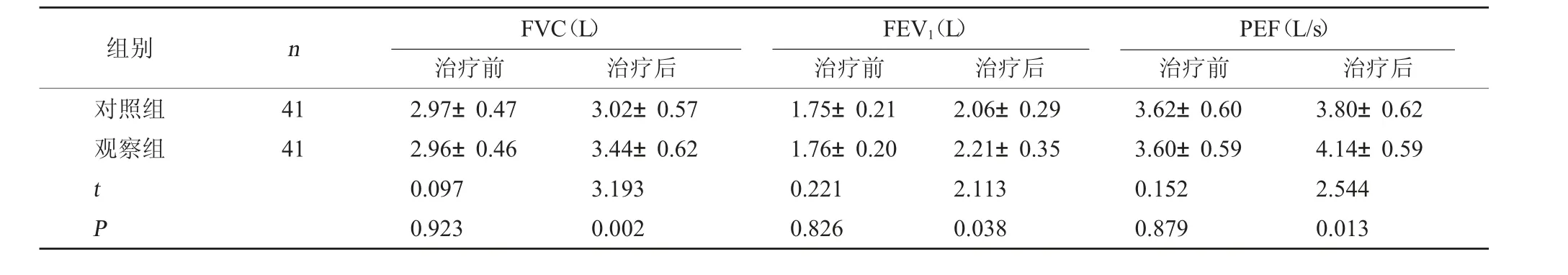
表3 两组肺功能指标比较(±s)
PEF(L/s)治疗前治疗后对照组观察组组别nFVC(L)治疗前治疗后FEV1(L)治疗前治疗后41 41 t P 2.97±0.47 2.96±0.46 0.097 0.923 3.02±0.57 3.44±0.62 3.193 0.002 1.75±0.21 1.76±0.20 0.221 0.826 2.06±0.29 2.21±0.35 2.113 0.038 3.62±0.60 3.60±0.59 0.152 0.879 3.80±0.62 4.14±0.59 2.544 0.013
2.4 两组免疫功能指标比较 治疗前,两组免疫功能指标比较,差异无统计学意义(P>0.05);治疗后,观察组CD3+、CD4+均高于对照组,CD8+低于对照组(P<0.05)。见表4。
表4 两组免疫功能指标比较(%,±s)
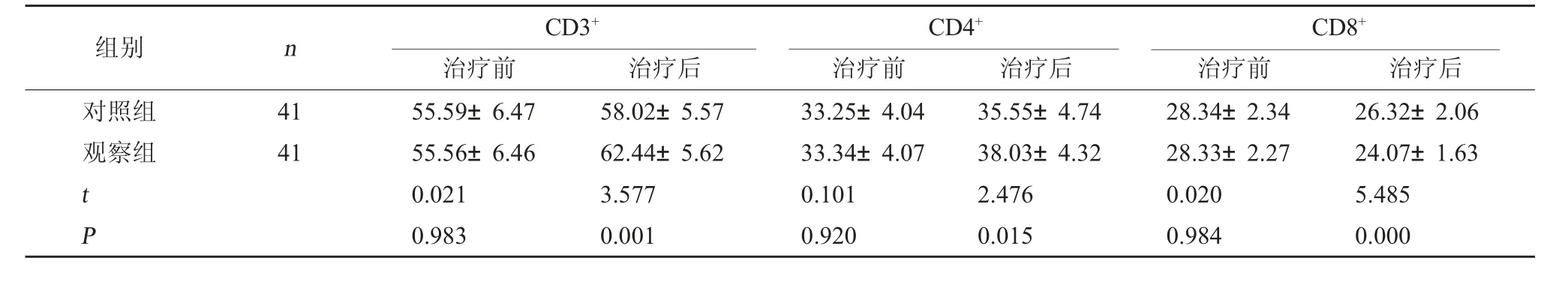
表4 两组免疫功能指标比较(%,±s)
CD8+治疗前治疗后对照组观察组组别nCD3+治疗前治疗后CD4+治疗前治疗后41 41 t P 55.59±6.47 55.56±6.46 0.021 0.983 58.02±5.57 62.44±5.62 3.577 0.001 33.25±4.04 33.34±4.07 0.101 0.920 35.55±4.74 38.03±4.32 2.476 0.015 28.34±2.34 28.33±2.27 0.020 0.984 26.32±2.06 24.07±1.63 5.485 0.000
2.5 两组不良反应比较 对照组出现头晕2 例,口干2 例,咽喉不适1 例,不良反应总发生率为12.20%(5/41)。观察组出现头晕1 例,口干1 例,不良反应总发生率为4.88%(2/41)。两组不良反应发生率对比,差异无统计学意义(χ2=0.625,P=0.429)。
3 讨论
COPD 大多由细菌感染引起,由于该病病程较长,且易反复发作,易造成肺功能及免疫功能水平下降,导致炎症介质被快速激活并释放,从而加重炎症反应,加剧气道痉挛、气流受阻、呼吸功能衰竭等临床症状,若未采取及时有效的治疗手段,患者易出现全身炎症反应,造成反复性呼吸道感染,严重者甚至导致死亡[9~11]。故治疗COPD 稳定期过程中有效抑制细菌感染,对改善临床症状及肺功能具有重要意义。
目前,临床对于COPD 稳定期多以对症治疗为主,如抗感染、营养补充等,同时采用噻托溴铵等药物配合[12]。该疗法主要用于缓解临床呼吸困难,延缓支气管扩张、气道重塑,通过清除气道内多余分泌物以改善气促、咳嗽、咳痰等症状,利于改善临床症状与肺功能指标[13]。细菌溶解产物胶囊是由多种菌类溶解而组成的免疫调节剂,在治疗过程中能够起到增强机体清除致病菌能力、提高免疫功能的作用,有效促进致病菌死亡并预防其再次入侵[14]。本研究结果显示,观察组治疗总有效率高于对照组,症状评分、CAT 评分、mMRC 评分均低于对照组,6MWT评分、FVC、FEV1、PEF 均高于对照组,CD3+、CD4+均高于对照组,CD8+低于对照组(P<0.05)。两组不良反应发生率对比,差异无统计学意义(P>0.05)。提示在常规治疗基础上加入细菌溶解产物胶囊治疗COPD 稳定期,利于提升治疗效果,改善患者各临床症状,促进肺功能、免疫功能各指标恢复,提升运动耐力,临床应用安全性较高。分析其原因在于,细菌溶解产物胶囊能够增加气道黏膜张力,调节呼吸道功能,通过抑制呼吸道内细菌感染,抑制已定植致病菌再次繁殖,以达改善肺功能的目的[15]。此外,相较于单独采用常规疗法而言,细菌溶解产物胶囊辅助治疗对于舒缓气促、咳嗽、咳痰等症状效果更加显著,能抑制肺部上皮组织细胞释放炎症介质,确保呼吸道畅通,从而减轻患者日常生活中气促、咳喘等困扰,有效缓解呼吸困难[16]。此外,细菌溶解产物胶囊还可作用于促进气道黏膜组织免疫球蛋白的分泌,通过提高唾液黏膜上皮趋化因子水平,发挥调节T 淋巴细胞循环等作用,有助于提升机体免疫应答机制,并通过降低恶化频率,降低不良反应发生率,可帮助患者稳定病情,缓解临床病症,改善预后效果显著[17]。
综上所述,细菌溶解产物胶囊在治疗COPD 稳定期中可获得理想效果,能够促进病情缓解,改善临床气促、咳嗽咳痰、呼吸困难等症状,利于缓解患者病情严重程度,改善肺部功能指标,且安全性较高,值得推广应用。
