电感耦合等离子体质谱法测定甜叶菊中25种元素
2024-03-19余秀萍蔡霞李变变胡丹
余秀萍,蔡霞,李变变,胡丹
(1.安徽省宿州市食品药品检验检测中心,安徽宿州 234000; 2.泰州市食品检验院,江苏泰州 225300)
甜叶菊为菊科甜叶菊属多年生草本植物,又名甜菊、蜜菊等[1]。叶片富含甜菊糖苷,因其低热值和高甜度而广为人知,其甜度为蔗糖的300倍,作为一种天然的甜味剂,被广泛应用于食品、饮料、医药等行业[2-3]。作为中草药的甜叶菊,还被用作预防龋齿、促进新陈代谢、降血压、抗癌的药用原料,用来治疗食物过敏、咳嗽、流感等[4-5]。近年来甜叶菊被广泛种植,国内主要集中在安徽、山东、浙江、河南、甘肃和新疆等地[6-7]。
在甜叶菊栽培和生长过程中,各种元素会通过土壤、水、大气等进入药材中,除了人体必需的微量元素外还有很多对人体有害的重金属,过量摄入重金属(如Cd、Pb、Hg、Cu 等)会对人体肝脏、肾脏、肺等造成危害,引发各类病变甚至癌症[8-10],因此,对甜叶菊进行元素分析是十分必要的。目前对甜叶菊的研究主要集中在种植和其主要成分的分离提取、合成应用等方面,对其元素方面的研究少有报道。《中华人民共和国药典》2020版四部制定了中药中元素测定指导原则,明确了首选电感耦合等离子体质谱(ⅠCP-MS)法进行多元素同时测定[11]。ⅠCP-MS 法能同时测定多种元素,具有分析速度快、检测限低、灵敏度高、线性范围宽的优点,适用于微量、痕量元素分析[12-13]。
笔者采用微波消解-电感耦合等离子质谱法同时测定甜叶菊中25种元素的含量,从元素方面对甜叶菊进行研究,考察甜叶菊中元素的特征,既能为甜叶菊质量研究和控制工作提供技术支持,又能为后期更好地对甜叶菊的药用价值进行综合利用、资源开发提供参考。
1 实验部分
1.1 主要仪器与试剂
电感耦合等离子体质谱仪:iCAP Q 型,美国赛默飞世尔科技公司。
微波消解仪:MARS6型,美国CEM公司。
电子天平:BSA124S 型,感量为0.1 mg,德国赛多利斯仪器有限公司。
25 种元素混合标准溶液:含有Al、As、B、Ba、Be、Ca、Cd、Co、Cr、Cu、Fe、Hg、K、Mg、Mn、Mo、Na、Ni、Pb、Sb、Se、Ti、Tl、V、Zn 等25 种元素,各元素质量浓度均为100 μg/mL,国家有色金属及电子材料分析测试中心。
混合内标溶液:含有Bi、Ca、Ⅰn、Li、SC、Tb和Y,各元素质量浓度均为100 μg/mL,国家有色金属及电子材料分析测试中心。
混合标准调谐液:编号为1323770,含有Ba、Bi、Ce、Co、Ⅰn、Li、U 元素,各元素质量浓度均为1.0 μg/L,美国赛默飞世尔科技公司。
硝酸、过氧化氢:均为优级纯,国药集团化学试剂有限公司。
高纯氩气、高纯氦气:纯度(体积分数)均为99.999%,宿州雨阳气体有限责任公司。
甜叶菊样品:共12 批次,收集场所涉及药材市场和种植基地,所有样品均经安徽中医药大学刘守金和杨青山教授鉴定为菊科甜叶菊属甜叶菊的干燥叶子。
实验所用玻璃仪器均在20%硝酸溶液中浸泡12 h 后用蒸馏水冲洗干净,于恒温干燥箱烘干后冷却至室温备用。
实验用水为屈臣氏蒸馏水。
1.2 系列混合标准工作溶液的制备
取25 种元素混合标准溶液,精密移取适量,用2%硝酸作为稀释剂,加入适量混合内标溶液,制备得到各元素质量浓度均分别为0.5、1.0、5.0、10.0、50.0、100.0、500.0 ng/mL 和1.0、5.0、10.0 μg/mL,其中内标元素质量浓度均为1 μg/mL的系列混合标准工作溶液。
1.3 仪器工作条件
射频功率:1 500 W;等离子体气流量:15 L/min;载气流量:0.8 L/min;采样深度:8~10 mm;辅助气流量:0.4 L/min;雾化室温度:2.0 ℃;测量模式:碰撞池模式(KED);碰撞气体积流量:4.0 mL/min;泵转速:40 r/min。
1.4 样品处理
精密称取甜叶菊样品粉末约0.5 g (过3#筛),置于消解罐中,加入5 mL 硝酸、3 mL 过氧化氢,充分进行混合,摇匀,放置12 h。预消解完成后,放入微波消解仪中消解,消解程序见表1。冷却后取出,缓慢打开罐盖,用少量水冲洗内盖,将消解罐放在赶酸器中,缓慢加热至红棕色蒸气挥尽,并继续浓缩至2~3 mL,冷却后转移至50 mL 容量瓶中,加入0.5 mL混合内标溶液,用体积分数为2%的硝酸溶液定容,混匀备用,作为样品溶液。同法制得试剂空白溶液。

表1 微波消解仪工作参数Tab.1 Operating parameters of microwave digestion instrument
1.5 样品测定
按照1.3仪器工作条件编辑测定程序,依次测定空白标准溶液、标准溶液、空白样品溶液与样品溶液,采用标准曲线法进行定量。
2 结果与讨论
2.1 样品处理方法的选择
分别考察了湿法消解、干灰化法和微波消解3种消解方式对甜叶菊样品加标回收率的影响,确定样品的最佳处理方式,扣除本底值后,回收率结果如图1所示。由图1可知,微波消解法回收率高于湿法消解和干灰化法。由于湿法消解温度不易控制,对结果影响较大;干灰化法消解会由于马弗炉温度高容易造成易挥发元素的损失,而且由于灰化不完全或者溶解不完全都会导致测定结果和回收率降低,因此选取微波消解法作为样品的消解方式。
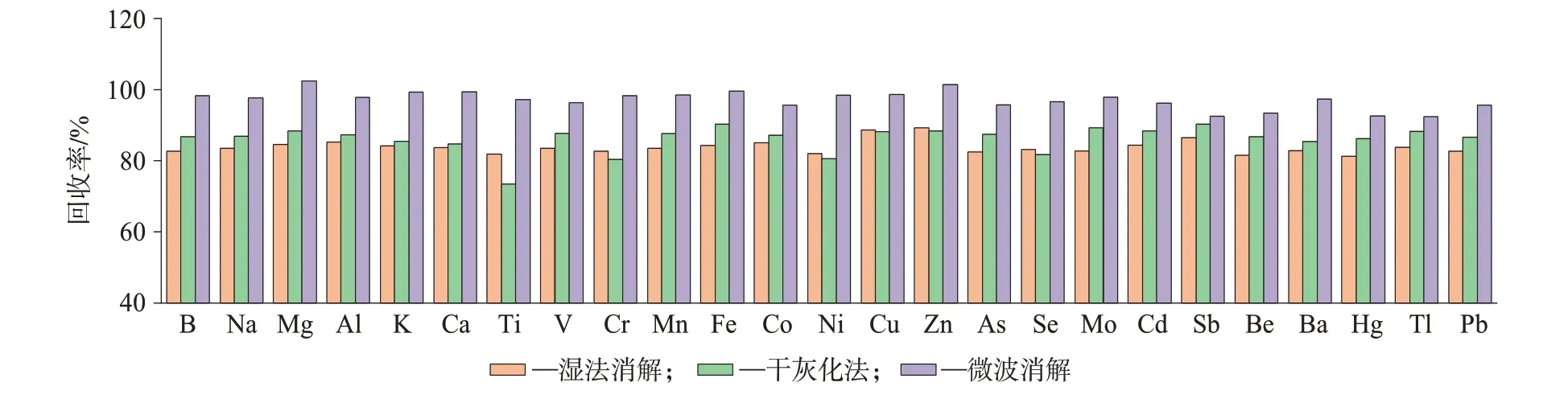
图1 不同消解方式对应的甜叶菊样品中25种元素回收率Fig.1 Recovery of 25 elements in the Stevia rebaudiana Bertoni samples corresponding to the different digestion methods
2.2 取样量与消解溶液的选择
分别设定取样质量为0.3、0.5、0.8 g 进行试验,结果表明,当取样质量为0.3 g 时,平行试验样品重复性较差;当取样质量为0.8 g时,硝酸需要量较大,加入10 mL硝酸样品也不能消解完全。由于仪器自身技术指标限制,消解罐内溶液总体积应不超过10 mL,因此需加入过氧化氢以增强氧化性,减少硝酸使用量。通过试验确定样品取样质量为0.5 g,消解体系为5 mL 硝酸和3 mL 过氧化氢,这种组合消解更完全,溶液更澄清,更有利于药材质量的控制。
2.3 赶酸温度的选择
由于As 和Hg 元素为易挥发元素,为避免赶酸温度过高导致损失,试验过程中要对赶酸温度进行控制[14-15]。分别设定赶酸温度为100、120、130、150、160 ℃进行试验,各种元素回收率如图2 所示。结果表明,赶酸温度较低时,赶酸时间比较长,如赶酸温度设定为100 ℃时,浓缩至实验要求的2~3 mL,至少需要7 h;而赶酸温度为150 ℃时,Hg元素测定结果差别较大,不太稳定,回收率明显偏低;赶酸温度为160 ℃时,As元素回收率开始变低。赶酸温度不超过130 ℃时,加热至无棕黄色烟雾挥出时,As和Hg元素的损失较小,回收率比较理想。为了节省赶酸时间,赶酸温度宜控制在120~130 ℃。
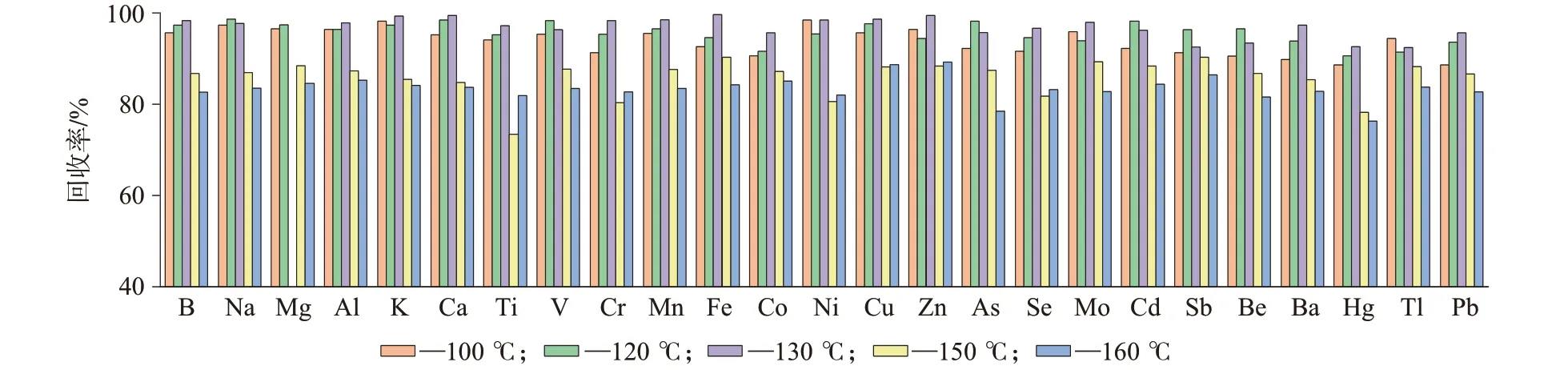
图2 不同赶酸温度条件下的元素回收率Fig.2 Recovery of elements at different deacidification temperatures
2.4 进样酸度条件的优化
仪器进样时的酸度环境对测定结果也有一定影响,分别用体积分数为0%(纯水)、1%、2%、3%、5%的硝酸溶液为稀释剂配制混合标准溶液(各元素质量浓度均为50.0 ng/mL),将标准溶液依次在仪器最佳条件下进行测定,计算各元素的回收率,结果见图3。由图3可见,当硝酸溶液体积分数大于2%时,标准回收率趋于最大且稳定,同时为了避免酸度过大对仪器造成的损坏和浪费,满足实验要求和节约成本,选择在2%的硝酸体系中进行测定。

图3 不同酸进样体积对应的各元素回收率Fig.3 Recovery of each element corresponding to the different acid injection volumes
2.5 干扰消除
ⅠCP-MS 分析法测定过程中会存在基体干扰、记忆效应干扰、物理干扰、质谱干扰等[16-17]。基体干扰主要是仪器的空间电荷效应和在采样锥与截取锥之间的物理变化导致的,可通过内标校正、控制样品盐分、延长样品冲洗时间、清洗锥体和稀释样品消除。记忆效应是由于上一个样品在进样系统内壁上过量分析物挥发引起的,可采用2%的硝酸溶液冲洗加以消除。物理干扰可通过多次清洗雾化室、进样锥及进样管路消除,同时增加测样时管路冲洗时间。质谱干扰可通过选择合适的同位素离子及仪器校正消除,如测定镉时,选择111Cd和114Cd进行试验,发现111Cd 干扰少,测定值更加准确,最终确定111Cd为镉测定同位素,同时加入内标校正仪器漂移及碰撞反应池技术(KED)消除干扰。各目标元素测定同位素及内标溶液的选择见表2。
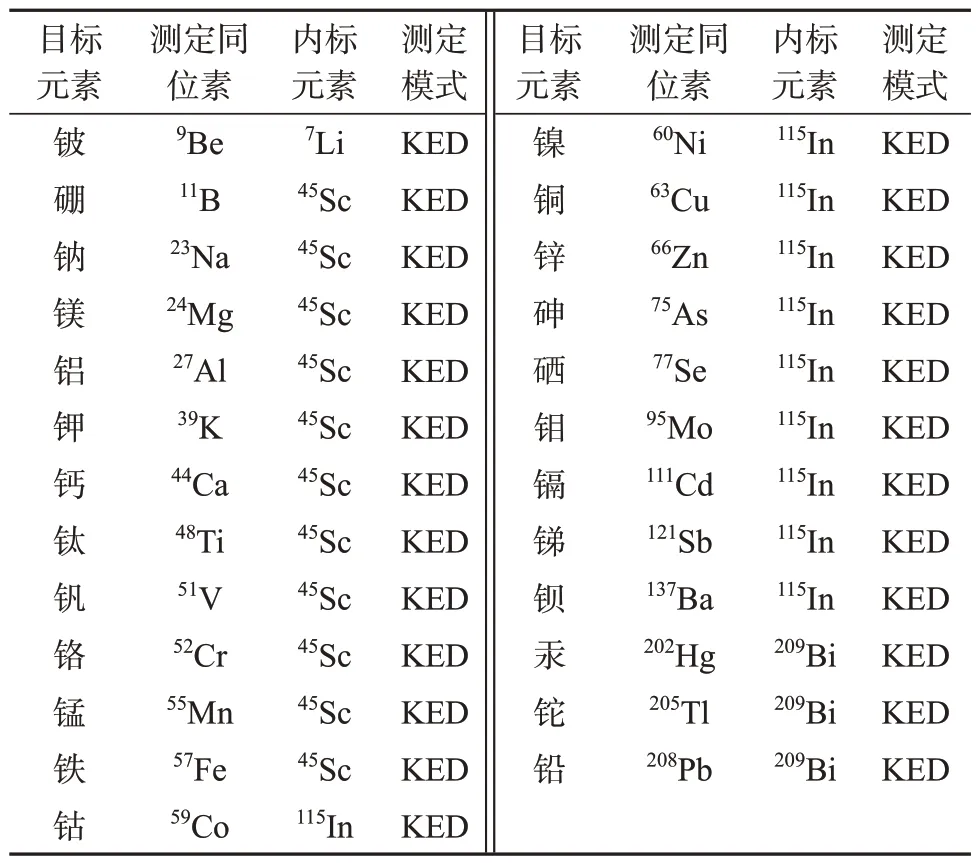
表2 各元素同位素及内标元素Tab.2 Each element isotope and internal standard element
2.6 标准曲线与方法检出限
将系列标准工作溶液注入电感耦合等离子体质谱仪中,按实验方法测定目标元素的强度信号值,以目标元素的质量浓度为横坐标、强度信号值为纵坐标,绘制标准曲线,并计算得到线性方程和相关系数(r)。
测定11次试剂空白溶液,计算响应值的标准偏差,以3倍的标准偏差计算方法检出限[18]。
25种元素线性范围、线性方程、相关系数、检出限见表3。结果表明,25 种元素的标准溶液在测定范围内均具有良好的线性,相关系数均在0.999 以上,表明线性关系良好,25 种元素的方法检出限为0.000 1~0.5 mg/kg。

表3 各元素的线性范围、线性方程、相关系数及检出限Tab.3 Linear range,linear equation,correlation coefficient and detection limit of each element
2.7 样品加标回收试验
由于各元素含量间差异较大,回收率采用分组测定,Hg和Tl未检出,以检出限为参考,其余元素按含量大小和标准曲线范围分为8组(Be、Sb为一组,加入5 ng;Co、As、Se为一组,加入50 ng;V、Cd、Pb为一组,加入200 ng;Na、Cr、Ni、Cu、Mo 为一组,加入2.0 μg;B、Zn、Ba、Ti为一组,加入5.0 μg;Al、Mn、Fe为一组,加入50.0 μg;Mg为一组,加入500 μg;K、Ca为一组,加入1 500 μg),分别试验并计算回收率。取已知含量的甜叶菊样品6份,每份约0.25 g,精密称定,分别加入和样品中各元素含量相近的标准元素溶液,按该方法进样测定,计算各元素的回收率,结果见表4。由表4可知,25种元素的平均样品加标回收率为92.4%~102.4%,相对标准偏差为1.09%~4.11%,均小于5%,表明该方法准确度和精密度均较高。
3 结语
利用电感耦合等离子体质谱法对甜叶菊中25种元素进行定量分析,该方法精密度和准确度良好,线性范围宽,灵敏度高,可为后期更好地对甜叶菊的药用价值进行综合利用、资源开发提供参考。
