沙格列汀联合利拉鲁肽对二甲双胍疗效不佳的肥胖2 型糖尿病患者脂糖代谢、胰岛素功能的影响*
2024-03-18王素侠孙雪涛吴久灵
王素侠,孙雪涛,吴久灵,谭 珺
(1. 安徽省利辛县人民医院,安徽 亳州 236700; 2. 皖西卫生职业学院附属医院,安徽 六安 237008)
2 型糖尿病(T2DM)为三大基础疾病之一[1],我国成人T2DM 的患病率高达10.4%,肥胖T2DM 患者占糖尿病患者的90%以上[2],严重威胁患者的生活质量。二甲双胍是肥胖T2DM 患者的首选药物[3],但单用疗效不佳。沙格列汀是一种二肽基肽酶- 4(DPP - 4)抑制剂[4],通过对胰岛α 细胞和胰岛β 细胞进行双向调节而改善血糖水平。利拉鲁肽是一种胰高血糖素样肽- 1(GLP- 1)长效类似物[5],用于治疗肥胖T2DM,改善血糖水平,长效保护胰岛β 细胞。本研究中探讨了沙格列汀联合利拉鲁肽对二甲双胍疗效不佳的肥胖T2DM 患者的脂糖代谢、胰岛素功能的影响。现报道如下。
1 资料与方法
1.1 一般资料
纳入标准:符合T2DM 诊断标准[3];体质量指数(BMI)不低于25.0 kg/m2;单纯服用二甲双胍(最大耐受剂量)[6]时间超过12 周,血糖控制不佳、糖化血红蛋白(HbA1C)超过7%;认知能力正常,社交无障碍。本研究方案经医院医学伦理委员会批准(批件号为20081225-1),患者签署知情同意书。
排除标准:1 型或其他类型糖尿病;备孕或妊娠期;近期服用过其他影响脂糖代谢的药物;心、肝、肾等重要器官的功能严重受损;对本研究中所用药物过敏。
病例选择与分组:选取安徽省利辛县人民医院内分泌科2019年1月至2022年1月收治的对二甲双胍疗效不佳的肥胖T2DM 患者100例,将2019年1月至2020年6月行沙格列汀联合利拉鲁肽治疗的患者作为联合组,将2020年7月至2022年1月行单纯沙格列汀治疗的患者作为对照组,各50 例。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。详见表1。

表1 两组患者一般资料比较(n=50)Tab.1 Comparison of the patients' general data between the two groups(n = 50)
1.2 方法
两组患者均予健康饮食、适量运动、T2DM 相关健康知识宣教等基础治疗。对照组患者晨起口服沙格列汀片(江苏豪森药业集团有限公司,国药准字H20203537,规格为每片5 mg),每天1 次,每次1 片;联合组患者加用利拉鲁肽注射液(Novo Nordisk A/ S,国药准字J20160005,规格为每支3 mL∶18 mg <预填充注射笔>)强化降糖治疗,每次0.6 mg,每日1 次。两组患者均治疗6个月。
1.3 观察指标与疗效判定标准
观察指标:1)血糖指标。采用酶联免疫吸附试验(ELISA)测定患者治疗前后的空腹血糖(FBG)、餐后2 h血糖(2 hPG)和HbA1c,检测仪器为Varioskan 型酶标仪(美国Thermo 公司)。2)血脂指标。采用7600 型日立全自动生化分析仪测定患者治疗前后的甘油三酯(TG)、总胆固醇(TC)、低密度脂蛋白胆固醇(LDL - C)、高密度脂蛋白胆固醇(HDL - C)水平。3)胰岛素功能[7]。采用ELISA 测定患者治疗前后的空腹胰岛素(FINS),并计算胰岛β细胞功能指数(HOMA-β)和胰岛素抵抗指数(HOMA-IR)。其中,HOMA-β=20×FINS/(FBG-3.5),HOMA - IR = FBG × FINS/ 22.5。4)BMI。记录患者治疗前后的BMI。5)脂肪分布。测定患者治疗前后的腹部总脂肪、皮下脂肪和内脏脂肪体积。6)不良反应。记录治疗期间患者的胃肠道反应、血糖水平降低等发生情况。
疗效判定[8]:治疗后,FBG ≤6.39 mmol / L,2 hPG ≤7.80 mmol/ L,为显著有效;6.39 mmol/ L <FBG≤7.80mmol/L,7.8mmol/L<2hPG≤11.10mmol/L,为有效;FBG 与2 hPG 均无改善,为无效。总有效=显著有效+有效。
1.4 统计学处理
采用SPSS 21统计学软件分析。计量资料以±s表示,行t检验;计数资料以率(%)表示,行χ2检验。P<0.05为差异有统计学意义。
2 结果
结果见表2至表7。

表2 两组患者临床疗效比较[例(%),n=50]Tab.2 Comparison of clinical efficacy between the two groups[case(%),n = 50]
表3 两组患者血糖比较( ± s,n=50)Tab.3 Comparison of blood glucose levels between the two groups(X ± s,n = 50)
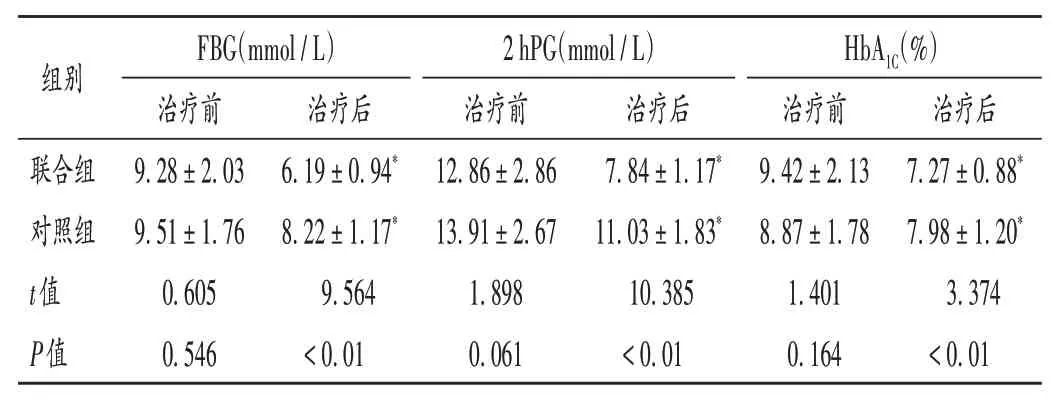
表3 两组患者血糖比较( ± s,n=50)Tab.3 Comparison of blood glucose levels between the two groups(X ± s,n = 50)
注:与本组治疗前比较,*P <0.05。表4至表6同。Note:Compared with those before treatment,*P < 0.05 (for Tab.3 - 6).
组别联合组对照组t值P值FBG(mmol/L)治疗前9.28±2.03 9.51±1.76 0.605 0.546治疗后6.19±0.94*8.22±1.17*9.564<0.01 2 hPG(mmol/L)治疗前12.86±2.86 13.91±2.67 1.898 0.061治疗后7.84±1.17*11.03±1.83*10.385<0.01 HbA1C(%)治疗前9.42±2.13 8.87±1.78 1.401 0.164治疗后7.27±0.88*7.98±1.20*3.374<0.01
表4 两组患者血脂水平比较( ± s,mmol/L,n=50)Tab.4 Comparison of blood lipid levels between the two groups(X ± s,mmol / L,n = 50)

表4 两组患者血脂水平比较( ± s,mmol/L,n=50)Tab.4 Comparison of blood lipid levels between the two groups(X ± s,mmol / L,n = 50)
组别联合组对照组t值P值TG治疗前3.88±1.13 3.74±1.43 0.543 0.588治疗后2.29±0.78*2.55±1.82*0.929 0.355 TC治疗前5.81±0.94 5.74±1.12 0.339 0.736治疗后5.35±0.85*5.52±0.98 0.927 0.356 LDL-C治疗前3.98±0.87 3.89±1.01 0.477 0.634治疗后3.69±0.52*3.63±1.32 0.299 0.766 HDL-C治疗前0.81±0.07 0.83±0.05 1.644 0.103治疗后0.90±0.08*0.91±0.11*0.520 0.604
表5 两组患者胰岛素功能和BMI比较( ± s,n=50)Tab.5 Comparison of insulin function and BMI between the two groups(X ± s,n = 50)
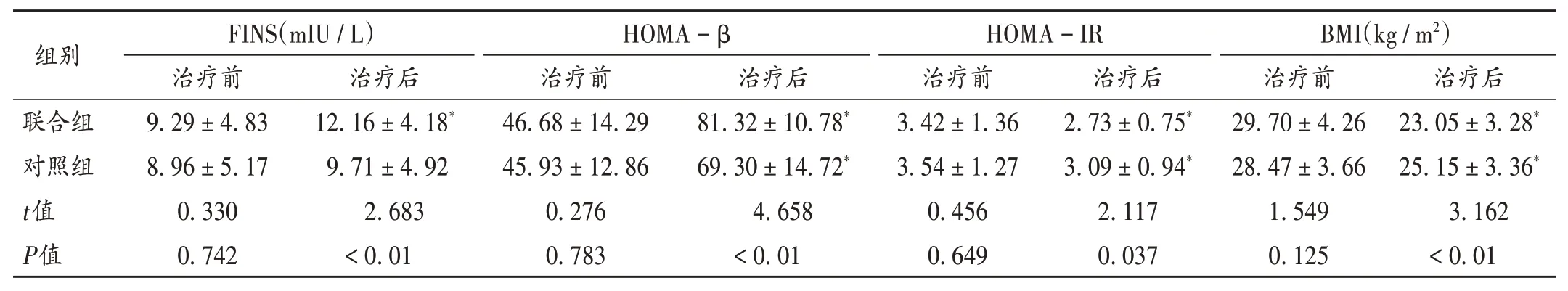
表5 两组患者胰岛素功能和BMI比较( ± s,n=50)Tab.5 Comparison of insulin function and BMI between the two groups(X ± s,n = 50)
组别联合组对照组t值P值FINS(mIU/L)治疗前9.29±4.83 8.96±5.17 0.330 0.742治疗后12.16±4.18*9.71±4.92 2.683<0.01 HOMA-β治疗前46.68±14.29 45.93±12.86 0.276 0.783治疗后81.32±10.78*69.30±14.72*4.658<0.01 HOMA-IR治疗前3.42±1.36 3.54±1.27 0.456 0.649治疗后2.73±0.75*3.09±0.94*2.117 0.037 BMI(kg/m2)治疗前29.70±4.26 28.47±3.66 1.549 0.125治疗后23.05±3.28*25.15±3.36*3.162<0.01
表6 两组患者脂肪分布比较( ± s,cm3,n=50)Tab.6 Comparison of fat distribution between the two groups(X ± s,cm3,n = 50)

表6 两组患者脂肪分布比较( ± s,cm3,n=50)Tab.6 Comparison of fat distribution between the two groups(X ± s,cm3,n = 50)
组别联合组对照组t值P值腹部总脂肪体积治疗前7 940±2 159 7 819±2 364 0.267 0.790治疗后4 530±1 765*5 297±1 478*2.356 0.021皮下脂肪体积治疗前3 919±1 344 3 825±1 298 0.356 0.723治疗后3 010±1 254*3 203±1 124*0.810 0.420内脏脂肪体积治疗前4 358±1 305 4 471±1 496 0.403 0.688治疗后3 510±1 037*3 819±1 142*1.416 0.160

表7 两组患者不良反应发生情况比较[例(%),n=50]Tab.7 Comparison of the incidence of adverse reactions between the two groups[case(%),n = 50]
3 讨论
肥胖T2DM 多由于生活方式不健康[9-10],如过量摄入高热量及不合理的饮食导致体质量增加,以及体育运动缺乏和胰岛素抵抗[11-12]的进行性加重会导致肥胖T2DM 的发生。T2DM 患者的治疗中,除控制血糖外,还需改善胰岛素抵抗,加用二甲双胍可改善胰岛素抵抗,达到降糖作用[13]。
本研究中,两组患者治疗后的血糖指标均显著降低,且联合组显著低于对照组。可见,沙格列汀联合利拉鲁肽的控糖能力更佳。沙格列汀为吡咯烷类衍生物,通过改善胰岛素功能发挥控糖作用,生物学活性较高,可高效、长效、稳定地发挥作用,是临床治疗肥胖T2DM的二线药物。利拉鲁肽是人工合成的GLP-1 长效类似物,与GLP-1 受体结合后能促进胰岛素分泌和抑制胰高血糖素分泌,稳定血糖。沙格列汀联用利拉鲁肽无明显拮抗作用,在体内的最终效应决定于内源性GLP-1水平。但T2DM 患者自身GLP-1水平低,沙格列汀可阻断DPP - 4 酶的作用,可避免患者体内的活性GLP-1向无活性转变[14],延长GLP-1的作用,其效应较低。沙格列汀联用利拉鲁肽能通过补充外源性GLP-1 而升高沙格列汀体内浓度,提高GLP - 1 的生物学效用,增加机体GLP-1含量[15]。
胰岛素抵抗是目前糖尿病治疗的重要研究目标[16-17]。本研究中两组患者治疗后的HOMA - β 均显著升高,HOMA-IR 均显著降低,表明均使患者机体对胰岛素的敏感性增强,拮抗胰岛素抵抗。本研究中联合组总有效率显著高于对照组,且对照组FINS 变化不显著。提示沙格列汀联用利拉鲁肽对胰岛素抵抗的作用更佳,与文献[18 - 20]的研究结果一致。分析原因,可能为利拉鲁肽对胰岛β 细胞分泌胰岛素有保护和修复作用,能有效改善胰岛功能。
联合组患者BMI 和腹部总脂肪体积均显著优于对照组。合并肥胖的T2DM 患者常伴腹型肥胖,其体内脂肪堆积造成的胰岛素抵抗是T2DM 发病率升高的重要因素之一[21]。利拉鲁肽可通过增加下丘脑饱食信号水平,延缓胃排空、肠胃蠕动、增加饱腹感等方式抑制食欲,减少食物摄取,改善肥胖T2DM 患者的病理生理缺陷和脂肪分布,减轻体质量[22-23]。治疗后,联合组血脂改善作用显著,但与对照组无显著差异。故认为联合用药的调血脂作用显著,但较单用沙格列汀无明显优势。分析原因,可能与本研究中样本量少,样本中心研究单一有关,后续将扩充样本量,进行多中心研究,并延长预后观察时间,获取更充分的研究数据,以完成更确切的研究分析。两组不良反应发生率相当,提示安全性良好。
综上所述,沙格列汀联合利拉鲁肽强化降糖治疗对二甲双胍疗效不佳的肥胖T2DM 患者的降糖效果良好,可促进患者的体质量下降,改善脂肪分布,改善血脂代谢的作用与沙格列汀相当,且安全性良好。
