美国“专利舞蹈”特性对我国构建生物仿制药诉前专利纠纷解决机制的启示*
2024-03-18王曦鹏
王曦鹏,张 岩,黄 哲
(1. 沈阳药科大学工商管理学院,辽宁 沈阳 110016; 2. 北京第二外国语学院校医院,北京 100011;3. 首都医科大学附属北京友谊医院,北京 100050)
欧洲的生物仿制药领先美国数年,由于专利框架的不同,欧洲专利终止较早,而美国的一些原研公司在美国制造了更多的专利壁垒[1]。2010年,美国颁布的《生物制品价格竞争和创新法案》(BPCIA)规定,生物仿制药申请人(BA)和参考产品赞助商(RPS)之间精心设计的信息交换流程被称为“专利舞蹈”,旨在通过有序和迅速的方式解决潜在的专利纠纷[2]。我国于2021年颁布《药品专利纠纷早期解决机制实施办法》(简称《实施办法》),其目的与美国“专利舞蹈”制度相同。但生物仿制药不是仿制药,仿制药被定义为同参考产品具有相同活性成分的等价物,活性成分可被准确复制,是合成药物的替代品[3]。生物仿制药被欧洲药物管理局定义为含有参考产品中发现的活性药物成分的生物医疗产品,美国食品和药物管理局(FDA)使用后续生物制剂表示生物仿制药。2 个机构都确定生物仿制药同参考产品相比具有不同的作用[4],故生物仿制药诉前专利纠纷解决机制应不同于仿制药法案。《实施办法》借鉴美国仿制药Hatch-Waxman 法案[5]的专利声明等制度构建我国生物仿制药诉前专利纠纷解决办法,可能会导致《实施办法》因高效性、公平性不足而无法达到快速提高生物仿制药市场竞争的目的,但其强制性为我国生物仿制药参与市场竞争起到了引导作用。随着生物仿制药行业的发展,我国可借鉴“专利舞蹈”构建生物仿制药诉前专利纠纷解决机制。本研究中分析了美国“专利舞蹈”的特性,并与我国《实施办法》进行对比分析,总结两者的异同,取长补短,为我国构建生物仿制药诉前专利纠纷解决机制提供建议。现报道如下。
1 美国“专利舞蹈”的法律基础
美国“专利舞蹈”是BPCIA 提供的一个框架,包括BA 和RPS 交换《简略生物制品许可申请》(aBLA)中披露的有关步骤和时间表的机密信息[6]。虽然BPCIA 中“专利舞蹈”的生物仿制药简略审批途径类似于仿制药法案Hatch - Waxman,且有些条款包含仿制药法案的概念,但两者还是存在差异。如“专利舞蹈”中无第四类声明,不需证明RPS 专利无效、不可执行或不侵权;“专利舞蹈”条款中的生物仿制药专利由RPS 和BA 相互交流而识别;“专利舞蹈”涉及的大部分专利诉讼是生物仿制药制造工艺专利,且未要求BA 在提交aBLA 时通知RPS。“专利舞蹈”是BA和RPS间的诉讼前交流,以确定并尽可能地缩小在第一阶段诉讼中所提供诉讼的专利清单。只有BA 才能决定是否“跳舞”,RPS 必须等待BA 是否启动“专利舞蹈”,RPS 此阶段不允许上诉[7]。如果BA 触发了“专利舞蹈”,在BA 提供180 d 的商业营销通知前,任何一方均不得对未包含在第一阶段诉讼中的专利提起宣告性判决诉讼[8],RPS 可指控侵权“专利舞蹈”中已确定的部分专利。在RPS 收到BA 的商业营销通知后,在第二阶段诉讼中RPS 可主张第一阶段诉讼未主张的任何剩余专利。
2 美国“专利舞蹈”的特性
2.1 高效性
高效性是“专利舞蹈”的关键,美国国会希望为生物仿制药的批准提供一个高效的过程,同时还可保持BA 和RPS 间微妙的平衡关系[9]。“专利舞蹈”为BA 和RPS同时提供交换与识别专利的沟通平台,将司法与行政中的生物仿制药专利纠纷问题提前到生物仿制药注册审评过程中,并在FDA的审评中促进双方达成和解。
aBLA 鼓励BA 提交申请:在“专利舞蹈”途径下,BA 可根据RPS 向FDA 提供的信息向FDA 提交aBLA。BA 只需证明其产品与参考产品高度相似,在安全性、纯度和有效性方面与参考产品无临床意义的差异,尽管临床无活性成分存在微小差异[10]。aBLA 为BA 在临床试验中节省了大量时间与金钱,旨在鼓励BA 提交aBLA。
“人为侵权”迫使RPS 缩小专利范围或达成和解:BA 在RPS 的专利期内推出生物仿制药,可能面对诉讼风险或诉前清除RPS 专利权。一旦BA 选择诉前清除RPS 专利权,FDA 接受BA 的aBLA,BA 就可启动“专利舞蹈”,此时提交的aBLA 更像是一份非专利小分子药物的上市申请,是一种“人为侵权”行为[11]。即BA 在RPS 专利保护期内向FDA 提交新药注册申请或仿制药注册申请的行为[12],BA 会迫使RPS 根据《美国法典》第42 卷第262(l)(3)(A)节列出可合理主张侵权的专利清单(3Alist),将专利纠纷提前到药品注册审批过程中,促使双方就有限的专利进行协商。“专利舞蹈”可确保与专利相关的诉讼在生物仿制药推出前得到解决,为BA 和RPS 提供确定性[13],迫使RPS 在第一阶段诉讼前缩小专利范围或达成和解。阿达木单抗(商品名修美乐)的RPS 艾伯维公司与BA 间的专利纠纷见表1。

表1 阿达木单抗(商品名修美乐)的RPS与BA间的专利纠纷Tab.1 Patent dispute between RPS of Adalimumab(trade name:Humira)and BA
2.2 公平性
“专利舞蹈”的公平性可保证双方在谈判中的利益。RPS 可先选择最相关和最有力的专利,再选择其他专利进行诉讼[14]。在任何一个诉讼阶段获胜,RPS 都可能被授予禁止令。“专利舞蹈”给予了RPS 对抗BA 最有效的方法,同时保证RPS 即使输了诉讼也可争取其他专利。但在传统专利诉讼中,RPS 可能要同时对抗所有专利[15]。BA 可预先了解RPS 认为有效、侵权的专利,评估相关事实和法律支持,并在一定程度上可控制哪些专利会被提起诉讼及何时会被提起;可享有“专利舞蹈”过程中交换的信息,并受到安全港法规的保护,使其免于受到起诉。
保证指定信息的有效交换:BA 和RPS 在生物仿制药进入市场前对专利侵权问题提起诉讼。指定信息的交换是有效解决专利问题的重要基石[16],“专利舞蹈”可保证BA 和RPS 间指定信息的有效交换,是双方妥协的一部分,但在传统的专利侵权中是不存在的,会削弱BA 所面临的专利阻碍,并有助于BA 和RPS 间保持平衡。BA启动“专利舞蹈”,则必须在FDA接受申请后20 d内将aBLA 的副本发送给RPS。RPS 在60 d 内提供主张的专利清单,并确定专利授权范围。BA在60 d内提供认为应包括在诉讼中的其他专利清单,并对RPS 的许可提议作出回应。BA 还必须提供详细的声明,说明无效、不可执行或不侵权的事实和法律依据,或者说明不打算在RPS 专利到期前销售其生物仿制药。若BA 提供了详细声明,RPS 在60 d 内对详细声明作出回应。信息交换后,双方商定第一阶段诉讼中最终要起诉的专利清单。如果双方在15 d 内就最终专利清单达成一致,RPS在30 d 内可提出专利侵权投诉。如果双方在15 d 内未就最终专利清单达成一致,双方将交换另一套专利清单。BA 要首先披露清单中所列专利,并在披露后的5 d内由双方同时交换专利清单。RPS所列专利数量可能不会超过BA,如果BA 列出零项专利,RPS 可列出1 项。随后RPS 在30 d 内提交专利侵权投诉,并主张双方所列专利。如果RPS 在30 d 内不提出诉讼,将会影响某些利益,如损失赔偿会被限制在合理的使用费范围内等。“专利舞蹈”诉前专利纠纷流程见图1。
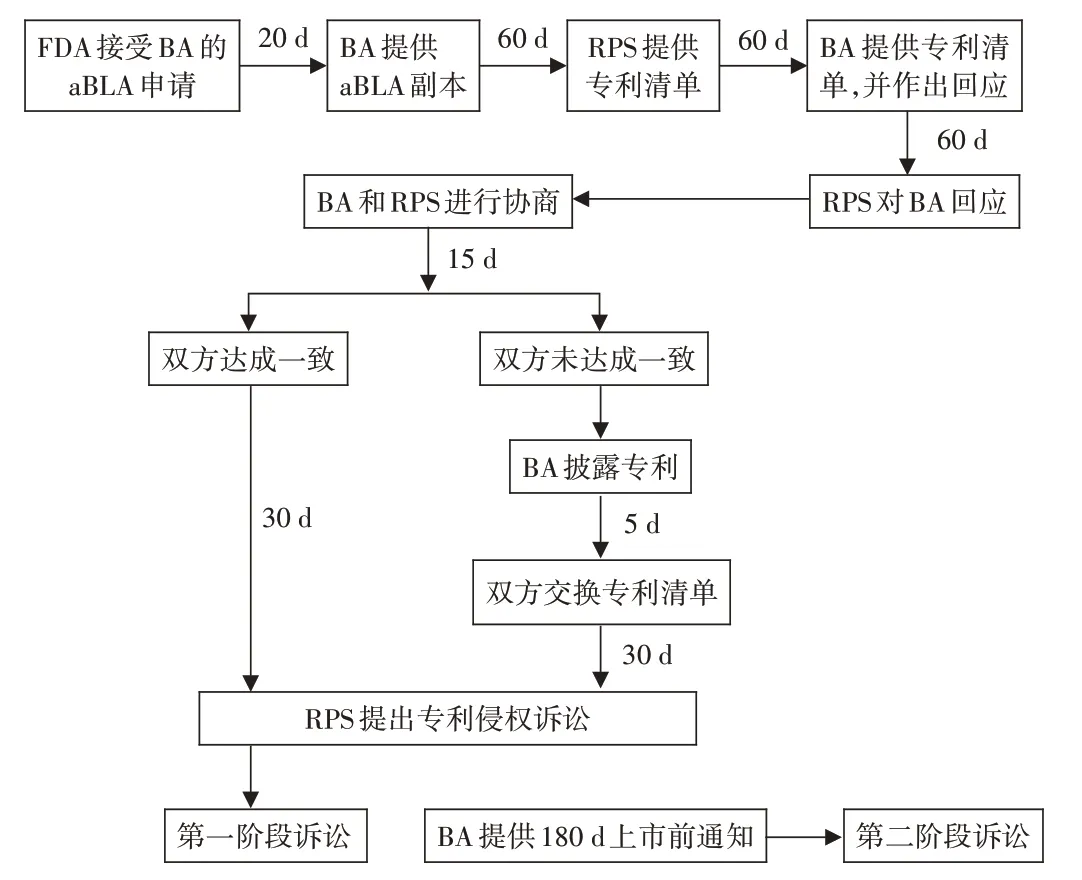
图1 “专利舞蹈”诉前专利纠纷流程Note:FDA refers to the Food and Drug Administration;aBLA refers to the Abbreviated Biologics License Application;BA refers to biosimilar applicants;RPS refers to reference product sponsors.Fig.1 Flow chart of the pre - litigation patent dispute of″patent dance″
专利信息公示:专利权人可围绕基础专利申请多种外围专利,采用专利密集战略构建“专利丛林”,排挤竞争对手达到垄断的地位,迫使竞争对手难以绕开相关专利,使其面临增加技术侵权的风险[17]。生物制药产业中的RPS 也在运用此策略。2021年,美国《生物产品专利透明法案》要求RPS 在接受aBLA 副本的60 d 内向BA 提供3Alist 初始清单补充专利清单,在BA 交换后的30 d 内将上述清单提交给FDA,并提供专利到期信息,且在紫皮书中公示,每30 天更新1 次。此法案旨在帮助BA 解决“专利丛林”造成的阻碍,利用这些信息确定已有专利许可的潜在伙伴关系、目标专利,围绕新技术的发展机遇进行设计,促进市场竞争,降低药费。专利信息公示上承“专利舞蹈”中的信息交换,下启诉讼纠纷解决程序,是BA 向RPS 发起专利挑战,迫使RPS 在诉前缩减专利数量的基础。
2.3 非强制性
“专利舞蹈”的非强制性是鼓励BA 选择“专利舞蹈”,给予BA 因自身利益制订策略的机会。在生物仿制药产业发展初期,BA 通过参加“专利舞蹈”提交aBLA,证明生物仿制药与参考产品的高度相似性,可降低监管批准的门槛。通过“专利舞蹈”专利信息交换程序,可降低不确定性专利形成的阻碍,使BA 获利。随着生物仿制药产业的成熟,以及大量生物制品专利保护的到期与公开,BA 参加“专利舞蹈”的时间与金钱成本可能会削弱自身收益,BA会考虑选择拒绝参加。因此,“专利舞蹈”的非强制性更适应美国生物仿制药的发展需要。
BA 选择遵守“专利舞蹈”的优点:1)可控制诉讼的专利数量;2)可确定与第一阶段诉讼相关的专利;3)可了解RPS 的上诉时间;4)较早的争论交流可深入了解RPS 的侵权和有效性立场;5)BA 可保留提起宣告性判决诉讼的能力;6)可迫使RPS 列出所有专利,否则BA会失去主张这些专利的权利;7)如果RPS 不遵守“专利舞蹈”严格的时间限制,合理的版权使用费将是RPS“唯一和专属的补救措施”[18-19]。
BA选择不遵守“专利舞蹈”的优点:1)不遵守“专利舞蹈”的最大动机是加快进入市场,如果BA 已知RPS拥有较少的专利组合,就没有必要将诉讼分为2个阶段及230 d 的时间,选择加速诉讼以清除妨碍进入市场的障碍更符合BA 的最佳财务利益,特别是BA 认为生物仿制药可在短期内获得FDA 的批准的情况下;2)可保护BA 免受某些专利的侵权索赔;3)如果RPS 不了解生物仿制药的制造信息,可迫使RPS放弃主张专利;4)“专利舞蹈”的止赎权可帮助BA 保护有关制造过程的敏感商业信息;5)可使BA 免于披露早期的非侵权和无效抗辩的义务。
BA 选择不遵守“专利舞蹈”的缺点:1)BA 不参与“专利舞蹈”将失去对诉讼范围和时间的控制;2)BA 参与或少部分参与“专利舞蹈”可迫使RPS 列出所有专利清单,但BA 不参与“专利舞蹈”将失去主张这些专利的权利;3)如果BA 跳过部分“专利舞蹈”,可能要直接接受RPS的宣告性判决[20],如果BA 未按要求提供申请和信息,则RPS 可根据《美国法典》第28 卷第2201 节的规定,对任何生物制品或生物制品用途专利的侵权、有效性或可执行性提起诉讼[21];4)跳过部分“专利舞蹈”的BA 将不会触发BPCIA 第一阶段诉讼中的30 d 诉讼时间,且如果在30 d 后提起诉讼,也不会触发随后的损害赔偿限制[18-19];5)如果RPS 持有多项专利,BA 可能会因跳过“专利舞蹈”而获得法院的初步禁令;6)在上市前通知发出后的第二阶段诉讼中,BA 可能被禁止提起宣告性判决诉讼,如果忽略其中任何一步,BA是否可再次启动“专利舞蹈”尚无肯定答案;7)法院可能会考虑BA 在“专利舞蹈”过程中缺乏善意,并作为确定禁令救济的考虑因素。
3 美国“专利舞蹈”对我国构建生物仿制药诉前专利纠纷解决机制的启示与建议
3.1 对我国《实施办法》的启示
3.1.1 高效性有待完善
根据《实施办法》第十二条专利声明制度,要求BA对照专利平台已公布的专利信息,对被仿制药的每件相关专利作出四类声明,并启动生物仿制药诉前专利纠纷解决程序。四类声明制度借鉴Hatch - Waxman 法案,适用于仿制药专利纠纷,与创新生物仿制药采取同样的审批途径,未提供生物仿制药独立的简化审批通道。同“专利舞蹈”中以提交aBLA 证明生物仿制药的高度相似性启动“人为侵权”、缩减诉前专利数量相比,《实施办法》的高效性有所欠缺,且适配性较低。
《实施办法》中的四类声明缺乏行政机关的实质性审查与专利有效性的确认程序,均为BA 单方面对相关专利真实性、有效性的声明。RPS如有异议,由相关专利行政部门裁决或向司法部门提起诉讼,缺乏促进BA 和RPS专利信息交换与沟通的程序,以及保障缩减诉前专利数量达成诉前和解的相关法律。四类声明要求对每项专利作出声明,可能会为BA 的诉前准备工作造成巨大压力,增加BA 落入专利陷阱的可能性,提高诉讼资金与时间成本,打击BA 提交药品上市申请的积极性。由于缺乏信息交换与沟通环节,RPS 无法及时、有效应对来自BA 的诉前专利挑战,会将专利侵权的维权诉讼转向药品上市后,降低了生物仿制药的市场竞争预期。可见,《实施办法》的专利声明制度可能会造成BA 和RPS间的利益失衡,导致其程序形同虚设,降低《实施办法》的效率。
3.1.2 公平性有待完善
专利信息公示缺乏相关法律强制性要求:专利信息公示是推动专利纠纷解决,保持BA 和RPS 间利益平衡的基础,更是加快生物仿制药上市参加药品竞争达到降低药费的手段。同“专利舞蹈”相比,《实施办法》中的专利信息公示属主动登记,缺少相关法律强制性要求,且缺少相应审查部门的监管与审查,可能导致专利信息登记的准确性缺失,专利范围的不确定性,造成BA专利搜索范围扩大,准确性降低。
专利登记范围有限:为防止“专利丛林”发生,“专利舞蹈”的信息交换过程包括制造信息[10],且在紫皮书中的专利登记类型不受限制。同“专利舞蹈”相比,《实施办法》第十二条只规定生物制品可登记活性成分的序列结构专利、医药用途专利,不包括晶型、代谢产物、检测方法、中间体、制备方法等专利,限制了专利登记类型。因此,BA不能完全依靠平台的专利登记信息进行判断,不利于BA 全面了解参考产品的专利布局,导致BA专利侵权的风险上升。
3.1.3 强制性更适合现阶段生物仿制药的发展需要
同“专利舞蹈”的非强制性相比,《实施办法》第十二条规定,BA按本法第六条进行相关专利声明;第十三条规定,对于生物类似药注册申请,药品监督管理部门依据技术审评结论,直接作出是否批准上市的决定,体现了《实施办法》的强制性。其通过司法与行政手段给予BA 明确的技术审评结论,提高了生物仿制药产业参加市场竞争、持续投入研发的信心,对促进我国生物仿制药行业由“以仿为主、创新为辅”向“创新为主、仿创兼顾”的发展起到了正向引导作用。
3.2 建议
建立生物仿制药专利诉前“人为侵权”机制:《实施办法》的专利声明制度应引入“专利舞蹈”的“人为侵权”机制,即提交aBLA 证明生物仿制药的高度相似性,简化BA 的诉前准备工作,鼓励BA 提交申请,迫使RPS诉前缩减专利数量,促进双方专利的诉前交流,以达到诉前高效解决专利纠纷的目的。
完善我国专利信息登记制度的公平性:《实施办法》中,专利信息公示应增加相关法律强制性要求,加强相关部门的审查与监管,增强专利信息登记的准确性和范围的确定性,达到帮助BA 缩小专利搜索范围和增加准确性的目的。为防止RPS 使用“专利丛林”延长专利保护时间与扩大保护范围,我国药品专利信息登记平台不应限制专利登记类型,尽可能帮助BA 全面了解RPS专利布局,减少BA陷入专利陷阱的可能性。
应根据生物仿制药行业的发展调整强制性:随着大量参考产品的专利到期与生物仿制药行业的发展成熟,应给予BA 是否参加诉前专利纠纷的选择性,以更好地适应行业的发展需要。
4 结语
虽然生物仿制药是仿制药市场的一部分,但仿制药并不能代表生物仿制药,生物仿制药具有特定的简略审批途径[22]。我国《实施办法》可借鉴“专利舞蹈”的特性,引入“人为侵权”机制的高效性,促进BA 和RPS缩小诉前专利范围达成和解,鼓励BA 快速参与市场竞争,达到迅速降低药费的目的;建立具有法律强制性且不限制专利登记类型的专利信息公示与登记制度,防止“专利丛林”的发生,保证BA 和RPS 诉讼中的公平性;根据生物仿制药市场的发展需求,可逐渐调整《实施办法》的强制性向非强制性转换,促进生物仿制药行业的快速发展,建立适合我国生物仿制药行业发展需要的诉前专利纠纷解决机制。
