重度子痫前期并发心功能不全的危险因素分析
2024-03-16吴秀秀胡文胜沈旭娜占思思
吴秀秀,胡文胜,沈旭娜,占思思
1.浙江中医药大学研究生院妇产科学,浙江杭州 310056;2.温州市中心医院妇产科,浙江温州 325100;3.浙江大学医学院附属妇产科医院妇产科,浙江杭州 310003
子痫前期(preeclampsia,PE)是指孕20 周以后出现的血压升高伴蛋白尿的疾病状态。重度子痫前期(severe preeclampsia,sPE)是PE 的严重类型,患者可出现收缩压>160mmHg(1mmHg=0.133kPa)或舒张压>110mmHg,或出现器官水肿、子痫、血管内溶血-肝酶升高-低血小板(hemolysis,elevated liverenzymes,and low platelets,HELLP)综合征、肝肾功能损害、脑水肿、神经系统损害、心功能不全甚至死亡等[1]。本研究通过分析sPE 患者出现心功能不全的危险因素,旨在为sPE 患者预防心功能不全的发生、改善sPE 患者的疾病结局提供参考。
1 资料与方法
1.1 一般资料
选取2020 年1 月至2023 年9 月于温州市中心医院住院的sPE 患者共107 例。根据患者是否出现心功能不全分为实验组(n=32)和对照组(n=75)。纳入标准:①符合《妊娠期高血压疾病诊治指南(2020)》诊断标准[1];②出现呼吸困难、活动受限或超声心动图提示射血分数异常,或心肌酶谱、B 型脑钠肽提示心功能不全[2];③孕期正常在温州市中心医院产检。排除标准:①资料不全;②既往合并慢性糖尿病、心脏病、肾脏疾病、免疫性疾病者。本研究经温州市中心医院伦理委员会审批通过(伦理审批号:202311251941000469795)。
1.2 方法
1.2.1 资料收集及观察指标 由医务人员统一收集两组患者的一般资料及分娩结局、实验室指标等。①一般资料:年龄、孕次及产次、孕前体质量指数(body mass index,BMI)、学历(高中以下,高中,大专以上)、妊娠糖尿病(gestational diabetes mellitus,GDM)(是、否)、高血压家族史(是、否)、双胎妊娠(是、否)、孕期体质量增幅(<15kg,15~20kg,≥20kg)、孕期及产后72h 血压。②实验室指标:血钙、血白蛋白、产后出血量、血红蛋白、血脂。③分娩结局:产科严重并发症、围生儿结局、新生儿结局。
1.2.2 诊断标准 参照《妊娠期高血压疾病诊治指南(2020)》[1]中sPE 的诊断标准。①子痫前期诊断标准:妊娠20 周后出现血压升高,伴尿蛋白≥0.3g/24 h,或尿蛋白/肌酐比值≥0.3,或随机尿蛋白≥(+);无蛋白尿但伴有重要器官或血液系统、消化系统、神经系统的异常改变,导致胎盘、胎儿受累。②sPE的诊断标准:子痫前期孕妇出现以下任意一项表现则诊断为sPE。a.血压持续升高不可控制;b.持续性头痛、视觉障碍或其他中枢神经系统异常表现;c.持续性上腹部疼痛及肝包膜下血肿或肝破裂表现;d.转氨酶水平升高;e.肾功能受损;f.低蛋白血症伴腹水、胸水或心包积液;g.血液系统异常;h.心功能衰竭;i.肺水肿;j.胎儿生长受限或羊水过少、胎死宫内、胎盘早剥等。
1.3 统计学方法
采用SPSS 27.0 统计软件对数据进行处理分析。计量资料以均数±标准差(±s)表示,组间比较采用独立样本t检验;计数资料以例数(百分率)[n(%)]表示,比较采用c2检验。采用二元Logistic回归模型分析sPE 患者出现心功能不全的因素。P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者的一般资料比较
两组患者的孕期收缩压、孕前BMI 差异有统计学意义(P<0.05);体质量增幅、孕次、产次、年龄、sPE 发病孕周、分娩孕周、新生儿体质量、产后出血量差异无统计学意义(P>0.05);实验组患者sPE 发病平均孕周(34.81±4.56)周,其中15 例(46.88%)发生在孕期,17 例(53.13%)发生在分娩后,见表1。
表1 两组患者的一般资料比较(±s )
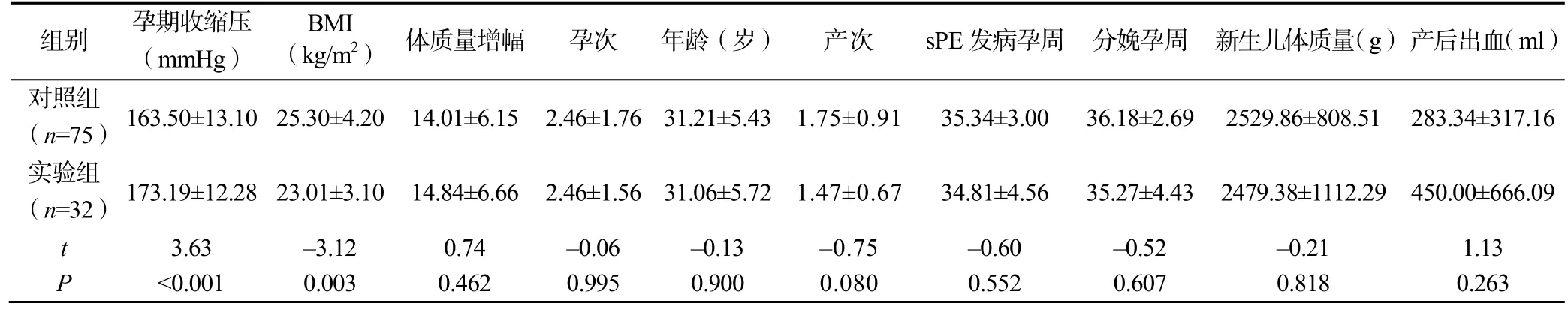
表1 两组患者的一般资料比较(±s )
组别 孕期收缩压(mmHg)BMI(kg/m2) 体质量增幅 孕次 年龄(岁) 产次 sPE 发病孕周 分娩孕周 新生儿体质量(g) 产后出血(ml)对照组(n=75) 163.50±13.10 25.30±4.20 14.01±6.15 2.46±1.76 31.21±5.43 1.75±0.91 35.34±3.00 36.18±2.69 2529.86±808.51 283.34±317.16实验组(n=32) 173.19±12.28 23.01±3.10 14.84±6.66 2.46±1.56 31.06±5.72 1.47±0.67 34.81±4.56 35.27±4.43 2479.38±1112.29 450.00±666.09 t 3.63 –3.12 0.74 –0.06 –0.13 –0.75 –0.60 –0.52 –0.21 1.13 P <0.001 0.003 0.462 0.995 0.900 0.080 0.552 0.607 0.818 0.263
2.2 两组患者出现严重并发症的情况比较
实验组患者出现呼吸衰竭、HELLP 综合征、感染的例数高于对照组,差异有统计学意义(P<0.05);两组患者出现胎盘早剥、肝肾功能不全、子痫等严重并发症的差异无统计学意义(P>0.05),见表2。

表2 两组患者出现严重并发症的情况比较(例)
2.3 两组围生儿及新生儿结局比较
对照组发生新生儿窒息、新生儿转重症监护的例数高于实验组,差异有统计学意义(P<0.05);两组胎儿生长受限(fetal growth restriction,FGR)、围生儿死亡例数比较,差异无统计学无意义(P>0.05),见表3。
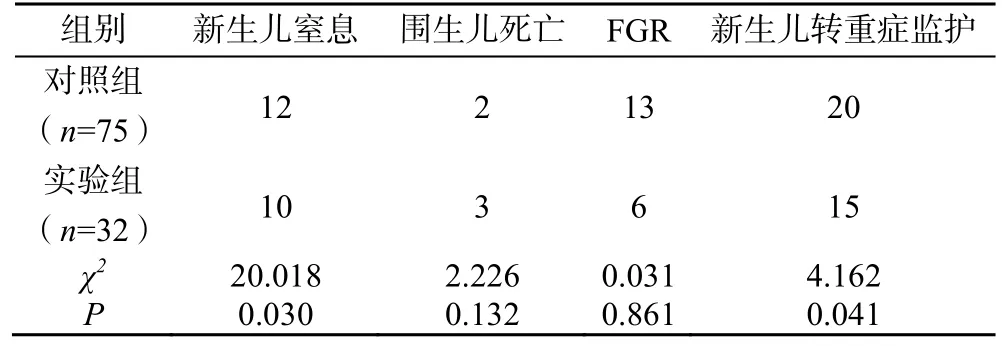
表3 两组围生儿及新生儿结局的比较(例)
2.4 影响sPE 并发心功能不全的单因素分析
两组高龄(年龄≥35 周岁)、大专以下学历、初产妇、孕期体质量增幅超过<15kg 或15~20kg、血小板减少(血小板计数<100×109/L)、轻度贫血(110g/L>血红蛋白≥90g/L)、高脂血症(符合以下任意一项:总胆固醇>5.72mmol/L、三酰甘油>1.7mmol/L,低密度脂蛋白>4.14mmol/L)、GDM、高血压家族史、产后出血(产后出血是指胎儿娩出后24h 内,阴道分娩出血量≥500ml,剖宫产出血量≥1000ml)的例数比较,差异无统计学意义(P>0.05);两组的孕期体质量增幅≥20kg、低钙血症(血钙<2.2mmol/L)、低白蛋白血症(血浆总蛋白<60g/L,其中白蛋白<30g/L)、中度贫血(90g/L>血红蛋白≥70g/L)、双胎比较,差异有统计学意义(P<0.05),见表4。

表4 影响sPE 并发心功能不全的单因素分析(例)
2.5 二元Logistic 回归分析
孕期收缩压增高、孕期体质量增幅≥20kg、孕前BMI 增加、低钙血症、低白蛋白血症、中度贫血是sPE 出现心功能不全的危险因素(P<0.05),见表5。

表5 sPE 合并心功能不全的危险因素Logistic 回归分析
3 讨论
有研究显示PE 患者中心功能受损者约占0.4%[3]。sPE 可出现左心室结构和功能的改变,其引起的心功能障碍及心脏结构肥大、心脑血管意外可致孕产妇严重不良结局[3-5]。PE 孕产妇主要死亡原因为呼吸循环衰竭,因此,预防sPE 患者出现心功能不全可减少孕产妇死亡[6]。
本研究发现sPE 并发心功能不全患者更容易出现呼吸衰竭、HELLP 综合征等严重并发症,也更容易发生严重的围生儿及新生儿不良结局;提示防治sPE 出现心功能不全可减少孕产妇及围生儿不良结局的发生。
分析sPE 患者出现心功能不全的危险因素如下。①孕前BMI 高、孕期体质量增加≥20kg:研究表明BMI 越高的患者越容易出现体内代谢紊乱,刺激血管内皮损伤产生血管紧张素、炎症因子,导致全身小血管痉挛,血管外周阻力增加进一步引发心功能不全[7-8]。sPE 患者孕期体质量增长可能提示水肿加重,预示心功能不全。②低钙血症、低蛋白血症:钙离子、蛋白质是肌钙蛋白的重要原料,低钙血症可引起心肌收缩力不足,引发心功能不全[9]。而低蛋白血症除减少肌钙蛋白的生成外,还可引发血容量增加、心包积液等病理状态,加重心脏负担,引起心功能不全[10-11]。③中度贫血:PE 的不良妊娠结局与中度贫血相关,贫血患者代偿性出现心博加快,也可出现红细胞生成素增多,诱导内皮细胞产生血清内皮素,引起血管收缩导致血压升高,从而导致心功能不全[12]。④孕期血压偏高:收缩压、舒张压、脉压升高均可能增加患心功能不全的风险,因此,sPE 患者控制血压非常关键[13-14]。⑤感染:感染是妊娠期高血压诱发心功能不全的因素之一,感染可导致体温升高、脉搏加快、营养消耗增加及机体炎症反应,导致心肌损伤加重,可引发心功能不全[15-16]。
综上,孕前BMI 升高、孕期体质量增幅≥20kg、低钙血症、低蛋白血症、中度贫血、孕期血压增高、感染是sPE 出现心功能不全的危险因素。因此,孕期应积极控制血压、补钙、补铁、补充白蛋白、控制体质量;对sPE 患者增加血钙、白蛋白、血红蛋白、血压相关指标监测的频率;积极控制血压、解痉、预防感染可减少sPE 患者心功能不全的发生。
利益冲突:所有作者均声明不存在利益冲突。
