N-甲基哌啶的合成方法研究
2024-03-15何小强郝磊向龙李倩文
何小强, 郝磊, 向龙, 李倩文
(重庆华歌生物化学有限公司, 重庆 404000)
N-甲基哌啶,分子式为C6H13N,是重要的精细化工中间体,主要用于医药、农药等的合成[1]。N-甲基哌啶也是合成甲哌鎓的重要中间体,与甲哌鎓具有相似的结构(见图1),普遍存在于甲哌鎓原料以及商品化甲哌鎓剂型中[2-3];还可以用作环氧树脂固化剂、橡胶促进剂、离子交换膜的合成等[4-7],具有广阔的应用市场。

图1 甲哌鎓与N-甲基哌啶的化学结构图
合成N-甲基哌啶主要有哌啶甲基化法[8-12]、酰胺还原法[13-15]以及胺醇脱水环化法[16-18],工业上以哌啶甲基化法为主。Da Silva 等[19]采用哌啶和甲醛溶液反应,锌粉为还原剂,乙酸为添加剂制得N-甲基哌啶,反应条件温和,安全性较高,但锌粉难回收,易产生固体废物。 罗超然等[20]以哌啶、多聚甲醛、氢气为原料,在γ-Al2O3的催化下,一锅法制得N-甲基哌啶, 产品纯度高, 但反应时间长(10~52 h),生产效率低,同时需高温反应(500 ℃~600 ℃),存在安全隐患且不易实现工业化。烷基化反应作为一种重要的合成手段,广泛应用于化工生产过程,由于该反应是放热反应,会导致反应体系快速升温或快速产生气体等,若不能延缓反应速率或及时移除热量可能会存在安全风险,甚至引发火灾和爆炸。 因此,通过优化工艺将其危险程度降低到易于控制的范围内,将更有利于工业化。 另外,N-甲基哌啶与水互溶,沸点相近,易共沸,导致含水哌啶除水相对困难。 虽然有报道用三元共沸或物理干燥的方式脱水[20],但三元共沸时间久、效率低、能耗高,而物理干燥方式需要大量干燥剂,干燥剂再生程序复杂,工业化生产成本也较高。
本研究以哌啶和甲醛为原料,甲酸钠和甲酸为还原剂, 经烷基化反应得到N-甲基哌啶溶液,再经环己烷萃取及精馏得到N-甲基哌啶。
1 实验部分
1.1 仪器和试剂
1.1.1 仪器
精馏塔(带智能磁力搅拌器),明远仪器设备有限公司;DF-101S 型集热式恒温加热磁力搅拌器,巩义市予华仪器有限责任公司;GC-2010 plus气相色谱仪,岛津企业管理(中国)有限公司;PHS-3C 型pH 计, 上海仪电科学仪器股份有限公司。以及托盘天平、恒压滴液漏斗、梨形分液漏斗、四口圆底烧瓶、球形冷凝管、玻璃棒、烧杯等。
1.1.2 试剂
哌啶、甲酸钠、88%甲酸溶液、37%甲醛溶液、液碱、环己烷、苯、二氯乙烷、三氯甲烷。
1.2 实验方法
将甲酸钠、甲酸、甲醛混合后向其中滴加哌啶,反应得到N-甲基哌啶溶液。 利用环己烷对所得反应液进行萃取,得到含水量为0.14%的N-甲基哌啶与环己烷粗产品,粗产品经简单精馏即可得到合格的产品。 水相中少量N-甲基哌啶可通过普通蒸馏回收, 同时馏分可直接回收利用,避免了常规萃取后再次干燥脱水的繁琐操作。 另外,精馏回收的环己烷也可直接回收利用,既降低反应成本又简化生产工艺。简易流程图见图2。

图2 实验简易流程图
2 实验过程
2.1 N-甲基哌啶的合成
将甲酸钠(126.9 g,1.85 mol)、88%的甲酸溶液(48.8 g,0.93 mol)和37%甲醛溶液(227.6 g,2.80 mol)混合,形成均匀的反应液A。将哌啶(200 g,2.34 mol)以3.33 mL/min 的速度滴加至反应液A 中, 控制反应温度低于70 ℃, 当滴加量剩余1/3 吡啶时,控制反应温度为80 ℃,滴加完毕后,继续搅拌反应2 h 后,使其自然降温至40 ℃,滴加液碱调节pH≈10,得N-甲基哌啶溶液475.6 g,气相色谱法(GC)检测,含量为99.1%。
2.2 N-甲基哌啶的快速纯化
将2.1 中制备的N-甲基哌啶溶液与环己烷以1:1.5 体积比进行萃取脱水,静置30 min 后分层。将油相在精馏塔中精馏,前馏分为含有少量N-甲基哌啶的环己烷,直接用于下次萃取脱水使用,在塔顶温度为80 ℃~82 ℃、 塔釜内温度为110 ℃~112 ℃的条件下采集馏分, 即得到N-甲基哌啶,GC 检测,含量为99.5%,收率为98.7%。
3 结果及分析
3.1 还原剂组分配比的影响
选择甲酸钠和甲酸为还原剂,在哌啶和甲醛的摩尔比为1:1 的条件下, 考察了还原剂组分配比对合成N-甲基哌啶的影响, 共设3 个批次,结果见表1。

表1 还原剂组分配比对合成N-甲基哌啶的影响
由表1 可以看出,当甲酸钠和甲酸的摩尔比为1:1 时,升温较快,产生大量白雾和气泡,反应较剧烈;当摩尔比为2:1 时,升温平缓,仅产生少量白雾和气泡,再增加甲酸钠比例,反应升温缓慢且产物含量降低。 综合考虑反应过程的安全性及经济性,确定还原剂组分甲酸钠和甲酸的摩尔比为2:1。
3.2 投料摩尔比的影响
在还原剂组分摩尔比为2:1 的条件下, 考察了投料摩尔比(哌啶、还原剂组分、甲醛)对合成N-甲基哌啶含量的影响,共设6 个批次,结果见表2。

表2 投料摩尔比对合成N-甲基哌啶含量的影响
由表2 可以看出,当投料摩尔比(n(哌啶):n(还原剂组分):n(甲醛))达到1:1.2:1.2 时,N-甲基哌啶含量几乎不随摩尔比增加而明显增加。 因此确定最佳投料摩尔比为1:1.2:1.2。 另外, 因为3.1 中确定还原剂组分中甲酸钠和甲酸的配比为2:1 时最佳,所以最佳投料摩尔比设定为1:0.8:0.4:1.2。
3.3 反应温度的影响
在投料摩尔比(哌啶、还原剂组分、甲醛)为1:1.2:1.2 的条件下,考察了反应温度对合成N-甲基哌啶的影响,共设4 个批次,结果见表3。

表3 反应温度对合成N-甲基哌啶的影响
由表3 可以看出,反应温度过低,哌啶反应不完全,底液浑浊;随着反应温度的增加,N-甲基哌啶的含量也增加, 当达到80 ℃时哌啶含量最高;继续增加温度,反应液体共沸,反应剧烈,产生大量白雾和气泡,反应体系呈不安全状态且含量略有降低。综合考虑确定最佳反应温度为80 ℃。
3.4 滴加速度的影响
在投料摩尔比(哌啶、还原剂组分、甲醛)为1:1.2:1.2,反应温度为80 ℃的条件下,考察了滴加速度(哌啶用量一定,以滴加时间控制速度)对合成N-甲基哌啶的影响,共设5 个批次,结果见表4。

表4 滴加速度对合成N-甲基哌啶的影响
由表4 可以看出,滴加速度过快,产生大量白雾和气泡,导致升温剧烈,后期反应温度偏高,反应体系不安全;滴加速度过慢,导致后期升温速度慢,需要二次供热,能耗偏高;随着滴加时间的延长,N-甲基哌啶的含量也增加,当达到60 min时含量最高,反应较为温和,再延长滴加时间,含量增加不明显。因此确定最佳的滴加时间为60 min,滴加速度为3.33 mL/min。
3.5 萃取剂种类及使用量的影响
在投料摩尔比(哌啶、还原剂组分、甲醛)为1:1.2:1.2,反应温度为80 ℃,滴加速度为3.33 mL/min的条件下,考察了萃取剂种类及使用量对合成N-甲基哌啶干燥脱水的影响,共设4 种类型,3 个体积比,结果见表5。
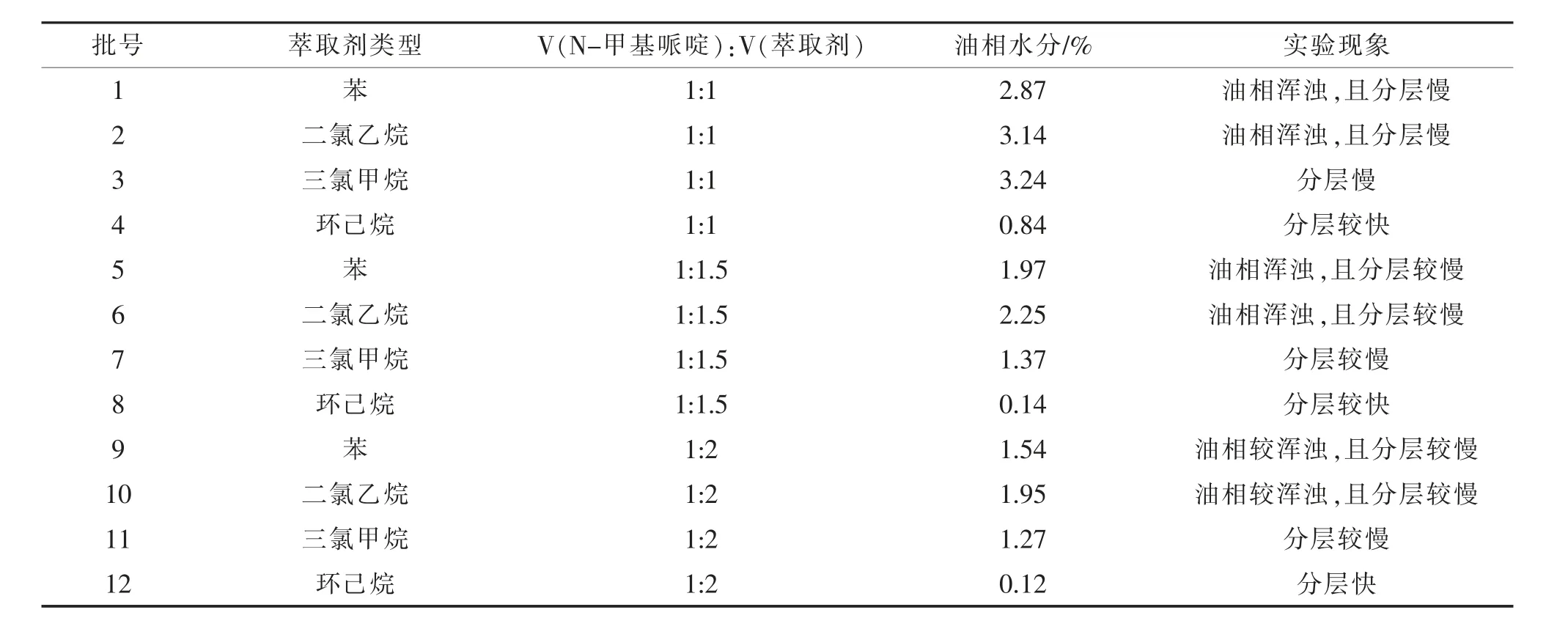
表5 萃取剂种类及使用量对油相含水量的影响
由表5 可以看出,用环己烷萃取时,分层较快,萃取后油相含水量相对较低,效果显著;当环己烷与N-甲基哌啶的体积比为1.5:1 时, 油相含水量为0.14%,继续增加环己烷用量,油相含水量降低不明显;另外,将环己烷萃取后的混合液置于精馏塔精馏,N-甲基哌啶含量为99.5%, 收率为98.7%。 因此选择环己烷为萃取剂, 环己烷与N-甲基哌啶的体积比为1.5:1。
4 结论
(1)以甲醛、甲酸钠、甲酸、哌啶为原料合成N-甲基哌啶,经环己烷萃取干燥,精馏后,含量为99.5%,收率为98.7%,成功开发出一种N-甲基哌啶的合成方法。
(2)最佳的合成条件:投料摩尔比(哌啶、还原剂组分、甲醛)为1:1.2:1.2,反应温度为80 ℃,滴加速度为3.33 mL/min,滴加时间为60 min,萃取剂为环己烷,环己烷与N-甲基哌啶体积比为1.5:1。
(3) 本研究的合成方法具有反应条件温和、反应过程平稳、工艺流程简单、易实现工业化的优点。
