抗神经束蛋白186抗体阳性的郎飞结区/结旁疾病的临床特点(附1例报告)
2024-03-11董思语孙美陈聪王静金庆文程虹
董思语,孙美,陈聪,王静,金庆文,程虹
郎飞结区/结旁疾病(NPP)是近年来提出的一个新的疾病概念,最初这类疾病被认为是Guillain-Barré综合征(GBS)或慢性炎性脱髓鞘性多发性神经根神经病(CIDP)的特殊亚型,与郎飞结区或结旁区抗体的产生有关[1-2]。随着对疾病认识的进一步加深,部分学者[3-4]提出NPP在发病机制、临床表现及治疗等方面与GBS、CIDP差别很大,应单独分类。现对我科近期收治的1例以颅神经损害为主要表现的抗神经束蛋白186(NF186)抗体阳性的NPP患者的临床资料进行总结,并结合文献做相关综述。
1 临床资料
患者,男性,70岁,因“言语不清伴吞咽困难1个月,缓解后再发5 d”于2021年8月2日收住我院。患者于2021年6月29日下午突发言语欠清,数分钟后好转,6月30日上午又出现类似症状,自行缓解。当日晚饭过程中患者再次出现言语及吞咽困难,进行性加重,于当地医院就诊,头颅CT未见明显异常,改善循环治疗后无缓解。予糖皮质激素治疗(地塞米松10 mg/d静脉滴注,后逐渐减量)1周后症状明显缓解,出院后自行停用糖皮质激素。7月29日患者再次出现言语、吞咽、咀嚼、抬头动作费力,逐渐加重至发声困难、完全无法吞咽、痰滞咽喉部、咀嚼动作需用手帮扶。数日内体重减轻5 kg,为进一步治疗来我院就诊。既往史:2018年始出现双侧眼睑下垂,逐渐加重,并影响日常生活,无晨轻暮重现象,多次眼科检查无异常,病因未明,未予特殊治疗;既往有高血压史,平素血压控制可。其他既往史、个人史、家族史无特殊。入院查体:生命体征平稳,心、肺、腹查体(-)。专科查体:神志清楚,高级智能检查正常。双侧眼睑下垂(遮盖瞳孔上缘至4~8点水平),双眼球运动充分,无眼震,双侧瞳孔等大等圆,双侧角膜反射消失,双侧咀嚼肌力弱,面部感觉正常,双侧额纹、鼻唇沟变浅,鼓腮漏气,言语不清,可单音节发音,双侧咽反射消失,悬雍垂左偏,伸舌左偏。抬头、耸肩肌力Ⅲ级。余颅神经(-)。四肢肌力、肌张力正常。四肢腱反射正常,双侧病理征(-)。共济运动、肢体感觉正常。脑膜刺激征(-)。辅助检查:血常规、尿常规、大便常规、肾功能、电解质、凝血功能、糖化血红蛋白、输血前八项、类风湿因子、抗链球菌溶血素O、免疫五项、肿瘤标志物、甲状腺激素及相关抗体检查均未见明显异常。血清神经元抗原谱抗体IgG检测均(-)。人血浆脂蛋白相关磷脂酶A2 335 ng/mL(正常值<200 ng/mL),C反应蛋白25.7 mg/L(正常值<0.2 mg/L),总胆红素37.4 μmol/L(正常值5.1~19.0 μmol/L),直接胆红素13.3 μmol/L(正常值0~6.8 μmol/L),间接胆红素24.1 μmol/L(正常值0~20 μmol/L),低密度脂蛋白胆固醇2.58 mmol/L(正常值2.6~4.1 mmol/L)。白蛋白37.1 g/L,IgG 10.5 g/L。腰椎穿刺检查(8月2日):CSF压力120 mmH2O(1 mmH2O=0.0098 kPa),糖3.44 mmol/L,蛋白0.27 g/L,氯化物122.5 mmol/L,白蛋白174 mg/L,IgG 23.5 mg/L。CSF/血清IgG比值(QIgG)2.24×10-3,CSF/血清白蛋白比值(QAlb)4.69×10-3,IgG指数0.48。CSF病原微生物、膜式病变细胞均阴性。外送血清及CSF郎飞结抗体检查(CBA法):血清抗NF186 IgG抗体阳性(1∶10)(图1A),CSF抗NF186 IgG抗体阳性(1∶1)(图1B),血清和CSF中抗神经束蛋白155(NF155)IgG4抗体、抗接触蛋白1 (CNTN1)IgG4抗体、CNTN2 IgG抗体、抗接触蛋白相关蛋白1(Caspr1)IgG抗体检测均阴性。ECG、颈部动脉超声、头颅MRI+MRA(图2)检查未见明显异常。新斯的明试验阴性。EMG检查:四肢感觉、运动神经传导测定正常,F波正常,重复神经电刺激检查正常,头面部EMG检查因疫情防控暂无法开展。诊断:抗NF186抗体阳性NPP。8月3日起予甲泼尼龙500 mg/d冲击治疗,每3 d递减。糖皮质激素治疗10 d后患者症状无明显缓解,8月13日起行血浆交换治疗(总交换量2000 mL,包括4%人血白蛋白+林格氏液500 mL+病毒灭活血浆900 mL+新鲜冰冻血浆600 mL),血浆交换3次后患者症状明显好转,言语、吞咽、咀嚼、鼓腮等颅神经异常(包括双眼睑下垂症状)明显恢复,接近正常水平。
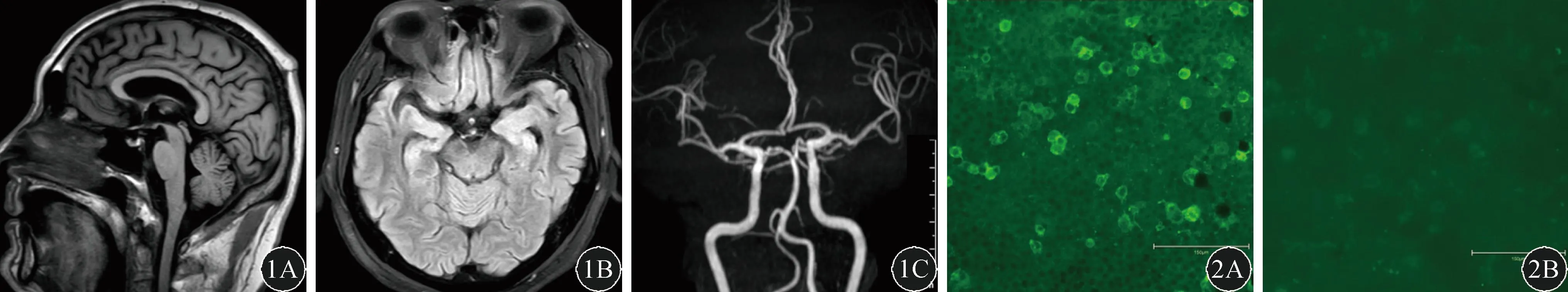
图1 血清及CSF抗NF186抗体检测结果A:血清NF186阳性(1∶10);B:CSF NF186阳性(1∶1)(图中细胞为NF186 IgG转染细胞,荧光标记物为异硫氰酸荧光素) 图2 头颅MRI+MRA检查 头颅MRI+MRA检查未见明显异常。
2 讨 论
随着分子生物学的发展,国内外学者开始重视郎飞结区/结旁区域在周围和中枢神经病理性损害中的影响,抗郎飞结抗体导致的NPP正逐渐成为自身免疫性神经疾病的研究热点。作为郎飞结区的重要粘附蛋白,NF186引起广泛的重视,但极少有NF186阳性病例的报道。CDIP和GBS相关荟萃分析[5]显示,抗NF186抗体阳性患者占总病例数的0~2.03%。而Notturno等[6]研究显示,60%的多灶性运动神经元病(MMN)和1%的CIDP患者血清中都存在抗NF186和神经胶质蛋白抗体,这一结果较其他研究差异较大,可能与该研究使用的是大鼠NF186蛋白片段,而其他研究[7]选用的是人类全长蛋白有关。
郎飞结是有髓神经纤维的重要结构,可分为结区、结旁区、近结旁区和结间区,其内的分子结构极其复杂,根据功能不同,可分为信号转导蛋白、细胞骨架/结构蛋白、离子通道及相关蛋白、粘附分子等[8]。NF155、NF186、CNTN1、CNTN2及Caspr1是目前发现常见的结区及结旁区抗原,既往多见于GBS、CIDP、多发性硬化、MMN等以周围神经病为主的个案报道中。NF186是位于郎飞结区的细胞粘附蛋白,与电压门控Na+通道共同锚定在郎飞结或轴突起始处。作为一种跨膜蛋白,NF186有6个免疫球蛋白样结构域,4个Ⅲ型纤维连接蛋白结构域和1个粘蛋白结构域[9]。在周围神经系统中,NF186与施万细胞微绒毛上的可溶性神经胶质蛋白和粘附分子相互作用;在CNS中,NF186与细胞外基质蛋白相互作用,是促进Na+通道聚集、保证神经信号高效传导的重要物质[10]。动物研究[11]发现,神经胶质蛋白而非神经束蛋白介导的免疫反应可损害郎飞结的结构及Na+通道聚集,从而诱导周围神经病变。还有研究[12]表明,抗神经束蛋白与抗体结合后可能会破坏神经传导的功能,使神经病变的持续时间延长、病变程度加重,但仅抗体存在时可能并不会出现神经损害,只有巨噬细胞、T细胞共同参与后才会导致神经病理性改变。随后Devaux等[13]报道自身抗体对郎飞结区NF186的攻击会使轴突上电压门控Na+通道减少,导致神经传导速度明显降低。Koike等[14]通过对抗NF155和CNTN1抗体阳性的CIDP患者腓肠肌活检发现,无巨噬细胞参与的结旁区隔膜样连接髓鞘脱失,提示抗体攻击郎飞结区/结旁区导致其结构破坏也是脱髓鞘性神经病的发病机制之一。抗NF186抗体阳性NPP患者发病年龄晚,亚急性起病,这类患者往往病情进展较快,也更易出现呼吸衰竭及颅神经受累症状,而无震颤、病理性疼痛等其他结旁抗体病的特异性表现。NPP患者可同时合并其他免疫缺陷性病变[15],部分患者除肢体周围神经受损外,还可合并出现面神经、眼球运动神经受损或球麻痹[15]。如本例患者仅出现颅神经受累,无脊神经和自主神经异常为国内外首例。值得注意的是,本例患者病程中多次出现发作性症状,患者无糖尿病、高脂血症等血管危险因素,头颅影像、EEG无异常,这种症状考虑为结区抗体病伴发的发作性神经缺损症状,而不是脑血管病或癫痫等其他疾病所致。Xie等[16]报告的16例抗NF186抗体阳性中枢和/或周围神经病患者中有2例分别出现了发作性眩晕和视觉缺损症状,但具体机制尚不明确,这种发作性症状是否是抗NF186抗体阳性NPP患者的特异性表现仍待进一步研究。
与CIDP/GBS类似,既往报告的抗NF186抗体阳性病例多出现周围神经脱髓鞘和/或轴索损害为主的神经传导异常,电生理检查是诊断的重要工具。而本例患者四肢EMG检查正常,这与本患者为单纯颅神经受累,未进行面肌、吞咽肌群等颅神经相关的检测有关。一项针对16例血清抗NF186抗体阳性患者的病例研究[16]显示,这类患者的临床表现并不典型,7例表现为CNS受累(4例出现头晕,3例出现视力损害),9例表现为周围神经损伤(7例出现肢体无力麻木,4例出现神经性疼痛),12例出现CSF蛋白升高。CSF蛋白-细胞分离是CIDP的特征性表现之一[17],部分患者的神经根炎性反应较轻,或CSF检查时间过早(发病1周内检查),可出现阴性结果。而本例患者行CSF检查时距发病时间较久,临床症状也较重,但CSF蛋白水平正常。有研究[18-19]曾报道过2例复发性GBS患者,均未见CSF蛋白-细胞分离现象,具体机制不明,这一阴性结果是否和“缓解-复发”的病程相关有待进一步探索。
免疫治疗是NPP的重要治疗手段,具体包括糖皮质激素冲击治疗、静脉注射免疫球蛋白(IVIG)、血浆交换和抗CD20单克隆抗体等,抗NF186抗体阳性NPP的发病率极低,无太多的治疗经验和证据可循。既往报道[15]显示上述治疗手段对本病均有一定效果。对IVIG或糖皮质激素疗效不佳的患者来说,血浆交换的临床获益可能更大[20]。NF155抗体中IgG4型抗体较少结合免疫球蛋白的Fc受体,且不能有效激活补体,因此IVIG或糖皮质激素疗效较差,血浆交换清除抗原抗体复合物可取得满意效果。作为NF155的同型异构体,抗NF186抗体阳性的部分患者可能具有类似特点。如本例患者所示,患者发病初始对糖皮质激素治疗短暂有效,再次发作后糖皮质激素疗效不明显,改为血浆交换后病情迅速恢复。目前部分研究[21]报道,使用美罗华(利妥昔单抗)治疗结旁抗体病,短期内取得较好疗效。但需要用药前给予全面的免疫状态评估,远期疗效仍在观察中。
与CIDP/GBS不同,NPP伴有特异性郎飞结区/结旁区抗体,除周围神经受损外,还可出现震颤、共济失调、病理性疼痛等相对特异性表现,且NPP无明显的炎症或巨噬细胞介导的脱髓鞘性病理改变,因此2021年欧洲神经病学学会/外周神经学会关于CIDP诊治指南将NPP从非典型CIDP分类中划分出来作为独立的疾病[22]。其具有独特的病理机制,临床表现和治疗方法也与传统的CIDP大相径庭,需要加强对该类疾病的认识。就该例患者而言,本次住院过程中仅表现多组颅神经受损,未出现典型的CSF蛋白-细胞分离现象,糖皮质激素治疗效果不明显,血浆交换疗效显著。
综上所述,以抗NF186抗体阳性为代表的NPP是一类发病年龄较晚、病情进展快、可累及颅神经的自身免疫性郎飞结病。该病发病率极低,部分患者早期即可转为重症,治疗方法相对特殊,常规糖皮质激素治疗效果可能不佳,血浆交换治疗有效。
作者贡献说明董思语负责采集、分析病例资料,撰写、修改文章;孙美收集影像资料,分析、解释数据;陈聪、王静、金庆文修改文章;程虹提出选题,指导文章修改
