罕见Ael 亚型的鉴定及探讨
2024-03-09周帆杨久扬赵恒丽
周帆 杨久扬 赵恒丽
(武安市第一人民医院输血科,河北 武安 056300)
ABO 血型系统最初于1900 年提出,至今仍是输血医学和器官移植医学中重要的血型系统[1]。 ABO 亚型是指红细胞或分泌液所含A 或B 抗原量不同的表现,其在临床工作中通常因血型正反定型不符而被发现[2]。 对亚型的正确鉴定是保证临床用血安全的重要前提。 我们在对住院患者的血型鉴定中发现Ael 亚型,现将家系调查及血型鉴定结果报告如下。
1 材料与方法
1.1 研究对象
先证者为本院患者,郝某某,女,47 岁,2022 年7 月12日因子宫肌瘤入院。 既往病史否认血液系统、肿瘤等重大疾病,无化疗史,无移植史,无输血史。 术前常规检查血型(微柱凝胶法)正定型为O 型RhD 阳性,反定型为A 型,提示ABO 正反定型不符,故送检标本要求做进一步血型鉴定。
1.2 试剂与仪器
抗-A、抗-B 血型定型试剂(单克隆抗体)(20220607)、抗-A1 凝集素(20220221)、抗-H 单克隆抗体(20220214),均为上海血液生物医药有限公司;抗-A,B(845000,DIAGAST); ABO 血型反定型试剂盒( 人血红细胞)(2022060102)、 意外抗体检测试剂(人血红细胞)(20220602),均为长春博迅生物技术有限责任公司;人源抗-A 及新鲜Ac、Oc、Bc 对照细胞均为自制。 实验室温湿度符合要求,仪器设备均在检定有效期内,所用试剂均严格按照说明书进行。
1.3 血清学试验
1.3.1 ABO 血型鉴定、意外抗体筛查
参照文献[3]对患者及其次子采用盐水试管法进行ABO、Rh 血型鉴定,盐水试管法和经典抗人球蛋白法进行意外抗体筛查试验,观察结果并记录。
1.3.2 抗-H 检测
取检测当日新鲜A、B、O 细胞做对照,先证者及其次子血清分别于与抗-H 试剂反应,观察结果并记录。
1.3.3 人源抗-A 血清的制备
参照文献[3]选取实验室内8 份抗体筛选阴性的B 型血标本,初筛1 ∶8稀释后血清与患者反定型A 细胞,1 000 g离心15 s 凝集达到4+混合备用。
1.3.4 人源抗-A 血清的质量验证
参照文献[4]采用试管法对上述制备的人源化抗-A 血清的抗体效价进行测定。
1.3.5 唾液血型物质检测
参照文献[5]采集患者及其次子的唾液10 mL,经离心、煮沸、再离心收集上清液,加入标化后的单克隆抗体试剂,中和后与相应红细胞反应,观察结果并记录。
1.3.6 吸收放散试验
参照文献[6],结合IgM 类抗体的性质进行冷吸收和热放散。 先证者及其次子在冷吸收时均同时采用上述试验制备的人源化抗-A 血清、标化的商品化单克隆抗-A 试剂及未标化的商品化单克隆抗-A 试剂进行试验,同步吸收,以检测用于吸收的抗体试剂的吸收能力。 同时使用新鲜O 型红细胞作为阴性对照与先证者及其次子的红细胞做平行试验。
1.4 基因测序
经与患者及家属沟通,除先证者次子外,其他家属尚未同意,故家系调查仅采集次子血样及先证者血样,委托中济万泰生物医药有限公司代为进行ABO 基因测序。
2 结果
2.1 血清学试验
2.1.1 ABO 血型鉴定、唾液血型物质、意外抗体筛查结果
先证者盐水试管法ABO 血型鉴定立即离心,正定型为O 型Rh D 阳性,反定型Ac 管镜下可见凝集;将试管置于4℃1 h 后可见Ac 管凝集增强,先证者血浆与Oc 及自身红细胞均无凝集。 先证者次子盐水试管法ABO 血型鉴定立即离心,正定型为B 型Rh D 阳性,反定型为B 型;将试管置于4℃1 h 后未见凝集强度增强,其血浆与Oc 及自身红细胞均无凝集,结果见表1。 先证者及其次子盐水抗人球蛋白法不规则抗体筛查结果均为阴性,结果见表2。

抗-A抗-B抗-D抗-A1抗-A,BAcBcOc自身对照唾液血型物质先证者IS004+00±2+s00H 物质4℃1 h004+--2+3+--次子 IS04+4+04+2+000B 物质4℃1 h04+4+--2+0--H 物质
2.1.2 抗-H 检测
先证者及其次子红细胞与抗-H 反应,见表3。

先证者 次子正常B细胞对照正常O细胞对照正常A细胞对照抗-H4+w3+1+s4+1+
2.1.3 人源化抗-A 血清的质量验证
参照文献[4]对制备的人源化抗-A 血清的抗体效价和意外抗体筛查进行鉴定,其效价>64,意外抗体筛查试验结果为阴性,符合试验要求。
2.1.4 吸收放散试验
先证者及其次子的红细胞经人源化抗-A 及标化的商品化单克隆抗-A 试剂吸收并放散后,放散液均与标准A 细胞反应,证实先证者及其次子的红细胞表面存在A 抗原;先证者及其次子的红细胞经未标化的单克隆抗-A 试剂吸收并放散后,与标准A 细胞反应未产生凝集现象。 阴性对照O 细胞经人源化抗-A、标化的单克隆抗-A 及未标化的单克隆抗-A 吸收后的放散液与标准A 细胞均不反应,见表4。

人源化抗-A 标化单克隆抗-A 未标化单克隆抗-A先证者2+2+0次子2+2+0阴性对照(O型红细胞)0 0 0末次洗涤液000
2.2 基因测序结果
委托中济万泰生物医药有限公司对其测序后发现,先证者及其次子A等位基因在A102(基因测序模板A102 在A101 基础上发生467 C>T 的错义突变)的基础上,第7 外显子发生767 T>C 的错义突变,导致多肽链第156 位(467 C>T 的错义突变)发生脯氨酸被亮氨酸替换、第256 位氨基酸发生异亮氨酸被苏氨酸替换,见图1。 综合基因测序结果先证者的基因型为AEL05/O01,其次子基因型为AEL05/B101,检索ISBT 官网[7],先证者的ABO 血型基因型ISBT 命名为ABO∗AEL.05//ABO∗O.01.01,其次子基因型ISBT 命名为ABO∗AEL.05//ABO∗B.01.01。
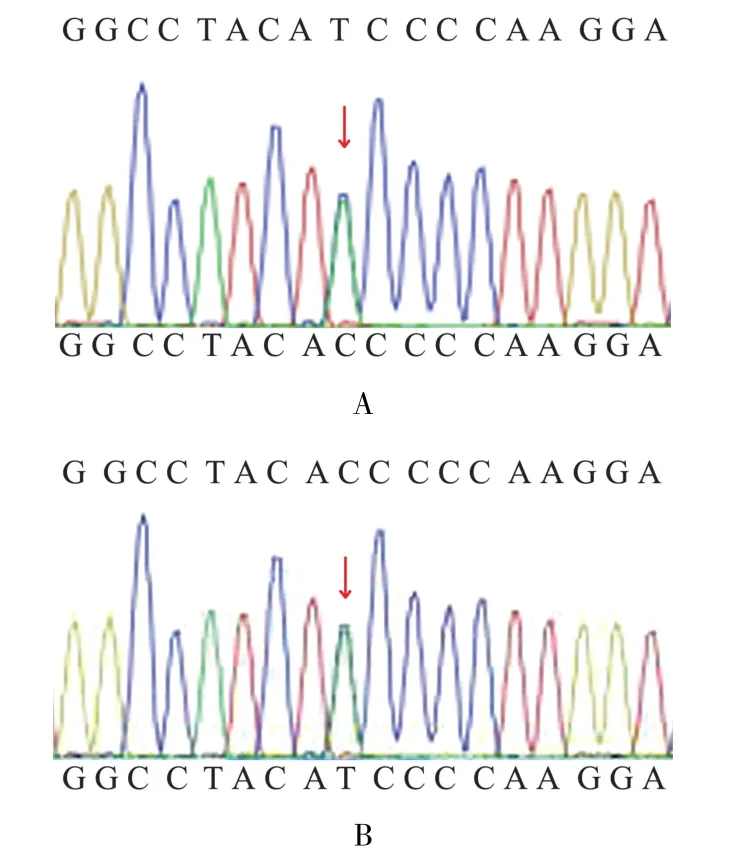
3 讨论
ABO 亚型是指红细胞或分泌液所含A 或B 抗原量不同的表现,是由基因变异而形成的。 ABO 亚型在临床工作中通常因血型正反定型不符而被发现[2]。 临床上较为常见的A 亚型按红细胞上A 抗原决定簇数量下降依次分为A1、A2、A3、Ax、Aend、Am、Ael 亚型等[8]。 大多数Ael 等位基因的先证人群为亚洲人, Ael 在人群中频率较低且存在差异,报道显示韩国约0.001%、日本约0.004 9%[9]。 Ael 血型亚型在我国人群表达概率约为八万分之一[9], 约为Rh 阴性血型的千分之一。
ABO 基因位于人类染色体9q34,全长19.5kb,由7 个外显子组成,长度超19.5kb,共编码354 个氨基酸。 其开放阅读框主要位于第6、7 号外显子,编码酶催化区,也是决定ABO 基因产物糖基转移酶功能的主要区域。 本案例中先证者及其次子经基因测序发现特征性突变位点均位于第7 外显子,为467 C>T、767 T>C 杂合突变,证明患者的这一特征性突变已遗传至下一代,符合ABO 亚型必须具有遗传学基础的特点[3]。 767 位碱基发生的T>C 突变可能导致α-1,3-N-乙酰半乳糖胺基转移酶的稳定性降低,从而使A 抗原表达减弱,形成Ael 亚型[10-12]。
现已报道的Ael 亚型等位基因共有12 种[13],检索血型抗原基因突变数据库, 767 位碱基突变只有Ael05 等位基因, 其他等位基因未发现在767 位发生突变,Ael05 型最早在我国被报道,并且主要发生在我国[13]。
利用基因测序的方法检测ABO 血型基因是目前血型鉴定的金标准[14],但由于价格、试验设备、试验场地、人员等条件限制,基因测序无法在基层医院开展,而吸收放散试验因无需特殊仪器设备、简单易学等优点适合基层医院开展。
有文献报道,在吸收放散试验中使用单克隆抗血清吸收并放散后检测不到相应抗原,需使用人源抗血清吸收放散才能检出[3],而人源化抗血清制备繁琐,并且需要鉴定抗体效价、抗体亲和力等指标,给吸收放散试验带来不便。 在本次吸收放散试验中同时使用人源化抗-A 血清、未经标化的单克隆抗-A 试剂以及标化的单克隆抗-A 试剂与患者及其次子的红细胞做平行试验,试验结果显示,未经标化的单克隆抗-A 试剂与红细胞吸收后,其放散结果为阴性,而人源化抗-A 血清及经标化的单克隆抗-A 试剂与红细胞吸收后,放散结果均为阳性。 此外,在本次试验中使用的是经标化的单克隆抗体试剂,目的是尽量避免商品化单克隆抗体试剂效价过高或放散液中的抗原量、唾液中的血型物质含量过低,而产生的前带现象,使试验结果产生假阴性。 本次试验发现的未经标化的单克隆抗体做吸收放散试验漏检弱抗原事件是偶然现象还是规律,其原因及影响因素尚需进一步试验验证。
吸收放散试验在血型抗体减弱或缺乏导致正反定型不符的血型鉴定中发挥重要作用[15]。 此外,吸收放散试验在亚型的鉴定[2,5,8]、类抗体的检测[16]、高效价冷凝集素标本的处理[17]中具有重要临床意义,其具有简单易学、无需特殊仪器设备及试剂等众多优点,非常适合基层医院开展。 正确、熟练、灵活应用吸收放散试验可大大提高血型鉴定结果的准确性,提高临床用血的安全性和科学性,避免血液资源的浪费。
