扩张型心肌病左心室辅助装置植入术后脑出血一例
2024-03-04位艳伟张云强田树光韩丽宋昱
位艳伟 张云强 田树光 韩丽 宋昱
300450 天津,泰达国际心血管病医院心衰科(位艳伟、张云强、田树光),医务部(韩丽),CCU(宋昱)
1 病例资料
患者男性,66岁,因“间断胸闷气短10年,加重9 h”于2020年9月12日入院。患者入院前10年出现活动后胸闷气短,休息后可缓解,当地医院诊断“扩张型心肌病、心力衰竭”,于3年前行心脏再同步治疗除颤器(CRT-D)治疗。2020年1月7日开始,患者因活动后呼吸困难加重,活动耐量下降,伴乏力、纳差、恶心、下肢水肿,反复住院10余次。此次经外院规范抗心力衰竭药物治疗后仍有活动后气短、阵发心悸伴呼吸困难,入院前9 h突发呼吸困难、端坐呼吸急诊来院。既往无高血压、糖尿病、高脂血症病史;吸烟40年,少量饮酒40年。查体:脉搏80次/min,呼吸22次/min,血压97/50 mmHg,体质指数21.8 kg/m2,体表面积1.73 m2。高枕卧位,神志清楚,颈静脉怒张,肝颈静脉回流征阳性。双肺呼吸音粗,双肺下野可闻及湿啰音。心界向两侧扩大,心律齐,二尖瓣听诊区可闻及收缩期吹风样杂音。腹软,无压痛、反跳痛,肝大,肋下2 cm,剑突下未及,脾肋下未及。双下肢凹陷性水肿。实验室检查(参考范围):N末端B型利钠肽原5 484 pg/ml(0~125 pg/ml),D-二聚体1.40 mg/L(0~0.50 mg/L),肌酐125 μmol/L(30~106 μmol/L),总胆红素22.8 μmol/L(1.7~20 μmol/L),直接胆红素9.4 μmol/L(0~6.8 μmol/L),间接胆红素13.4 μmol/L(3.4~17.1 μmol/L)。血、尿、便常规,血脂、电解质、肌酸激酶同工酶、肌酸激酶、肌红蛋白、肌钙蛋白、甲状腺功能等无明显异常。超声心动图示左心室舒张末内径90 mm,左心房前后径51 mm,右心房左右径35 mm,左心室射血分数24%,肺动脉收缩压73 mmHg,下腔静脉内径22 mm;室间隔、左心室壁运动不同程度减低,二尖瓣前叶脱垂并中-大量反流,考虑腱索断裂;左心室舒张功能、收缩功能减低,重度肺动脉高压。心电图示窦性心律,心房感知心室起搏,完全性左束支传导阻滞,QRS时限161 ms。胸部X线片示心影增大,肺淤血(图1A)。头颅CT示双侧基底节区及半卵圆中心散在腔隙灶。冠状动脉CT血管成像未见异常。颈部血管、下肢血管超声未见异常。考虑患者扩张型心肌病,终末期心力衰竭,纽约心脏病协会(NYHA)心功能分级Ⅳ级,美国国立卫生研究院-各机构间机械辅助循环支持协会(INTERMACS)心力衰竭分级2级,慢性心力衰竭患者预后评估(MAGGIC)1年死亡率26.9%,有左心室辅助装置(left ventricular assist device,LVAD)植入治疗指征,无禁忌证。经药物治疗改善心功能后,于2020年9月22日成功行LVAD植入术(转速:2 400 r/min,流量:3.25 L/min,功率:3.62 W)+二尖瓣成形术+三尖瓣成形术。术中取心内膜活检(左心室心尖部)显示,心肌细胞变性、肥大、核大、深染,间质纤维组织增生,少量慢性炎症细胞浸润(图2)。术后应用肝素桥接华法林抗凝、阿司匹林抗血小板聚集、沙库巴曲缬沙坦钠片适当降压等治疗,控制平均压70~80 mmHg、国际标准化比值(INR)2.0~2.5,术后1个月恢复顺利。但在LVAD植入术后36 d,2020年10月28日约凌晨2:00患者梦醒后出现右侧头痛;晨起感视物模糊,伴乏力,神志清楚,精神欠佳;6点测血压96/78(84) mmHg,脉搏84次/min,体温36.0℃,呼吸19次/min。查体左眼颞侧、右眼鼻侧视野缺失,急查头颅CT示右侧顶枕叶脑出血(出血量约15 ml)(图3A)。患者同向偏盲,诊断急性右侧顶枕叶脑出血,立即停用华法林和阿司匹林,强化降压治疗,严格控制平均压65~70 mmHg,给予降颅压、利尿等内科保守治疗,同时保证全身血液灌注,避免体位性低血压、少尿、末梢凉情况发生。29日晨患者出现嗜睡,仍有头疼、乏力不适,偏盲症状减轻,左眼颞侧、右眼鼻侧45°视野较前恢复。30日复查头颅CT示右侧顶枕叶团块状及线样高密度影较前增大,出血量约22 ml,周围片状水肿带范围较前增大,继续脱水、降颅压治疗。31日头颅CT示右侧顶枕叶团块状及线样高密度影较前稍缩小,出血量约20 ml,水肿带范围较前稍缩小。本例患者LVAD植入术后,存在泵内血栓及栓塞高风险,经我院多学科讨论后决定,于11月1日00:28即出血后第3天给予华法林1 mg口服抗凝治疗,控制平均压65~70 mmHg、INR 2.0~2.2。患者全身灌注良好,精神好转,乏力不适逐渐好转,当日15:00复查INR 1.61,为防止出血范围扩大,调整平均血压目标为60~65 mmHg,22:00再次给予华法林1 mg口服,同时给予肝素钠静脉泵入桥接治疗,监测活化部分凝血活酶时间(APTT)目标为45~50 s。2日患者头疼、乏力、嗜睡不适同前,左侧视野范围较前好转,头颅CT示右侧顶枕叶团块状及线样高密度影较前无著变,出血量约20 ml。患者出血量及水肿范围未再扩大,上调平均压目标为65~75 mmHg。3日患者症状好转,左侧视野范围较前扩大。9日患者已无乏力、头疼、嗜睡等不适,左侧视野较前无明显变化,复查头颅CT示右侧顶枕叶团块状高密度影较前缩小、边缘较前模糊,出血量约9 ml,水肿带范围较前缩小。12月23日复查头颅CT示右顶枕叶出血基本吸收、局部软化灶形成(图3B)。患者LVAD植入术后1个月还曾出现发热,PET-CT检查考虑纵隔感染,行心包、纵隔探查及引流管置入术,术后抗感染、纵隔冲洗引流、胸部切口处持续负压吸引,并定期换药后好转;此外,术后早期偶有鼻黏膜出血,量少,局部压迫可止血。患者于2020年12月17日出院,出院后规律服用华法林、螺内酯、沙库巴曲缬沙坦、美托洛尔,院外应用远程心电监护,每日监测生命体征及LVAD机械参数,维持血压、抗凝、参数稳定。3个月后随访,超声心动图示左心房收缩末期内径41 mm,左心室舒张末期内径76 mm,左心室射血分数33%,NYHA心功能分级Ⅰ级,体力耐量良好;术后6个月随访,患者视野已完全恢复,神经系统查体未见异常;术后1、2和2.5年随访,患者均无不适,右心房、心室大小正常,右心功能正常,左心房收缩末期内径波动在41~47 mm,左心室舒张末期内径波动在85~88 mm,左心室射血分数波动在19%~27%,NYHA心功能分级Ⅰ级,2023年2月24日复查胸部X线片示心影较前缩小,肺淤血较前改善(图1B),平均压控制在65~70 mmHg,INR控制在2.0~2.5,病情稳定,未发生再次感染及出血、右心衰竭、泵血栓形成、泵机械故障、心律失常、主动脉瓣关闭不全等并发症。患者应用LVAD耐受良好,生命体征稳定,未再因心力衰竭加重住院,生活质量明显提高。

A:此次入院时示心脏再同步治疗除颤器植入术后,心影增大,肺淤血;B:2023年2月24日复查时示心影较前缩小,肺淤血较前改善
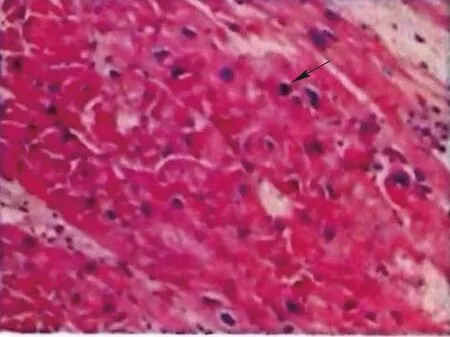
取材左心室心尖部,大小1.6 cm×0.8 cm×0.2 cm,剖面浅褐色,质软;心肌活检病理示心肌细胞变性、肥大、核大、深染,间质纤维组织增生,少量慢性炎症细胞浸润(箭头所示)
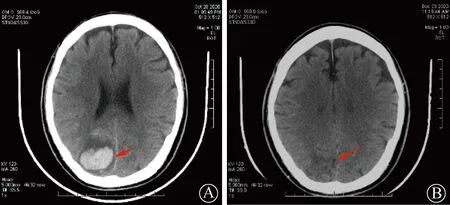
A:2020年10月28日示右侧顶枕叶脑出血,出血量约15 ml(箭头所示);B:2020年12月23日复查时示右侧顶枕叶出血基本吸收、局部软化灶形成(箭头所示)
2 讨论
目前,LVAD植入术已从最初心脏移植前的过渡治疗,逐渐成为终末期心力衰竭患者的最终治疗手段。我国心室辅助装置目前处于起步阶段,本病例中患者使用的LVAD是由泰达国际心血管病医院和中国运载火箭技术研究院联合开发的最新一代磁液双悬浮离心式LVAD(HeartCon),已于2022年7月13日上市,截至2023年12月1日已完成129例患者植入。颅内出血是LVAD植入术后最严重的并发症之一。一项关于全世界LVAD植入术后颅内出血的荟萃分析显示,其发生率高达23%,其中58.6%为脑实质出血,总体死亡率高达49.3%;阿司匹林联合华法林是LVAD植入术后最常用的抗栓治疗方案[1]。LVAD植入术后脑出血具有发病急、高致残率、高死亡率的特点,需紧急治疗,因此合理控制血压、把握重启抗栓治疗时机至关重要。
2.1 LVAD植入术后脑出血的血压管理
LVAD植入术后脑出血的血压控制目标尚无统一标准。国际心肺移植协会(ISHLT)指南建议,使用非搏动式机械循环支持装置的患者平均动脉压(mean artery pressure,MAP)目标≤80 mmHg[2]。脑出血急性期常合并高血压,血压升高与血肿扩大、脑水肿加重、死亡等不良预后密切相关,早期强化降压对防止出血量进一步扩大有益;脑出血的复发风险很高,Santos等[3]的队列研究中其复发率为14.6%,Cho等[4]的报道中复发率高达23.5%,而降压治疗可明显降低脑出血复发风险。LVAD植入术后患者与一般患者的脑出血后降压治疗方案有所不同,一项搏动性LVAD模型研究报告了脑出血时患者的血压水平,平均收缩压范围为92~102 mmHg,平均舒张压范围为59~61 mmHg[5]。本例患者LVAD植入术后控制MAP范围在70~80 mmHg,发生脑出血后给予强化降压治疗,早期严格控制MAP在60~65 mmHg,同时保证重要脏器血液灌注,有效减少了出血量,缩小了血肿扩大范围。患者脑出血吸收后,远期MAP控制目标为65~70 mmHg。经过精准强化降压治疗,本例患者的脑出血控制,预后良好,未遗留后遗症且未再复发脑出血。
2.2 LVAD植入术后脑出血恢复抗凝和抗血小板治疗方案
国内外关于LVAD植入术后脑出血抗栓治疗的恢复时机尚无统一标准,多项研究关于恢复抗凝和抗血小板治疗方案的报道也不一致。有研究指出恢复抗凝的平均时间由6.8至10.5 d不等[1],也有研究提出脑出血后恢复抗凝时间为6 d和14 d[3-4]。恢复抗凝治疗后INR目标也有所不同,Lai等[6]和Cho等[4]将INR目标定为2.0~3.0,而Ramey等[7]则根据情况使用1.5~2.5或2.0~3.0,Santos等[3]使用了1.9~2.5。本例患者LVAD植入术后,持续机械循环支持,存在栓塞高风险,于脑出血后第3天开始低剂量华法林抗凝治疗,控制INR范围在2.0~2.2。
抗血小板治疗恢复需要充分权衡药物引起的再出血风险及未用药时的栓塞风险。Wilson等[8]提出抗血小板药物恢复的平均时间为6 d,Santos等[3]认为抗血小板药物恢复的平均时间从6 d到7.2 d不等,这可能是因为医生在恢复引起脑出血范围扩大的抗凝药物之前更愿意恢复抗血小板药物。尽管在脑出血后14 d内恢复抗血小板药物后再使用抗凝药物是安全有效的,但并未提出具体恢复时间。Cho等[9]指出30 d可能是一个更合理的恢复的窗口期,因为抗血小板药物及抗凝药物恢复后脑出血复发时间为7 d,而恢复后发生缺血性事件的时间为373 d。这表明脑出血复发导致的死亡风险在短期内较高,应接受血栓栓塞事件的风险,以尽量减少再出血。LVAD植入术后患者使用抗血小板药物的必要性尚需要进一步的前瞻性研究来确定。本例患者恢复华法林抗凝治疗后,未再启用抗血小板药物治疗。
本例患者LVAD植入术后需长期服用抗凝药物,出现脑出血并发症后应立即停用抗凝药物,因此治疗方面存在明显冲突;且患者存在高龄等危险因素,临床处理上尚无相关指南及专家共识可提供指导;通过内科保守治疗,脑出血急性期大胆强化降压治疗,MAP控制目标达60~65 mmHg,于术后第3天积极重启华法林抗凝治疗,INR控制标准低限2.0~2.2,在多学科协作下,患者逐渐痊愈且随诊2.5年未再复发脑出血及出现其他并发症,为临床上此类患者的处理提供了一定的参考。
利益冲突:无
