左心室辅助装置联合短期右心室辅助治疗巨细胞心肌炎一例
2024-03-04曹亚琼任海波
曹亚琼 任海波
430056 武汉科技大学附属武汉亚心总医院重症医学科 武汉科技大学医学部医学院
1 病例资料
患者女性,52岁,因“胸闷、胸痛4 d,呼吸、心脏骤停1 d”于2022年7月14日入院。患者入院前4 d突感胸闷伴背部疼痛,疼痛持续不缓解至当地医院就诊。次日突发反复室性心动过速,血压无法测出,予以心肺复苏、气管插管、体外膜氧合(extracorporeal membrane oxygenation,ECMO)+主动脉内球囊反搏(intra-aortic balloon pump,IABP),大剂量血管活性药物维持,患者既往有干燥综合征病史十余年,初步诊断“暴发性心肌炎”,转入我院。入院后查血肌钙蛋白T:14 210 ng/L,血清白蛋白:25.9 g/L,血清总胆红素:43.3 μmol/L,丙氨酸氨基转移酶:116 U/L,血清直接胆红素:29.8 μmol/L。肾小球滤过率:39 ml/min,血清肌酐:134 μmol/L。心电图示心室扑动。超声心动图示主动脉瓣未见开启,左心室射血分数15%,右心室射血分数(right ventricular ejection fraction,RVEF)28%,三尖瓣环收缩期移位(tricuspid annular plane systolic excursion,TAPSE)0.9 cm。入院后患者持续出现恶性心律失常,左心房压力高,主动脉瓣无法打开,行房间隔造口术减轻左心压力,术后继续ECMO+IABP+呼吸机辅助。多次复查超声心动图示主动脉瓣不能开放(图1A),考虑为心肌收缩力差且ECMO使左心室后负荷增加所致。左心室及主动脉根部血流云雾影(图1B),ECMO无法撤机,持续呼吸机辅助,连续肾脏替代治疗(continuous renal replacement therapy,CRRT)及支持治疗。8月3日冠状动脉造影示右冠状动脉近段狭窄10%,前降支中段狭窄20%,回旋支通畅(图2)。考虑美国国立卫生研究院-各机构间机械辅助循环支持协会(INTERMACS)心力衰竭分级[1]1级,决定行左心室辅助装置(left ventricular assist device,LVAD)植入术,但其右心功能不全,TAPSE<1.5 cm,右心室面积变化分数(right ventricular fractional area change,RVFAC)20%~25%,EUROMACS右心衰竭积分[2]9.5分,属高危,术后右心衰竭可能性大,需术中评估是否同期行右心室辅助装置(right ventricular assist device,RVAD)植入。患者于8月7日全麻下行LVAD植入+RVAD植入+房间隔修补+左心耳夹闭+IABP撤出+心脏表面临时起搏器安置(术中因考虑患者存在右心功能不全,决定行RVAD植入)。RVAD使用ECMO,于右心房置入19#静脉导管(美敦力),使用8#GORE-TEX人工血管与主肺动脉端侧吻合,将17#动脉导管(美敦力)插入人工血管并固定,动静脉插管经剑突下穿出皮肤后连接ECMO(图3)。LVAD采用苏州同心医疗慈孚®VAD,植入后顺利脱离体外循环,中心静脉压(central venous pressure,CVP)12~15 cmH2O,肺动脉压45/28 mmHg,计算肺动脉脉动指数1.13,且超声心动图示RVFAC 20%,予以肾上腺素、去甲肾上腺素维持循环。术中心肌病理活检示巨细胞心肌炎(giant cell myocarditis,GCM)(图4)。术中管理:控制体外循环时间和心肌保护,LVAD植入后先低流量运行(图5),当心跳自动复律为交界性心律时,再将LVAD吻合,使用经食管超声心动图指导滴定转速,装入临时起搏器,逐渐调大LVAD流量至4~4.5 L/min,RVAD流量3 L/min,仔细检查,减少右心压迫可能。术后管理:心脏辅助装置植入后,每日监测TAPSE(图6),右心与左心容积之比,室间隔位置,用来调整左右心辅助流量,术后复查超声心动图均未见主动脉瓣开放。术后早期LVAD流量4~4.5 L/min,RVAD流量3 L/min,平均动脉压(mean arterial pressure,MAP)可维持在80 mmHg左右,但CVP持续12~14 cmH2O,下腔静脉宽度2.2 cm,呼吸无变异度,予CRRT脱水后改善不明显,考虑左右心不匹配,右心容量负荷过重,逐渐下调LVAD转速,维持流量在3.5~4 L/min,MAP 70 mmHg左右,并继续予CRRT脱水,CVP逐渐下降。针对右心功能不全,选用增强心肌收缩力而不增加右心后负荷的药物;使用CRRT控制出量,根据CVP、下腔静脉宽度调整出入量,逐渐降低CVP,维持CVP 6~8 cmH2O,使液体量达到负平衡,直到“干体重”,同时避免患者容量不足;呼吸机辅助期间吸入一氧化氮,扩张肺血管,减轻右心后负荷。术后第9天拔除气管插管,术后第11天复查超声心动图示TAPSE 1.2 cm,RVEF 40%,CVP 5 cmH2O,下腔静脉1.3 cm,变异度>50%,无正性肌力药,考虑右心功能较前改善,逐渐缓慢下调RVAD流量至1 L/min,超声心动图、血流动力学、CVP及内环境参数无明显变化,考虑可撤离RVAD。术后第13天入手术室行RVAD撤除术。术后CVP 10~12 cmH2O,TAPSE 1.0 cm,RVFAC 30%,下腔静脉2.4 cm,变异度<18%,小剂量血管活性药物维持血压。考虑患者右心功能仍较差,结合患者氧代谢,再次下调LVAD转速,维持流量3.2~3.5 L/min,MAP 65~70 mmHg,并继续予负平衡,CVP逐渐下降至6~8 cmH2O。二次术后第2天拔除气管插管。术后第37天肝功能恢复正常,术后第63天肾功能基本正常,术后第91天患者顺利出院。术后6个月随访,患者纽约心脏病协会(NYHA)心功能分级Ⅰ级,6 min步行距离420 m,超声心动图示TAPSE 1.5 cm,RVEF 45%。
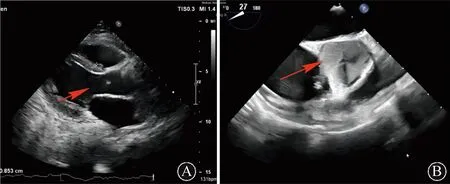
A:主动脉瓣未见开启(箭头所示);B:左心室及主动脉根部血流云雾影(箭头所示)

A:前降支中段狭窄20%(箭头所示);B:回旋支通畅;C:右冠状动脉近段狭窄10%(箭头所示)

图3 双心室辅助示意图
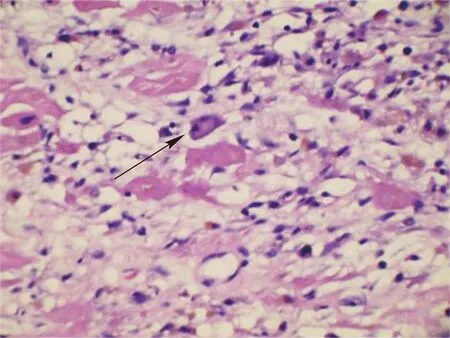
弥漫性单核细胞浸润,心肌细胞坏死,间质水肿、纤维化,可见典型巨细胞(箭头所示)

A:左心室辅助装置目标转速与实时转速的关系图;B:实时左心室辅助与左心流量的动态变化图

MAP:平均动脉压;CVP:中心静脉压;TAPSE:三尖瓣环收缩期移位
2 讨论
心肌炎是由感染、自身免疫、药物等多种因素所引发的一种心脏炎症,而GCM是由自身免疫所致,属于暴发性心肌炎的特殊类型,是一种病情凶险、并发症多、病死率高的心脏急症。
暴发性心肌炎血流动力学不稳定,难以通过血管活性药物维持,而器械治疗心肌炎的存活率为57%~80%[3],其临床症状不典型,早期诊治对改善预后有重要意义[4]。本例患者初始考虑为急性心肌梗死,但行冠状动脉造影未见明显阻塞,初步考虑诊断为暴发性心肌炎,经术中病理活检后可明确诊断为GCM。在多中心GCM患者记录中,75%的患者表现为迅速进展的充血性心力衰竭[5],除非进行机械支持或心脏移植,否则死亡率很高[6]。
LVAD是严重心力衰竭的重要生命支持装置,LVAD期间右心衰竭是死亡的重要原因,虽然LVAD植入后可显著减轻左心室压力,从而减轻左心房压力和肺动脉压力,有效改善二尖瓣反流,但与植入前相比,左心排血量增加,右心静脉回流急剧增加,右心室室壁压力增加,约15%~40%的患者发生右心衰竭,最终导致灌注不足、终末器官功能障碍,增加了LVAD患者的死亡率[7-8]。一项回顾性研究发现,与轻度或中度右心衰竭患者相比,无右心衰竭患者3个月的累积死亡率较低[9]。因此,应重视LVAD患者右心衰竭的治疗和预防。本例患者出现心原性休克后,予以ECMO+IABP辅助近1个月,心功能仍不能恢复,同时合并多器官功能衰竭,存在心脏移植禁忌证,此时LVAD是唯一可行的治疗方案,可避免长时间ECMO+IABP辅助导致的血液破坏、感染等风险,恢复器官灌注,改善患者预后,但围术期右心衰竭风险极高。
术前对右心衰竭进行预测,EUROMACS右心衰竭积分[2]是LVAD植入后并发右心衰竭的预测工具,为以下变量之和:右房压/肺毛细血管楔压>0.54(2分),血红蛋白<10 g/dl(1分),多种静脉正性肌力药物(2.5分),INTERMACS心力衰竭分级1~3级(2分),术前超声心动图示严重右心室功能障碍(2分),低危组考虑0~<2分,中危组考虑2~≤4分,高危组考虑>4分。中危和高危组的患者有较高的住院死亡率。术中因素也会影响右心功能,长期体外循环,冠状动脉旁路移植或侧支损伤,植入期间血液制品输注也可进一步增加右心衰竭风险[10]。容量复苏可导致较大的液体波动从而加重右心室扩大及三尖瓣反流。在有创血流动力学监测中,CVP和MAP应被注重用于右心衰竭预测(考虑到连续泵的特点,MAP是最好的灌注压测量方法,适当的MAP对患者至关重要)[11],以及右心室与左心室容积之比、肺动脉收缩压也可用于预测右心衰竭[12-13]。
在持久LVAD后右心衰竭的治疗需关注四大方面:(1)心室容积管理和心室前负荷优化;(2)减少后负荷;(3)改善心室收缩状态;(4)优化心律:在心脏手术后的重症监护中,通常需要临时起搏器以确保最佳心房刺激[14-15]。国内暂无RVAD专用设备,术者使用右心房-肺动脉插管ECMO行右心室辅助,此过程需在开胸状态下完成,术前及术中需仔细评估右心功能,及时行双心室辅助(biventricular assist),避免术后出现右心功能不全再次开胸手术行延迟双心室辅助。双心室辅助期间,重点关注左右心匹配,LVAD流量过低可导致左心室引流不充分,流量过高则导致右心回心血量过多,因此需根据超声心动图、机体氧代谢动态调整流量。术后早期在左心引流充分及满足机体氧代谢前提下适当减少LVAD流量,可避免高流量导致的容量负荷过重。右心功能不全时应结合扩血管药物、改善心肌顺应性使CVP维持在较理想的状态。肺动脉压过高对右心有较大的影响,肺动脉高压的治疗可分为两个阶段:围术期和术后慢性维持(术后30 d),尤其在术后即刻优化右心室前负荷、后负荷以及心肌收缩力。由于LVAD速度的增加导致LVAD流量线性增加,脉压变窄,较高的速度会导致血流不稳定、左心室塌陷、左心室流量和心脏指数急剧下降。而一氧化氮可引起肺血管平滑肌舒张,降低肺血管阻力和左心室扩张,提高左心室流量、心脏指数和左心室直径,增加右心室射血量,促进左心室充盈,改善左心室功能。研究显示,一氧化氮和PDE5抑制剂在LVAD植入术后预防右心衰竭方面具有一定的应用价值[15-16]。另有研究表明,左西孟旦治疗右心衰竭是安全有效的,可显著降低肺动脉压和收缩期容积,而心脏指数、射血分数、混合静脉氧饱和度明显升高[17-18]。
GCM合并心原性休克预后差,LVAD对此类患者具有支持效果,能帮助他们渡过急性期,但右心衰竭仍是其死亡的重要原因,解决LVAD合并右心衰竭仍面临许多挑战。本例患者GCM合并心原性休克,并且随着疾病进展合并多器官功能衰竭,加之患者既往有干燥综合征病史,整体治疗上除手术本身难度大以外,术后的右心管理也至关重要。应对此类患者综合管理,全方位多系统协调治疗,及早确定正确的治疗方案,降低患者死亡风险,从而提高临床疗效。
利益冲突:无
