国标法和新型试剂盒法测定维B12 含量的方法比较
2024-02-29蔡晓霞吴家碧陈叶兰李诗华陈紫媚卢靖怡谢黔兰
蔡晓霞,吴家碧,陈叶兰,李诗华,陈紫媚,卢靖怡,芦 平,谢黔兰
(汤臣倍健股份有限公司,广东珠海 519040)
0 引言
维B12也叫钴胺素,是指一类具有含三价金属钴键的多环系物质,4 个被还原后的呋咯环连接在一起可转变而成的1 个咕啉大环系(与卟啉相似)化合物,为自然界唯一的含有钴金属单质子的维生素,也是人类目前所知的分子量最大、系统最复杂的维生素分子,按其溶解性分为水溶性和脂溶性维生素[1]。维B12对于人体来说非常的重要,这种元素可以帮助人体维持中枢神经系统的正常运转,也会影响到细胞间质的功能和神经胶质,以及细胞髓磷脂的人体含量。另外,维B12在部分临床疾病的治疗上发挥着重要作用,可参与制造骨髓红细胞,防止恶性贫血,防止大脑神经受到破坏等,而缺乏维B12则可能导致恶性贫血、精神抑郁、血管性痴呆及阿尔茨海默病等疾病[2]。因此,适量补充维B12,对于维持人体的健康来说非常重要,但是维B12的摄入量也不是越多越好。有研究表明,服用过量的维B12,可能导致面部浮肿、腹痛泄泻、低血钾症等。因此,对于婴幼儿配方乳品和营养补充食品中维B12的含量检测准确性要求越来越高。
目前,食品中维B12的检测方法越来越丰富[3],包括微生物法[4-6]、试剂盒法[7-9]、高效液相色谱法[10-12]、化学发光法[13]、酶联免疫法[14]等。其中,微生物法具有检测灵敏度较高、检出限低等显著优点,是目前美国、中国等许多国家采用的一种官方微生物分析方法。我国现行国家标准GB 5413.14—2010、美国政府机构的实验室、FDA 和AOAC 均采用该方法[2]。
维B12试剂盒检测方法为《GB 5413.14—2010 食品安全国家标准 婴幼儿食品和乳品中维B12的测定》的简化方法,具有简单、高效、准确度高及稳定性好的优点,主要适用于检测外添加的营养膳食补充剂的维B12含量。采用国标法和新型试剂盒法测定婴儿配方乳粉定量分析质控样品中维B12的含量,通过方法的专属性、线性、精密度和回收率对比2 种检测方法结果的差异,为实验室在乳粉类样品中维B12含量的检测提供理论依据。
1 材料与方法
1.1 材料
1.1.1 菌株和样品
标准菌株:莱氏曼氏乳杆菌,ATCC 7830,来源于广东微生物菌种保藏中心。
质控样品:婴儿配方乳粉中维B12定量分析质控样品(维B12特性值5.09 μg/100 g,满意范围为4.16~6.02 μg/100 g),购自中国检验检疫科学研究院测试评价中心,货号QC-IP-741。
1.1.2 标准品和培养基
维B12标准品:纯度≥91.3%,中国食品药品检定研究院提供;培养基:乳酸杆菌肉汤培养基,青岛高科技工业园海博生物技术有限公司提供;维B12测定培养基,美国BD 公司提供。
1.1.3 试剂盒
维B12检测试剂盒,批号RS12.170424,深圳市瑞赛生物技术有限公司提供;其组成为维B12冻干菌、维B12冻干标品、维B12测定培养基、无菌水、96 孔微孔板,封板膜等。
1.1.4 仪器与设备
AL-204 型分析天平,梅特勒-托利多科学仪器有限公司产品;BXM-30R 型立式压力蒸汽灭菌器,上海博讯实业有限公司医疗设备厂产品;UV-2600型紫外-可见分光光度计,岛津公司产品;BSC-1600-Ⅱ-A2 型生物安全柜,苏州市华宇净化设备有限公司产品;SPX-250BSH-Ⅱ型生化培养箱,上海新苗医疗器械制造有限公司产品;1~5 mL 移液枪(编号:19E62016)、100~1 000 μL移液枪(编号:16G12712),上海安谱实验科技股份有限公司产品;TGL-10C 型离心机,上海安亭科学仪器厂产品;HH-8 型水浴锅,常州普天仪器制造有限公司产品;MULTISKAN FC 型酶标仪,美国赛默飞世尔科技公司产品。
1.2 试验方法
1.2.1 标准曲线制作
(1)国标法。参考GB 5413.14—2010,配制维B12标准曲线工作液,按照标准系列管制备方法,配制0~0.440 0 ng 范围内的标准系列管,每个梯度做3 个平行。以标准系列管维B12含量为横坐标,吸光度为纵坐标,绘制国标法维B12标准曲线。
(2)试剂盒法。取出1 包试剂盒提供的维B12冻干标准品(2 板共16 孔),加入适量无菌水后,按照说明书,配制0.00,0.025,0.050,0.100,0.160,0.360 μg/100 g 系列质量浓度的标准溶液。每个质量浓度做2 个平行,培养后进行测定,以维B12标准管质量浓度为横坐标,吸光度为纵坐标,绘制维B12检测试剂盒标准曲线,该方法定量限为0.025 0 μg/100 g。
1.2.2 样品处理及测定
选取定量标准乳粉质控样品,按照GB 5413.14—2010 和试剂盒说明书对样品进行相应处理,并进一步稀释,加样并接种菌液后于37 ℃条件下培养24 h,国标法采用紫外分光光度计测定吸光度,试剂盒法采用酶标仪测定吸光度。
2 测试指标
2.1 标准曲线线性
根据测定结果拟合的标准曲线考查曲线的线性。
2.2 方法专属性
通过测定试验中培养基的本底值,以此判断培养基的本底对试验带来的影响,从而确定方法的专属性是否良好。国标方法中,以S0调零,S0+菌的OD值作为测定的培养基本底值;试剂盒方法中,以标准曲线中S1(即为空白点)的OD 值作为测定的培养基本底值。
2.3 精密度试验
分别取6 份乳粉质控样品,按照国标方法和试剂盒说明书进行样品处理,并进行适当稀释,加样并接种菌液后于37 ℃条件下培养24 h,国标法采用紫外分光光度计测定结果,试剂盒法采用酶标仪测定结果。
2.4 准确性试验
分别取9 份乳粉质控样品,分成低、中、高3 组(每组3 份),并且分别加入50%,100%,150%维B12含量的标液,按照国标方法和试剂盒说明书进行样品处理,并进行适当稀释,加样并接种菌液后于37 ℃条件下培养24 h,国标法采用紫外分光光度计测定结果,试剂盒法采用酶标仪测定结果,通过测定加标试验中维B12含量,计算回收率。
2.5 稳定性试验
选用乳粉质控样品进行稳定性试验,测试同一批样液在不同时间段的稳定性,即将样品提取液在4 ℃冰箱中贮存0,3,6,9,12,24,48 h 后,分别测试放置不同时间段的提取液中维B12的含量,比较测试结果之间的差异。
3 2 种方法的数据对比与分析
3.1 标准曲线的线性
国标法采用Labslution 绘制标准曲线,维B12质量浓度为0.044 0~0.440 0 ng/mL。
国标法维B12标准曲线见图1。
试剂盒法采用试剂盒提供的软件Elisa 制作标准曲线,维B12含量为0.025~0.360 μg/100 g。
试剂盒法维B12标准曲线见图2。

图2 试剂盒法维B12 标准曲线
由图1 可知,国标法维B12标准曲线方程为Y=16.070 0X3-16.410 1X2+6.577 59X-0.047 675 3,R2=0.996 44,相关系数R=0.998 21>0.99,即在含量为0.044 0~0.440 0 ng 范围内,曲线线性关系良好。
由图2 可知,试剂盒法维B12标准曲线方程为Y=(0.973 28-0.054 24)/[1+(X/0.168 40)-1.714 77]+0.054 24,R2=0.999 05,相关系数R=0.999 52>0.99,即在含量为0.025~0.360 ng 范围内,曲线线性关系良好,该方法定量限为0.025 0 μg/100 g。
3.2 方法专属性
国标方法中,以S0调零,测定S0+菌的OD 值3 次;试剂盒方法中,测定S1的OD 值10 次。
空白管试验结果见表1。

表1 空白管试验结果
由表1 可知,2 种方法的空白管OD 值都<0.1,但该OD 值对标液和样液的测定结果有一定的影响,因此,每次测定国标法时都以该标液空白管调零,然后再进行标准曲线和样液的紫外吸光度测定;采用试剂盒方法进行测定及结果计算时,每次都需将标准曲线和样液的OD 值扣除空白管的OD 值后进行计算。
3.3 精密度试验
分别取6 份样品,按照国标方法和试剂盒说明书进行样品处理,并进行适当稀释,加样并接种菌液后于37 ℃下培养24 h 后测定吸光度。
精密度试验结果见表2。
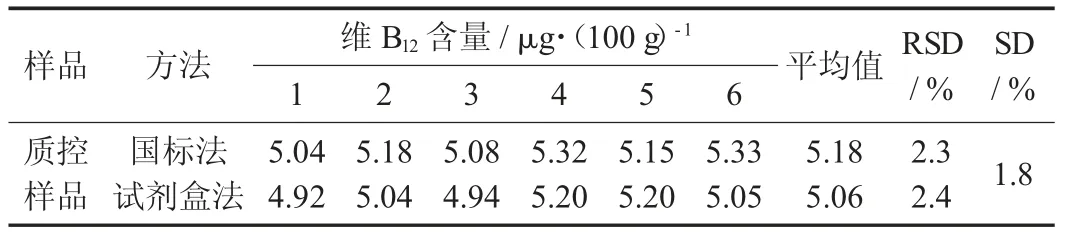
表2 精密度试验结果
由表2 可知,传统国标法测定质控样品的精密度试验结果为5.18 μg/100 g,试剂盒法测定质控样品的精密度试验结果为5.06 μg/100 g,精密度均符合《GB/T 27404—2008 实验室质量控制规范》的要求(精密度要求≤7.5%);2 种方法测定结果的偏差为1.8%<15%,对2 种方法的6 次测定结果的平均值采用F 检验(95%的置信度),F0.05(5,5)=1.02<F 表(5.05),说明2 种方法的测定结果无明显差异,表明2 种方法的精密度及重复性良好。
3.4 准确性试验
分别取9 份乳粉质控样品,分成低、中、高3 组(每组3 份),并且分别加入50%,100%,150%维B12含量的标液,按照国标方法和试剂盒说明书进行样品处理,并进行适当稀释,加样并接种菌液后于37 ℃条件下培养24 h,国标法采用紫外分光光度计测定结果,试剂盒法采用酶标仪测定结果,通过测定加标试验中维B12含量,计算回收率。
回收率试验结果见表3。

表3 回收率试验结果
由表3 可知,国标法和试剂盒法测定乳粉质控样品的回收率分别为97.3%和113.6%,符合GB/T 27404—2008《实验室质量控制规范》 的要求“GB/T 27404—2008 要求回收率为90%~120%”,2 种方法测得的回收率偏差为7.7%,偏差<10%,表明2 种方法的准确度较高。
3.5 稳定性试验
分别采用国标方法和试剂盒法对质控样品和健乐多乳清蛋白粉进行稳定性试验,测试同一批样品提取液在4 ℃冰箱贮存0,3,6,9,12,24,48 h后样品的维B12含量。
稳定性试验结果见表4。

表4 稳定性试验结果
由表4 可知,国标法和试剂盒法测定乳粉质控样品提取液放置0~48 h 后的维B12含量平均值分别为5.25 μg/100 g 和5.15 μg/100 g,2 种方法的RSD值分别为2.0%和2.8%,均小于5%,说明样品提取液于4 ℃冰箱中储存48 h 后,样液中维B12的含量稳定,2 种方法的稳定性良好。
4 讨论
试验采用GB 5413.14—2010[15]和维B12检测试剂盒测定婴儿配方乳粉中维B12定量分析质控样品中维B12的含量,2 种方法标准曲线相关系数均在0.99以上,曲线拟合度较好,培养基本底值较低,方法专属性良好;定量标准质控样品检测的结果均在满意范围内且接近特性值,结果准确;2 种方法的精密度均符合GB/T 27404—2008《实验室质量控制规范》[16]的要求,且精密度较高、重复性较好;2 种方法的回收率均符合GB/T 27404—2008《实验室质量控制规范》 的要求,且2 种方法的回收率偏差均小于10%;2 种方法的稳定性试验结果RSD 均小于5%,方法稳定性良好。
国标方法检测维B12的过程较为复杂繁琐,包括了菌株活化、传代、保藏和接种液的制备等,要严格控制菌株的活化、培养过程,保证菌株对维B12的特异性,这对实验室检测人员的技术操作水平提出了较高的要求;其次,采用国标法检测维B12含量时,需要选择合适的测定培养基,尤其需要关注培养基的本底值。本底值低,标准曲线拟合度高,线性良好是获得准确检测结果的前提;最后,采用国标法检测维B12含量时,还需要关注到所用玻璃器皿的洁净度。少量的外源物质可能导致试验的失败。因此,需要使用活性剂对硬玻璃测定管及其他必要的玻璃器皿进行清洗,清洗之后要在180 ℃以上干热灭菌2 h 以上,从而确保去除残留的微量生长因子。
试剂盒方法是基于国标方法研制的一种快速检测方法。与国标方法相比,试剂盒方法有较为明显的优势,首先,采用试剂盒方法进行样品中维B12的含量测定时,前处理使用试剂盒提供的提取液进行水浴提取,操作步骤简便,无需调pH 值,操作误差小,且样品处理时间短;其次,试剂盒方法采用的是即用型冻干菌粉,节省了每次转接菌株及制备菌悬液的步骤,保证每次试验各微孔中菌液量及活性一致[17];另外,试剂盒方法采用的是即用型冻干标准品,即将标准品按梯度固定的量以冻干粉的形态储存于微孔板中,试验时只需要将无菌水加入到每个微孔中进行吹打溶解即可,节省了每次配制标液的步骤,操作误差小,操作过程方便快捷。
另外,试剂盒方法主要用酶标仪进行标准曲线和样液的OD 值测定。1 次可测定96 个微孔的OD值,整个测定过程只需要3~5 min,非常简便、快捷,省去了国标方法中每支试管分别测定OD 值的繁杂过程。最后,对于检测纯外添加营养素的样品,试剂盒方法可以一次提取出维B12、叶酸、泛酸和生物素含量,节省了国标方法中多测提取不同营养素的过程,检测效率更高。总体而言,与传统的国标方法相比较,新型的试剂盒方法具备操作简便、检测效率高、检测结果准确的优点,这与史贇学[7]、王赢[8]、黄晓林等人[9]的研究结果基本一致。
5 结论
试验采用国标法和试剂盒方法测定婴儿配方乳粉定量分析质控样品中[9]的含量。结果表明,2 种方法的标准曲线线性均良好(R>0.99),方法的专属性良好,质控样品检测的结果均在满意范围内且接近特性值,结果准确、重复性和稳定性好,2 种方法的检测结果差异性不显著[17-18],可根据实验室的经济能力及实验室自身条件选择适当的方法进行测试。