TKI类药物治疗HER2阳性乳腺癌的疗效与安全性的Meta分析 Δ
2024-02-28徐吟雪沈晓岚陆秀芬张学会南京医科大学附属江苏盛泽医院药学部江苏苏州215228
徐吟雪,沈晓岚,陆秀芬,张学会 (南京医科大学附属江苏盛泽医院药学部,江苏 苏州 215228)
乳腺癌是全世界女性最常见的恶性肿瘤[1]。人表皮生长因子受体2(human epidermal growth factor receptor 2,HER2)过度表达在乳腺癌患者中占15%~20%[2]。HER2 过表达虽然是一个消极的预后因素,但也是抗HER2靶向治疗反应的积极预测因素,在过去几十年中,抗HER2 治疗显著提高了乳腺癌患者的生存率[2]。因此,抗HER2 靶向小分子抑制剂,如酪氨酸激酶抑制剂(tyrosine kinase inhibitor,TKI)已被研究证实对HER2阳性乳腺癌患者具有良好的治疗效果。基于TKI 类药物的治疗方案已被纳入HER2 阳性乳腺癌患者的管理中,目前已在临床实践中使用[3]。用于治疗HER2 阳性乳腺癌的TKI类药物有拉帕替尼、吡咯替尼、图卡替尼、奈拉替尼和阿法替尼,其中图卡替尼上市较晚,于2020 年在美国上市。与此同时,近年来其他的TKI类药物又有新的临床研究数据公布,但其疗效和安全性尚不明确。因此,评价TKI 类药物治疗HER2 阳性乳腺癌的疗效与安全性是十分重要的。本研究采用Meta分析的方法,系统评价了TKI类药物治疗HER2阳性乳腺癌的疗效和安全性,旨在为临床用药提供循证依据。
1 资料与方法
1.1 文献检索策略
采用主题词和自由词相结合的方法,以“乳腺肿瘤”“乳腺癌”“TKI”“ 拉帕替尼”“ 吡咯替尼”“ 图卡替尼”“奈拉替尼” 和“ 阿法替尼”为检索词,检索中国知网、万方数据库和维普网;以 “breast neoplasms”“breast cancer”“TKI”“lapatinib”“pyrotinib” “tucatinib”“neratinib”“afatinib”为检索词,检索PubMed、Cochrane Library、Embase和Web of Science数据库。检索时限均为建库至2023年4月。
1.2 文献纳入和排除标准
1.2.1 纳入标准
本研究的纳入标准包括:(1)研究对象——确诊为HER2阳性乳腺癌的患者;(2)公开发表的随机对照试验(randomized controlled trial,RCT),语种限定为中文或英文;(3)比较与干预措施——试验组患者给予含TKI类药物方案治疗,对照组患者给予不含TKI类药物的方案治疗;(4)结局指标——至少包含无进展生存期(progression-free survival,PFS)、总生存期(overall survival,OS)、客观缓解率(objective response rate,ORR)、病理完全缓解率(pathological complete response rate,pCR)及3/4 级药品不良反应(adverse drug reaction,ADR)发生率中的任一项结局指标。
1.2.2 排除标准
本研究的排除标准包括:(1)属于同一临床试验的文献,只选取信息最丰富且发表最新的文献,以免重复;(2)数据不全的RCT;(3)无主要结局指标的研究。
1.3 文献筛选与资料提取
数据提取由2 名研究人员独立进行,如遇分歧则进行讨论或寻求第三方解决。提取的文献数据包括以下内容:作者和发表年份、样本量、干预措施(试验组和对照组)、临床试验编号、结局指标。
1.4 文献质量评价
采用Cochrane 系统评价员手册5.1.0 作为文献质量评价标准,文献质量评价包括随机分配方法、分配方案隐藏、盲法的实施、结果数据的完整性、选择性报告研究结果和其他偏倚来源等方面。评价的判断包括“偏倚低风险”“偏倚风险未知”“偏倚高风险”。
1.5 统计学方法
采用RevMan 5.4.1 和Stata 17 软件进行统计分析。以χ2检验分析各研究间异质性,若P>0.1,Ⅰ2<50%,则说明各研究间无统计学异质性,采用固定效应模型进行Meta分析;反之,说明各研究间存在异质性,选择随机效应模型,并进一步行亚组分析讨论异质性来源;若找不到异质性来源,则采用描述性分析。采用敏感性分析评价结果的稳健性;采用倒漏斗图和Egger’s 检验进行发表偏倚分析[4]。
PFS 及OS 使用风险比(hazard ratio,HR)及其95%置信区间(confidence interval,CI)作为效应分析统计量。ORR 和pCR 及3/4 级ADR 发生率使用比值比(odds ratio,OR)及其95%CI 作为效应分析统计量。以α=0.05作为检验水准。
2 结果
2.1 文献筛选流程及结果
初检共获得14 179篇文献,依据上述纳入和排除标准进行筛选,最终纳入文献24篇,均为RCT,共计15 538例患者,其中试验组8 024 例,对照组7 514 例。具体筛选流程图如图1。

图1 文献筛选流程图
2.2 纳入研究基本特征
纳入文献的基本特征如表1所示,其中16项RCT的试验组使用拉帕替尼[5—20],2 项RCT 的试验组使用奈拉替尼[21—22],1 项RCT 的试验组使用图卡替尼[23],1 项RCT的试验组使用阿法替尼[24],4 项RCT 的试验组使用吡咯替尼[25—28]。
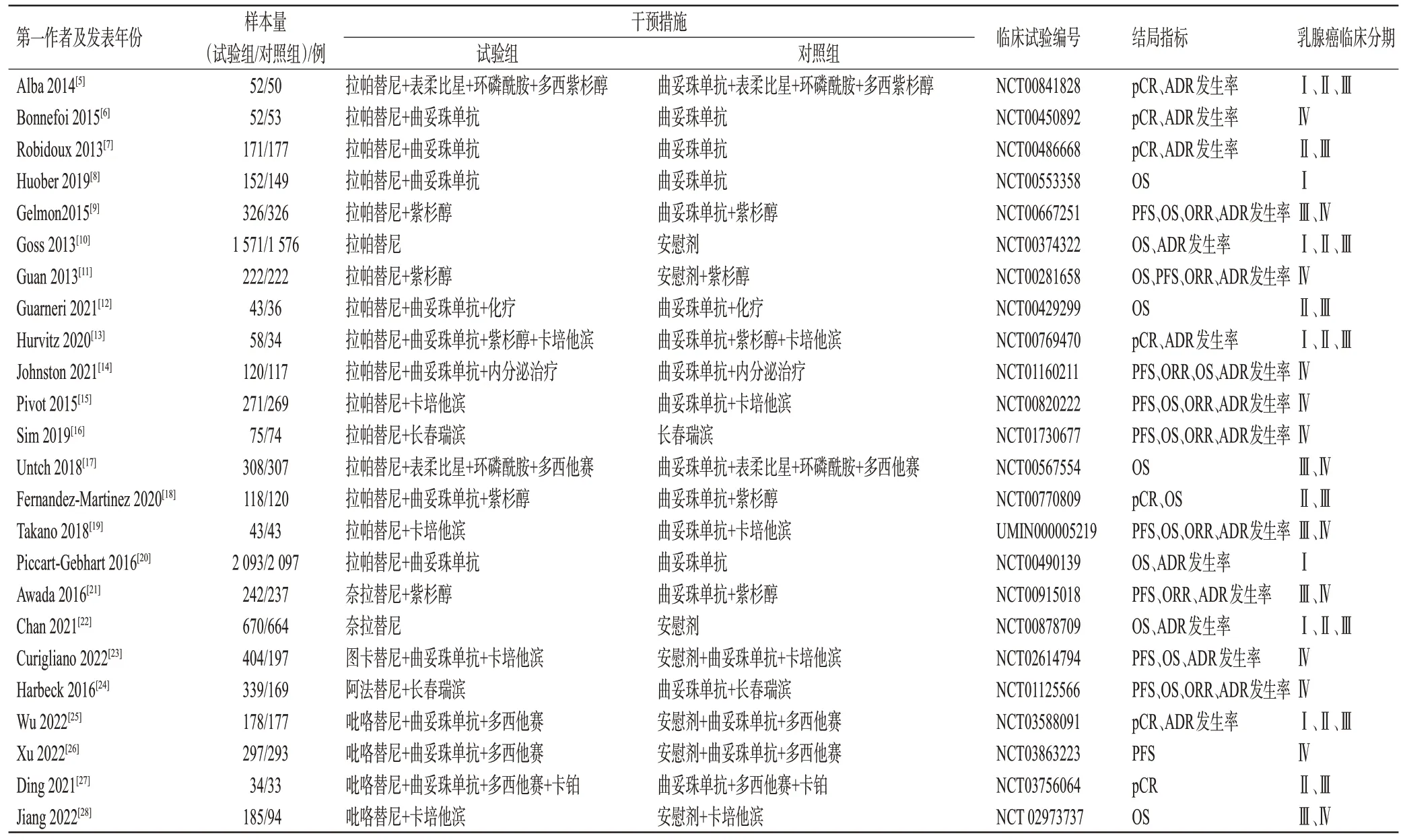
表1 纳入研究的基本特征
2.3 纳入研究的质量评价
24项研究均为RCT;所有研究的随机分配方法均是低风险;8 项研究[7,10,12,14,16—17,21,24]的分配隐藏为低风险;6项研究[5,10—11,22—23,25]对研究者和受试者均采用盲法,所有研究在结局评估时使用盲法;所有研究结局数据完整;所有研究未选择性报告结果;所有研究均不清楚是否存在其他偏倚来源,详见图2、图3。
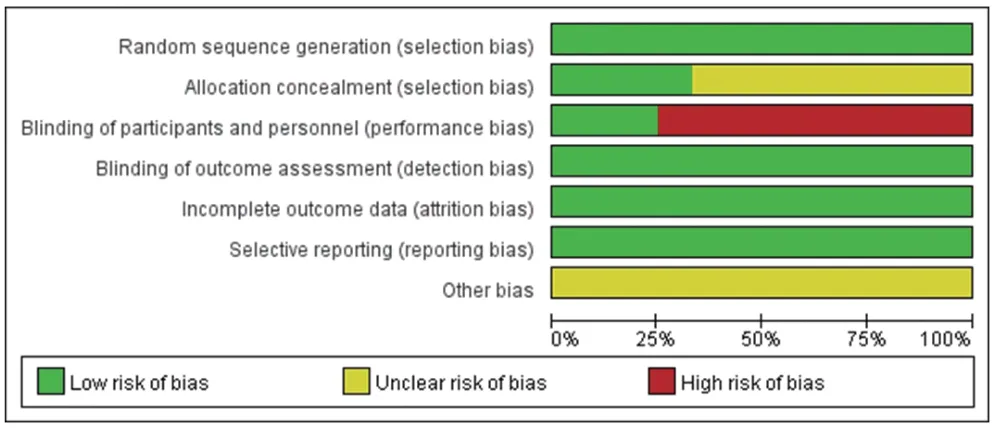
图3 偏倚风险条形图
2.4 疗效指标Meta分析结果
2.4.1 PFS
10 篇文献[9,11,14—16,19,21,23—24,26]报道了PFS,各研究间异质性检验结果为P<0.000 01,Ⅰ2=92%。采用随机效应模型的Meta分析显示,两组间的PFS差异无统计学意义[HR=0.91,95%CI(0.80,1.02),P=0.12],见图4。
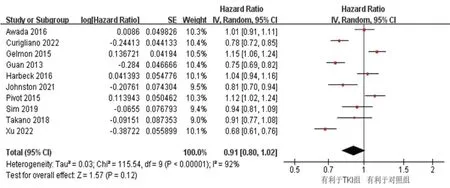
图4 PFS的Meta分析森林图
2.4.2 OS
16 篇文献[8—12,14—20,22—24,28]报道了OS,各研究间异质性检验结果为P=0.000 3,Ⅰ2=63%。采用随机效应模型的Meta 分析显示,两组间的OS 差异无统计学意义[HR=0.95,95%CI(0.89,1.01),P=0.11],见图5。
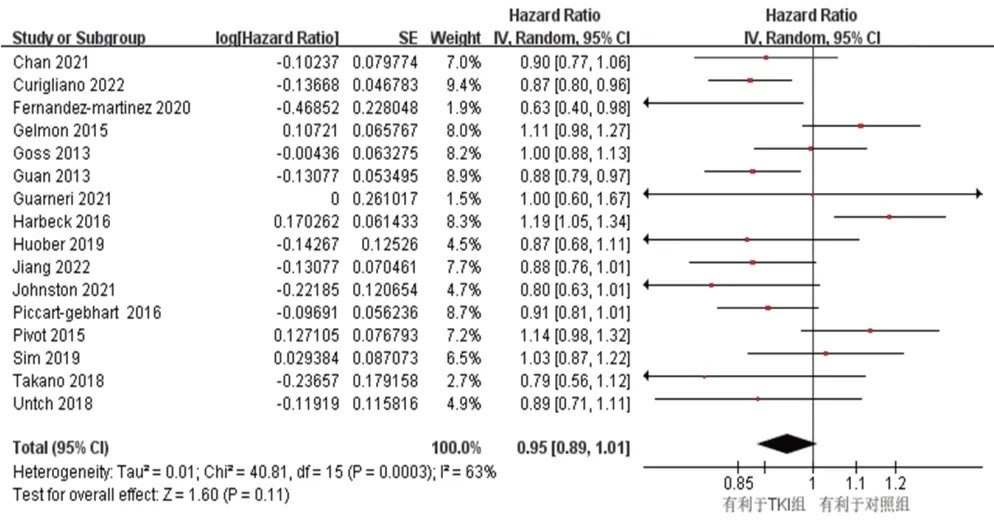
图5 OS的Meta分析森林图
2.4.3 ORR
8篇文献[9,11,14—16,19,21,24]报道了ORR,各研究间异质性检验结果为P=0.0003,Ⅰ2=75%。采用随机效应模型的Meta分析显示,两组间ORR的差异无统计学意义[OR=1.21,95%CI(0.86,1.69),P=0.27],见图6。
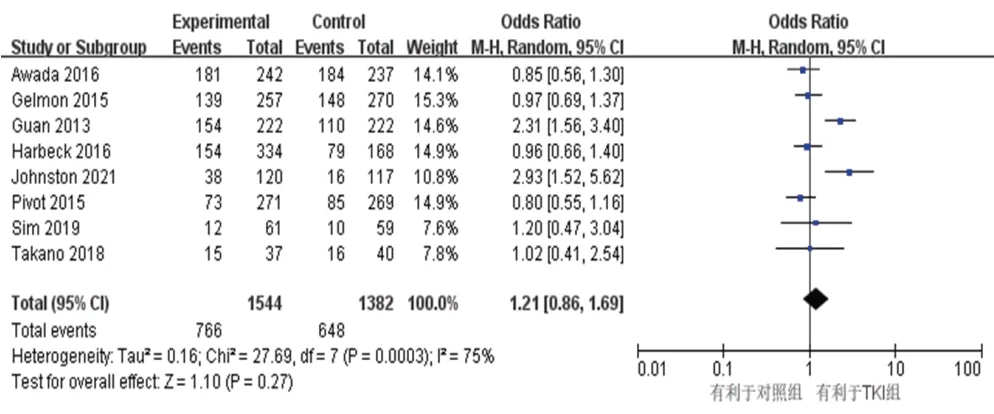
图6 ORR的Meta分析森林图
2.4.4 pCR
7 篇文献[5—7,13,18,25,27]报道了pCR,各研究间异质性检验结果为P=0.002,Ⅰ2=71%。采用随机效应模型的Meta分析显示,两组间的pCR差异无统计学意义[OR=1.44,95%CI(0.91,2.27),P=0.12],见图7。
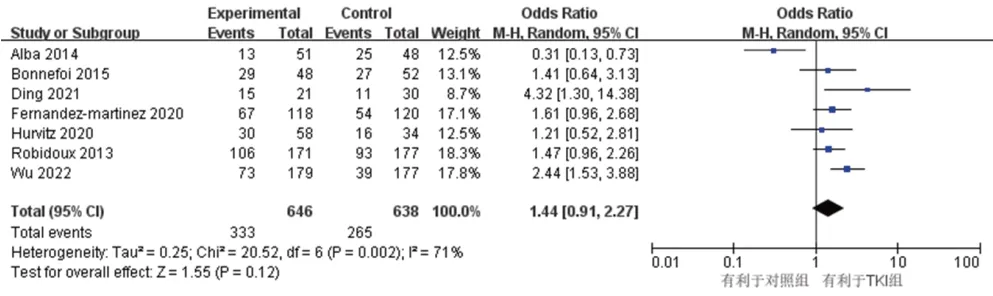
图7 pCR的Meta分析森林图
2.5 安全性指标的Meta分析
17 篇文献[5—7,9—11,13—16,19—25]报道了3/4 级ADR。Meta分析结果显示,试验组患者贫血、皮疹、甲沟炎、腹泻、口腔黏膜炎、天冬氨酸转氨酶(aspartate aminotransferase,AST)升高和低钾血症的发生率显著高于对照组;而丙氨酸转氨酶(alanine aminotransferase,ALT)升高和胆红素升高的发生率与对照组相比,差异无统计学意义。详见表2。
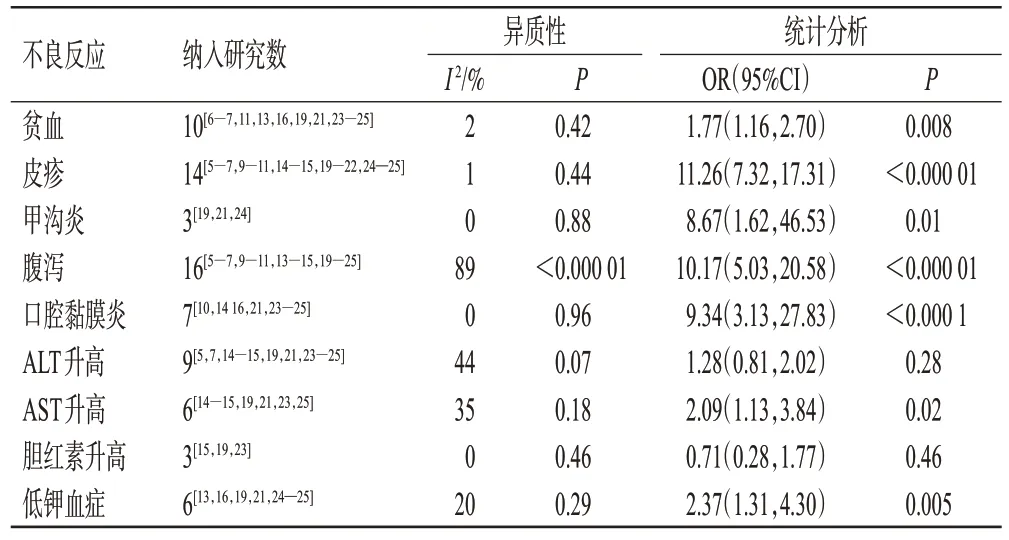
表2 两组3/4级不良反应发生率的Meta分析
2.6 亚组分析
以PFS、OS、ORR 和pCR 为指标,按患者用药类型进行亚组分析,结果如表3所示。结果显示,经亚组分析后异质性有减小。TKI±化疗组患者的OS[HR=0.75,95%CI(0.69,0.82),P=0.01]和ORR[OR=2.09,95%CI(1.46,2.99),P<0.000 1]显著高于安慰剂±化疗组,PFS[HR=0.83,95%CI(0.67,1.03),P=0.09]的差异无统计学意义(pCR 指标未纳入文献)。TKI±化疗组患者的PFS[HR=1.06,95%CI(0.99,1.14),P=0.10]、OS[HR=1.07,95%CI(0.96,1.20),P=0.24]和ORR[OR=0.90,95%CI(0.75,1.09),P=0.28]与曲妥珠单抗±化疗组的差异无统计学意义(pCR 指标仅纳入1 篇文献)。TKI+曲妥珠单抗±化疗组患者的PFS[HR=0.75,95%CI(0.68,0.84),P<0.000 01]、OS[HR=0.87,95%CI(0.82,0.93),P<0.000 1]和pCR[OR=1.76,95%CI(1.39,2.23),P<0.000 01]显著高于曲妥珠单抗±化疗组(ORR指标仅纳入1篇文献)。
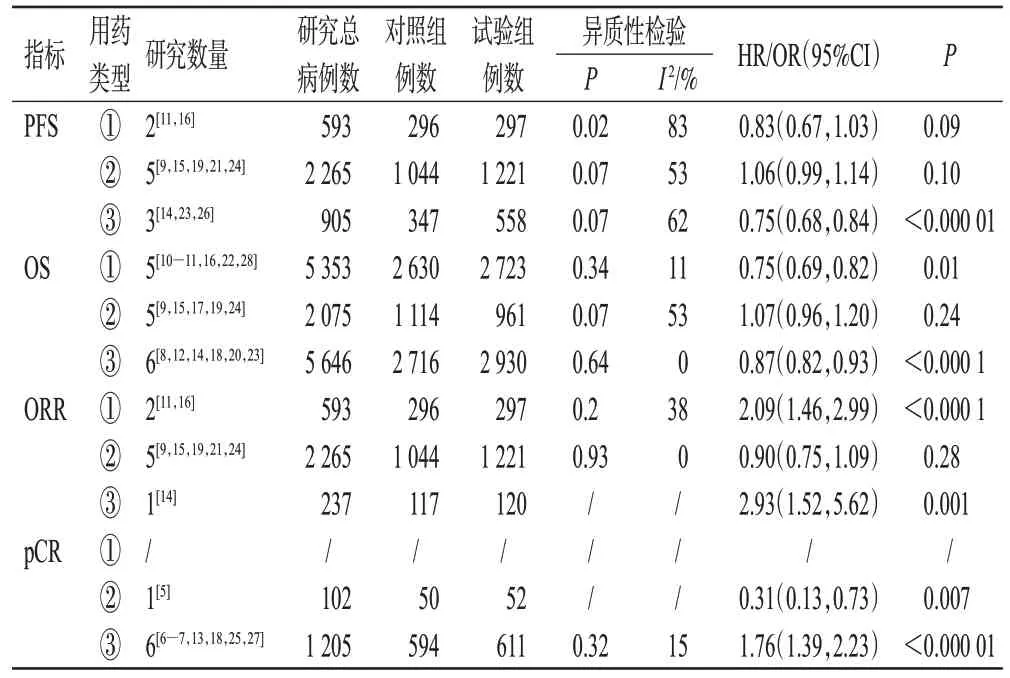
表3 两组患者的亚组分析结果
2.7 敏感性分析
以PFS、OS、ORR 和pCR 为指标进行敏感性分析,结果显示,逐一剔除各项研究后,得到的95%CI 均未跨过无效线,且合并效应量的点仍在原95%CI 内,提示本研究结果较为稳健,详见图8。
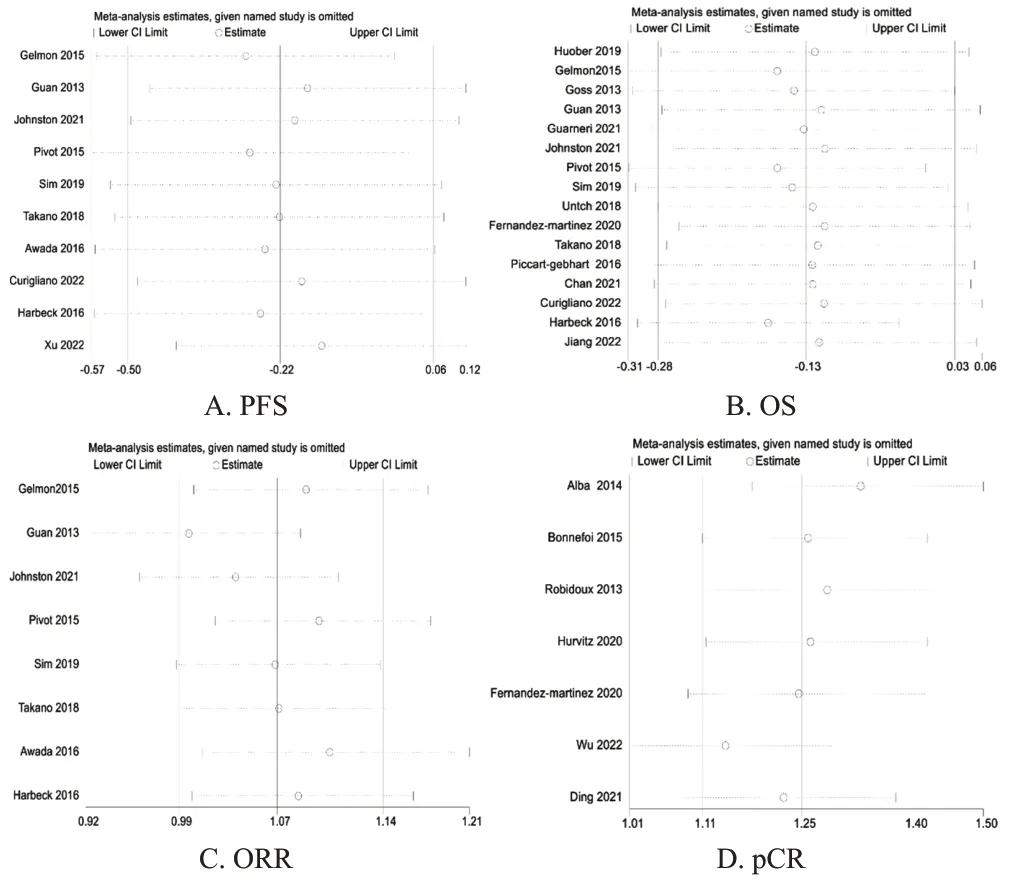
图8 各指标的敏感性分析图
2.8 发表偏倚分析
以PFS 为指标,得到Egger’s 检验的P值为0.697,各研究散点分布基本对称,表示本研究存在发表偏倚的可能性较小,详见图9A。以OS为指标,得到Egger’s 检验的P值为0.508,各研究散点分布基本对称,表示本研究存在发表偏倚的可能性较小,详见图9B。由于其他指标纳入的研究少于9篇,所以没有进行发表偏倚评价。
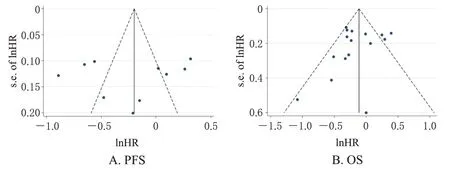
图9 PFS与OS的倒漏斗图
3 讨论
过度表达HER2 的乳腺癌具有侵袭性,并与不良预后相关[2]。HER2 靶向疗法的发展彻底改变了HER2 阳性乳腺癌患者的治疗模式和结果。在过去的几年里,多种HER2 靶向药物已被批准用于乳腺癌,如TKI 类药物拉帕替尼、吡咯替尼、图卡替尼、奈拉替尼和阿法替尼。
本文Meta 分析显示,与曲妥珠单抗相比,TKI 类药物在PFS、OS、ORR 和pCR 指标上是没有优势的,这提示以曲妥珠单抗为基础的治疗仍然是HER2阳性乳腺癌患者的首选治疗方法。
亚组分析发现,与安慰剂相比,TKI 类药物在改善OS、ORR指标上有显著优势。ExteNET研究结果显示,奈拉替尼与安慰剂相比,在改善OS上有着显著优势[22]。同时,PHENIX研究显示,在曲妥珠单抗治疗失败的患者中,吡咯替尼联合卡培他滨可提高ORR和PFS[29]。而本研究的亚组分析显示,TKI类药物与安慰剂组相比,患者的PFS 差异无统计学意义,可能原因是仅纳入了2 篇文献,样本量较小,因此需要更多大样本的临床试验进行验证。最新中国临床肿瘤学会相关指南指出,对于曲妥珠单抗治疗失败的患者,Ⅰ级推荐为吡咯替尼联合卡培他滨,Ⅲ级推荐为TKI 类药物联合其他化疗。这提示TKI类药物可作为HER2阳性乳腺癌患者曲妥珠单抗耐药后的治疗药物。
亚组分析结果还显示,TKI 类药物联合曲妥珠单抗与曲妥珠单抗相比,能显著改善患者的PFS、OS、ORR和pCR,这提示TKI 类药物与曲妥珠单抗双药联合可有效改善患者预后。
本研究结果还显示,试验组患者3/4 级贫血、皮疹、甲沟炎、腹泻、口腔黏膜炎、AST升高和低钾血症的发生率显著高于对照组,而ALT升高和胆红素升高的发生率差异均无统计学意义。皮疹、腹泻、甲沟炎、口腔黏膜炎和肝损伤是TKI类药物特有的ADR,目前临床上尚缺乏对TKI 类药物所致ADR 的统一诊治策略。值得注意的是,本研究发现,TKI类药物引发低钾血症的风险较高,这是说明书上未记载的新ADR,提示临床上使用TKI类药物时应注意监测血钾水平,如若发生低钾血症应及时补钾。
敏感性分析和发表偏倚结果显示,本研究所得结果较为稳健,且发表偏倚风险较小。
综上所述,HER2 阳性乳腺癌患者的首选治疗方法仍然是曲妥珠单抗,若患者发生曲妥珠单抗耐药,则可选择TKI 类药物;TKI 类药物虽然对HER2 阳性乳腺癌治疗有效,但仍存在诸如3/4 级贫血、皮疹、甲沟炎、腹泻、黏膜炎、AST 升高和低钾血症等ADR。本研究的局限性包括:(1)部分文献样本量较小;(2)少数研究质量偏低;(3)部分指标间的异质性较高,可能与临床试验的样本量小、不同组间使用的对照药物不同、研究环境不同有关。由于上述局限性的存在,本研究的结论仍需大样本、高质量的随机对照试验进行确证。
