全球肿瘤相关性血栓栓塞症风险评估工具的循证研究 Δ
2024-02-28秦小莉高秀容藕顺龙成都市第三人民医院药学部成都600成都医学院药学院成都6000四川省肿瘤临床医学研究中心四川省肿瘤医院研究所四川省癌症防治中心电子科技大学附属肿瘤医院药学部成都600电子科技大学医学院成都600成都市第二人民医院药学部成都600
秦小莉 ,高秀容 ,何 琴 藕顺龙 ,罗 静 ,魏 华 ,蒋 倩 (.成都市第三人民医院药学部,成都 600;.成都医学院药学院,成都 6000;.四川省肿瘤临床医学研究中心/四川省肿瘤医院研究所/四川省癌症防治中心/电子科技大学附属肿瘤医院药学部,成都 600;.电子科技大学医学院,成都 600;.成都市第二人民医院药学部,成都 600)
静脉血栓栓塞症(venous thromboembolism,VTE)包括深静脉血栓(deep vein thrombosis,DVT)和肺血栓栓塞症(pulmonary thromboembolism,PTE),其发生率仅次于急性心肌梗死和脑卒中[1],已成为患者非预期性死亡的主要原因之一,也是肿瘤患者常见的并发症之一。肿瘤患者并发血栓风险是非肿瘤患者的4~7倍,约占所有VTE的20%,已成为肿瘤患者死亡的第二大原因[2—3]。而正确评估、早期预防可降低患者血栓发生率和病死率[4],但过度预防又会增加出血风险和经济负担。因此,使用恰当的风险评估工具预测肿瘤相关性血栓栓塞症(cancer-associated thromboembolism,CAT)至关重要。目前国内外针对CAT风险评估工具的研究虽然较多,但我国尚未发布统一的标准或规范。本研究基于循证方法对全球CAT风险评估工具进行评价,以期为构建我国CAT风险评估工具提供方法学参考与循证依据。
1 资料与方法
1.1 纳入与排除标准
本研究的纳入标准包括:(1)CAT风险评估工具、量表或模型;(2)肿瘤类型不限,语种限制为中文与英文;(3)同一机构发布的评估工具,仅保留最新版本。本研究的排除标准包括:(1)关于CAT风险评估工具的评述、系统评价;(2)复发性CAT 风险评估工具;(3)CAT 风险评估的临床研究;(4)重复发表的研究。
1.2 文献检索策略
全面检索中国知网(CNKI)、万方数据库(Wan-Fang)、维普网(VIP)、中国生物医学文献数据库(CBM)、PubMed 及Embase,同步检索21 个相关机构与学会网站,纳入CAT风险评估工具量表、模型,检索截止时间为2022 年6 月30 日,并于2023 年1 月再次补充检索。另外手动检索相关研究的参考文献,以避免检索遗漏。检索采取主题词与自由词相结合的方式,英文检索词包括:venous thromboembolism、deep vein thrombosis、pulmonary embolism、cancer、tumor、neoplasms、risk assessment tool/score/model、risk evaluation tool/score/model;中文检索词包括:肿瘤相关静脉血栓、深静脉血栓、肺栓塞、肺血栓栓塞症、风险评估工具、风险评估模型、风险评估量表、风险评估评分。21 个相关机构及学会网站包括:(1)中国、美国、日本、加拿大等国家的15个卫生相关网站;(2)中华医学会、中国临床肿瘤学会、美国国家综合癌症网络(National Comprehensive Cancer Network,NCCN)、美国临床肿瘤学会(American Society of Clinical Oncology,ASCO)、欧洲肿瘤内科学会(European Society for Medical Oncology,ESMO)、国际血栓与止血学会(International Society of Thrombosis and Hemostasis,ISTH)共6个学会网站。以PubMed为例的具体检索策略见图1。
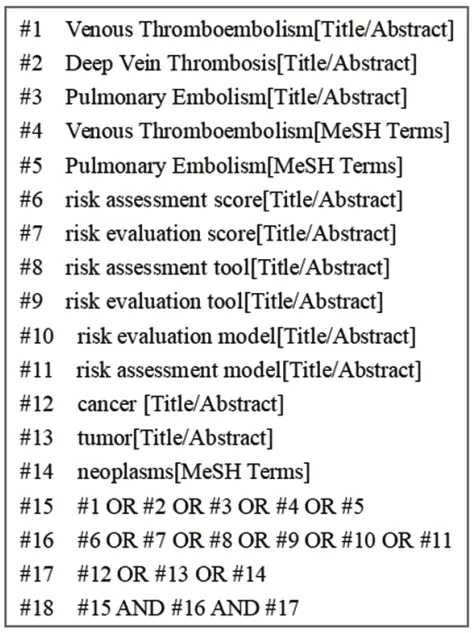
图1 PubMed检索策略示例
1.3 文献筛选与资料提取
2名研究者独立通过阅读文题、摘要,排除明显不符合纳入标准的文献后阅读全文,确定文献是否纳入。如遇分歧,由第3位研究者协助裁定。资料提取内容主要包括:(1)基本特性——发布作者、年份、国家、研究设计类型、VTE 定义以及纳入与排除标准、数据来源、样本量、适用人群及随访期等;(2)工具评估维度、CAT 风险因素或预测因子;(3)工具形成方法、特异性、敏感性、是否风险分层、是否验证、结果呈现形式等。
1.4 统计分析
采用定性分析描述纳入评估工具适用人群,发布国家、机构、年份,评估工具构建方法等基本特征;重点比较工具评价维度、工具性能、风险分层能力等关键要素。
2 结果
2.1 文献检索流程及结果
初检共获得文献717篇,补充检索25篇,经过筛选,最终纳入14个CAT风险评估工具,见图2。
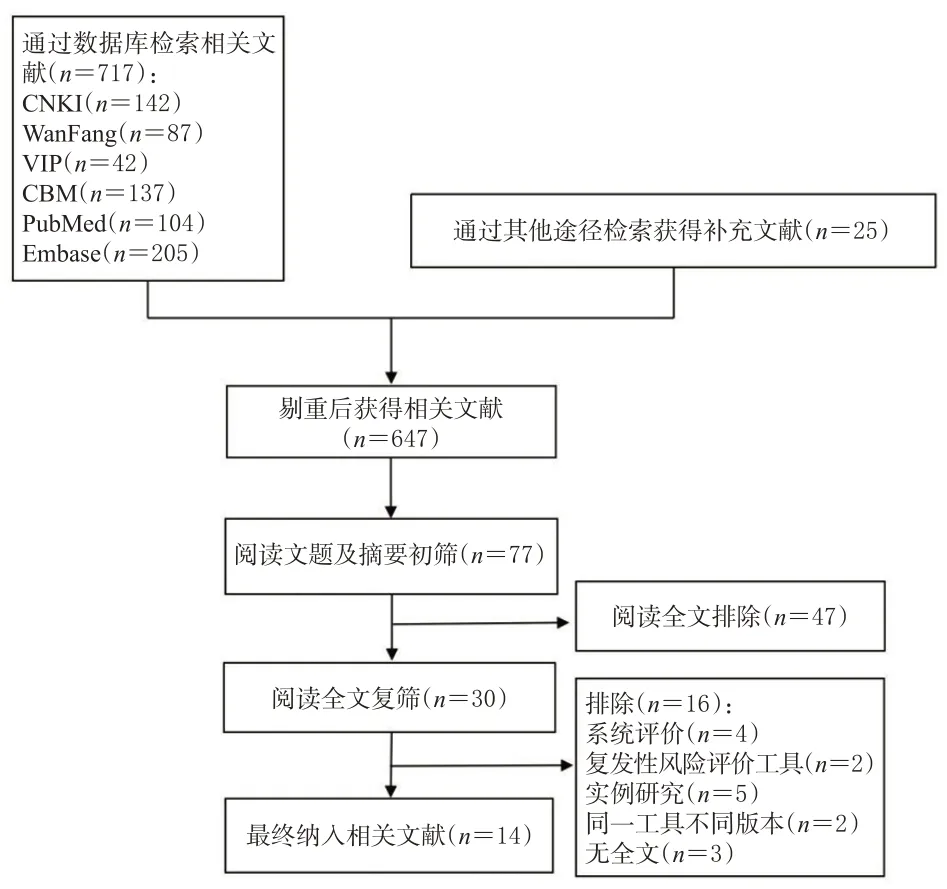
图2 文献筛选流程图
2.2 CAT风险评估工具概述
全球迄今共发布CAT风险评估工具14个[5—18],发布于2008-2021年,来自美国、意大利、西班牙等国家。其中美国5 个、中国1 个。2008 年,美国学者Khorana 等[5]研制了Khorana predictive model,为全球首个适用于评估门诊化疗肿瘤患者VTE 风险的评估工具。随着对CAT 风险的广泛关注,风险评估工具发布数量逐年增加,仅2016-2021年就发布了11个,详见图3。
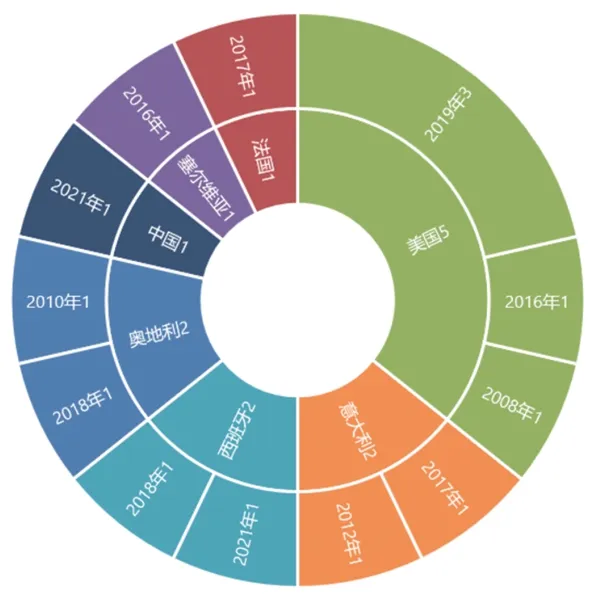
图3 CAT风险评估工具发布国家和数量
2.3 纳入工具的基本特征
纳入的14 个工具研究样本量为208~18 956 例,受试者平均年龄为53.1~74.0 岁(2 项研究未报道[5,7]),女性受试者比例为3.0%~81.3%(3项研究未报道[5,7,17]),随访时间3~24 个月不等;其中,4 个工具采用回顾性研究[7—8,15—16],8 个采用前瞻性或观察性研究[5—6,9—14],2 个采用病例对照研究[17—18];9个工具的构建基于Logistic回归模型[5,8—9,11—12,14—15,17—18];2个基于其他模型改进所得[6—7];1个基于多变量模型[16];1 个基于惩罚回归模型[13];1 个基于竞争风险模型[10];纳入工具的主要研究对象为门诊肿瘤患者(n=6)[5,10—14]、淋巴瘤患者(n=2)[9,18]、多发性骨髓瘤患者(n=2)[15—16]、肺癌术后患者(n=1)[17]、住院或接受化疗的肿瘤患者(n=3)[6—8]。全球CAT风险评估工具的基本特征详见表1。
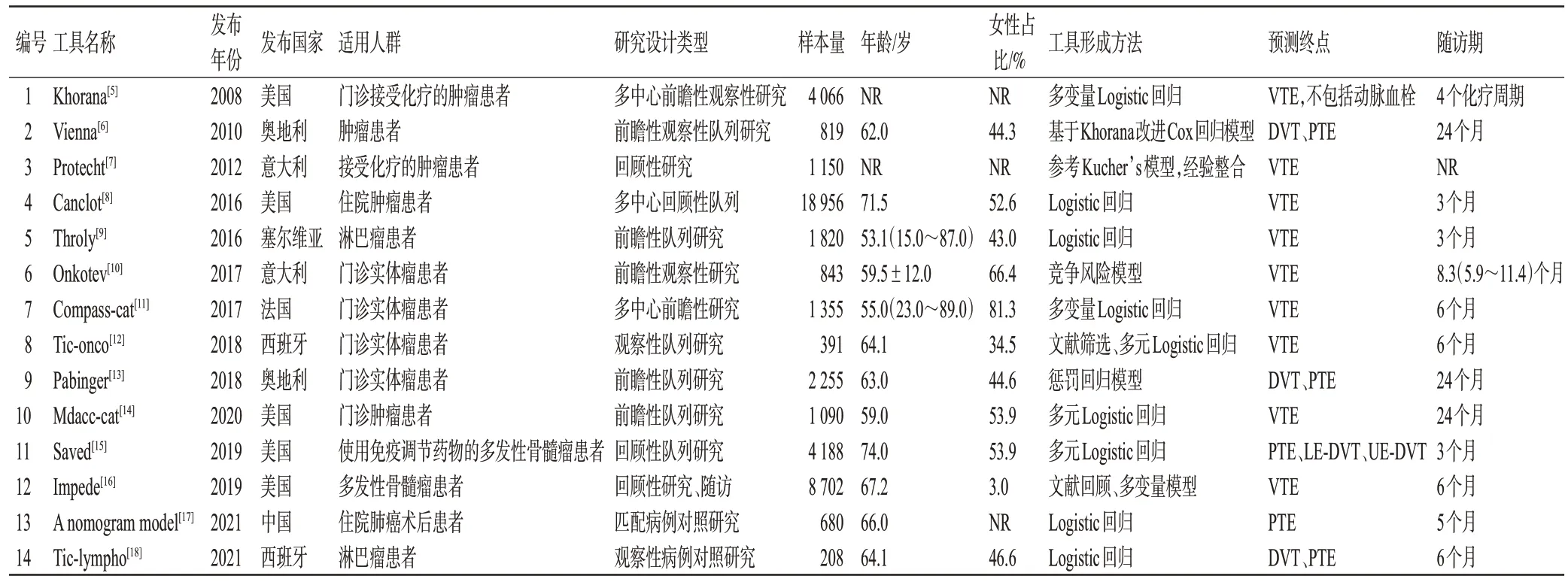
表1 全球CAT风险评估工具的基本特征
2.4 CAT风险评估工具评价维度和风险因素
患者、疾病、治疗因素及实验室指标是工具中常见评价维度,各维度囊括多种风险因素。大部分工具将身体质量指数(body mass index,BMI)和VTE 既往史作为风险因素,7 个工具均将此因素纳入最终的预测因子。但不同工具之间定义肥胖的BMI阈值却不尽相同,包括BMI≥16~19 kg/m2(n=1)[17]、>25 kg/m2(n=2)[12,16]、>30 kg/m2(n=1)[9]、≥35 kg/m2(n=3)[5—7];VTE 既往史包括VTE 个人史(n=6)[8,11—12,15—16,18]、PTE 或下肢深静脉血栓史(n=1)[10]。原发性肿瘤部位是风险评估工具中常见的影响因素(n=5)[5—7,12—13],胃癌、胰腺癌归为极高危风险因素,肺癌、淋巴瘤、妇科肿瘤等归为高危风险因素,其赋予权重评分也不同。实验室指标中:血红蛋白和血小板计数是常见的风险因素,分别有4个工具将此纳入最终风险预测因子。2个工具将活动能力下降作为最终的预测因子[9,18],但不同工具对此项目的定义差异较大。CAT 风险评估工具的评价维度和风险因素比较详见表2。
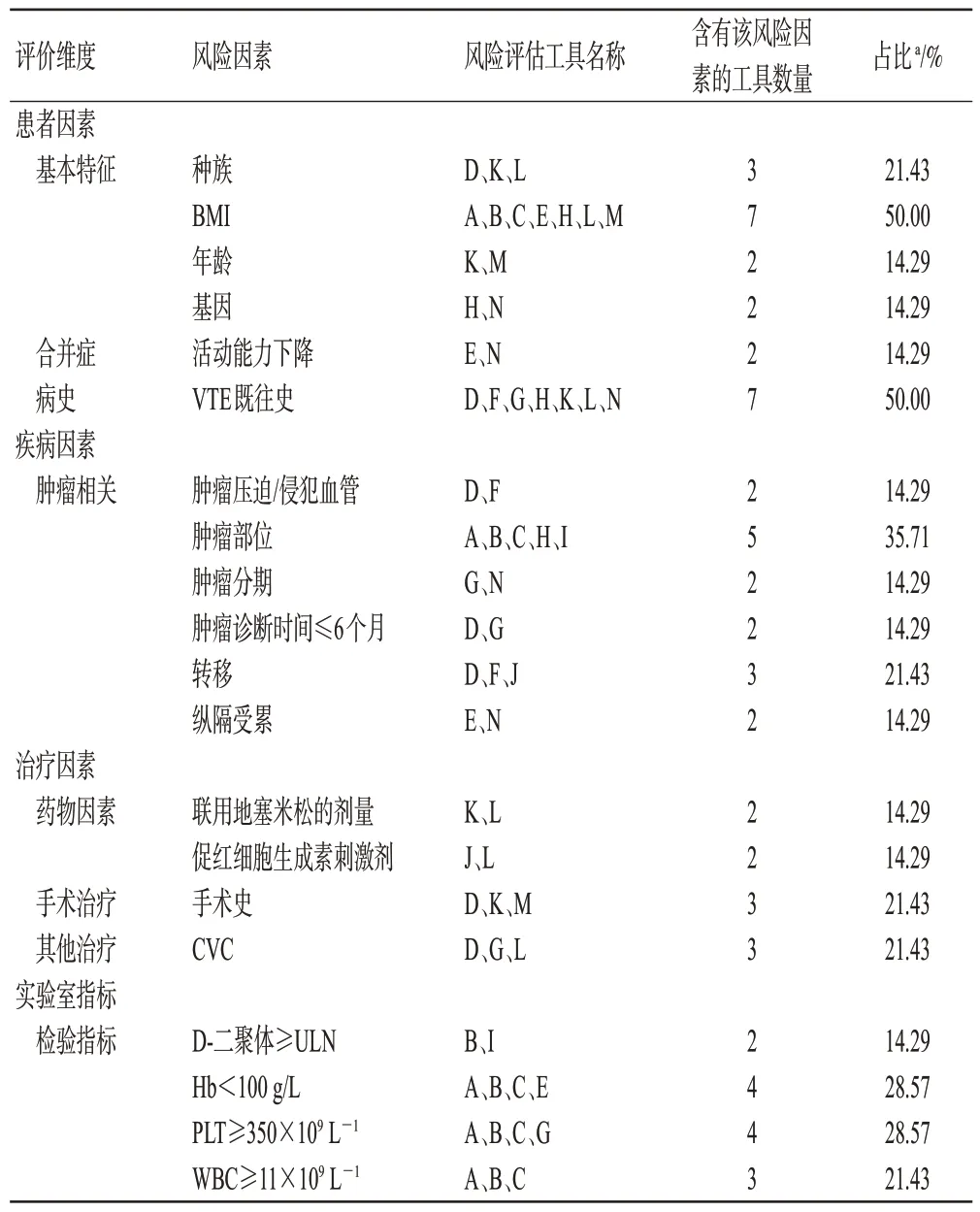
表2 风险评估工具评价维度和风险因素比较
2.5 CAT风险评估工具预测因子及性能指标
纳入工具的预测因子数量为2~9个,占比较高的是VTE 既往史和BMI。其中9 个工具进行了风险分层[5—11,15—16],即根据权重加和评分或风险预测因子数量区分CAT 高、中、低风险,以便识别高危患者并及早干预。纳入的工具均进行了方法学验证,主要采用内部验证(n=8)[5—6,9—12,15,17]、内外部验证(n=1)[16]、外部验证(n=1)[13]、对比验证(n=3)[7—8,18]和引导验证(n=1)[14]。9个工具以风险评分的方式呈现[5—11,15—16],2个以列线图模型量化[14,17],3个工具结果呈现形式不明确[12—13,18]。另外,在工具性能方面,4 个工具[11—12,17—18]采用曲线下面积(area under the curve,AUC)(0.73~0.85)检验工具的区分度,AUC值>0.7提示预测性能较好;5个工具[5,9,13—14,16]采用C统计量(0.66~0.88),C统计量<0.7 提示工具性能较弱,>0.8提示工具性能较优秀;2个工具[10,15]采用相关系数进行检验;另有3 个工具[6—8]未提及其性能指标。同时进行了特异性、敏感性、阴性预测值(negative predictive value,NPV)、阳性预测值(positive predictive value,PPV)和AUC 或C统计量分析的工具仅有7个[5,9,11—13,17—18],见表3。

表3 工具预测因子及性能指标比较
3 讨论
3.1 现有CAT风险评估工具的方法学质量有待提高
3.1.1 工具构建偏倚风险较高
大部分工具(n=13)[5—6,8—18]均明确了研究对象的纳排标准,以减少选择性偏倚,提高工具适用性;但部分工具[5,7,17]构建纳入患者信息不完整、未报告盲法、未恰当处理缺失数据、缺少性能评估、随访时间不足,增加了偏倚风险。9 个工具[5,8—9,11—12,14—15,17—18]构建采用Logistic 回归模型,虽适用性较好,但整体偏倚风险高。而部分工具研发仅基于专家意见或经验[7],主观性较强;或是根本未报告其建立的具体方法和细节,导致偏倚风险较高。
3.1.2 工具验证结果异质性较大
研究设计类型(包括前瞻性、回顾性、多中心研究)及纳入人群基本特征的不同是导致异质性增加的主要原因。再者VTE 定义存在差异:某些工具[5,15—16]仅使用国际疾病分类第九次修订本(international classification of diseases ICD-9)诊断代码定义VTE,其并不足以确诊VTE,建议将ICD-9代码与急性VTE诊断试验阳性证据相结合。另外VTE 预测终点方式不同:Saved[15]将慢性VTE、上肢VTE或单纯浅表VTE纳入模型终点,然而几乎没有证据表明这些VTE类型预防有益,从而导致工具验证结果异质性增加[19]。
3.1.3 工具风险分层能力有待考究
尽管纳入的14个工具都有不同的验证方式,但部分工具[13,16]验证结果显示预测性能不佳。再者某些工具即使在其原始研究中表现良好,但缺乏相关外部效度的验证研究,或者与已经进行的验证研究报道矛盾[20]。
3.2 现有工具在临床实践中仍存在一定局限性
(1)评估维度和预测因子不完全一致:几乎所有工具均将患者因素、疾病因素、治疗因素纳入评估维度,但工具最终风险预测因子却差异较大,无法区分其导向性和重要性。再者预测因子过于简单或复杂,都会造成CAT 风险评估偏差。(2)相同预测因子、权重评分不同:Saved[15]和Impede[16]同样用于评估多发性骨髓瘤患者VTE 风险,但对同一风险预测因子如VTE 既往史,赋予权重评分有所差异——前者赋予3分、后者赋予5分,导致其CAT风险评估结果不同,最终可能影响临床预防决策的实施。(3)工具实施方法与结果呈现形式不同:部分工具[12—13,18]未交代具体实施方法,透明度低,以定性描述为主,临床可操作性差。再者不同工具结果呈现形式也有所差异,不便解读与比较,大部分工具通过权重评分加和进行风险分层,少数工具仅按风险因素数量进行评估。
3.3 构建中国本土CAT风险评估工具的建议
截至目前,中国本土唯一的CAT风险评估工具仅有Li等[17]研发的A nomogram model(用于肺癌),但与国外基于大量临床资料及充分文献回顾构建的工具相比还需更多前瞻性研究来验证其有效性。因此,迫切需要开发符合我国人群特征的CAT风险评估工具。据此,笔者针对我国CAT风险评估工具的构建提出以下建议:
(1)不宜直接照搬国外工具,而应充分参考借鉴其构建方法和实践经验,兼顾我国人群特点,探索研发具有我国知识产权和可操作性强的CAT风险评估工具,例如中国人群与西方人群BMI均值的差异,直接影响风险评估对象的纳入,进而影响工具的准确性。(2)CAT风险高低受疾病治疗进展或患者基本特征的改变而动态变化,故应赋予风险评估工具更新功能与机制,能够动态评估患者入院前、出院后和随访过程中的风险水平等级。(3)克服现有工具主要基于回顾性研究和Logistic回归模型开发的局限性,补充长期观察性高质量研究作为重要证据来源,拓宽工具适用性。同时,按照循证医学方法及学科决策理念开发评价工具,强调证据的重要性,提升工具可信度[21]。(4)基于科学研究构建全方位、多层次的风险评估维度,确定各维度指标的重要性、并进行权重赋分,以提高工具适用性和可行性,最终构建符合我国实际需求、全面、重点明确、可操作性强并可持续更新与改进的CAT 风险评估工具。(5)将工具与医疗机构电子警报系统整合统一,并控制警报疲劳,以提高工具在临床实践中的可操作性。(6)在工具验证研究中,建议对有预防和无预防患者进行亚组测试,以证明工具的预测价值不受先前预处理的影响。综上,理想的CAT风险评估工具应当涵盖患者特点、肿瘤特征、治疗因素和检验指标等全方位、多层次的评估维度,并能动态识别抗凝预防的风险-收益阈值,赋予医务人员和目标使用人群多维度评估能力,且结果应简单清晰,方便区分高、中、低风险,辅助临床决策,以降低CAT 发生率和病死率,提升医疗质量。
本研究的局限性包括:(1)仅纳入了中文和英文文献;(2)部分研究样本量较小、证据质量可能较低,所得结论尚需更多大样本、多中心研究进一步证实。
综上所述,本研究对CAT风险评估工具进行了循证研究,对于推进我国CAT风险评估工具研发和临床应用具有重要意义,有助于推动CAT风险评估工具领域的进一步发展。
