基于“关开”型掺杂碳量子点检测食用油中特丁基对苯二酚的研究
2024-02-27包泽伟林建原于佩斓郭善才蒋力豪
包泽伟, 林建原, 于佩斓, 郭善才, 蒋力豪
(浙江万里学院,宁波 315100)
特丁基对苯二酚(TBHQ)作为一种常用的酚类抗氧化剂,能有效抑制细菌、霉菌的繁殖,起防腐作用,又因其良好的热稳定性及低毒等特点,被广泛应用于油脂抗氧化领域中[1-3]。研究表明,过量摄入TBHQ可引发恶心、呕吐、窒息等风险,对人体具有一定毒副作用[4,5],因此使用中需严格控制用量,其中GB 2760—2014规定TBHQ在油脂中的添加量不得超过0.2 g/kg。
目前TBHQ的检测方法主要有高效液相色谱法[6,7]、气相色谱法[8,9]、色谱-质谱联用[10]、电化学法[11,12],此类方法灵敏度高、选择性好,但对于检测样品的前处理要求繁琐,测定成本较高,且耗时长。近年来,对于TBHQ的快速检测技术应运而生,李满秀等[13]制备了碳量子点与纳米金的复合材料,因TBHQ可增强该纳米材料在445 nm处的荧光发射强度,从而构建了一种检测新方法。Farajmand等[14]采用微液-液萃取与差分脉冲伏安法相互结合的方式,发现将玻璃碳电极于1.9 V电压与0.1 mol/L硫酸中预氧化,能够大幅调节对TBHQ的电化学响应,检测灵敏度高。
碳量子点(CQDs)是一种绿色、低毒的纳米级材料,具有较大的比表面积、较多的活性位点,可通过不同官能团调节其表面状态,制备特定波长的荧光材料[13,14],广泛应用于免疫荧光、成分分析、离子检测等领域[15]。其中碳量子点的制备方法之一水热法具有经济、环保、产率高等特点,在合成领域广泛应用。本研究采用Tris与CA通过水热法合成N-CQDs,并基于Fe3+与N-CQDs的络合作用,使激发电子转移至Fe3+的d轨道导致荧光猝灭[16],借助TBHQ与Fe3+的强络合作用与CQDs产生竞争,构建“关-开”型荧光探针对TBHQ进行快速检测。
1 材料与方法
1.1 材料与仪器
山茶油,调和油,纯净水,特丁基对苯二酚、一水合柠檬酸、三羟甲基氨基甲烷、乙酸铵、三氯化铁:分析纯。
100 mL反应釜(防爆型),100 mL PPL内衬,F-4600型荧光分光光度计,LGJ-12冷冻干燥机,UV-3 000PC紫外分光光度计,VERTEX70 型傅里叶变换红外光谱仪。
1.2 实验方法
1.2.1 溶液配制
TBHQ标准溶液配制:准确称取0.166 g TBHQ,定容于100 mL容量瓶中,即为100 mmol/L TBHQ标准溶液,再分别配制成1.000、0.100 mmol/L TBHQ标准溶液。
Fe3+淬灭剂配制:称取0.270 g FeCl3·6H2O,定容于100 mL容量瓶中,浓度为10 mmol/L。
1.2.2 N-CQDs制备
称取1.000 g Tris与1.700 g CA溶于50 mL纯净水,充分搅拌后超声10 min,转移至100 mL反应釜中,放置于200 ℃烘箱中8 h,取出,待其冷却后得到淡褐色溶液[17]。将得到的溶液进行高速离心并使用0.22 μm滤膜过滤以去除大颗粒物质,使用透析袋透析48 h,得到N-CQDs,于4 ℃冷藏保存。
1.2.3 N-CQDs结构表征
将1.2.2 制备的N-CQDs溶液经旋蒸浓缩后,冷冻干燥48 h得到固体粉末,取少量样品与经干燥的KBr粉末混合、碾碎、压片,采用傅里叶变换红外光谱仪对样品进行红外光谱分析。
1.2.4 油脂样品预处理[18]
称取10.000 g油脂样品于50 mL锥形瓶中,加入20 mL 石油醚,超声10 min,转移至分液漏斗,加入质量分数为1.67%乙酸铵溶液20 mL充分振荡后静置分层萃取,分离出水层,再加入质量分数为1.67%乙酸铵溶液进行2次萃取,收集合并水层,加入10%乙酸铵溶液2.5 mL,定容至100 mL容量瓶中,摇匀,得到待测样品。
1.2.5 荧光光谱测定
取5 mL比色管,依次加入200 μL N-CQDs,2 mL纯净水,150 μL Fe3+淬灭剂及200 μL 10 mmol/L TBHQ标准溶液,定容至5 mL,摇匀后静置孵育18 min。取1 mL溶液进行荧光光谱分析。
2 结果与讨论
2.1 N-CQDs光谱表征
2.1.1 N-CQDs 的紫外吸收光谱
图1为N-CQDs的紫外吸收光谱,在240 nm处存在明显π-π*跃迁的特征吸收峰,表明N-CQDs具有多个不饱和碳键形成形成碳骨架结构的共轭体系[19,20],在328 nm处有明显的吸收特征峰,这是由于CQDs表面捕获激发态能量所产生,此吸收峰通常会产生蓝色荧光[21]。
2.1.2 N-CQDs 红外光谱


图2 N-CQDs红外吸收光谱图
2.1.3 N-CQDs 荧光光谱
N-CQDs的荧光光谱见图3。以270、300、330、345、360、390 nm为激发波长,分别测定N-CQDs在360~480 nm范围的发射波长,实验确定其最佳激发波长和发射波长分别为330、405 nm。当激发波长逐渐远离330 nm时,其发射波长荧光强度不断降低,该现象可能是由于N-CQDs的表面缺陷及不同官能团粒径大小所致,导致N-CQDs对激发光具有依赖性[27]。随着激发波长的增加,发射波长最高峰略出现红移。

图3 N-CQDs荧光光谱图
2.2 N-CQDs检测条件优化
2.2.1 Fe3+浓度优化
于N-CQDs体系中分别加入0.1、0.2、0.3、0.4、0.5 mmol/L不同浓度的Fe3+,探究荧光猝灭剂添加量对N-CQDs荧光强度的影响。图4所示,随着Fe3+浓度增大,N-CQDs荧光强度随之降低,当Fe3+浓度为0.3 mmol/L时,TBHQ荧光强度变化达最大,再继续升高浓度,TBHQ无法络合过量的Fe3+离子。
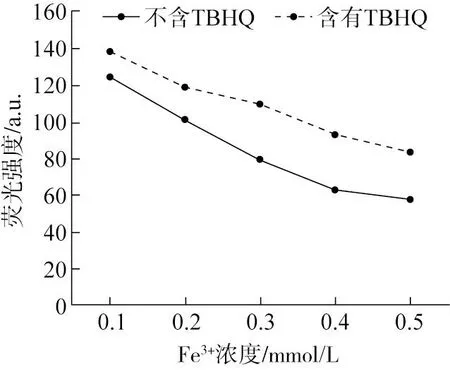
图4 Fe3+对N-CQDs荧光强度的影响
2.2.2 孵育时间优化
实验探究0~30 min不同孵育时间对TBHQ检测灵敏度的影响,结果如图5所示。开始阶段TBHQ没有与N-CQDs充分结合,使得荧光恢复值较低,在孵育18 min后荧光恢复值达到最高,对TBHQ的检测更为灵敏,且趋于稳定,因此实验选择18 min孵育时间为宜。

图5 孵育时间对N-CQDs荧光强度的影响
2.2.3 金属离子干扰实验
选择0.01 mol/L多种常规干扰金属离子对N-CQDs荧光强度的影响,干扰结果如表1所示,Ba2+、Mg2+、Mn2+、Na+、Ca2+、Cu2+、Fe2+、K+、Zn2+对N-CQDs的影响均小于5%,表明Fe3+对N-CQDs的猝灭具有良好的特异性,不易受其他金属离子的干扰。

表1 10种金属离子对N-CQDs荧光强度的影响
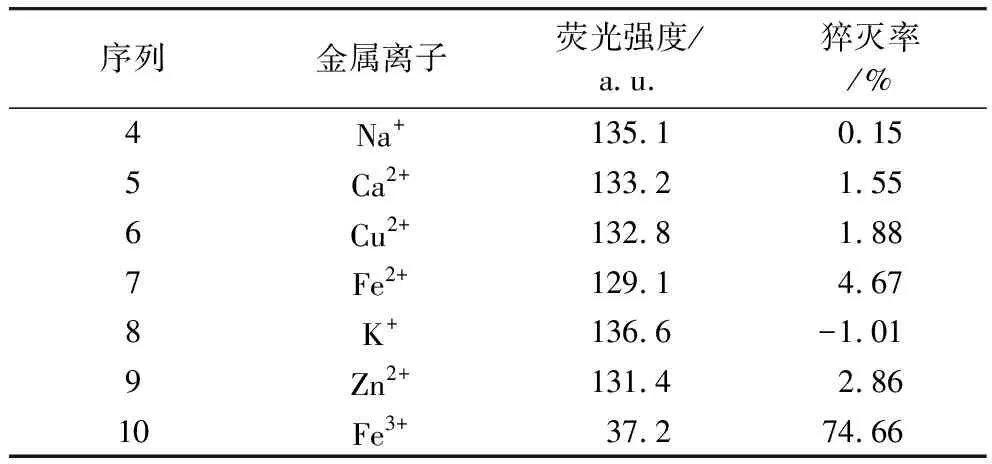
续表1
2.3 N-CQDs对TBHQ的检测
2.3.1 检测原理
TBHQ的检测是通过待测物对N-CQDs荧光“关-开”实现的。由N-CQDs,N-CQDs与Fe3+(0.3 mmol/L), N-CQDs、Fe3+(0.3 mmol/L)与TBHQ(0.5 mmol/L)作用的荧光光谱图见图6,N-CQDs表面官能团与Fe3+结合,发生非辐射电子转移,导致荧光猝灭。加入TBHQ,由于TBHQ与Fe3+的络合能力高于Fe3+与N-CQDs的结合能力,使得N-CQDs的荧光得以恢复,实现对TBHQ的检测。
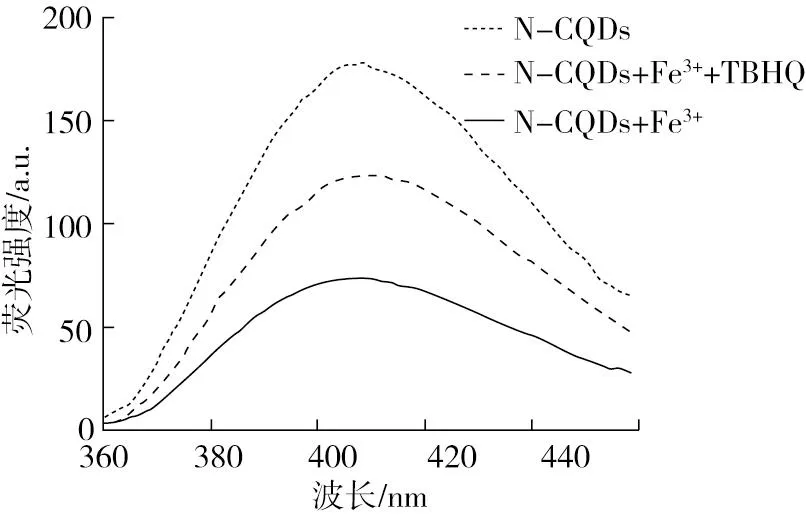
注: Fe3+、TBHQ的浓度分别为0.3、0.5 mmol/L。图6 荧光光谱图
2.3.2 TBHQ标准曲线模型建立
配制质量浓度梯度为1.00、1.33、1.66、2.49、3.32、8.31、16.62、24.93、33.24 μg/mL的TBHQ标准工作曲线,在最优实验条件下测量其荧光值。TBHQ质量浓度在1.00~33.24 μg/mL范围内荧光强度与其浓度具有良好线性关系,回归方程为y=0.283x+72.295,相关系数为0.995,对食用油中TBHQ的检出限达5.6 mg/kg。
2.3.3 样品加标回收率测定
根据1.2.4所述方法处理食用油,设置2组平行测定食用油样品中TBHQ含量的加标回收率实验,结果见表2。方法的样品回收率在90.51%~105.80%之间,表明该方法准确可行,适用于食用油中TBHQ的快速检测。
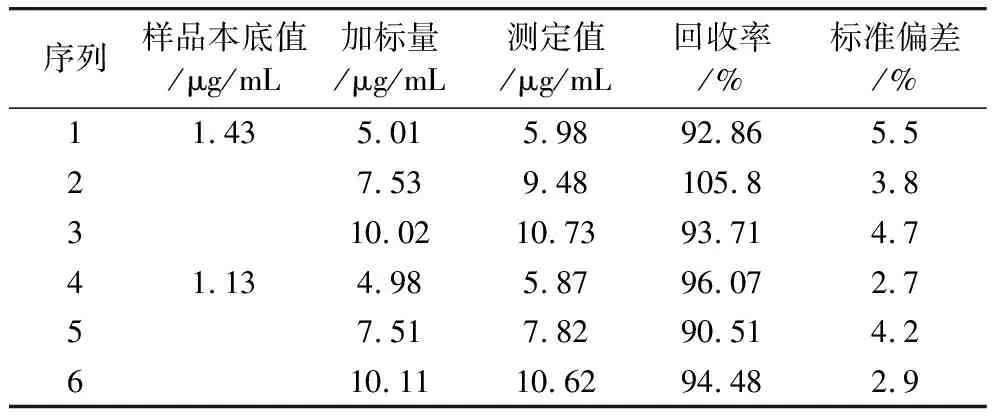
表2 样品的加标回收率
3 结论
实验基于N-CQDs、Fe3+与TBHQ之间的相互作用关系构建了一种“关-开”模型用于对食用油中TBHQ的检测方法。实验方案中采用的碳量子点具有良好的荧光性能,且易于制备、绿色环保,基于此优势建立了用于检测食用油中TBHQ的新方法,相较于国标气相色谱法而言,该方法的检测精度略不及后者,但由于其检测条件不易受外界环境干扰,更适用于市场食用油中TBHQ添加量的初步快速筛查。
