B族链球菌定植产妇的产程管理与围生结局的研究
2024-02-27陈璐璐
陈璐璐 王 繁
B族链球菌(group B streptococcus,GBS)是定植于女性生殖系统及消化系统的正常菌群,在妊娠期间,GBS可发展为具有侵袭性的病菌,致使母婴发生感染性疾病[1~3]。GBS通过分娩期间或胎膜破裂后的垂直传播,引起新生儿感染、败血症,严重者可致新生儿死亡[4]。目前,我国的产程管理采取新产程标准,目的是给予产妇充分机会进行阴道试产。但是,随着分娩时间或胎膜破裂时间的延长,势必增加母婴感染GBS的风险。国内外关于足月GBS定植产妇的产程管理研究较少,探讨其胎膜破裂持续时间与围生结局关系的研究更不多见。本研究通过对355例足月GBS定植产妇产程特征、胎膜破裂持续时间和围生结局的分析,旨在为GBS阳性产妇产程处理提供依据。
对象与方法
1.对象:选取2020年10月~2021年11月于笔者医院产科住院并接受GBS筛查阳性的足月产妇355例为GBS阳性组,355例GBS筛查阴性为GBS阴性组。纳入标准: ①头位、单胎、孕周≥37周;②均于孕36 周~37周+6天或分娩前行阴道及肛周GBS筛查并有相应结果。排除标准:①霉菌、滴虫性阴道炎症;梅毒、艾滋病等性传播疾病;②双胎、早产、胎位不正、有阴道分娩禁忌证(如前置胎盘、胎盘早剥);③妊娠并发症如子痫前期、妊娠期糖尿病等;妊娠合并症,如合并心脏病、肝肾功能不全等严重的内外科疾病;④分娩前产妇已感染(包括宫内感染、肺部感染、泌尿感染等);⑤胎儿本身存在严重畸形或者严重先天性疾病者;⑥采取选择性剖宫产术结束分娩。本研究经温州医科大学附属第二医院、育英儿童医院医学伦理学委员会批准(伦理学审批号:LCKY2020-312)。
2.研究方法:(1)收集产妇临床资料,包括产妇年龄、孕周、产次、产程发动方式、分娩方式、新生儿出生体重和新生儿性别。产程特征包括胎膜破裂持续时间(计算时间从发生胎膜破裂开始至分娩结束)、第一产程、活跃期、第二产程。围生结局包括产时发热(体温超过38℃),产后发热(体温超过38℃),临床绒毛膜羊膜炎,组织学绒毛膜羊膜炎,住院时间,产后出血≥500ml,会阴损伤情况,新生儿转入新生儿重症监护病房 (neonatal intensive care unit,NICU)、新生儿败血症、胎窘及新生儿黄疸。根据不同胎膜破裂持续时间,将GBS阳性组分为<12h组、≥12且<24h组和≥24h组, <12h作为对照组。根据新生儿是否发生败血症,将GBS阳性组分为新生儿败血症组与新生儿无败血症组。比较各组之间临床资料、产程特征及围生结局的差异。(2)GBS取材方法:采用两根无菌棉签,一根从阴道下1/3采集标本,另一根从肛门同时采集标本,放入无菌培养管中立即送检进行培养,取材过程中无需使用窥阴器。(3)细菌培养与鉴定方法:在5%的羊血脂平板培养基上接种采集的标本,5%CO2中培养24~48h,将可疑菌落进行培养,并做革兰染色涂片。显微镜下的革兰阳性球菌排列呈链状,触酶试验呈阴性,采用WalkAway-96 plus全自动微生物鉴定系统进行生化试验,确定为链球菌属。
结 果
2020年10月~2021年11月期间,笔者医院≥37周分娩量共8848例,阴道分娩率57.45%(5083/8848),足月产妇GBS定植率为8.01%(709/8848)。根据本研究纳入标准,足月单胎头位、无妊娠合并症或并发症进入产程管理的产妇GBS定植率为8.39%(355/4231)。
1.两组产妇临床资料比较:GBS阳性组与GBS阴性组,产妇年龄、孕周、产次、产程发动方式、分娩方式、胎膜早破、新生儿出生体重和新生儿性别比较,差异无统计学意义 (P>0.05),GBS阳性组住院时间略长于GBS阴性组(P<0.05),详见表1。

表1 两组产妇临床资料比较
2.两组产妇产程特征及围生结局比较:GBS阳性组与GBS阴性组,胎膜破裂持续时间、第一产程、活跃期、第二产程、临床绒毛膜羊膜炎、产后出血≥500ml、会阴损伤、胎儿宫内窘迫及新生儿黄疸比较,差异无统计学意义(P>0.05)。GBS阳性组,产时发热14.08%、产后发热12.11%和组织学绒毛膜羊膜炎5.07%,发生率均高于GBS阴性组5.91%、5.63%和1.41%,差异有统计学意义(P<0.05)。GBS阳性组,新生儿NICU转入率22.25%、新生儿败血症发生率11.83%,均高于GBS阴性组7.32%和0.85%,差异有统计学意义(P<0.05),详见表2。
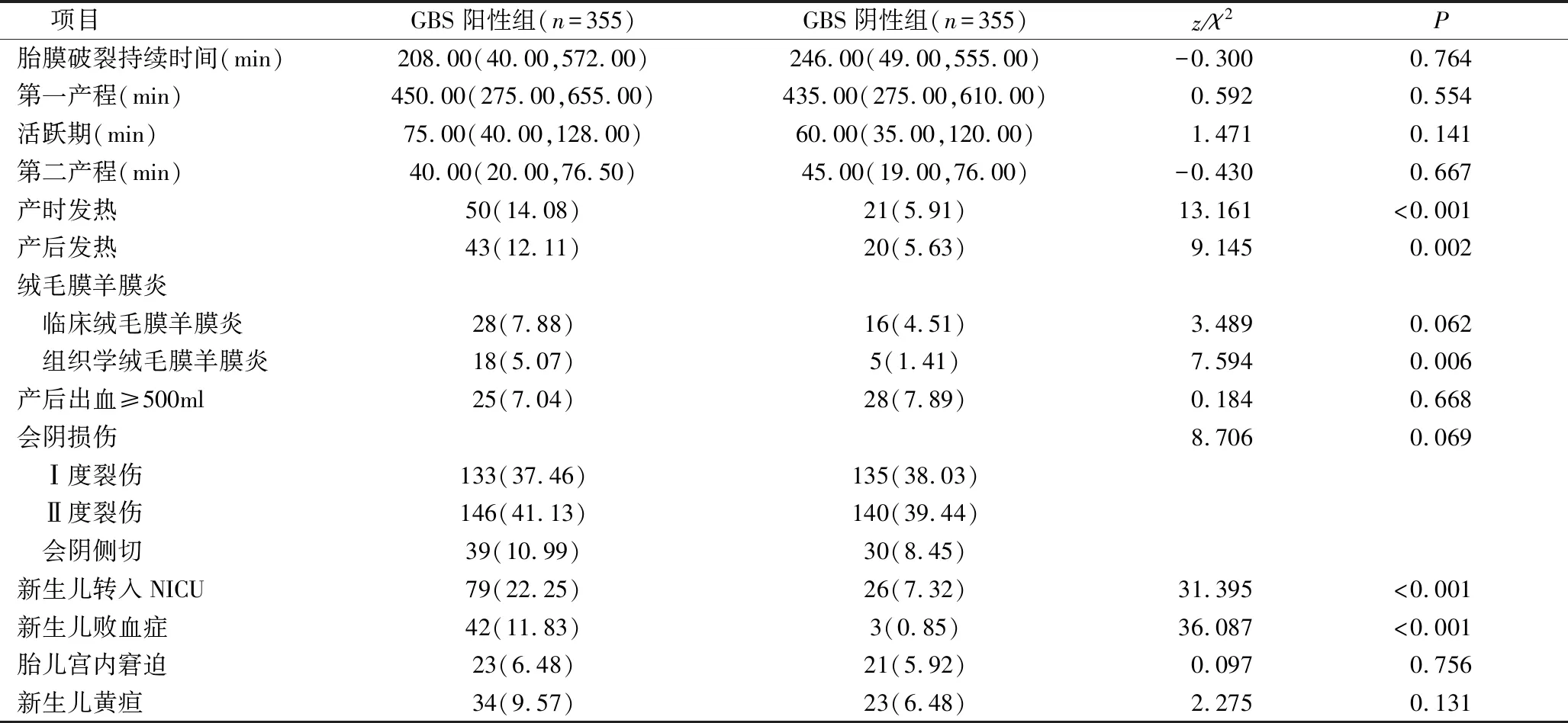
表2 两组产妇产程特征及围生结局比较[n(%),M(Q1,Q3)]
3.GBS阳性产妇不同胎膜破裂持续时间与围生结局关系的比较:3组产妇在产时发热、产后发热、组织学绒毛膜羊膜炎、第一产程、活跃期、第二产程、胎膜破裂方式、胎膜早破、分娩方式、住院时间比较,差异有统计学意义(P<0.05)。≥12且<24h组,第一产程、活跃期、第二产程、住院时间长于对照组,胎膜早破发生率和产钳助娩率高于对照组,差异有统计学意义(P<0.017)。≥24h组,第一产程、第二产程、住院时间长于对照组,胎膜早破、产时发热、产后发热、组织学绒毛膜羊膜炎和剖宫产率高于对照组,差异有统计学意义(P<0.017)。3组临床绒毛膜羊膜炎、产后出血≥500ml、人工破膜、新生儿转入NICU、新生儿败血症、新生儿黄疸及胎儿宫内窘迫比较,差异无统计学意义(P>0.05),详见表3。

表3 GBS阳性产妇不同胎膜破裂持续时间与围生结局关系的比较[n(%),M(Q1,Q3)]
4.GBS阳性新生儿败血症与新生儿无败血症的比较:GBS阳性产妇中,新生儿败血症组与新生儿无败血症组在产妇产程发动方式、分娩方式、胎膜破裂方式、组织学绒毛膜羊膜炎、胎膜破裂持续时间、第一产程、第二产程等方面比较,差异无统计学意义(P>0.05),详见表4。
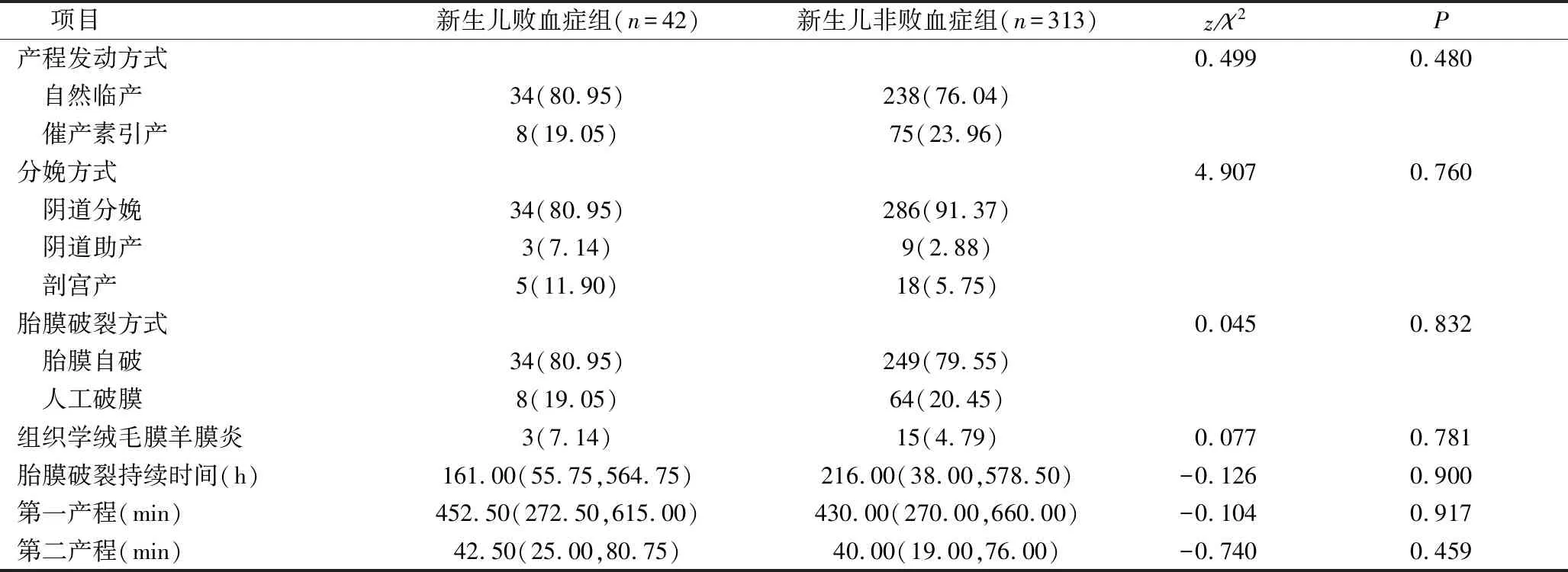
表4 GBS阳性新生儿败血症与新生儿无败血症的比较[n(%),M(Q1,Q3)]
讨 论
GBS是女性阴道常见的定植菌。国内外定植情况并不完全相同,我国GBS定植率为11.3%[2];美国为10%~30%,其中有1/2的产妇在分娩时通过产道将GBS传播给新生儿[4]。本研究中足月头位单胎、无妊娠并发症及合并症产妇的GBS 定植率为8.39%。正确管理GBS定植者的产程,是促进其安全分娩的关键。本研究参考《正常分娩指南》,使用连续电子胎心监护,每4h记录一次生命体征。第一产程,阴道检查频率潜伏期4h一次,活跃期2h一次,当出现产程延长倾向,使用缩宫素加强宫缩,人工破膜促进产程进展,间苯三酚等药物软化宫颈等手段。第二产程末,胎儿娩出时进行单手会阴保护,控制胎头匀速且缓慢娩出。GBS定植产妇一旦临产或者发生胎膜早破,启用全产程抗生素预防感染直至新生儿出生,抗生素首选青霉素。GBS定植产妇,除积极使用抗生素外,余产程处理同GBS阴性产妇。
本研究显示,GBS定植产妇的产程与胎膜破裂持续时间与足月GBS阴性产妇比较并未延长。GBS定植产妇这一产程特征以往的研究较少报道。两者在剖宫产、产后出血、胎膜早破等方面比较差异无统计学意义,这与时春艳等[5]、孟婵等[6]研究结果一致。但Jiao等[7]、王婷婷等[8]报道妊娠晚期GBS与胎膜早破相关,不同研究结果不同,可能与纳入研究的GBS阳性对象标准不一致以及不同地区GBS定植率不同有关。根据上述结果,GBS不影响产程进展。但GBS定植者产时发热、产后发热、组织学绒毛膜羊膜炎、新生儿转科及新生儿败血症等感染相关性分娩并发症发生率明显升高。这是由于GBS产生多种毒力因子,如黏附和侵袭因子、溶血素、透明质酸酶等,干扰宿主受其激发产生的免疫应答,通过黏附和侵袭阴道、绒毛膜、羊膜腔、胎儿等组织,引起绒毛膜羊膜炎和新生儿败血症[9]。
本研究中与对照组比较,当GBS定植产妇的胎膜破裂时间超过12h,分娩并发症并未增加,但是当胎膜破裂时间超过24h,产时发热、产后发热、组织学绒毛膜羊膜炎增多,围生期并发症明显增多(P<0.05)。本研究探讨的是,GBS定植产妇的胎膜破裂时间与分娩并发症之间的关系,产科医生迫切需要一个胎膜破裂持续时间的干预标准,从而对GBS定植者的产程进行更好的管理。随着破膜时间延长,产程也相应延长的原因是由于宫腔内羊水减少,子宫壁紧贴胎儿,宫腔内由于受力不均导致宫缩不协调,影响分娩机转[10]。GBS通过胎膜的破裂孔隙上升到羊水、胎盘及绒毛膜,到达胎儿,胎膜破裂时间超过24h后,GBS与产妇及新生儿的接触时间更长,持续性上行感染的风险增大。GBS作用机制的研究有赖于许多动物模型的建立。有动物实验发现,GBS通过激活整合素和β-连环素信号通路诱导阴道上皮细胞脱落,上皮细胞的脱落反过来促进GBS定植及上行感染[11]。GBS上行感染机制是目前发现的不良妊娠结局的主要原因[9]。GBS带菌者更容易发生组织学绒毛膜羊膜炎。产程延长(尤其是第二产程延长)、胎膜早破和胎膜破裂持续时间≥24h是GBS发生组织学绒毛膜羊膜炎的危险因素[12~17]。
本研究结果显示,GBS定植产妇随着破膜时间延长而出现的分娩并发症与上述报道一致。另外,第二产程延长,会阴Ⅲ、Ⅳ度裂伤及剖宫产率同样增多[12]。本研究中没有出现会阴Ⅲ、Ⅳ度裂伤,但是GBS定植产妇破膜时间≥24h后,会阴侧切率20%(6/30)和剖宫产率20%(6/30),均高于对照组8.76%(25/289)和4.5%(13/289)(P<0.05)。分娩时间延长,GBS引起的发热、组织学绒毛膜羊膜炎增多,感染风险增加,产妇出现疲劳、对难产的担忧等负面分娩体验,都与剖宫产率升高相关,因此提出GBS产妇胎膜破裂持续时间的关键时间节点,GBS定植产妇尽可能在胎膜破裂24h内结束分娩,以减少GBS带来的分娩并发症。
破膜时间过长是GBS引起新生儿败血症的危险因素之一[18]。本研究中GBS阳性组新生儿发生败血症的风险没有显示出与胎膜破裂持续时间、产程的相关性,考虑本研究采取的是全产程的产时抗生素预防措施。美国妇产科医师学会建议GBS阳性者均需接受产时预防性使用抗生素,可降低新生儿早发型GBS感染(group B streptococcal early-onset disease,GBS-EOD)[3, 19]。尽管少部分产妇产程过快,已有研究发现2h的抗生素暴露减少GBS阴道菌落计数,也减少新生儿败血症[3]。本研究中抗生素的使用对于预防新生儿败血症取得一定成效,却没有降低组织学绒毛膜羊膜炎、产时发热发生率。但本研究的样本量较小,仅为一家医院数据,数据可能存在偏倚,后续研究需继续扩大样本量。
综上所述,GBS不影响产程进展,但增加母婴感染风险。为了促进GBS定植产妇安全的阴道分娩,在产时抗生素预防措施下,建议积极采取干预措施确保GBS产妇在胎膜破裂24h内结束分娩。
