肝细胞癌复发进程中DNA修复调节的蛋白质组学分析及验证
2024-02-26王艳艳江忠勇刘晨霞那琬琳许宏宣
常 凯, 王艳艳, 江忠勇, 孙 巍, 刘晨霞, 那琬琳, 许宏宣, 谢 静, 刘 媛, 陈 敏,5
1 中国人民解放军西部战区总医院检验科, 成都 610083
2 成都市第七人民医院检验科,成都医学院附属肿瘤医院, 成都 610041
3 四川省疾病预防控制中心微生物检验所, 成都 610041
4 成都市实验外国语学校生物教学与研究组, 成都 611134
5 西南大学药学院/中医药学院, 重庆 400715
我国每年肝细胞癌(HCC)新发病例数超全球50%以上,死亡率逐年升高[1]。HCC 的发生发展受一系列遗传和环境因素共同作用,致病机制复杂多样。手术切除目前仍是主要治疗方法,但术后的高复发率(5 年复发率>60%)使得预后并不理想[2]。影响肝癌术后复发的因素众多,如临床病理学特征、伴发的肝病背景、宿主炎症免疫反应状态等[3]。近年来提出,细胞稳态的破坏及遗传信息的不稳定性是肿瘤复发的重要诱因。随着细胞生物学、遗传与表观遗传学,特别是组学技术的进步与发展,对肝癌复发的分子机制认识也逐渐加深,但仍不明确[4]。本研究应用蛋白质组学标记定量分析技术对肝癌复发相关差异蛋白进行检测和注释分析,以期进一步对遗传信息稳定性遗传机制进行探讨。
1 材料与方法
1.1 材料 来源于西部战区总医院2013—2020年冻存的肝癌组织样本。确诊HCC 且行肝切除术后5 年预后良好的肝癌组织10 例作为HCC 未复发组;确诊HCC 且行肝切除术后2 年内复发的肝癌组织10 例为HCC 复发组。20 例样本pTNM 分期均为Ⅱb 期,中低分化。排除糖尿病、冠心病、高血脂、高血压、肾病、遗传病和自身免疫系统疾病。采用样本为患者首次肝癌切除术中所切除的组织,并置于保护液中液氮保存,备用。
1.2 药物及试剂 十二烷基硫酸钠-SDS(中国索莱宝)、甲酸钠(美国Sigma-Aldrich 公司);蛋白酶抑制剂(瑞士Roche公司);尿素、二硫苏糖醇、四乙基溴化铵(美国Sigma-Aldrich 公司);BCA 蛋白检测试剂盒(美国Millipore 公司),胰蛋白酶(美国Promega 公司);甲酸铵(美国Sigma-Aldrich公司);乙腈(美国Supelco公司)。
1.3 方法
1.3.1 总蛋白提取 将7 mol/L 尿素,1 mg/mL 蛋白酶抑制剂和2% SDS 充分混合配置样本裂解缓冲液,加入待测样本后于冰面上进行超声破碎,5 min 后进行冷冻高速离心,15 000 r/min,20 min,吸取上清液待用。
1.3.2 蛋白消化与标记 使用BCA 蛋白检测试剂盒测定上清液中的总蛋白浓度。将每100 μg 蛋白移至新的试管中,并用8 mol/L 尿素稀释至100 μL。样本中加入11 μL二硫苏糖醇(浓度为1 mol/L),37 ℃孵育1 h。将样品置于10 K 超滤管,14 000 r/min 离心10 min。取120 μL 碘乙酰胺(浓度为55 mmol/L)加入样品中,避光孵育20 min,8 mol/L尿素被10 mmol/L三乙基碳酸氢铵替换3次。测序级别改良的胰蛋白酶于37 °C 孵育12 h。消化后的样品13 500 r/min 离心15 min。真空干燥机干燥后在0.5 mol/L三乙基碳酸氢铵中溶解。取等量蛋白进行Trypsin酶切,得到相应样品的多肽;分别用不同的串联质量标签(TMT)对样品进行标记,室温下放置2 h。标记样本在真空中混合并干燥。
1.3.3 高pH 反相分离 配置缓冲液A:20 mmol/L 甲酸铵溶液,使用氢氧化铵滴定至pH 为10.0;配置缓冲液B:20 mmol/L 甲酸钠,溶剂为80%乙腈,使用氢氧化铵滴定至pH为10.0。使用缓冲液A对肽混合物进行溶解,使用Thermo Fisher Scientific Ultimate 3000 高效液相色谱系统对样本进行分离,反向分离柱为美国Waters 公司C18反相柱(4.6 mm×250 mm,5 μm)。高pH分离用线性梯度方式进行,缓冲液B 从5%起始至45%,时长40 min,柱温30 ℃,流速1 mL/min。分离12个馏分用于下一步检测。
1.3.4 低pH nano-HPLC-MS/MS 检测 肽段分馏组分用溶剂C(含0.1%甲酸的超纯水)分别溶解,液相色谱分离,串联质谱分析。10 μL样品上样过色谱柱(Thermo Scientific Acclaim PepMap C18,100 μm×2 cm),流速10 μL/min,3 min。随后将线性梯度为2%~40%的D 液(含0.1%甲酸的乙腈)分别流经分析柱(Acclaim PepMapC18,75 μm×15 cm)70 min,流速300 nL/min,电压2 kV。
1.4 数据处理
1.4.1 蛋白鉴定与定量 在所有样本的蛋白中光谱值≥2的样品定义为特定蛋白并进行蛋白定量。蛋白相对定量是基于报告离子比率,其反映了肽的相对丰度。使用medians 对Mascot 搜索结果进行平均和量化。蛋白的倍比差异>1.2或<0.83,且P<0.05认为具有差异表达[5]。
1.4.2 蛋白功能注释与富集分析 用GO、KEGG 和COG/KOG数据库对蛋白进行注释,以获得其功能。在P≤0.05差异表达蛋白中筛选关键信号通路[6]。
1.4.3 统计学方法 应用SPSS 24.0 软件对数据结果进行统计分析。正态分布的计量资料以±s表示,2组间比较采用成组t检验;多组间比较采用单因素方差分析,进一步两两比较采用LSD-t检验。P<0.05 为差异有统计学意义。
20世纪60年代已经开始利用近红外光谱对谷物的蛋白质及其他成分进行检测。同时研究人员还采用近红外光谱技术对小麦的蛋白质、脂肪、淀粉等多种检测指标进行检测与分析。近红外光谱技术有效地提高了小麦的检测,对小麦的检测具有重要意义。近年来,近红外光谱技术在脱氧萎镰菌醇与小麦优良品种筛选检测中有了新的发展。
1.5 差异蛋白验证分析 应用差异蛋白ELISA 试剂盒对差异蛋白进行验证分析,ELISA 试剂及抗体购于成都元极生物科技有限公司,使用分光光度仪对荧光值进行判读分析。
2 结果
2.1 HCC复发组与未复发组表达量差异蛋白富集 经全蛋白质组学定量分析后,共鉴定得到唯一肽段数38 575个,蛋白14 578 个,通过对信号通路的分析确定蛋白参与的最主要生化代谢途径和信号转导途径,结果表明排名第一位的为癌症通路(ko05200),共有476 个蛋白参与。HCC 复发组与未复发组富集结果显示,富集因子排名前5 位分别是:DNA 复制(0.414)、错配修复(0.409)、鞘脂信号通路(0.250)、碱基切除修复(0.172)、核苷酸切除修复(0.171)(图1)。其中DNA 复制、错配修复、碱基切除修复、核苷酸切除修复均属于复制与修复层级,表明在肝癌复发的进程中,DNA修复具有重要作用。
在富集蛋白数量中,18个蛋白富集在DNA复制、17个蛋白富集在错配修复、6 个蛋白富集在碱基切除修复、9个蛋白富集在核苷酸切除修复。结合差异蛋白数量和Q值绘制评分前10 位通路富集气泡图(图2),DNA 修复相关的4 个通路在蛋白数量、相关性和富集因子三个参数中均位居前列。
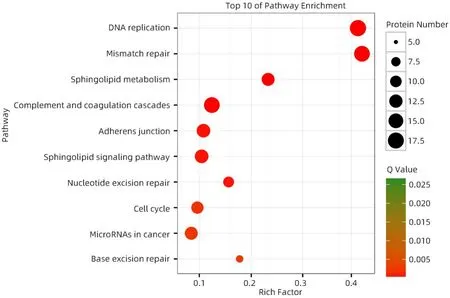
图2 京都基因和基因组百科全书的本体论(KO)富集气泡图Figure 2 Bubble maps of Kyoto Encyclopedia of Genes and Genomes ontology
2.2 肝癌复发进程中复制复合体调控通路的蛋白表达本研究在真核生物复制复合体通路中共检出13 个蛋白(图3):小染色体维持复杂组件2~7(minichromosome maintenance complex component,MCM2~7)、增殖细胞核抗原(proliferating cell nuclear antigen,PCNA)、复制因子C 亚基1(replication factor C subunit 1,RFC1)、复制因子C 亚基4(replication factor C subunit 4,RFC4)、复制因子C 亚基5(replication factor C subunit 5,RFC5)、皮瓣结构特异性内切酶1(flap structure-specific endonuclease1,FEN1)、DNA连接酶1(DNA ligase 1,LIG1)、复制蛋白A3(replication protein A3,RPA3)。其中10 个蛋白在肝癌复发组织中显著减少,分别是MCM2(P=0.018)、MCM3(P=0.047)、MCM4(P=0.014)、MCM5(P=0.008)、MCM6(P=0.006)、MCM7(P=0.007)、PCNA(P=0.019)、RFC4(P=0.002)、RFC5(P<0.001)、LIG1(P=0.042)。
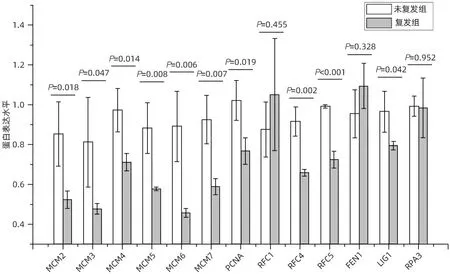
图3 复制复合体(真核生物)富集通路蛋白表达差异Figure 3 Differential protein expression of replication complex (eukaryotic) enriched pathways
2.3 肝癌复发进程中核苷酸切除修复通路的蛋白表达核苷酸切除修复通路中共检出6个蛋白。其中PCNA(P=0.019)、RFC4(P=0.002)、RFC5(P<0.001)、LIG1(P=0.042)共4 个蛋白表达水平显著减少。DNA 聚合酶δ(DNA polymerase delta,POLD)和RFC1 在该研究中检出,但差异无统计学意义(图4)。
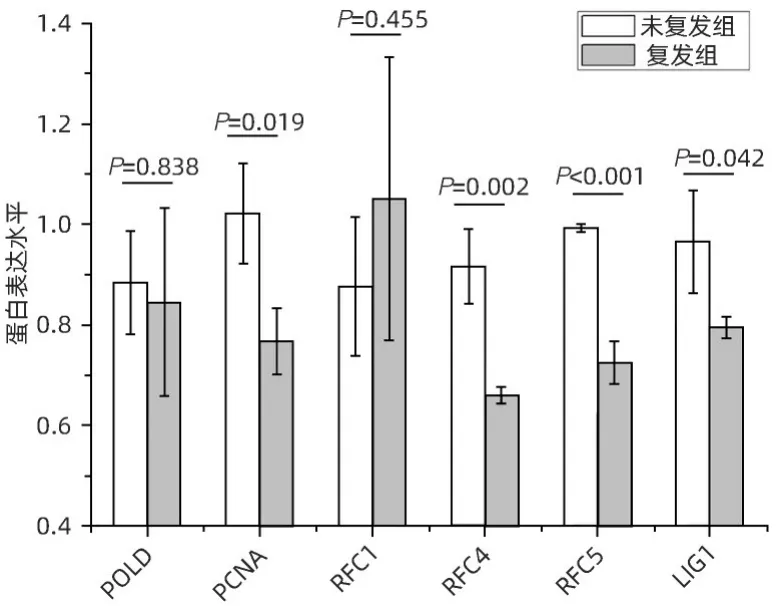
图4 核苷酸切除修复富集通路蛋白表达差异Figure 4 Differential protein expression of nucleotide excision repair-enriched pathway proteins
2.4 肝癌复发进程中碱基切除修复通路的蛋白表达全蛋白质组学定量分析共检出7个蛋白富集在碱基切除修复通路中,分别是PCNA、FEN1、LIG1、DNA 聚合酶β(DNA polymerase beta,POLB)、无嘌呤/无嘧啶内脱氧核糖核酸酶(apurinic/apyrimidinic endodeoxyribonuclease,APEX)、聚(ADP- 核糖)聚合酶[poly(ADP-ribose)polymerase,PARP]、POLD。其中PCNA(P=0.019)和LIG1(P=0.042)在HCC 复发组中显著降低。FEN1、POLB、APEX、PARP和POLD在该研究中有检出,但差异无统计学意义(图5)。
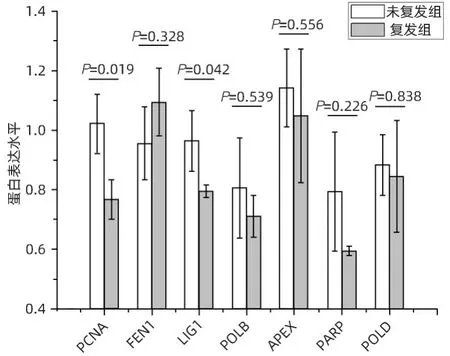
图5 碱基切除修复富集通路蛋白表达差异Figure 5 Differential protein expression of base excision repair-enriched pathways
2.5 肝癌复发进程中错配修复富集通路的蛋白表达该研究中,在错配修复富集通路中共检出9 个蛋白:MSH2、MSH6、RFC1、RFC4、RFC5、PCNA、PRA、POLD、LIG1。其中6 个蛋白在肝癌复发组织中显著减少,分别是MSH2(P=0.026)、MSH6(P=0.006)、RFC4(P=0.002)、RFC5(P<0.001)、PCNA(P=0.019)、LIG1(P=0.042),其他蛋白(RFC1、RPA、POLD)的表达差异无统计学意义(图6)。
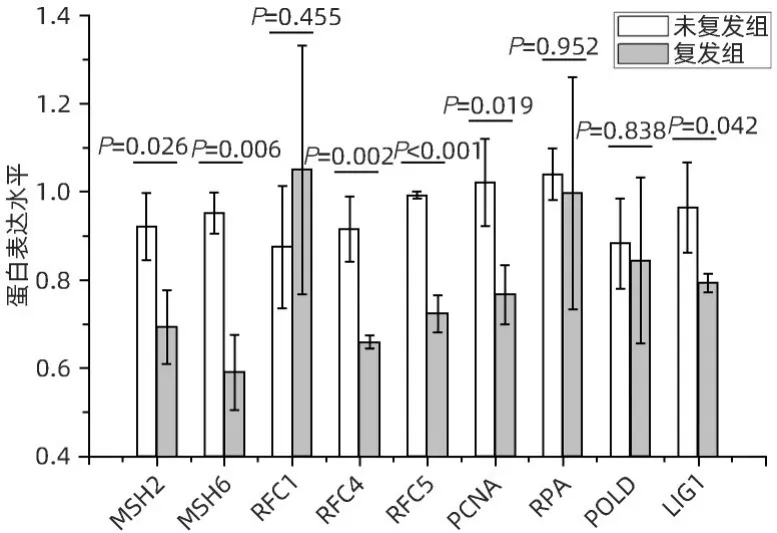
图6 错配修复富集通路蛋白表达差异Figure 6 Differential protein expression of mismatch repairenriched pathways
2.6 差异蛋白在不同组织间的差异表达 将HCC 复发进程中发现的DNA 修复通路差异蛋白进行生物信息学组织表达分析。比较4 个维度中倍比差异(log2FC),包括:(1)HCC/全部癌旁组织(TCGA数据);(2)HCC/癌旁组织(HCCDB数据);(3)HCC/全部肿瘤(TCGA数据);(4)正常肝组织/其他正常组织(GTEx 和TCGA 数据)。HCC/癌旁组织中差异最大的为MCM2(log2FC=1.16),其次为RFC4(log2FC=1.07);正常肝组织MCM2、MCM3、MCM4、MCM6、MCM7和MSH2明显低于其他正常组织(图7)。
2.7 肝癌复发进程中DNA 修复通路差异蛋白富集分析在生物体内,不同蛋白相互协调行使其生物学行为,基于KEGG pathway 分析DNA 修复相关表达差异蛋白在肝癌复发进程中的生物学功能。在真核生物复制复合体通路中,MCM 复合体中7 个组分蛋白表达减少,致使解旋酶能力下降。PCNA、RCF4 和RCF5 的蛋白表达减少使DNA 聚合酶复合体ε 的固定能力减弱。同时LIG1 减少也使连接酶能力降低。这些都可能降低生物体遗传复制能力,并增加突变风险。在肝癌复发进程中,复制蛋白A(RPA)复合体、RNA 酶(HⅠ和HⅡ)和解旋酶Dna2并未发现其蛋白表达变化(图8a)。
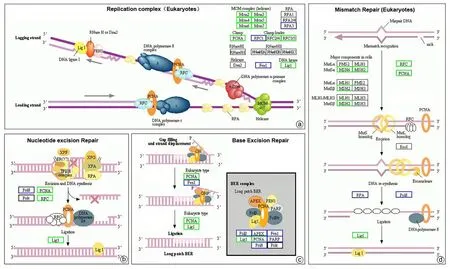
图8 HCC复发组与未复发组差异蛋白富集通路图(差异分析基于KEGG pathway数据库)Figure 8 Differential protein enrichment pathway map in the HCC recurrent and unrecurrent groups(Differential analysis was based on the KEGG pathway database)
核苷酸切除修复主要包括DNA 剪切合成和连接两个部分。在肝癌复发进程中,主要通过减少PCNA、RCF4 和RCF5 蛋白表达降低DNA 聚合酶复合体ε 固定能力,并通过降低LIG1 影响连接酶功能。RPA、XPA、XPG 和转录因子TFⅡH 复合体的蛋白组分不受影响(图8b)。
碱基剪切修复通路中影响肿瘤复发的作用可能是通过降低PCNA 和LIG1 蛋白表达影响长补丁碱基剪切修复复合体(long patch Base excision repair,long patch BER)功能(图8c)。短补丁碱基剪切修复复合体(short patch Base excision repair,short patch BER)功能不受影响。
真核生物错配修复通路中,肝癌复发组织中主要复合体中的DNA 错配修复蛋白MSH2 和MSH6 蛋白减少,DNA 错配修复系统中三大复合体功能减弱,影响错配DNA 的正确剪切及连接,降低了错配DNA 修复能力(图8d)。
2.8 肝癌复发进程差异蛋白验证分析 结合log2FC(T/C)值和P值对上述差异蛋白进行综合分析后,筛选出对DNA 修复调节存在显著差异(P<0.01)的蛋白MCM5、MCM6、MCM7、RCF4、RCF5和MSH6进行临床样本重新采集验证分析(每组10例)。结果表明复发组中除MCM6表现出下降趋势外,MCM5、MCM7、RCF4、RCF5 和MSH6蛋白相对表达量均显著降低(P值均<0.001)(图9)。

图9 HCC复发组与未复发组差异蛋白验证分析Figure 9 Differential protein validation analysis between HCC recurrence and unrecurrence groups
3 讨论
HCC 复发与DNA 结构/表达差异关系密切[7-8],然而是何种原因导致这一现象的发生却鲜有报道。本研究基于TMT标记的定量蛋白质组学方法,就能够导致上述现象的调控通路进行宏观分析,以求精确定位到关键信号通路进行重点剖析。
细胞稳态的破坏及遗传信息的不稳定性是肿瘤及肿瘤复发的重要诱因,由于其分子机制尚不明确,导致缺乏有效的治疗靶点和手段[9-10]。DNA 损伤应答是保障基因组稳定性的关键,能确保将遗传信息准确无误地传给子代细胞[11]。当损伤发生时,细胞启动一系列损伤监控和修复机制,主要包括损伤信号激活和传导[12]、损伤修复和基因转录等生物学过程[13]。本研究应用蛋白质组学标记定量分析技术对HCC 复发相关差异蛋白进行检测和注释聚类分析,发现聚类分值最高且具有重要作用的是DNA 修复相关途径,包括DNA 复制、错配修复、碱基切除修复、核苷酸切除修复通路。
该研究共发现DNA 修复相关差异蛋白12 个,在复发组中MCM2、MCM3、MCM4、MCM5、MCM6、MCM7、PCNA、RFC4、RFC5、LIG1、MSH2 和MSH6 的蛋白表达量显著降低。对DNA 修复相关蛋白进行组织表达谱分析表明:正常肝细胞中上述蛋白的基因表达量均低于其他正常组织;肝癌细胞中的基因表达量均高于癌旁组织。Liu等[14]发现高表达MSH 基因是HCC复发的高危因素;Marshall 等[15]和Liao 等[16]也证明MCM 基因的高表达与肿瘤复发密切相关。然而在本研究中复发组的MSH2等DNA 修复相关蛋白表达显著降低,通过HPA 数据库分析表明MCM2 等DNA 修复相关基因在肿瘤细胞中具有较高的基因表达量,但蛋白的表达量并不高[17]。说明在DNA 修复相关基因的翻译过程中还可能存在其他因素影响其蛋白翻译。
分别对DNA复制、错配修复、碱基切除修复、核苷酸切除修复4 条通路进行注释和蛋白表达分析发现:(1)DNA 复制通路中主要是MCM 复合体和夹子装置主要成分蛋白减少;(2)错配修复通路中主要是夹子装置主要成分蛋白减少;(3)碱基切除修复通路中主要是BER 主要成分蛋白减少;(4)核苷酸切除修复通路中主要是MutS 同聚物主要蛋白减少。表明DNA 修复进程中功能蛋白的显著减少或缺失在HCC 复发进程中具有至关重要的作用。然而其与HCC 复发的因果关系及其具体机制有待进一步研究。
伦理学声明:本研究方案经由西部战区总医院医学伦理委员会批准,批号为2023xjsxxm-3。
利益冲突声明:本文不存在任何利益冲突。
作者贡献声明:常凯、王艳艳、刘媛、陈敏负责课题设计,资料分析,撰写论文;江忠勇、孙巍、刘晨霞、那琬琳、许宏宣、谢静参与收集数据,修改论文;常凯、王艳艳、江忠勇、刘媛、陈敏负责拟定写作思路,指导撰写文章并最后定稿。
