《2023年欧洲器官移植学会共识声明: 肝移植中的生物标志物》摘译
2024-02-26李金明张雅敏
白 易, 李金明, 张雅敏
天津市第一中心医院肝胆胰外科, 天津 300392
共识确立过程由欧洲器官移植学会(ESOT)及其各部门专门的工作组负责,工作组确定了与肝移植(liver transplantation,LT)中生物标志物相关的关键问题。生物标志物被定义为可以客观地测量和评估治疗干预措施在正常生理过程、病理过程或药理学反应中作用的特征性指标。在该共识中,工作组根据PICO 方法(PICO=人群、干预、比较者和结果)制定具体的临床问题。根据PICO的定义,文献检索由移植证据中心的专家人员进行系统评价,随后由指导委员会专家根据需要进行整合。近年来,在临床和基础科研方面,肝细胞癌(HCC)的生物学标志物研究取得了一些进展,有关LT的生物标志物也逐渐引起了人们的关注。因此,大规模的研究,包括LT 术后患者群,对于评估生物标志物的疗效尤为重要。为了更好地指导临床实践,ESOT 于2023 年8 月在Transplant International在线发表了《2023 年欧洲器官移植学会共识声明:肝移植中的生物标志物》[1],以期为医务工作者对LT 的生物标志物的研究提供重要参考和更为准确的建议。
1 LT后肝脏疾病的复发
自身免疫性疾病,如原发性硬化性胆管炎(PSC)、原发性胆汁性胆管炎(PBC)和自身免疫性肝炎(AIH),约占LT 适应证的8%。疾病复发是移植物存活受限的主要原因,因PSC 移植的患者复发率为8.6%~27%,因PBC 移植的患者复发率为10.9%~42.3%,因AIH 移植的患者复发率为7%~42%。复发性疾病的诊断是基于临床、生物学和组织学标准的结合,因此常常具有挑战性。
一些基于组织学,甚至推荐进行肝活检的研究提出可以在没有生化和免疫异常的情况下对疾病复发作出诊断。对于复发性PBC(rPBC),其诊断金标准是组织学指标,包括上皮样肉芽肿导致的胆管破坏、淋巴细胞胆管炎、导管增生、淋巴细胞聚集和胆管缺陷。而碱性磷酸酶和抗线粒体抗体水平升高是不可靠的诊断指标。对于复发性PSC(rPSC),在轻度胆汁淤积的情况下,观察到胆管造影成像和肝活检结果与PSC 相似时,可以作出诊断。LT 前免疫球蛋白G 水平、高转氨酶水平、严重的炎症活动或移除肝浆细胞浸润、伴随自身免疫性疾病、受体年龄<42 岁、供体-受体性别不匹配与AIH 复发(rAIH)的高风险相关。移植后自身抗体,如抗核抗体、抗平滑肌抗体和高滴度抗肝肾微粒体抗体,也可预测rAIH,尽管它们也出现在64%的非自身免疫性肝病移植患者中,但不是特异性指标。
代谢功能障碍相关脂肪性肝炎(MASH)是美国和欧洲最常见的肝脏疾病之一,其患病率在代谢功能障碍相关脂肪性肝病患者中占7%~30%。在美国,MASH 已成为继酒精性脂肪性肝病(ASH)之后的第二大LT适应证,目前在欧洲占LT 适应证的8.4%。移植预后方面,与非MASH 患者相似,MASH 的10 年移植存活率为62%。而另一项来自美国的研究表明,MASH 与PSC、PBC 和AIH相比,LT 后的患者生存率明显较低。移植前因素,如代谢综合征、胰岛素抵抗和动脉高血压,不是疾病复发的可靠预测因素。然而,LT 前和LT 后的高BMI 和LT 后甘油三酯水平升高是重要的预测因子。与自身免疫性肝病类似,肝活检仍然是评估LT后复发MASH(rMASH)的最可靠方法。
对于上述所有疾病,肝活检仍然是诊断原发性疾病复发的金标准。因此,迫切需要发现更可靠的生物标志物。
1.1 方法及结果 使用Medline 和Embase 数据库检索相关文献。LT复发性疾病关键问题的证据见表1。

表1 LT后复发性疾病生物标志物的证据总结Table 1 Summary of evidence for biomarkers in recurrent diseases after LT
1.2 建议 在发布任何关于应用生物标志物可靠地预测和诊断LT 后疾病复发的建议之前,还需要进行更多的研究(证据质量:极低;推荐等级:强)。
1.3 未来研究方向 LT后初始疾病复发过程在表现和严重程度上是不同的。鉴于其对长期预后的影响,确定新的生物标志物用于早期诊断是非常重要的。
总之,解决这一问题的研究数量较少,而且均为回顾性观察,患者数量较少,纳入标准和结果不一致,使得在某些情况下数据集不完整,因此对于使用特异性生物标志物检测LT 后原发性肝病复发不能给出强有力的建议。必须进行大规模的前瞻性研究,以确定生物标志物在预测和诊断方面中的作用。
2 LT后HCC的复发
HCC 是世界范围内最常见的癌症之一,预计未来几十年发病率将增加。并且与HCC相关的死亡率也很高。事实上,治疗策略只对早期肿瘤有效。其中,根据米兰标准,LT 被认为是治疗BCLC A 期患者的最佳选择。尽管米兰标准的应用使复发率显著降低,但一些符合标准的患者仍然会出现复发,更重要的是,忽略了很大一部分尽管不在米兰标准范围内但可能通过LT 治愈的患者。已经提出的几种扩大HCC的纳入标准的模型,通常基于形态学特征、简单的生物标志物(如甲胎蛋白)、移除肝病理和对局部治疗的反应。这些模型已被证明可以充分预测复发风险,但其仍然缺乏反映HCC生物学复杂性的分子因素,在这方面只能部分预测。
事实上,HCC 肿瘤中发生了许多已知的基因突变和其他分子改变,并且多项研究报告了分子生物标志物与肝癌患者LT 预后之间的关联。已在人体组织中评估的生物标志物可能有助于将HCC 分类为指示疾病侵袭性和预后的亚类。此外,依赖于组织的分子分析是侵入性的,通常需要对移除肝进行评估,这严重限制了其在LT前患者的分类和选择以及优化同种异体LT 的使用。在这方面,液体活检是一个很有前途的工具,它代表了一种无需组织就能分析肿瘤成分(细胞或肿瘤细胞释放的DNA、RNA 或其他分子的小碎片)的微创方法。液体活检是动态的,可以在LT前后的不同时间点进行评估。
2.1 方法及结果 使用Medline 和Embase 数据库检索相关文献。解决HCC关键问题的证据见表2。
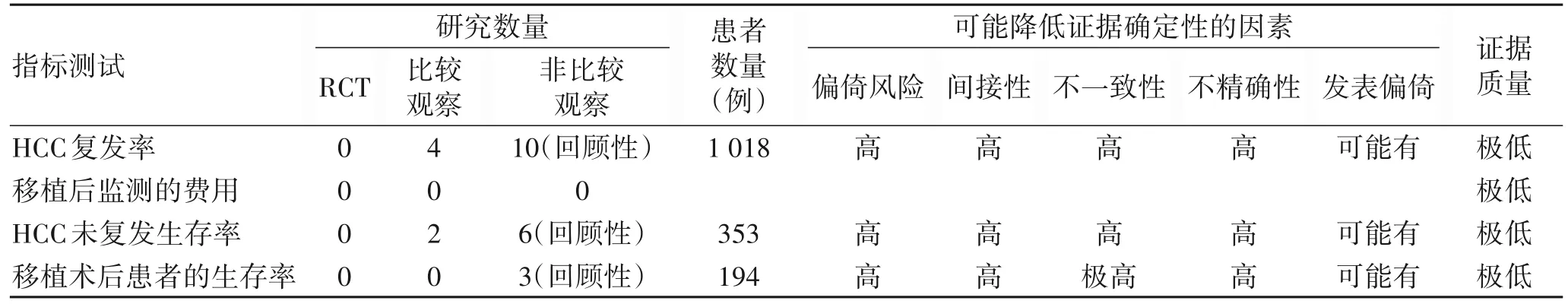
表2 LT后HCC中生物标志物的证据总结Table 2 Summary of evidence for biomarkers in HCC after LT
2.2 建议 综上所述,基于证据质量较低,针对“生物标志物能否用于预测LT 术后HCC 复发”的问题,提出以下建议:虽然研究初步表明液体活检中测量的生物标志物在预测HCC 复发中的作用,但无论是选择作为LT 患者的预测因素还是指导移植后管理,在将其应用于临床实践之前,需要进行更多的研究(证据质量:低;推荐强度:弱)。
2.3 未来研究方向 HCC 是LT 最常见的适应证之一。尽管使用米兰标准进行了谨慎的选择,但HCC仍会在一些符合标准的患者中复发,而其他可能从这种治疗中获益的患者则被排除在外。目前,有一些模型主要基于临床变量和传统生物标志物来预测HCC复发,从而帮助甄选移植患者。目前已知HCC有许多遗传变异,其中一些与移植后预后有关,因此旨在确定新的生物标志物在预测HCC 复发中的作用。本文的目的是评估发现新的生物标志物的证据,并确定它们在甄选患者和复发监测中的潜在作用。本研究结果表明,虽然有可能更好地甄选HCC 患者,但证据质量仍然很低。因此,在收集到更多证据之前,这些生物标志物不能在临床实践中推荐。
HCC 分子生物标志物不仅可以作为LT 前选择候选者的明确标准,还可以指导LT 后的患者管理。然而,在LT 后随访期间进行的连续液体活检可能会造成一种复杂的情况,即可能检测到HCC 复发,但横断面成像却无法显示。这种情况是否会经常出现,遇到这种情况时该如何采取最佳治疗方案,选择观察等待还是无根据地进行系统治疗,仍不确定。但需要注意的是,这两种方法都会给患者和医生带来一定的麻烦。
3 LT中摆脱免疫抑制(immunasuppression,IS)
在过去的三十年中,免疫抑制剂的使用使LT 的预后有了显著改善。然而,长期IS治疗与严重并发症的发生相关,并增加了毒性反应、机会性感染和恶性肿瘤的发生率。例如,使用钙调神经磷酸酶抑制剂(calcineurin inhibitors,CNI)会增加LT受者慢性肾脏疾病(CKD)的发生率。因此,建立长期的移植物耐受性而不需要持续的IS 是移植的主要目标。然而,目前缺乏必要的工具来识别可能从IS最小化和停药中受益的患者,甚至包括那些在IS 减少后存在急性排斥风险的患者。最近的文献描述了来自外周血和同种异体移植物的各种分子、细胞和组织学标志物,这些标志物可能有助于预测LT 后患者能否成功脱离IS 或在IS 减少后可能存在急性排斥反应风险。
3.1 方法及结果 使用Medline 和Embase 数据库检索相关文献。解决IS 最小化和停药关键问题的证据总结见表3~5。
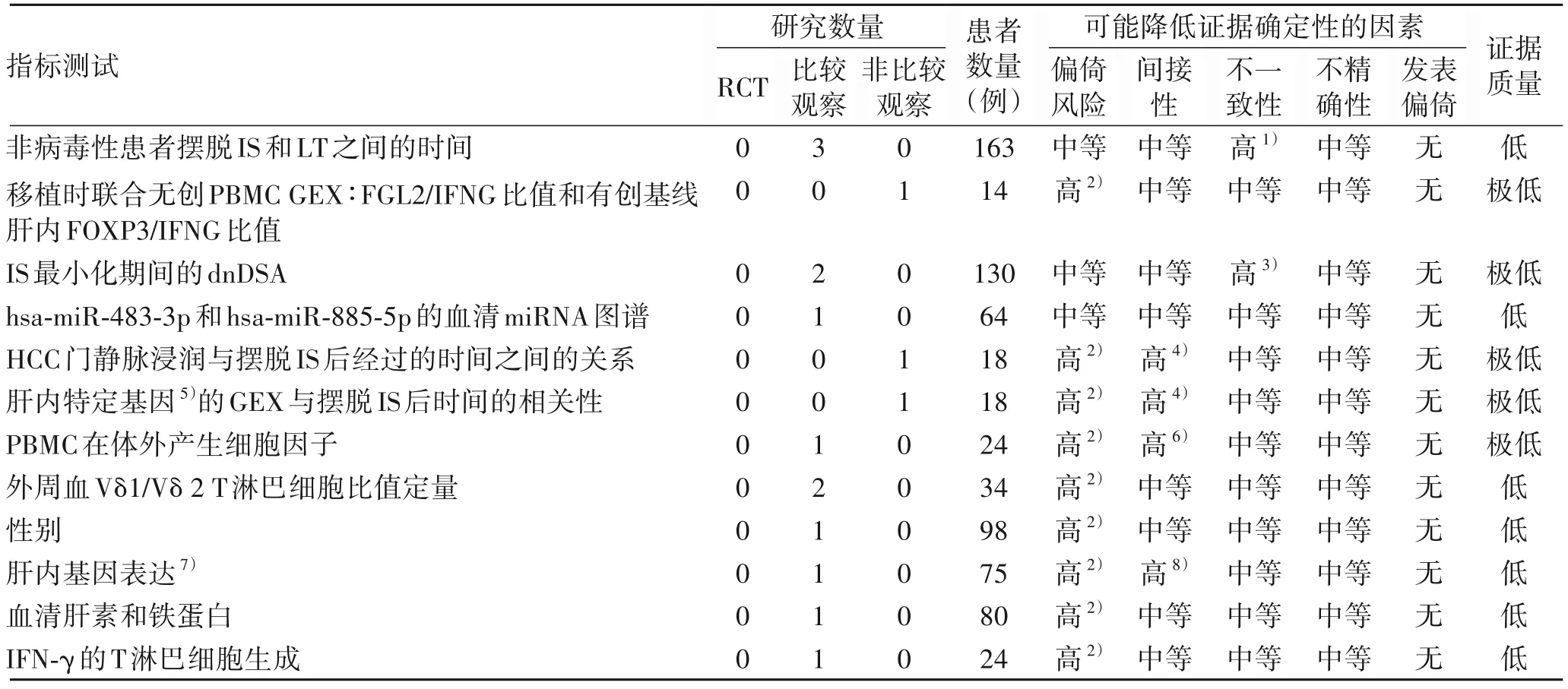
表3 基于GRADE的IS解除后手术耐受性或损伤风险的证据总结Table 3 GRADE approach-based summary of the quality of evidence for the development of operational tolerance or risk of injury upon weaning of immunosuppression

表4 基于GRADE的IS期间亚临床移植物损伤和急性损伤标志物的证据总结Table 4 GRADE approach-based summary of the quality of evidence for the identification of subclinical graft injury and acute injury markers during IS

表5 基于GRADE的LT后急性损伤后基因组标志物的证据总结Table 5 GRADE approach-based summary of the quality of evidence for the genomic markers of acute injury post-liver transplantation
3.2 建议 基于现有证据的质量中等,提出以下建议:生物标志物检测可能通过监测肝损伤来帮助指导摆脱IS。使用非侵入性标志物进行纵向评估可能会对摆脱IS的患者进行更准确的分层(证据质量:中等;推荐强度:弱)。
3.3 未来研究方向 在LT 中,侵入性和非侵入性生物标志物在优化IS 和评估移植物损伤方面的预后及诊断价值已被广泛探讨。然而,目前仍没有可用于临床实践的LT 生物标志物。大型多中心临床试验已经在各种分子水平上产生了大量的数据和信息,为细胞游离生物标志物引入临床治疗提供了大好机会。由于样本量小,缺乏适当的对照组或独立验证,研究结果尚未转化为常规临床应用。
4 LT受者CKD
据估计,40%的LT 受者会发展为3 期CKD,约18%会在LT后5年内发展为终末期肾脏疾病,移植后肾功能恶化的原因之一是CNI。虽然移植后1 年内早期CNI 的减少与长期肾功能的改善有关,但CNI 剂量的减少也与较高的急性排斥反应发生率相关。因此,确定预测LT受者CKD 的生物标志物将有助于选择进行早期CNI 剂量减少和其他肾保护干预措施的患者。
4.1 方法及结果 维持IS的成人LT接受者是文献检索的重点。表6总结了稳定LT受者中CKD预测的证据。

表6 关于预测CKD的证据总结Table 6 Summary of the evidence addressing the prediction of CKD
4.2 建议 基于可获得的证据质量非常低,提出以下建议:生物标志物检测可能有助于预测LT 后的CKD(证据质量:极低;推荐强度:弱)。
4.3 未来研究方向 鉴于肾移植后患者CKD的高患病率,早期识别有CKD风险的患者对于有针对性地干预以预防肾脏恶化至关重要。生物标志物如uGAL、β2 微球蛋白、CD40 抗原等可能有助于早期识别易发展为CKD的LT 患者。然而,现有的数据不足以推荐使用生物标志物指导LT 后患者肾保护干预的具体临床方案。评估LT 后CKD 生物标志物的研究数量有限,大多采用小型单中心队列,缺少独立验证队列,导致这些研究发现难以推广到更广泛的LT 人群。与使用单一生物标志物相比,多种生物标志物和临床变量的结合可能是预测LT后CKD 的最佳策略。未来需要进一步的研究来验证CKD 生物标志物的有效性,然后将其纳入LT 后的患者临床管理。
5 总结
虽然手术并发症和感染通常发生在LT 后早期,但大多数的长期并发症多与疾病复发和持续IS 治疗的不良反应(特别是癌症、心血管疾病和CKD)有关。传统上,需要进行非特异性监测,有时还需要进行侵入性监测,以检测复发或新发疾病过程,并指导干预措施。然而,近年来,移植界的重点已经转移到识别更多的非侵入性生物标志物,以便客观地预测移植受者不良事件的出现。在未来,需要进行更大规模的研究,以验证在初步临床试验中发现的与LT 相关的生物标志物的效用。表7 总结了该工作组关于在LT 后患者预后中使用生物标志物的研究问题和建议。

表7 研究问题和建议的总结Table 7 Summary of research questions and recommendations
利益冲突声明:本文不存在任何利益冲突。
作者贡献声明:白易、李金明负责文章翻译;张雅敏负责文章审校。
