微塑料在某水厂水源与处理工艺中的时空分布
2024-02-26张山风蔡佳男王建华
张山风,高 乐,刘 朵,蔡佳男,王建华
(北京市自来水集团有限责任公司,北京市供水水质工程技术研究中心,北京 100012)
微塑料被定义为粒径小于5 mm的塑料颗粒[1],有很多研究调查了微塑料在水体中的分布情况。孙晓楠等[2]通过总结相关文献,发现我国自然水体的微塑料平均丰度为(3 604.2±5 926.4)个/m3,我国城市水体的微塑料平均丰度为(7 722.6±9 505.7)个/m3,进一步分析数据发现我国地表水体的微塑料污染情况受到周围地区社会经济发展情况的影响显著;葛琦等[3]在查阅了相关文献后发现微塑料已经在世界各地的各类水体中被广泛检出;Gonzlez-Pleiter等[4]在南极洲也检测到了存在于淡水介质中的微塑料。由此可见,微塑料已经广泛存在于水环境中。
环境中的微塑料能够在水力、风力等作用下发生迁移,并最终赋存于水体和土壤中。刘超等[5]总结了相关文献发现,微塑料由人类生活用品、垃圾、基础设施等释放进入环境后,存在多种迁移途径。在水体环境中,微塑料非常容易随雨水径流迁移,雨水径流直接或间接将微塑料送至河流,进而随支流汇入干流,最终进入海洋。与此同时,部分微塑料在水环境中发生老化、分解并逐渐沉降,从而进入其他介质中。在土壤介质中,微塑料可直接从城市垃圾、农用物品中释放进入土壤,也可以通过地表径流、大气沉降等方式进入土壤。
水环境中的微塑料会被生物摄入体内并随食物链传递。赵培强等[6]基于全球鱼类相关文献分析发现,大部分地区的半数以上鱼类受到了微塑料污染。在微塑料对鱼类毒性效应的研究中,还存在微塑料经食物链传递后进入鱼类体内的研究。周刚等[7]在对比相关文献时也发现,水环境中的微塑料容易被水中的生物吞噬,并沿食物链富集,微塑料也可以被微生物定殖,并随其长距离迁移。
北方某市的自来水以“南水北调”水与本地水共同作为水源,已有研究调查了相关水体的微塑料分布情况。李丹文[8]研究了作为南水北调工程起点的丹江口水库中微塑料分布情况,该研究对比了不同采样时期与采样点深度对微塑料分布产生的影响,汛期库区水体平均微塑料丰度为(7.205±4.438)个/L,非汛期库区水体微塑料平均丰度为(8.228±4.687)个/L,均以小于0.5 mm尺寸的微塑料为主,且越小尺寸的微塑料占比越大;何文宣等[9]研究了北京密云水库中的微塑料空间分布情况,水库表层水体中微塑料平均丰度为(6.83±1.87)个/L,其中小于等于0.5 mm的聚对苯二甲酸乙二醇酯(PET)占比最高,并分析了微塑料的主要来源与其进入水库的途径。
水厂的常规工艺对10 μm以上的微塑料有较好的去除效果。孙晓晨等[10]总结了相关文献发现,水厂混凝沉淀工艺对微塑料的总体去除率在40.5%~62.0%,其中大粒径(大于50 μm)与纤维状的微塑料更容易被混凝沉淀去除,各水厂去除率的差异可能由水质、微塑料浓度与种类、水厂处理条件等造成。过滤工艺对微塑料的去除效果会受过滤介质和微塑料本身性质的影响,同时不同研究中过滤工艺的进水微塑料情况受前置工艺影响较大,对微塑料的整体去除率在29.0%~51.1%,其中石英砂滤料对50 μm以上的微塑料去除效果优于50 μm以下的微塑料。在臭氧-活性炭工艺中,微塑料去除率在38.7%~60.9%,其中臭氧处理部分可能出现负去除率,推测原因为水流的剪切力作用使微塑料破碎或微塑料表面附着的有机物被氧化导致其重新暴露在水中,从整体去除效果上看,臭氧-活性炭工艺对小粒径和球状的微塑料的去除效果更好。
本研究通过检测北方某水厂中采集的样品,分析净水工艺对微塑料的影响,以及不同水源、不同时期的水厂原水中微塑料分布情况。
1 材料与方法
1.1 样品采集方法
采样地点位于北方某水厂中,该水厂以“南水北调”水(以下简称“南水”)与本地水库水共同作为水源,于不同时期共进行了3次采样,研究期间水源进行过两次切换,水厂工艺流程与采样点位置如图1所示。
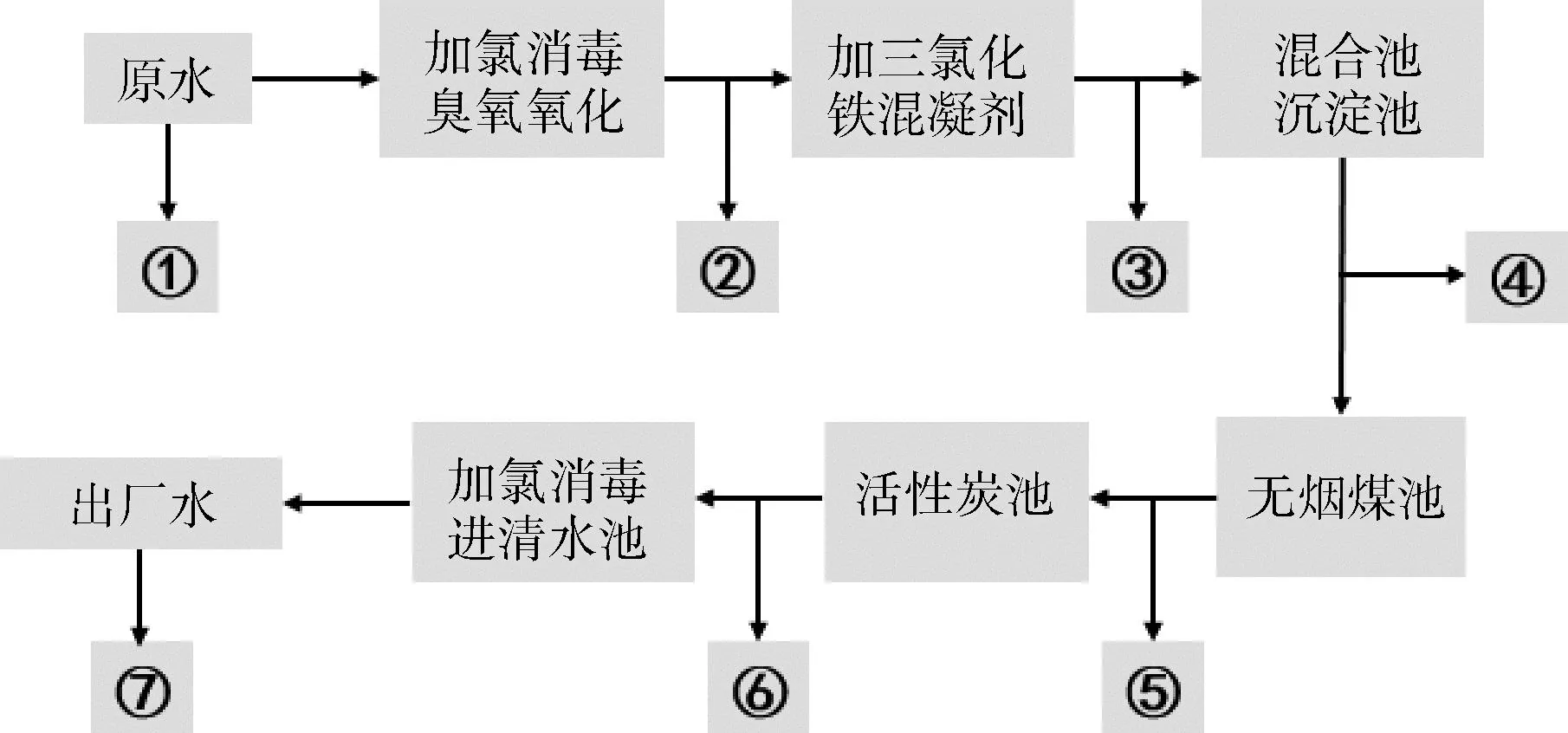
注:①—原水;②—预氧化出水;③—混凝进水;④—沉淀池出水;⑤—煤池出水;⑥—炭池出水;⑦—出厂水。
于2021年7月(第一次采样,夏季丰水期,原水为南水)采集了全部采样点的样品,分别于2021年12月(第二次采样,冬季枯水期,原水为本地水库水)和2022年3月(第三次采样,春季枯水期,原水为南水)采集了原水、炭池出水、出厂水的样品。
每个采样点采集3个平行样,使用2 L玻璃样品瓶与金属取水器,经润洗后取满,带回实验室进行预处理。采样与预处理过程中,试验人员穿着棉质试验服,佩戴丁腈手套,试验用具尽量避免使用塑料制品,并在试验前用纯水清洗干净。
1.2 样品预处理方法
取一定量样品在真空抽滤装置上用10 μm不锈钢滤膜抽滤,将滤膜放入50 mL 30%过氧化氢溶液中,在65 ℃下避光振荡消解24 h。消解后的液体用10 μm不锈钢滤膜抽滤,将滤膜放入甲酸钾浮选液中超声30 min使微塑料从滤膜上脱落后取出滤膜。含有微塑料的浮选液静置12 h后,每2 h对其进行密度浮选,共3次。将浮选完成的液体用10 μm不锈钢滤膜抽滤,将滤膜放入100 mL 30%过氧化氢溶液中再次消解24 h,以去除残留的浮选液。消解后的液体用10 μm不锈钢滤膜抽滤,将滤膜放入15 mL无水乙醇中超声30 min使微塑料被洗入乙醇中,取出滤膜,使用氮吹仪吹脱乙醇进行浓缩,当乙醇余量很少时密封冷藏保存,等待上机检测。
1.3 样品检测方法
使用安捷伦8700LDIR型激光红外成像系统检测预处理完毕的样品,该仪器利用自动识别技术与红外光谱技术,可以扫描并识别样品中粒径在20~500 μm的微塑料颗粒,并检测得到微塑料的数量、成分与粒径。样品的检测时间受样品中颗粒数量影响,颗粒越多,耗时越长。本研究中用此仪器检测每个样品的平均用时约为7 h。
由于本研究所用仪器仅能检测20~500 μm的颗粒,在样品预处理过程中选用10 μm的滤膜进行过滤,且文中仅讨论粒径为20~500 μm的微塑料分布情况。因此,受检测手段的限制,本研究检测得到的微塑料丰度数据较真实值低。
目前最常见的微塑料检测方法为红外光谱法与拉曼光谱法,红外光谱法可用于检测粒径为20 μm以上的颗粒,拉曼光谱法可检测粒径大于1 μm的颗粒,而表面增强拉曼光谱法可检测1~100 nm的纳米微塑料,若要检测全部小粒径的微塑料则需要用裂解气相色谱-质谱法或液相色谱法,得出微塑料在样品中的质量浓度。但后两种方法的缺点是必须用分级过滤的方法来筛选不同粒径的微塑料颗粒,无法获得单个颗粒的粒径与形状信息,并且可以检测的微塑料种类少于前两种方法[11-13]。
2 结果与讨论
2.1 全工艺流程中样品检测结果
2.1.1 微塑料丰度
如图2所示,2021年7月夏季丰水期采样(第一次采样),原水为南水,采集了全工艺流程的水样。从检测结果中可以看出,每个采样点3个平行样的检测结果偏差较大。采样点为水厂内的水渠、滤池或专用取样口,基本可以排除采样深度产生的影响,推测是微塑料本身的性质造成的。微塑料因其种类繁多、形态各异而导致其在水体中的分布不均匀,故难以保证样品检测结果的稳定性,采样时必须多采集平行样使检测结果更具参考性。
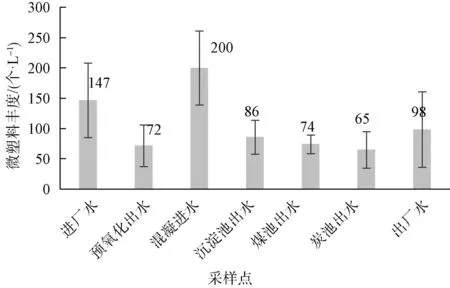
图2 2021年7月微塑料丰度检测结果
预氧化出水的样品为原水经过预臭氧和预加氯消毒后的水样,预氧化工艺的去除率约为51%,由于臭氧和加氯之间没有可进行采样的点位,故微塑料减少的原因未能确定。由于未见研究表明次氯酸钠会对微塑料产生去除效果,推测产生此现象是臭氧氧化工艺造成的。研究[10]表明臭氧氧化可能会造成微塑料丰度增加,其原因是水流的剪切力作用使微塑料破碎或微塑料表面附着的有机物被氧化导致其重新暴露在水中进而被检测到,但在本研究中微塑料丰度下降明显,这与文献中的现象有较大差异,推测产生这种现象的原因是部分微塑料颗粒受到臭氧工艺影响而破碎,粒径变小。而本研究所用检测方法仅能检测20~500 μm的样品,破碎后的微塑料颗粒过小,未能被检测到,所以产生了微塑料丰度大幅下降的结果。
在混凝进水中微塑料丰度大幅增加,此采样点与预氧化出水采样点之间仅存在“投加混凝剂”这一步处理工艺,微塑料丰度的上涨极有可能来源于投加的三氯化铁混凝剂。同时,出厂水中的微塑料丰度高于炭池出水,这两个采样点之间也仅存在“加入消毒剂并进入清水池”这一步,说明净水药剂很可能会引入微塑料污染。混凝剂、消毒剂等净水药剂在生产过程中很可能存在塑料制品的参与,在药剂运输与储存时也可能使用了塑料容器,甚至制造药剂时所用的水中也可能已经存在微塑料,但在本研究中没有对净水药剂进行检测,故此推论有待进一步研究加以证实。
混凝沉淀工艺对微塑料有明显去除效果,去除率为57%,这与文献中的现象相似[10,14-15]。无烟煤与活性炭对微塑料的去除效果均较差,分别约为14%和12%。混凝进水与出厂水两处的微塑料丰度异常增加,导致整体工艺的微塑料去除率仅有约33%,若仅计算混凝沉淀、无烟煤、活性炭对微塑料去除效果,去除率可达约68%。由此可见,在没有引入外部微塑料污染的情况下,常规净水工艺可以较为有效地去除微塑料。
2.1.2 微塑料粒径
如图3所示,水厂中微塑料粒径以20~50 μm为主,占比为58%~86%,且所有样品中绝大多数微塑料的粒径都小于100 μm,可见对于净水处理而言,应将研究重点放在粒径100 μm以下的颗粒上。
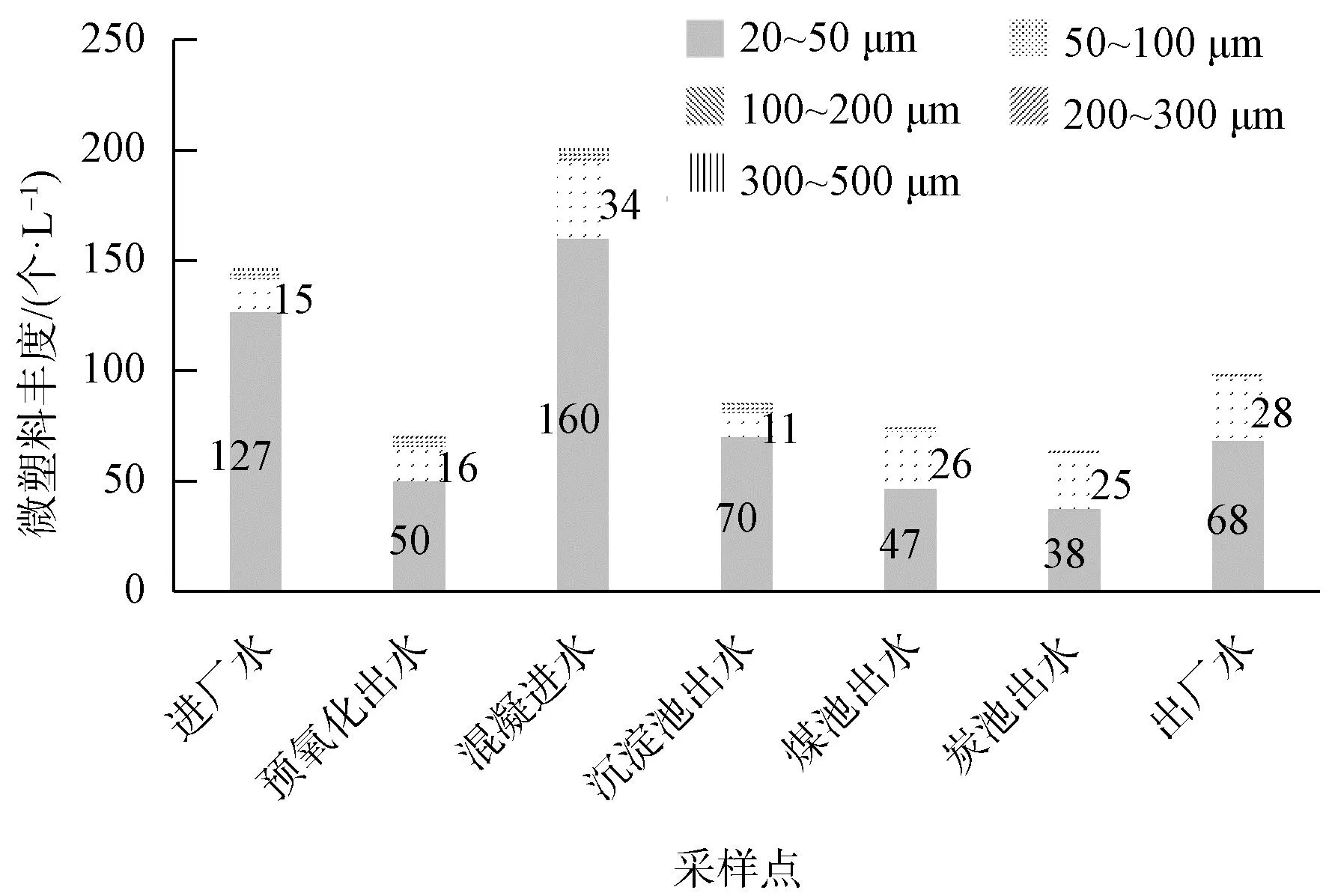
图3 2021年7月微塑料粒径检测结果
图3中可以看到,20~50 μm粒径的微塑料受净水工艺影响更加明显,在预氧化出水处的微塑料丰度下降原因可能与前文所做的推测相同。混凝沉淀工艺对20~50 μm和50~100 μm微塑料的去除率分别约为56%和68%,对粒径较大的微塑料去除效果更好,这与文献[10]中的现象一致。在煤池与炭池中对20~50 μm的微塑料去除效果优于50~100 μm的微塑料,且在煤池中50~100 μm的微塑料增多。目前无法确定出现此现象的原因,微塑料的来源可能包括滤料中的微塑料析出,但这部分微塑料是滤料截留后再析出的,或是类似于净水药剂,在制造过程中就引入了微塑料,还需要进一步研究。另外,在混凝进水与出厂水中,疑似由净水药剂引入的微塑料主要粒径为20~50 μm。
2.1.3 微塑料组分
如图4所示,样品中微塑料优势组分为聚丁二酸丁二醇酯(PBS)、聚丙烯酰胺(PAM)、PET、聚酰胺(PA)、聚丙烯(PP)。
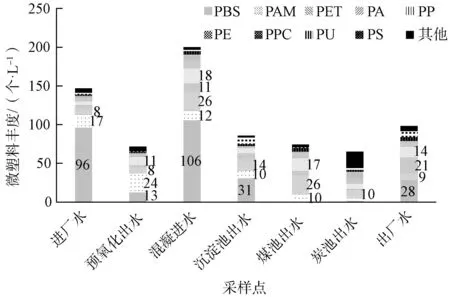
注:PE—聚乙烯;PPC—聚甲基乙撑碳酸酯;PU—聚氨基甲酸酯;PS—聚苯乙烯。
PBS微塑料在水厂工艺中的丰度变化最大,预氧化、混凝沉淀和煤滤工艺均对PBS微塑料有很好的去除效果。PBS是一种生物可降解塑料,但降解速度通常以天为单位,故无需考虑其在水处理过程中降解的可能性。原水中的PBS占比达到65%,这可能与人类活动有很大关系,通过不同方法制造或加入不同添加剂的PBS应用十分广泛,应用范围包括一次性餐具、包装袋、日用品、农用材料、医用材料等。当今社会越发关注环境保护,PBS作为一种性能优异的新型可降解材料而被广泛使用,可能导致水中的PBS微塑料含量多于其他组分。另外,在可能引入了微塑料污染的混凝进水与出厂水样品中,PBS微塑料也明显增加,这代表在混凝剂与消毒剂中可能也含有较多此种微塑料。鉴于PBS广泛的用途,在混凝剂的制造过程中引入的可能性较大,例如产品的容器、原材料的包装袋、制造用水等都可能是其污染源。
本试验测得的PAM微塑料不溶于水,在经过预处理后依旧保持固体状态,所以此PAM微塑料与水处理中常用的PAM助凝剂为不同物质。PAM微塑料在样品中含量不多,其在工艺中的变化也不明显。
PET可纺成聚酯纤维,即涤纶,应用范围包括饮料瓶、产品包装、绝缘膜、电器插座、开关、多种电子电器零件、汽车零件、机械工业齿轮及叶片等。PET微塑料在原水中含量很少,而在加入混凝剂与经过煤池时含量明显增加,此现象增加了混凝剂与煤滤料中含有微塑料的可能性,PET可能是在作为容器或包装袋时脱落进入其中的。
PA是最早工业化的合成纤维,俗称尼龙,产品种类繁多,应用范围包括衣物、医疗用品、捕鱼工具、缆绳、帐篷、电器零件、汽车零件、机械设备的耐磨部件等。原水中PA微塑料的含量很低,普遍认为其主要来源为洗衣废水与捕鱼工具[2,7]。其中,洗衣废水会先经过污水处理后再排放进入环境,而捕鱼工具脱落的PA会直接进入环境中。可以观察到在混凝进水与出厂水处PA微塑料有少量增加,这可能是从混凝剂与消毒剂中引入的微塑料污染。
PP在合成树脂一类中产量仅次于PE,近年来随着我国的经济快速增长,PP的需求量也不断增加,生产规模也随之增长,应用范围包括口罩、食品及产品包装、家用物品、汽车零件、化工原料、建筑管材等。PP是口罩过滤材料的主要成分之一[16],近年的疫情导致口罩使用量剧增,口罩被随意丢弃而进入环境的可能性增加,这可能是PP微塑料产生的原因之一。PP微塑料在混凝进水、煤池出水和出厂水中均有少量增加,与PET和PA类似,也可能是从混凝剂、消毒剂和煤滤料中引入的。
综上,PBS、PET、PA和PP 4种成分的微塑料值得进一步关注,因为其存在从外部引入的风险,其中PBS含量远高于其他成分,但同时也更容易被净水工艺去除。
2.2 不同水源的比较
2021年12月冬季枯水期采样(第二次采样)的原水为本地水库水,2022年3月春季枯水期采样(第三次采样)的原水为南水,对比这两次的检测结果以研究不同水源产生的影响。
2.2.1 微塑料丰度
如图5所示,不同水源微塑料丰度差异极大,南水水源的进厂水微塑料含量为(244±41)个/L,本地水库水源的进厂水微塑料含量为(449±241)个/L。推测造成水库水的微塑料丰度高于南水的原因有两种:其一是2021年10月—2022年3月为本地水库的捕鱼期[9],捕鱼工具是微塑料污染的其中一种主要来源;其二是2021年夏季发生的洪水灾害,部分洪水因泄洪进入水库,洪水中携带有大量从地表冲刷至水体中的塑料制品,可能导致水中微塑料的增多。在水源不同的情况下,水厂净水工艺对微塑料去除效率相近,冬季和春季分别约为69%和78%。
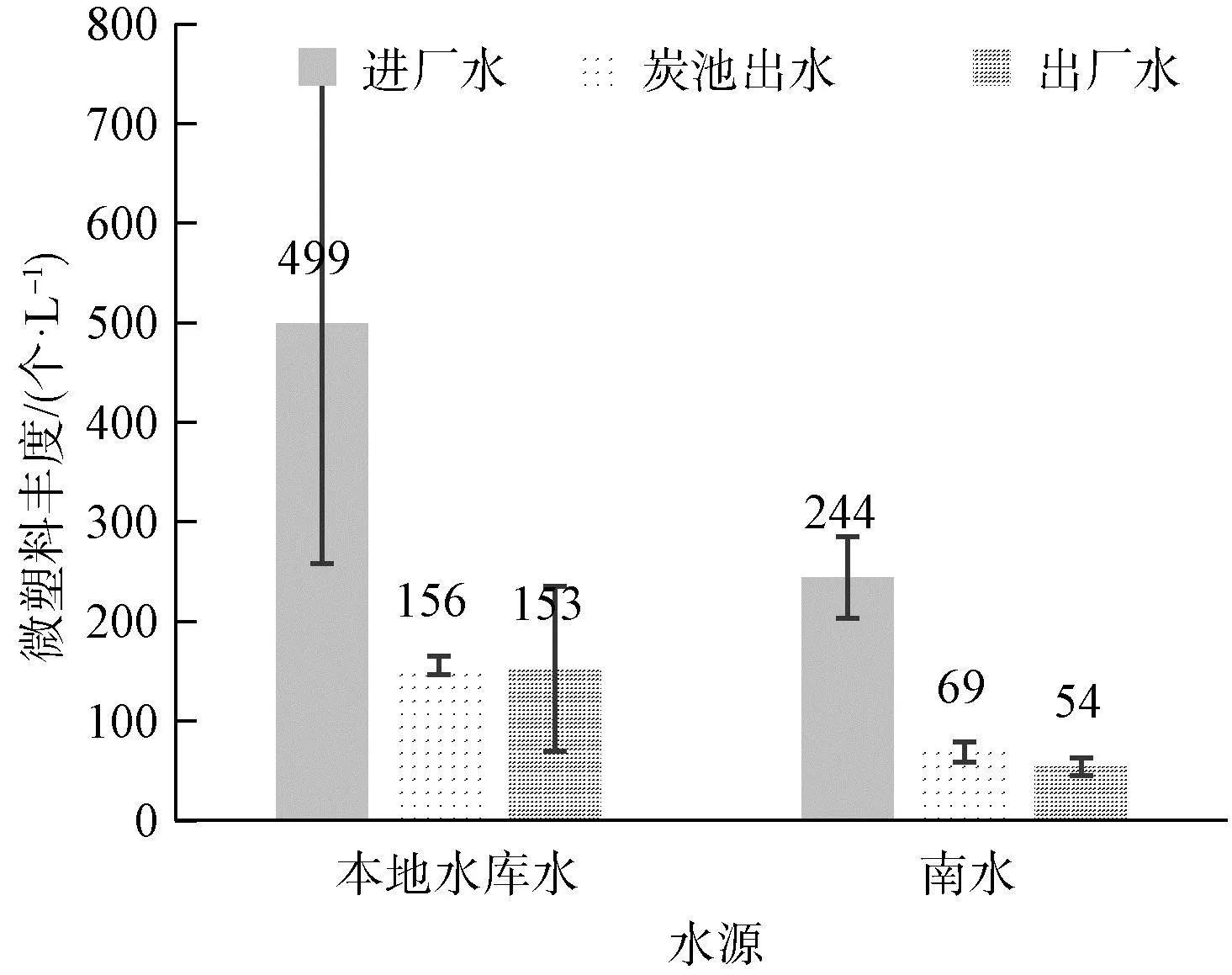
图5 不同水源微塑料丰度对比
2.2.2 微塑料组分
如图6所示,南水的微塑料优势组分为PBS、PET和PA;本地水库水的微塑料优势组分为PBS、PET、PA和PP。可以观察到,水库水中PA含量明显高于南水,推测是因为采样时正处于水库的捕鱼期,且PA为渔网的主要组成材料,脱落进入水中的可能性较高,加之长江与“南水北调”干渠均禁止捕鱼,故产生了如此明显的差异。两次采样原水中PBS含量均较多,且净水工艺对其去除效果较好,这与第一次采样的结果一致。
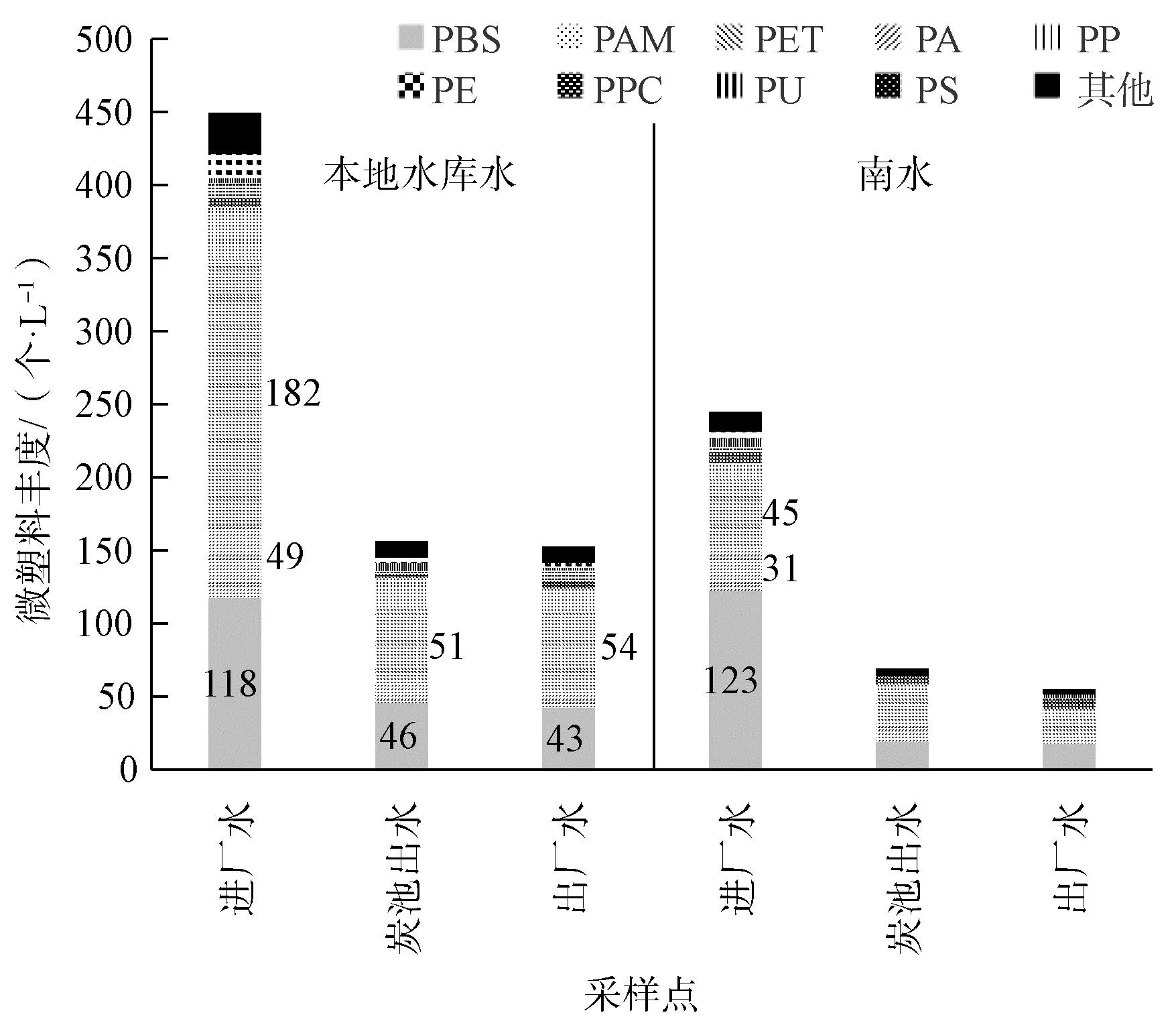
图6 不同水源微塑料组分对比
2.3 丰水期与枯水期的比较
2021年7月夏季丰水期采样(第一次采样)和2022年3月春季枯水期采样(第三次采样)的原水均为南水,对比这两次的检测结果以研究丰水期与枯水期产生的影响。
2.3.1 微塑料丰度
如图7所示,第一次采样的丰水期样品中进厂水微塑料丰度为(147±62)个/L,第三次采样的枯水期样品中进厂水微塑料丰度为(244±41)个/L,枯水期微塑料丰度高于丰水期,此现象与国内外的一些淡水河流微塑料研究一致[17-19]。此现象产生的原因推测为受到春季桃花汛影响,地表径流增大,更多地表的塑料制品进入水体环境(桃花汛期间因冰凌融化或降雨,会造成一过性污染水平增高)。
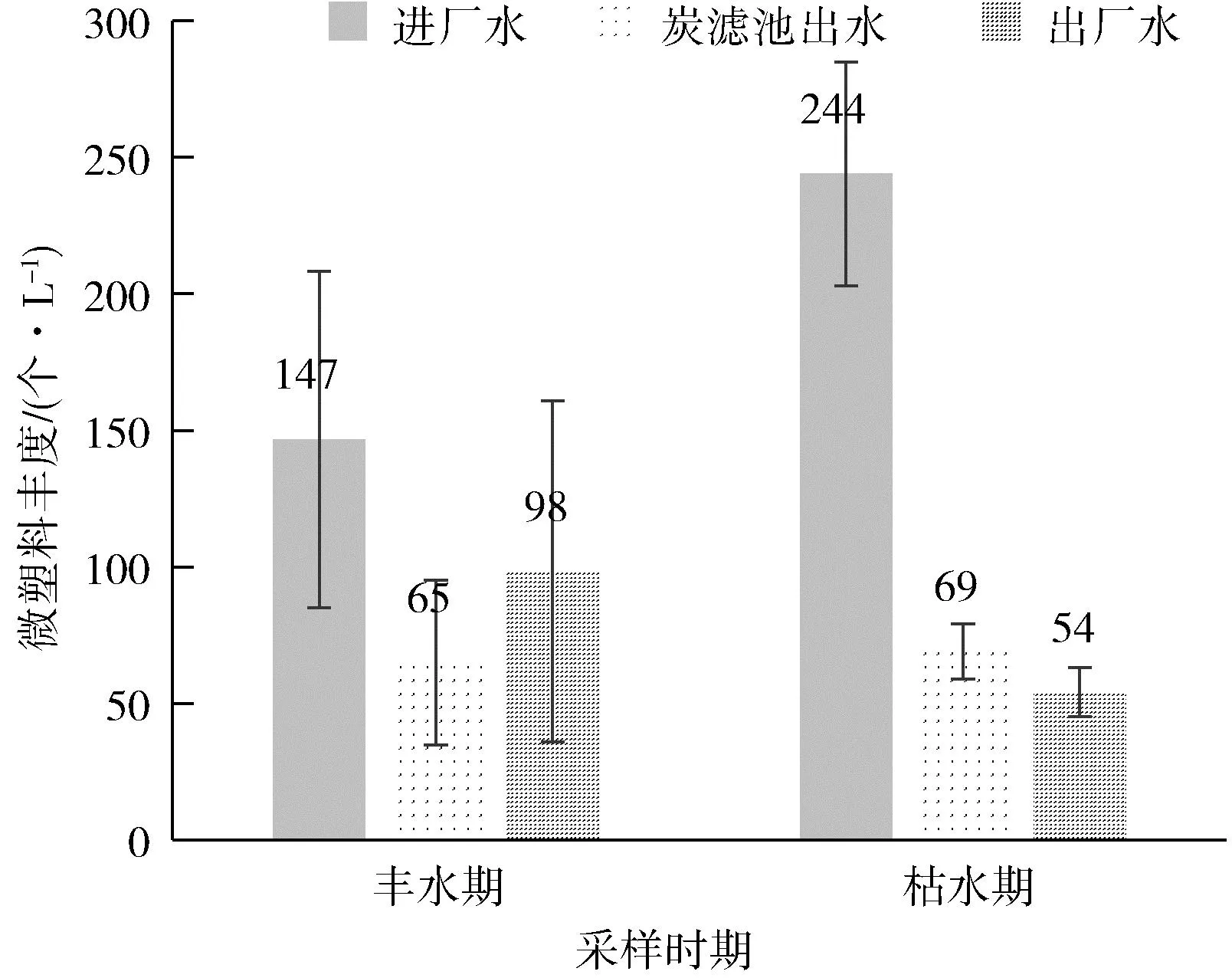
图7 不同时期微塑料丰度对比
在第一次采样中,出厂水中微塑料丰度相比炭池出水有小幅增加,可能是从次氯酸钠消毒剂中引入的微塑料污染。但从图5中可以看到,在第二次与第三次采样中出厂水微塑料丰度与炭池出水基本持平,这与第一次采样中的现象不一致。由于本研究未对消毒剂进行检测,所以消毒剂中含有微塑料的推论还有待进一步研究证实。
2.3.2 微塑料组分
如图8所示,南水丰水期微塑料优势组分为PBS、PAM、PET和PA;南水枯水期微塑料优势组分为PBS、PET和PA。可以观察到枯水期南水原水中的PA占比明显多于丰水期,但长江及“南水北调”干渠均禁止捕鱼,故可以排除该时期PA来自捕鱼工具引入的可能性,推测其来源更可能为春季降雨增加造成的地表径流带入。
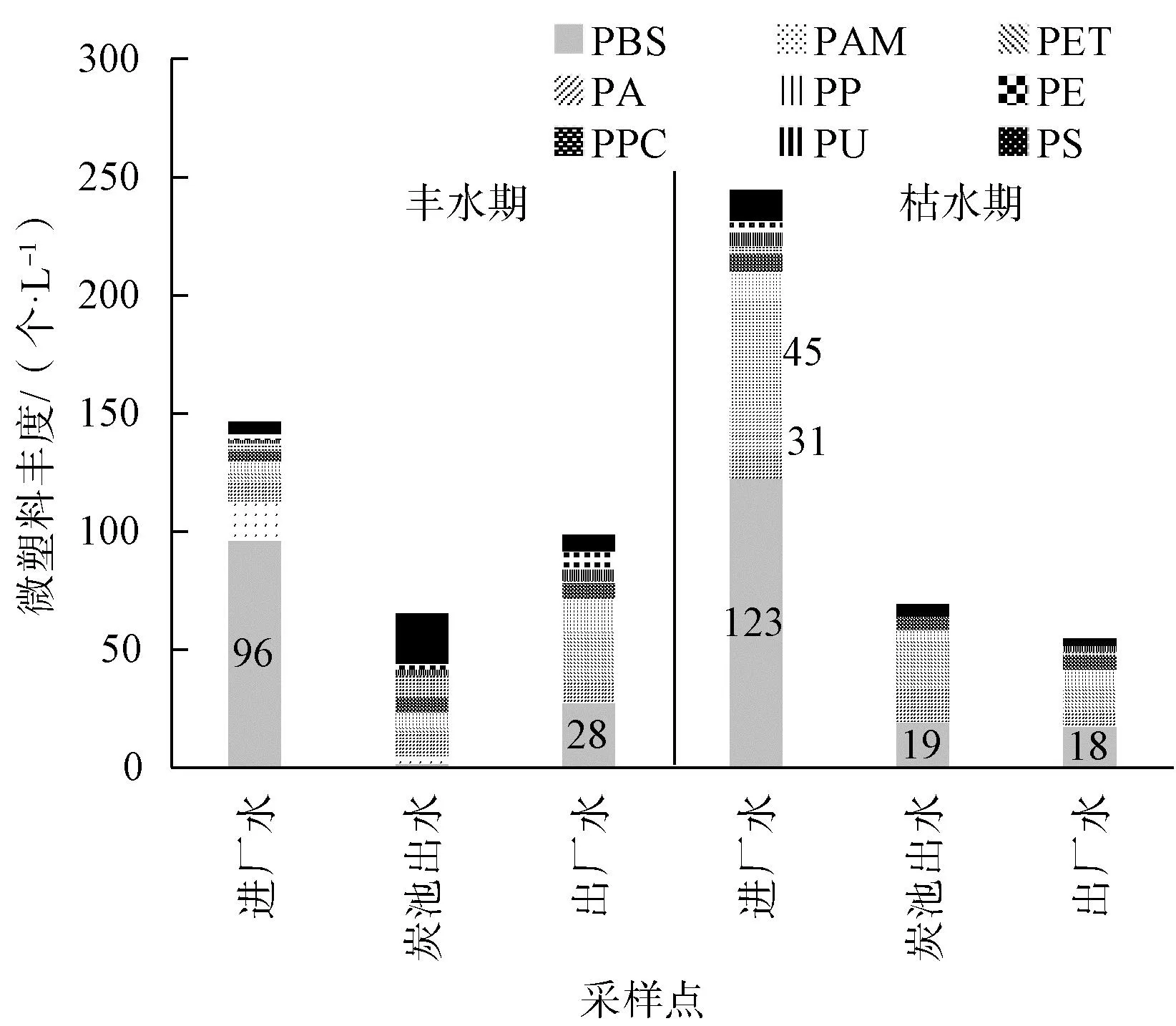
图8 不同时期微塑料组分对比
3 结论与展望
3.1 结论
(1)原水中的微塑料含量规律为枯水期多于丰水期,本地水库水源多于南水水源,主要受到人类活动和季节特性影响。
(2)净水厂工艺对微塑料有较好去除效果,其中混凝沉淀的处理效果最好,但混凝剂、消毒剂和滤料可能存在引入微塑料污染的风险,有待进一步研究对其进行验证。
(3)在20~500 μm粒径内,“南水北调”水源中的微塑料粒径主要集中在20~50 μm,大于100 μm的微塑料颗粒极少;疑似由净水药剂引入的微塑料粒径主要为20~50 μm。
(4)本研究所检测的不同水源、不同时期采集的原水样品中均出现了PBS、PET和PA,在研究微塑料去除方法时应重点关注这3种成分的微塑料;PBS微塑料含量远大于其他组分,且其更容易被净水工艺去除;当水源地存在捕鱼活动时,PA微塑料含量可能会大幅增加。
3.2 展望
现在由于没有统一的方法,各个研究之间数据的可比性较差,有必要建立一个微塑料采样与检测的标准方法。从本研究中也可看出,微塑料在水中的分布很不均匀,同一采样点的3个平行样之间检测结果差异可能比较大,可见微塑料的采样方法还有待改进。
