西黄胶囊联合XP方案治疗晚期胃癌的近期疗效及对外周血肿瘤标志物、细胞免疫功能和血管生成调节因子的影响Δ
2024-02-26李超,王玉,李爽,汪钰,任欣
李 超,王 玉,李 爽,汪 钰,任 欣
(1.北京航天总医院血液肿瘤科,北京 100076; 2.唐山市中心血站质控科,河北 唐山 063000)
胃癌是最常见的消化系统恶性肿瘤,我国胃癌的发病率在所有恶性肿瘤中居第2位。早期胃癌多无明显自觉症状,随着病情进展部分患者可能会出现上腹部不适或隐痛、反酸和烧心等非特异性消化道症状,容易被忽视,因此临床确诊时多数胃癌患者病情已属晚期,化疗等保守治疗成为其主要的治疗方法[1-4]。卡培他滨+顺铂(XP方案)是晚期胃癌的经典化疗方案,具有良好的抗肿瘤作用,但不良反应较大,部分患者难以耐受,不仅影响化疗效果,还可明显降低患者的生活质量[5]。中医药治疗恶性肿瘤具有悠久的历史,可从多靶点、多途径降低肿瘤负荷。西黄胶囊是纯中药抗肿瘤药,是古方犀黄丸(出自清代王洪绪的《外科证治全生集》)的改进剂型,具有清热解毒、祛瘀止痛和消肿散结等功效。目前,该药也被应用于恶性肿瘤的治疗中,且对于化疗的不良反应有良好的缓解作用[6]。本研究对北京航天总医院(以下简称“我院”)收治的晚期胃癌患者在常规XP化疗方案基础上联合西黄胶囊治疗,取得了满意效果,现报告如下。
1 资料与方法
1.1 资料来源
按照随机对照试验两组率的比较公式N=2×(Zα+Zβ)2×Q(1-Q)/(Q1-Q2)2计算最小样本量。公式中α=0.05,Zα=1.96,β=0.2,Zβ=0.84,Q为两组有效率平均值,Q1代表观察组有效率,Q2代表对照组有效率。参照既往研究结果[7-8],初步估算中西医结合治疗疾病控制率为90%,西药对照组为77%,经计算得出每组最小样本量约为64,按照10%脱落率,每组最小样本量为71,最终确定最小总样本量为142例,即在确定样本量时,总样本量≥142即可,本研究选取的总样本量为152例。
选择2019年1月至2022年3月在我院接受治疗的152例晚期胃癌患者。纳入标准:(1)符合胃癌的诊断标准[9],可表现为上腹部压痛感、贫血、消瘦和腹部坚硬包块等症状体征,经X线气钡双重对比造影、内镜、病理或细胞学检查等确诊;(2)胃癌TNM分期(第8版)为Ⅳ期[10];(3)年龄18~80岁;(4)近6个月内未接受过放化疗治疗;(5)预计生存期≥3个月;(6)卡诺夫斯凯计分≥70分;(7)血常规、心电图和肝肾功能基本正常;(8)存在≥1个可测量病灶;(9)自愿签署知情同意书。排除标准:(1)合并其他原发性恶性肿瘤者;(2)严重心肺肝肾功能不全者;(3)严重自身免疫性疾病者;(4)血液系统疾病或凝血功能障碍者;(5)严重恶病质、感染或高热者;(6)精神疾病患者,不能配合治疗;(7)对本研究所用药物过敏者;(8)妊娠期或哺乳期女性;(9)正在参与其他临床试验者。
采用随机数字表法将患者分为观察组76例和对照组76例。观察组患者中,男性41例,女性35例;年龄为37~78岁,平均(58.76±10.90)岁;体重指数(BMI)为18.7~26.2 kg/m2,平均(22.86±1.37) kg/m2;病理分型:腺癌41例,黏液腺癌18例,印戒细胞癌17例;肿瘤分化程度:低分化19例,中分化42例,高分化15例。对照组患者中,男性44例,女性32例;年龄为35~76岁,平均(57.86±11.27)岁;BMI为19.0~26.8 kg/m2,平均(22.52±1.24)kg/m2;病理分型:腺癌44例,黏液腺癌17例,印戒细胞癌15例;肿瘤分化程度:低分化20例,中分化44例,高分化12例。两组患者性别、年龄、BMI、肿瘤病理分型和分化程度等资料具有可比性。本研究通过我院医学伦理委员会批准同意(批准号:HT2021076)。
1.2 方法
两组患者均给予XP方案治疗,即口服卡培他滨片(规格:0.15 g),1次1 000 mg/m2,1日2次,第1—14日;顺铂注射液(规格:20 mL∶20 mg),80 mg/m2,第1日,避光静脉滴注。21 d为1个疗程,连续治疗4个疗程。在此基础上,观察组患者联合西黄胶囊(规格:每粒装0.25 g)口服,1次8粒,1日2次,服用至4个周期化疗结束。
1.3 观察指标
(1)不良反应:参照美国国立癌症研究所不良事件通用术语标准5.0版[11]进行不良事件分级,分为1—5级。(2)肿瘤标志物:治疗前后,抽取两组患者外周静脉血6 mL,离心后分离血清,置于-70 ℃冰箱保存待测。使用cobas e 601型电化学发光免疫分析仪,以电化学发光法检测血清糖类抗原(CA)19-9、CA72-4和癌胚抗原(CEA)水平。(3)细胞免疫功能:治疗前后,采用FACSCanto Ⅱ型流式细胞仪检测外周血CD3+、CD4+和CD8+T细胞百分比,并计算CD4+/CD8+比值。(4)血管生成调节因子:治疗前后,采用iMark型酶标仪,以酶联免疫吸附试验检测血清血管内皮生长因子(VEGF)、碱性成纤维细胞生长因子(bFGF)和转化生长因子-β1(TGF-β1)水平。(5)远期生存情况:以微信、电话和门诊复查等方式对患者进行长期追踪随访,记录其无进展生存期(PFS)和总生存期(OS)。
1.4 疗效评定标准
完全缓解(CR):靶病灶消失,维持时间至少4周;部分缓解(PR):靶病灶长径总和缩小≥50%,维持时间至少4周;疾病稳定(SD):靶病灶长径总和缩小<50%,或增大<25%;疾病进展(PD):靶病灶长径总和增大≥25%,或有新病灶出现[12]。客观缓解率(ORR)=(CR病例数+PR病例数)/总病例数×100%;疾病控制率(DCR)=(CR病例数+PR病例数+SD病例数)/总病例数×100%。
1.5 统计学方法
2 结果
2.1 两组患者近期疗效比较
观察组患者的ORR、DCR分别为51.32%、93.42%,对照组分别为30.26%、82.89%;观察组患者的ORR、DCR显著高于对照组,差异均有统计学意义(χ2=6.974、4.033,P=0.008、0.045),见表1。

表1 两组患者近期疗效比较
2.2 两组患者不良反应比较
两组患者治疗过程中均出现了不同程度的白细胞减少、血小板减少、胃肠道反应、肝肾功能异常和手足综合征,其中观察组患者白细胞减少、血小板减少和胃肠道反应的发生率(22.37%、13.16%和38.16%)显著低于对照组(63.16%、44.74%和80.26%),差异均有统计学意义(P<0.05),见表2。
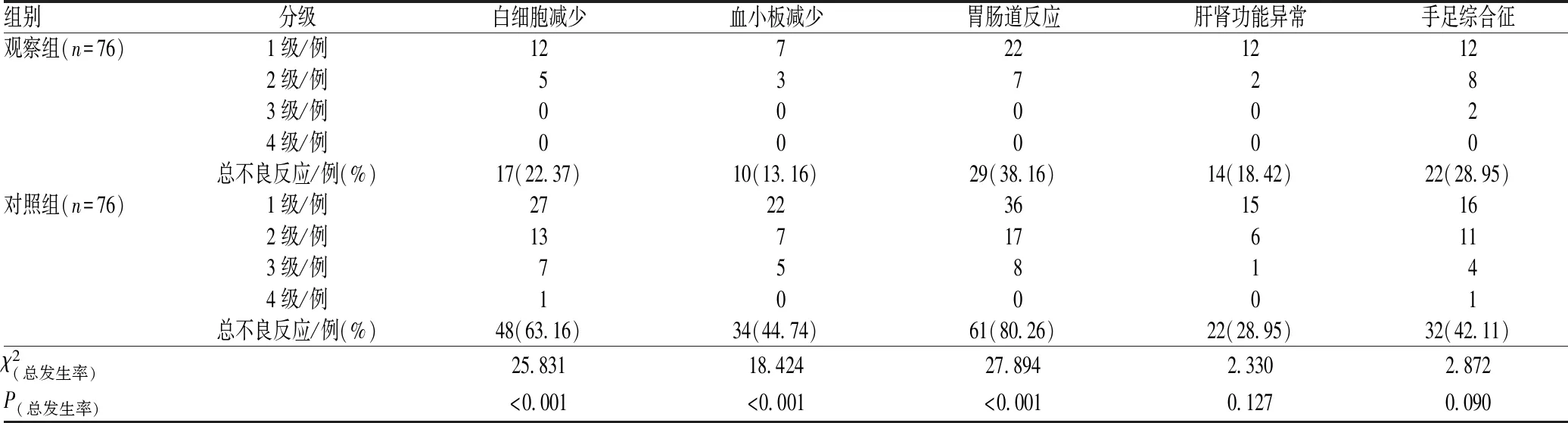
表2 两组患者不良反应比较
2.3 两组患者治疗前后血清肿瘤标志物水平比较
治疗后,两组患者血清CA19-9、CA72-4和CEA水平显著降低,观察组患者较对照组降低更显著,差异均有统计学意义(P<0.05),见表3。

表3 两组患者治疗前后血清肿瘤标志物水平比较
2.4 两组患者治疗前后外周血T淋巴细胞亚群水平比较
治疗后,观察组患者外周血CD3+、CD4+水平和CD4+/CD8+显著升高,对照组患者上述指标显著降低,差异均有统计学意义(P<0.05),见表4。

表4 两组患者治疗前后外周血T淋巴细胞亚群水平比较
2.5 两组患者治疗前后血清血管生成调节因子水平比较
治疗后,两组患者血清VEGF、bFGF和TGF-β1水平显著降低,观察组患者较对照组降低更显著,差异均有统计学意义(P<0.05),见表5。

表5 两组患者治疗前后血清血管生成调节因子水平比较
2.6 两组患者远期生存情况比较
所有患者均获得随访,随访时间7~39个月(末次随访时间为2022年12月31日)。观察组、对照组患者的中位PFS分别为6.1个月(95%CI=3.94~7.46)、4.7个月(95%CI=3.26~6.55),组间差异有统计学意义(Log Rank检验:χ2=4.564,P=0.039)。观察组、对照组患者的中位OS分别为12.9个月(95%CI=9.05~18.74)、9.8个月(95%CI=8.87~14.03),组间差异有统计学意义(Log Rank检验:χ2=4.007,P=0.046)。
3 讨论
XP方案是目前常用的治疗晚期胃癌的化疗方案,其中卡培他滨为口服氟尿嘧啶前体药物,本身无毒性,口服吸收后可通过肿瘤组织中胸苷磷酸化酶催化,转化为具有细胞毒性的5-氟尿嘧啶,进而发挥抗肿瘤作用[13]。顺铂是含金属铂元素的抗肿瘤化疗药,可通过阻滞G2期细胞周期,与脱氧核糖核酸(DNA)链交叉连接,阻止DNA和核糖核酸复制,抑制细胞有丝分裂。化疗药尽管对肿瘤细胞具有较好的杀灭作用,但由于缺乏靶向性,加之晚期胃癌患者机体免疫功能相对低下,化疗药容易引起一系列不良反应[14]。本研究中,对照组患者采用XP方案治疗后出现了1—4级不同程度的白细胞减少、血小板减少、胃肠道反应、肝肾功能异常和手足综合征,发生率分别为63.16%、44.74%、80.26%、28.95%和42.11%。因此,探寻安全性高、疗效好的联合治疗方案是目前临床研究的热点。
西黄胶囊出自《外科证治全生集》,是清代著名医家王洪绪所创犀黄丸的改进剂,主要由牛黄、麝香、没药和乳香组成,具有解毒散结、消肿止痛和活血化瘀的功效。研究表明,西黄胶囊可通过促进肿瘤细胞凋亡、抗肿瘤血管生成和调节机体免疫功能等途径发挥抗肿瘤作用[15]。西黄胶囊能有效抗血管生成,抑制肿瘤转移,改善机体高凝状态,调节T淋巴细胞亚群以及自然杀伤细胞活性,从而增强机体免疫清除能力[16]。目前,西黄胶囊在乳腺癌、肺腺癌和结肠癌等恶性肿瘤的治疗中均显示出了良好的抗肿瘤效果。本研究中,观察组患者在XP方案基础上联合西黄胶囊治疗后,ORR、DCR分别达到了51.32%、93.42%,显著高于对照组;且观察组患者的中位PFS和中位OS均较对照组明显延长。提示西黄胶囊联合XP方案治疗相对于单用XP方案能更有效地提高晚期胃癌的近期疗效及延长生存期。安全性方面,两组患者治疗过程中均出现了不同程度的治疗相关不良反应,但观察组患者不良反应主要为1—2级,其中观察组患者血小板减少、白细胞减少和胃肠道反应的发生率均较对照组明显降低。提示在XP方案基础上联合西黄胶囊治疗能有效减少化疗药引起的不良反应,减轻不良反应程度。彭美玲等[17]研究发现,西黄胶囊能有效减少头颈部肿瘤放化疗所致骨髓抑制的发生,并减轻其严重程度。刘小红等[18]研究发现,西黄胶囊能减少TP方案(紫杉醇+顺铂)引起的恶心呕吐、血小板减少、白细胞减少和肝肾损伤等不良反应的发生。可见,西黄胶囊联合化疗治疗恶性肿瘤具有明显的增效减毒作用。
肿瘤进展与化疗均可引起组织损伤,激活炎症通路,降低机体免疫功能,抑制机体对于肿瘤细胞的杀伤作用,使肿瘤细胞发生免疫逃逸[19]。本研究中,对照组患者在采用XP方案治疗后,外周血CD3+、CD4+水平和CD4+/CD8+比值均较治疗前显著降低,提示化疗药的使用可导致晚期胃癌患者外周血T淋巴细胞亚群表达下降,降低了细胞免疫功能,而观察组患者治疗后外周血T淋巴细胞亚群水平则较治疗前显著改善。表明在XP方案基础上联合西黄胶囊治疗有助于提高晚期胃癌患者机体细胞免疫功能,改善化疗药所致的免疫抑制状态,细胞免疫功能的改善也有助于进一步抑制肿瘤细胞的增殖。肿瘤标志物是指与肿瘤有关的抗原活性物质,是目前用于鉴别恶性肿瘤组织与正常组织的常用特异性指标,在恶性肿瘤的早期筛查和疗效评估中具有重要价值[20-21]。本研究中,两组患者治疗后各项血清肿瘤标志物水平均较治疗前显著降低,但以观察组患者更为显著。提示在XP方案基础上联合西黄胶囊治疗能更有效地下调血清肿瘤标志物水平,抑制肿瘤生长。
VEGF、bFGF和TGF-β1是促肿瘤血管生成相关指标,可参与肿瘤血管新生,促进肿瘤侵袭。VEGF的表达与胃癌肿瘤浸润程度、远处转移等密切相关,肿瘤细胞可促使VEGF大量分泌,进而诱导血管新生,新生血管又可为肿瘤病灶输送养分,促进肿瘤细胞的生长与转移,加快病情进展[22]。bFGF可通过自分泌与旁分泌的方式参与肿瘤血管生成,研究表明其在肿瘤组织中呈现高表达状态,在胃癌组织中bFGF表达越高,患者预后越差。TGF-β1是一种蛋白多肽,在恶性肿瘤早期时可促进肿瘤细胞凋亡,晚期时则可促进肿瘤细胞增殖。本研究中,两组患者治疗后血清VEGF、bFGF和TGF-β1水平均显著降低,但观察组患者各项指标均较对照组降低更明显。可见,西黄胶囊联合XP方案能进一步调控血管生成相关调节因子表达,从而利于抑制肿瘤新生血管生成。
综上所述,西黄胶囊联合XP方案治疗晚期胃癌可有效下调患者血清肿瘤标志物、血管生成相关调节因子水平,改善外周血T淋巴细胞亚群水平,提高近期疗效,为患者带来生存获益,且相对于单用XP方案能有效减轻不良反应,降低发生不良反应的风险,增效减毒作用明显。
