不同酚类与乳清蛋白共价交联对松仁油Pickering 乳液的影响
2024-02-23赵鑫磊包怡红骆嘉原贾铭杰蒋世龙
赵鑫磊,包怡红,2*,骆嘉原,高 博,贾铭杰,蒋世龙
(1 东北林业大学生命科学学院 哈尔滨150040 2 黑龙江省森林食品资源利用重点实验室 哈尔滨150040 3 黑龙江飞鹤乳业有限公司 北京 100015)
蛋白质与酚类化合物相互作用可以改变蛋白质的结构和疏水特性,进而影响功能性质,如溶解性、乳化性、胶凝性、热稳定性等,也会影响植物多酚的生物活性和生物利用度等[1]。疏水性不仅与蛋白质表面的接触程度有关,还与从水相向有机相间迁移的氨基酸残基的自由能有关,加工条件、加工方法、蛋白的物理化学性质、结构特征等都可对表面疏水性产生干预作用[2],性能也会因蛋白的性质发生变化。乳清分离蛋白(Whey protein isolate,WPI)是干酪、酪蛋白制备工业中所产生的副产物,在食品行业中得到广泛应用,作为食品中的双亲性生物大分子,WPI 表面含有大量的氨基酸,具有带电亲水区域和疏水性区域以及复杂的空间结构[3]。另外,WPI 能在油-水界面上均匀分布,并能有效阻止油脂氧化[4],因此,它在乳液递送体系中广泛应用,并有作为Pickering 乳液乳化剂的潜力。Zhao 等[5]制备了没食子酸-玉米醇溶蛋白纳米粒子,并将其用作Pickering 乳液液滴的界面稳定剂,其乳液中的颗粒层通过物理屏障效应防止相邻乳液液滴聚结,并通过脂质氧化抑制剂扩散来延缓脂质氧化。
酚类化合物的基本骨架结构是芳香环,整体结构是由1 个或多个芳香环结合羟基组成,将其按照结构进行分类,可分为羟基苯甲酸、羟基肉桂酸、黄烷醇、黄酮醇和花色苷等。没食子酸(Gallic acid,GA)又名3,4,5-羟基苯甲酸,常作低分子质量的天然抗氧化剂广泛使用[6]。香草酸(Vanillic acid,VA),又称4-羟基-3-甲氧基苯甲酸,是植物中常见的羟基苯甲酸类成分之一。食品加工中,蛋白质与酚类物质间容易发生相互作用,酚类中的酚羟基与蛋白质的氨基或羧基进行共价结合形成复合物。没食子酸可以通过对鱼肌原纤维蛋白的表面疏水性、巯基和羰基含量的改变,使蛋白质二级、三级结构发生变化,并且对其添加量有剂量依赖性[7]。Cao 等[8]研究表明,没食子酸能抑制猪肉肌原纤维蛋白质羰基的形成,而高浓度的没食子酸降低了蛋白质的凝胶性能。松仁油含有约90%的不饱和脂肪酸,可降低血压和血胆固醇[9],由于易氧化以及其它特性限制了其在食品生产中的应用。乳液是最常见的食用油脂的形式,含有不饱和脂肪酸的乳状液食品在加工和储存过程中容易发生脂质氧化,也会促使蛋白质氧化,从而产生一系列不良反应,甚至形成有毒化合物,对人类健康构成威胁。Pickering 乳液由吸附在油-水界面的固体颗粒组成,通过乳液液滴表面的固体颗粒界面层吸附到油-水界面,产生强烈的空间排斥,防止液滴聚集[10],从而防止油滴的积累,稳定体系[11]。
深入了解不同结构、剂量的酚类与WPI 共价结合后在结构、功能特性上的差异,可为松仁油Pickering 乳液在食品体系的开发与利用奠定基础。本研究测定了与不同剂量的羟基苯甲酸化合物(没食子酸和香草酸)共价结合的WPI 的表面疏水性和巯基含量,并通过红外光谱和荧光光谱表征蛋白质的二级和三级结构,探讨颗粒表面疏水性与松仁油Pickering 乳液乳化性能、流变性质及氧化稳定性的关系,为进一步提高蛋白性能,拓宽应用领域,以及充分利用松仁油等农林资源提供理论参考。
1 材料与方法
1.1 材料与设备
松仁油,由黑龙江省伊春市林业局提供;乳清分离蛋白(91%),新西兰Fonterra 公司;没食子酸(GA)、香草酸(VA)、叠氮钠,美国MP Biomedicals公司;β-巯基乙醇、磷酸盐、ANS 等,国药化学试剂有限公司;NaCl、NaOH、NaN3等,科龙化工试剂厂。
FE20 pH 计,梅特勒-托利多仪器(上海)有限公司;UV2550 紫外-可见分光光度计、PL203 型电子分析天平,日本岛津公司;Discovery DHR-1 流变仪,美国TA 公司;F-7000 荧光分光光度计,日本日立公司;LSM 800 激光共聚焦显微镜,德国卡尔蔡司光学仪器有限公司;FD-1A-50 型冷冻干燥机,北京博医康实验仪器有限公司;T6 新世纪紫外分光光度计,北京普析通用仪器有限责任公司;Zetasizer ZS90 型激光粒度仪,英国Malvern 仪器有限公司;TENSOR27 傅里叶变换红外光谱仪,德国Bruker 公司。
1.2 试验方法
1.2.1 WPI-酚类化合物复合颗粒的制备 制备4 g/L 的乳清分离蛋白溶液,室温(25.0 ℃)下以200 r/min 的速度磁力搅拌2 h 后,于4 ℃条件下过夜备用,使其充分水合。将没食子酸和香草酸2 种酚类化合物溶于水,没食子酸和香草酸的添加量均为5~10 g/L,使用1 mol/L NaOH 溶液将酚酸溶液的pH 值调至9.0。以1∶1 的体积比将pH 值同样调至9.0 的蛋白溶液与酚类混合均匀,在持续接触氧气的条件下,不间断搅拌24 h。反应结束后,重新调整溶液pH 值为7.0,透析48 h,间隔6 h 换水,随后真空冷冻干燥获得粉末状颗粒,放置于干燥皿中备用。
1.2.2 游离巯基和总巯基含量的测定 参考Huang 等[12]的方法测定游离巯基和总巯基含量。
1.2.3 表面疏水性的测定 使样品的蛋白质质量浓度为0.2 mg/mL,将ANS(8mmol/L)溶解于10 mmol/L PBS 中,取4 mL 的样品溶液放入5 mL 离心管中,加入20 μL 的ANS,涡旋30 s,静置3 min。在激发波长为390 nm,发光波长为400~600 nm[13]的条件下,最大荧光强度最大值即为表面疏水性。
1.2.4 红外光谱的测定 通过傅里叶红外光谱仪配备衰减全反射池测定FT-IR 光谱,在4 000~500 cm-1的扫描范围内以4 cm-1的分辨率测量样品光谱。
1.2.5 荧光光谱的测定 室温下通过荧光分光光度计测定样品的荧光光谱[14]。将样品用磷酸盐缓冲液(pH 7.4)稀释,以获得0.05 mg/mL 的样品溶液,然后在波长295 nm 处激发WPI 并记录其在280~400 nm 波长范围内的发射光谱,其中激发和发射狭缝的长度均为5 nm。
1.2.6 松仁油Pickering 乳液的制备 取1.2.1 制备所得的颗粒500 mg 分散于10 mL 去离子水中,将颗粒分散液和松仁油油相混合(50 wt%颗粒分散液,50 wt%松仁油)后,利用高速剪切乳化分散机(11 000 r/min)乳化3 min。向样品中加入0.2 g/L NaN3以防止微生物生长。
1.2.7 界面蛋白含量的测定 取适量乳液进行离心(10 000×g,30 min),收集下层清液(水相),用0.22 μm 滤膜进行过滤。BCA 试剂盒测定滤液及乳液中的蛋白质含量代入公式(1):
式中,Ctotal——原乳液中蛋白质含量(mg);Cserum——离心分离后滤液中的蛋白质含量(mg);B——用于BCA 试剂盒检测体系的溶液体积(m3)。
1.2.8 粒径和Zeta 电位的测定 使用激光纳米粒度仪测量乳液的粒径和电位,为避免多重散射效应,测量分析前将样品溶液稀释200 倍。
1.2.9 流变学行为的测定 静态流变特性:向具有1.0 mm 间隙的厚度50 mm 的平行板的流变仪上添加样品,剪切速率范围为0~1 000 s-1,于20 ℃下测定各样品的表观黏度,对所得流变特性曲线进行拟合。
动态流变特性:在线性黏弹区域内对待测样品进行频率扫描,其中固定振荡应变为0.1%,振荡频率范围为0.1~100 rad/s,测定样品的贮能模量G′和损耗模量G′′。
1.2.10 乳析指数的测定 取新鲜的乳液于透明玻璃瓶中,室温下存放14 d,定期测量乳液的高度(Ht)与分层后下层清液的高度(Hq),代入公式(2)进行计算:
式中,Hq——乳液的高度(cm);Ht——乳清层的高度(cm)。
1.2.11 初级氧化产物的测定 根据Shao 等[15]的方法测定POV 值,根据氢过氧化物标准曲线来计算乳液样品中脂质氢过氧化物值。
1.2.12 次级氧化产物的测定 根据Shen 等[16]的方法测定TBARS 值,根据1,1,3,3-四乙氧基丙烷的标准曲线计算乳液样品中脂质过氧化物值。
1.3 统计分析
所有试验做3 次重复,结果均以“平均值±标准差”表示。使用Origin Pro 9.5 软件分析数据。运用SPSS 25.0 软件对试验数据进行统计分析,通过单因素方差分析确定统计差异(ANOVA),P <0.05表示差异显著。
2 结果与分析
2.1 酚类化合物对WPI 理化性质及结构变化的影响
2.1.1 酚类化合物对WPI 游离巯基和总巯基含量的影响 巯基是蛋白质分子中存在的具有较高化学活性的组分,对蛋白质的功能起着重要作用。酚类化合物很容易被氧化成醌,再通过Michael 加成与巯基反应生成巯基-醌的加成物,酚和巯基发生的共价交联降低了巯基含量[17],巯基基团对蛋白质的功能性质有很大影响。由表1 可知,酚类化合物显著降低了WPI 的游离巯基和总巯基含量(P<0.05),WGA 与WVA 的巯基含量具有统计学意义(P<0.05)。对照WP 的游离巯基含量为(2.319±0.068)μmol/g;而试验组中,随着酚类化合物添加量的增加,WGA 的游离巯基含量分别为(1.672±0.238),(1.543±0.284)μmol/g 和(1.878±0.427)μmol/g,WVA 的游离巯基含量分别为(1.351±0.113),(1.105±0.106)μmol/g 和(1.042±0.046)μmol/g。由于绿原酸和EGCG 之间共价交联生成巯基-醌加成产物,可显著降低肌原纤维中的巯基含量[18],该结果与本研究一致。巯基含量降低还可能是因为巯基之间生成二硫键。疏水基团的暴露加速了蛋白质的疏水性聚集,使其结构更加紧凑[19]。

表1 不同酚类化合物添加量对WPI 总巯基和游离巯基含量的影响Table 1 The influence of different phenolic compound concentration on the total sulfhydryl and free sulfhydryl content of WPI
总巯基含量包括暴露在蛋白质表面以及埋在蛋白质中的蛋白质分子的所有巯基含量。表1 中,当酚类化合物添加量增加时,WGA 的总巯基含量分别为(3.209±0.154),(2.529±0.280)μmol/g 和(2.600±0.219)μmol/g,WVA 的总巯基含量分别为(4.013±0.084),(3.974±0.193)μmol/g 和(3.851±0.156)μmol/g,与对照(6.291±0.290)μmol/g 相比,总巯基含量呈急剧下降的趋势,分析原因为共价键可能会破坏蛋白质的结构,使蛋白质分子展开,包埋于蛋白质分子中的巯基团暴露出来。而当酚类化合物添加量增加时,这些暴露的巯基会氧化邻近蛋白质链上的2 个半胱氨酸残基,从而降低蛋白质的巯基含量[20]。
总体而言,巯基含量随着酚类化合物添加量的增加呈先增加后减小的趋势,表明酚类化合物对WPI 的结构有显著影响,使其三级结构的解折叠程度发生改变。随着酚类化合物添加量的增加,蛋白质分子越裸露,共价交联程度越大;当酚类物质达到一定浓度时,蛋白质构象变化趋向稳定。
2.1.2 酚类化合物对WPI 表面疏水性的影响 表面疏水性用于表征表面蛋白疏水基团,它反映了蛋白质构象和功能的变化[21],对蛋白质的整体功能特性的影响发挥着主要作用,是表征与外界极性水环境相连的蛋白质的表面疏水性基团数量的一个重要标志[22]。由图1 可知,WGA 与WVA 的表面疏水性之间存在显著差异(P<0.05),这可能与表面疏水性残基的暴露程度,蛋白质的氨基酸组成和空间结构展开程度等因素密切相关[23]。当酚类化合物添加量增加时,表面疏水性显著增加(P<0.05),酚类化合物添加量为7.5 g/L 时,表面疏水性分别达到最大值。由于酚类化合物与蛋白发生相互作用,蛋白质结构展开,使其内部的疏水性氨基酸暴露在表面,因此表面疏水性增加[24]。随着体系中酚类化合物添加量的增加,表面疏水性也发生显著变化(P<0.05),蛋白质空间结构变化趋于稳定。由此,WPI 的表面疏水性指数为218.74;WGA 的表面疏水性指数最高可达532.47,而WVA 的表面疏水性指数最高则为468.05,表明发生共价反应后的WGA 分子表面有更多的疏水基团,分子结构被拉伸的程度更大,该结果与巯基含量的测定结果一致,原因可能是与VA 相比,GA含有的羟基数量较多(3 个),暴露了较多疏水性氨基酸,使表面疏水性更强。
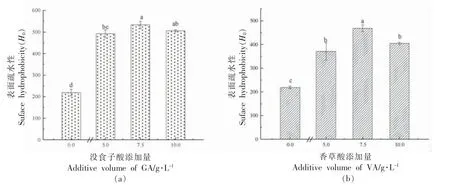
图1 酚类化合物添加量对WPI 表面疏水性的影响Fig.1 The effect of phenolic compound addition on the surface hydrophobicity of WPI
2.1.3 酚类化合物对WPI 的荧光光谱的影响 一般可由波长约340 nm 处的蛋白质的荧光来反映色氨酸残基的变化,而发射强度之差则反应色氨酸残基周边环境的改变,而最大发射强度(λmax)的位移量则能反映出色氨酸分子及蛋白疏水空穴的极性变化[25]。色氨酸残基的吲哚基团被掩埋在蛋白质结构中时,发生λmax蓝移,蛋白质结构展开时,发生红移[26]。随着酚类化合物添加量的增加,颗粒的荧光强度均显著下降,证明WGA 与WVA均发生猝灭,在碱处理条件下,WPI 与2 种酚类化合物之间均发生了共价交联。图2 中WPI 的最大发射峰出现在波长360.00 nm 左右处,WGA 和WVA 最大发射峰均红移到波长361.07 nm 处。然而,随着酚类添加量的增加,荧光强度随之下降,其中WGA 的荧光强度猝灭率分别为91.05%,89.98%,94.02%,而WVA 的荧光强度猝灭率分别为20.12%,27.49%,31.19%。荧光强度的降低也可以证明羟基苯甲酸类化合物对于蛋白质具有荧光猝灭的作用,Yue 等[27]也得出了同样的结论。这是由于发生共价交联反应时,酚类物质被氧化成醌,从而与WPI 中的氨基发生亲核反应。由于分子质量的增大,醌主要结合在蛋白质表面位点处,因此发生了荧光猝灭。

图2 酚类化合物共价复合处理对WPI 内源荧光光谱的影响Fig.2 Effect of covalent compound treatment of phenolic compounds on intrinsic fluorescence spectra of WPI
2.1.4 酚类化合物对WPI 红外光谱的影响 4000~500 cm-1范围内的WGA 与WVA 颗粒的FTIR 红外谱图,如图3 所示。所有样品的光谱都包含4 个主峰,且都在酰胺Ⅰ带都具有最强的吸收强度。WPI 与酚类物质共价交联后,酰胺I 带的峰位置发生变化,表明WPI 的构象即三级结构发生变化[28]。WGA 和WVA 酚羟基的O-H 振动具体表现为在3 365~3 368 cm-1范围内均有广泛的吸收峰,-C-O 和C-O-C 振动表现为1 093 cm-1和1 039 cm-1的吸收峰。谱带向更低波数位移,变化越明显,表明共价交联反应越强烈[29]。与酚类化合物共价交联后,随酚类化合物添加量的增加,WPI 的酰胺I 带向低波数移动的幅度越大;复合颗粒酰胺I带面积和峰位置均发生了变化,表明酚基接枝到蛋白质上,与蛋白质中某些基团发生了共价结合。与WGA 类似的是,WVA 的-OH 吸收峰变宽,且向低波数移动,表明WPI 与VA 同样通过共价交联结合形成复合物。

图3 酚类化合物共价复合处理对WPI 傅里叶红外光谱的影响Fig.3 Effect of covalent compound treatment of particles on fourier infrared spectroscopy of WPI
2.2 酚类化合物对松仁油Pickering 乳液性质的影响
2.2.1 酚类化合物对Pickering 乳液粒径分布和Zeta 电位的影响 如图4 所示,WGAP、WVAP 和WPP 的粒径分布均呈单峰分布,与对照WPP 相比,WGAP 粒度分布的主峰向小粒子尺寸方向移动,主峰位置集中在204.1~276.4 nm 之间;与之类似的是,WVAP 的主峰也逐渐向小粒子尺寸方向移动,主峰位置集中于217.7~256.2 nm 之间;而WPP 的主峰位置则集中于475.5 nm 处。产生这种现象的原因为GA 和VA 提供了反应性羟基和疏水基团,与蛋白结合后,蛋白质相互排斥展开,使乳液平均粒径变小。该结果与Li 等[30]的研究结果一致。酚类化合物所能提供羟基基团数量的不同可使乳液粒径之间产生显著差异,具体表现为,羟基基团数量多的酚类物质更容易与蛋白质结合[31]。对于反映乳液平均粒径的d4,3,WGAP、WVAP 和WPP 之间也存在显著差异。当酚类化合物添加量为7.5 g/L 时,平均粒径最小,WGAP 和WVAP 的平均粒径分别为204.1 nm 和217.7 nm,GA 添加量为5.0 g/L 时,WGAP 的d4,3最大,为276.4 nm;当VA 添加量为10.0 g/L 时,WVAP 的d4,3达到最大值(256.2 nm),表明添加适度剂量的酚类化物形成的乳液液滴d4,3较小。原因可能为酚类化合物添加量增加,WPI 容易吸附在表面,造成复合物之间产生空间位阻,从而阻止乳液液滴之间发生相互作用,有利于改善稳定性[32]。
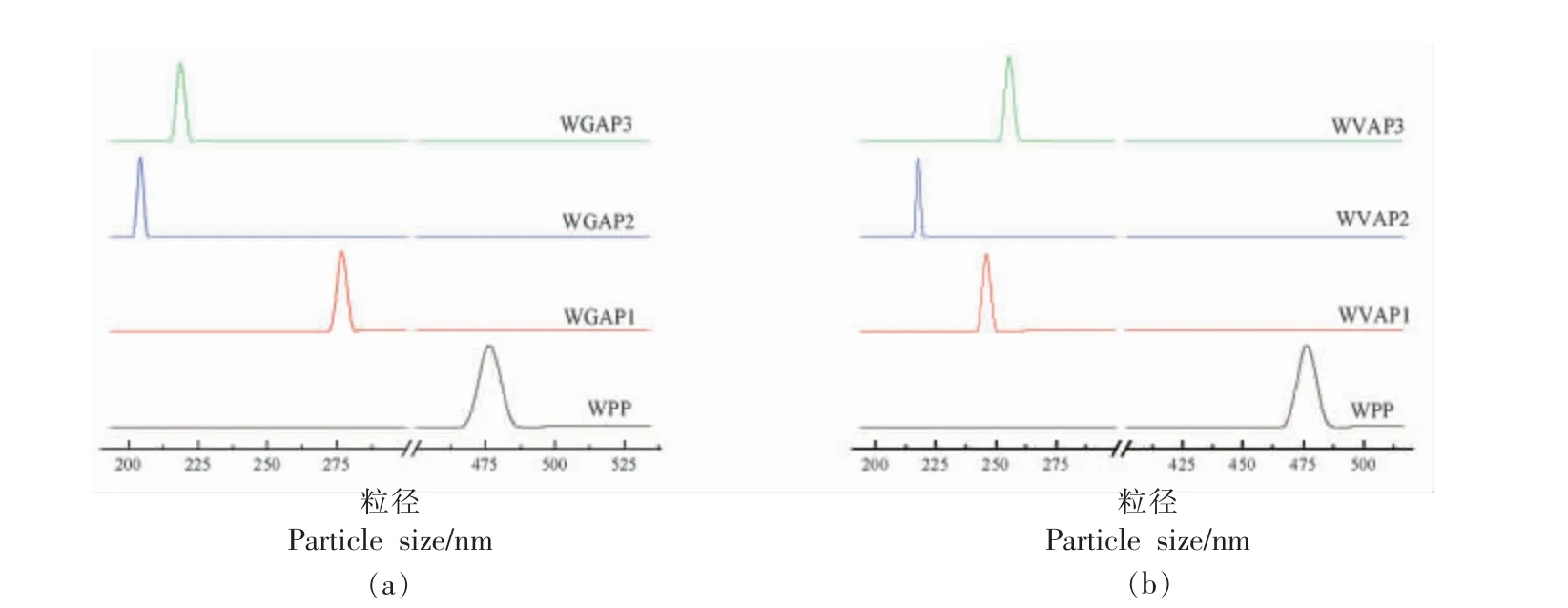
图4 不同添加量酚类化合物对WGPP、WVPP 和WPP 乳液粒径分布的影响Fig.4 The effect of different concentrations of phenolic compounds on the particle size distribution of WGPP,WVPP and WPP emulsions
Zeta 电位是判断分散体系稳定性的重要指标,在一定程度上能够反映乳液液滴之间相互作用的强度,其绝对值越大,液滴之间的排斥越大,从而避免乳液液滴聚结,体系因此更加稳定[33]。不同酚类化合物添加量制备乳液结果如图5 所示。随着酚类化合物添加量的增加,Zeta 电位的绝对值呈先增加后减小的趋势。酚类化合物添加量为7.5 g/L 时,绝对值最大。综上所述,酚类化合物添加量为7.5 g/L 时,此时粒子间的静电斥力最大,分子不易聚集,稳定性最高,该结果与粒径分布结果一致。酚类化合物添加量为7.5 g/L 时,电位绝对值分别为40.33 mV(WGAP)和20.14 mV(WVAP),此时电位绝对值达到最大值,产生的静电斥力大[34],意味着乳液稳定性最好。在该制备条件下,更多颗粒吸附在液滴表面,电位绝对值增加,油滴表面电荷和静电斥力也随之增加,因此阻止了液滴聚集情况的发生,提高了体系的稳定性。分析WGAP 与WVAP 电位值存在差异的原因,可能为没食子酸水溶性较好,没食子酸在乳液微环境中的分布对油滴表面电荷产生了影响,进而改变乳液的ζ-电势[35]。

图5 酚类化合物添加量对Pickering 乳液Zeta 电位的影响Fig.5 The effect of the addition of phenolic compounds added on the Zeta potential of Pickering emulsion
2.2.2 酚类化合物对Pickering 乳液界面蛋白含量的影响 图6 可知,所有乳液的界面蛋白含量均在1.5~4 mg/m2之间,WGAP 和WVAP 的界面蛋白含量最大分别可达3.22 mg/m2和2.51 mg/m2。与WPP 相比,界面蛋白含量提高了57.84%和18.82%(P <0.05)。酚类化合物添加量越大,乳液的界面蛋白含量也越高。在界面面积相同的情况下,界面蛋白含量越高,油水界面可吸附蛋白质的量就越多[36]。WGAP 和WVAP 的界面蛋白含量显著高于WPP(P<0.05),分析原因为界面蛋白含量的变化由界面面积和蛋白吸附率两种因素决定。酚类化合物共价结合在乳清分离蛋白上,由于疏水性的增加,油-水界面吸附更多蛋白质,从而在液滴表面形成较厚的界面膜,该界面膜可防止液滴之间发生聚集,有助于保持乳状液的稳定性。Ding 等[37]研究结果表明,在蛋白含量不变的条件下,粒径越小,界面空隙越大,可吸附的蛋白含量越高,乳液越稳定。界面蛋白含量的差异与WGA和WVA 分子的聚集状态有关,根据疏水性结果可知,WGA 分子疏水性更强,因此蛋白分子可吸附程度更大,有较多的蛋白聚集体吸附在油-水界面上,导致其界面蛋白含量较高。
2.2.3 酚类化合物对Pickering 乳液流变特性的影响 液滴间的聚集程度及稳定性与乳液的表观黏度关联性很大[38]。图7 显示了在剪切扫描中测定的不同颗粒所稳定乳液的流动特性。在0.1~1 000 s-1的范围内,随剪切速率增加,乳液的表观黏度逐渐减小,该变化趋势表明Pickering 乳液均为剪切稀化的非牛顿流体,乳液内部单元的取向与剪切方向一致或者平行,外部的剪切应力拉伸了乳液中的分子,因而不同分子之间发生解缠作用,降低了乳状液体系的流动阻力,具体表现为Pickering 乳液的流变学行为呈现剪切变稀的特性。根据Stokes 规律可知,颗粒的表观黏度越大,液滴越不容易发生沉降或上浮现象,因此乳液的物理稳定性也因此提高[39]。当酚类化合物添加量增加时,乳液的表观黏度在整个剪切速率变化范围内也会增加。不同种类的酚类化合物稳定的Pickering 乳液的表观黏度存在差异,具体表现为WVAP 的表观黏度大于WGAP。

图7 酚类化合物对Pickering 乳液的表观黏度的影响Fig.7 Effects of phenolic compounds on apparent viscosity of pickering emulsion
由表2 可知,由酚类化合物稳定的乳液的拟合精度都达到0.99 以上,说明其是典型的屈服-假塑性流体且曲线与模拟度良好。随酚类化合物添加量的增加,K 逐渐降低,n 逐渐靠近1,乳液的流体性质变强。以上结果可以看出,屈服应力值随着酚类添加量的增加而增大。这表明酚类化合物添加量越大,乳液的网络结构越强,结构就越坚固,抗应变能力就越强。因此,屈服应力增加可能为蛋白颗粒间静电斥力的降低和空间位阻的增加等多种原因综合引起。当VA 添加量增至10.0 g/L时,乳液的表观黏度最大,分析其原因为流变特性与乳液稳定性相关。

表2 酚类化合物添加量对乳液的流动曲线特征指数的影响(Power-Law 模型)Table 2 Effect of phenolic compound addition on flow curve characteristic index of lotion(Power-Law model)
酚类化合物添加量对乳液储能模量(G')及损耗模量(G″)的影响见图8,扫描一定频率(0.1 Pa)可知,所有样品的储能模量(G′)始终大于损耗模量(G″),表明在此状态下的乳液流变学性质均以弹性为主。储能模量越高,乳液在特定外力作用下发生形变的可能性就越低。可能因为添加了酚类化合物,所以试验组的黏弹性模量显著高于对照组,酚类化合物与WPI 之间形成的网络结构使乳液弹性模量增加。酚类化合物添加量增加,乳液的G′和G″均随角速度的增加而降低。当酚类化合物添加量为7.5 g/L 时,G′和G″显著大于酚类化合物添加量为5.0 g/L 及10.0 g/L 条件下的乳液,这表示添加7.5 g/L 的酚类化合物时,乳液内部的弹性更大,极有可能是酚类化合物可促进大多数蛋白分子展开,提高了WPI 与酚类化合物之间的共价结合程度,从而使生成的网络结构不可逆。酚类化合物添加量增加,则蛋白质的结构展开,分子之间重新排列,更加有利于共价反应的发生。以上流变性质表明,引入不同酚类化合物的乳液存在差异,其中引入GA 的Pickering 乳液可获得更好的流变学特性,这是因为不同颗粒所稳定的乳液液滴之间有不同的共价结合程度,致使产生的流变学特性也存在差异。

图8 Pickering 乳液的储能模量(G')和损耗模量(G″)随角速度变化的关系Fig.8 The relationship between the storage modulus(G')and loss modulus(G″)of Pickering emulsion with angular velocity

图9 酚类化合物添加量对Pickering 乳液乳析指数的影响Fig.9 The influence of the addition of phenolic compounds on the emulsification index of Pickering emulsion
2.2.4 酚类化合物对Pickering 乳液乳析指数的影响 乳析指数是衡量乳液物理稳定性的重要参数,乳析指数越大,液滴移动越快,液滴越易聚集,乳液物理稳定性越差。从图10 可以看出,随贮藏时间延长,乳液的乳析指数也随之增加,贮藏14 d 时,试验组的乳析指数均小于50%,其中WPP的乳析指数显著高于WGAP 和WVAP 的乳析指数(P<0.05),并且乳析指数先减小后增加。该结果表明共价复合颗粒所稳定乳液的液滴间斥力较强,液滴可以有规则地分布并紧密堆积,乳脂层更厚,因此改善了乳液的分层稳定性[40]。这是因为当酚类化合物添加量增加时,乳液的表观黏度也随之增加,液滴的移动速度变慢,从而提高了分层稳定性。

图10 酚类化合物添加量对松仁油Pickering 乳液一级氧化产物的影响Fig.10 Effects of phenolic compounds addition on primary oxidation products of pine nut oil Pickering emulsion
2.2.5 酚类化合物对Pickering 乳液脂质氧化程度的影响 如图10 所示,WPP 的POV 值高于引入酚类化合物Pickering 乳液的POV 值,表明在乳液中引入酚类化合物后,氢过氧化物的形成受到了很好的抑制。Staszewski 等[41]使用绿茶多酚-β-乳球蛋白纳米复合物制备了鱼油乳液,氢过氧化氢在整个贮存过程中保持相对较低的生成量,这表明酚类化合物明显改善了乳液的氧化稳定性。Pan 等[7]也发现多酚交联能显著降低乳清蛋白乳液的POV 和TBARS 值,提高乳液的氧化稳定性。WPP 在贮藏第3 天开始POV 值有明显的增加趋势,而对于引入酚类化合物的乳液,整个一级氧化过程均表现得较为平缓,因此可知WPI-酚类化合物颗粒稳定的乳液在一级氧化过程中更为稳定。在贮藏的前2 d,较低质量浓度酚类化合物(5.0,7.5 g/L)能够促进过氧化物的生成,相反较高质量浓度(10.0 g/L)的酚类化合物表现出抑制油脂体过氧化物生成;而贮藏4 d 后,酚类化合物的抑制能力与剂量呈正相关。作为来自天然植物的天然无毒抗氧化剂,酚类化合物含有多个酚羟基,因此具有很强的提供氢原子的能力,在脂质氧化过程中,脂肪酸自由基可以与之结合,自由基成为更稳定的惰性化合物,阻止脂质氧化连锁反应,从而起到抑制脂质自动氧化的作用[42]。2 种酚类化合物对乳液中过氧化物形成的不同影响,可能是由于它们吸收自由基的能力[43]和它们不同的氢原子释放率导致[44]。
如图11 所示,乳液二级氧化物TBARS 值随着贮藏时间的延长而逐渐增大,趋势与一级氧化产物大致相同。WPP 的TBARS 值在第4 天后陡然增加,而WPI-酚类化合物稳定的Pickering 乳液TBARS 值增长相对缓慢,而到达第14 天时,测得的TBARS 值分别达到最高值,WGAP 次级氧化物的生成量始终小于WVAP。在贮藏的14 d 内,乳液的TBARS 值均呈上升趋势。两种酚类物质均表现出抑制油脂体次级氧化产物生成的能力,这归因于酚类抗氧化物可以将氢离子提供给过氧化自由基,从而避免进一步降解。以上结论得出,酚类化合物的加入对Pickering 乳液中次级氧化物的生成起到了很好地抑制作用。本研究中,改善Pickering 乳液的氧化稳定性与酚类化合物结构中的酚羟基提供强大的氢原子储备能力有关[42],在油脂氧化过程中,能与油脂上的某些基团发生反应,生成不易氧化的物质,使之氧化过程减缓。Wan 等[45]研究表明,脂质过氧化物和挥发性己醛生成量显著减少,大豆分离蛋白-白藜芦醇复合物乳状液的的氧化稳定性得到改善。

图11 酚类化合物添加量对松仁油Pickering 乳液二级氧化产物的影响Fig.11 Effects of phenolic compounds addition on secondary oxidation products of pine nut oil Pickering emulsion
3 结论
本研究结果表明,没食子酸和香草酸2 种酚类化合物对WPI 蛋白颗粒表面疏水性均有显著影响,与酚类化合物共价结合后,WPI 蛋白颗粒游离巯基和总巯基含量降低;2 种酚类物质均能不同程度提高乳液的理化性能和氧化稳定性,高剂量的2 种酚类化合物均可诱导WPI 巯基和表面疏水性发生变化,对乳液特性产生影响显著,并且表面疏水性的变化对乳液特性的改变起主导作用。WGP 和WVP 的最大发射峰均红移到361.07 nm 处,WGP 的荧光强度猝灭率分别为91.05%,89.98%和94.02%,而WVP 的荧光强度猝灭率分别为20.12%,27.49%和31.19%。与对照WPP 相比,WGPP 粒径分布的主峰位置集中在204.1~276.4 nm 之间;WVPP 粒径分布的主峰位置则集中在217.7~256.2 nm 之间。一定剂量范围内,较高添加量的酚类可以降低Pickering 乳液粒径,提高流变性能并且延缓油脂体的氧化,其中没食子酸的作用较为显著。因此,在开发天然乳化剂或乳液相关产品时,可以考虑通过添加相对高剂量的没食子酸,以提高产品的理化稳定性,抑制脂质氧化。本研究可为食品研究人员开发出更健康的天然松仁油食品或为相关产品提供参考。
