贝利尤单抗治疗系统性红斑狼疮的临床疗效分析*
2024-02-23黄文辉邓运明黄晓春陈腾云苏晓燕
黄文辉,邓运明,黄晓春,陈腾云,苏晓燕
(东莞东华医院风湿免疫科,广东东莞 523000)
系统性红斑狼疮(systemic lupus erythematosus,SLE)是一种多因素参与,累及全身多系统、多脏器,且以免疫性炎症为突出表现的弥漫性结缔组织病[1]。目前临床上的治疗药物主要包括激素和免疫抑制剂,但激素的不良反应随剂量增加及使用时间延长而增多,免疫抑制剂的使用也可能造成器官损害及感染风险。SLE的发病与B细胞刺激因子(B lymphocyte stimulator,BLyS)水平升高相关,针对 B 细胞的靶向治疗是目前SLE治疗的主要方向。贝利尤单抗(Belimumab)是近年来被批准用于治疗SLE的新药,通过抑制可溶性 BLyS 的生物活性来抑制 B 细胞的分化,减少活化 B 细胞和浆细胞的数量[2-3]。国外已有大量的临床试验和真实世界研究表明其具有良好的临床疗效和安全性[4-6]。而贝利尤单抗在中国刚上市不久,国内用于治疗SLE的相关临床研究仍较少。因此本研究旨在探讨贝利尤单抗治疗中、重度活动性SLE真实世界临床中的疗效及安全性,为其临床应用提供参考。
1 资料与方法
1.1 一般资料
选取2019年9月至2022年3月在本院风湿免疫科就诊的60例中、重度活动性SLE患者为研究对象。根据患者是否使用贝利尤单抗治疗将患者分为对照组(激素+免疫抑制剂)30例和试验组[激素+免疫抑制剂+贝利尤单抗(≥8次)]30例。纳入标准:(1)符合1997年美国风湿病协会(American College of Rheumatology,ACR)关于SLE的修订分类标准[7]或2019年欧洲抗风湿病联盟(European League Against Rheumatism,EULAR)SLE分类标准[8];(2)年龄≥18岁,抗核抗体(ANA)阳性和/或抗双链DNA抗体(Ds-DNA)阳性;(2)SLE疾病活动指数-2K(SLEDAI-2K) 评分[9]≥8分;(3)入组前受试者接受稳定的SLE治疗方案至少30 d;(4)4个月内未使用过贝利尤单抗。排除标准:(1)接受贝利尤单抗治疗时被纳入其他SLE临床试验;(2)接受贝利尤单抗治疗前30 d内需要治疗干预的重度活动性中枢神经SLE;(3)具有重要器官移植或造血干细胞/细胞/骨髓移植或肾移植史;(4)需要治疗的急性、慢性感染:乙型肝炎或丙型肝炎阳性、HIV阳性等;(5)使用静脉输注环磷酰胺或其他生物制剂(IL-6/CD20/TNFi/阿巴西普等)。本研究已通过本院伦理委员会批准(审批号2021-KY-025)。
1.2 方法
所有患者均给予甲泼尼龙及免疫抑制剂治疗。两组患者使用的免疫抑制剂主要包括羟氯喹、吗替麦考酚酯(mycophenolate mofetil,MMF)。试验组治疗方案:激素+免疫抑制剂+贝利尤单抗(10 mg/kg,共8次,按照首次用药后每2个月用药1次,连用2次,之后每4个月用药1次,连用5次);对照组治疗方案:激素+免疫抑制剂。
1.3 评价指标
由本院风湿免疫科专职医生负责收集患者临床资料,评估SLE患者在治疗过程中的疾病状况及药物使用的变化情况。分别在基线及治疗第3、6、9、12个月时评估患者疾病活动度、激素(甲泼尼龙片)用量、实验室检测(包括血常规、尿常规、肝肾功、补体、Ds-DNA等)及不良事件发生。主要有效性终点为SLE 应答指数(SRI-4)应答率[10],须同时满足以下3项:(1)SLEDAI-2K评分与基线相比减少≥4分且要求完全消除≥1种疾病表现;(2)任意器官系统无恶化且无新的英伦三岛狼疮性评估组(BILAG)A类器官评分,和≤1个新的BILAG B类器官评分;(3)总体状况无恶化,患者总体病情评估(PGA)未见加重,PGA自基线增加<0.3分。次要终点:SLEDAI-2K评分、Ds-DNA、补体C3、补体C4、甲泼尼龙片用量、血尿常规、肝肾功等指标变化。安全性评价:记录12个月内包括输液反应、超敏反应、胃肠道症状和感染等在内的不良事件。
1.4 统计学处理
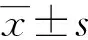
2 结 果
2.1 两组患者基线资料比较
两组患者的性别比、年龄、病程、SLEDAI-2K评分、Ds-DNA、补体C3、补体C4、甲泼尼龙片用量等比较,差异无统计学意义(P>0.05),见表1。两组患者均应用甲泼尼龙片、羟氯喹和MMF治疗,基线时两组羟氯喹和MMF初始剂量基本一致,在治疗过程中基本无变化。

表1 两组治疗前基线资料比较
2.2 两组患者主要有效性终点SRI-4应答率比较
从治疗第3个月开始,试验组SRI-4应答率高于对照组,并持续保持至治疗第12个月试验结束。治疗12个月时,试验组的SRI-4应答率明显高于对照组(P<0.05),见表2。

表2 两组患者SRI-4应答率比较[n(%)]
2.3 两组患者治疗前、后的临床症状、脏器受累状况比较
治疗前,试验组和对照组患者临床症状相近,脏器受累多为肌肉骨骼、血液系统、肾脏和皮肤黏膜。治疗12个月时,两组患者多数临床症状和脏器受累均有不同程度改善,其中两组患者白细胞下降、血红蛋白下降、白蛋白下降、肌肉骨骼受累均较治疗前明显改善,试验组肾脏受累较治疗前明显改善,差异均有统计学意义(P<0.05);而在白蛋白下降、肾脏受累的改善方面,试验组较对照组更为明显,差异有统计学意义(P<0.05),见表3。

表3 两组患者治疗前、后的临床症状、脏器受累状况比较[n(%)]
2.4 两组患者治疗过程中的SLEDAI-2K、Ds-DNA、补体C3、补体C4及甲泼尼龙片用量比较
在治疗3、6、9、12个月,两组患者的SLEDAI-2K评分、Ds-DNA、补体C3、补体C4及甲泼尼龙片用量均较本组治疗前有明显的改善,差异有统计学意义(P<0.05);治疗12个月,试验组SLEDAI-2K评分较对照组降低,差异有统计学意义(P<0.05);治疗9、12个月,试验组患者补体C3、补体C4较对照组明显升高,差异有统计学意义(P<0.05);而在治疗3、6、9、12个月,试验组甲泼尼龙片用量较对照组明显减少,差异有统计学意义(P<0.05),见表4。

表4 两组患者治疗过程中的SLEDAI-2K、Ds-DNA、补体C3、补体C4及甲泼尼龙片用量比较
2.5 两组患者治疗期间的安全性情况分析
试验组患者治疗期间发生感染相关不良事件12例,其中上呼吸道感染6例,尿路感染4例,带状疱疹病毒感染1例,肺部感染1例,给予对症治疗后感染均好转。对照组患者治疗期间发生感染相关不良事件13例,其中上呼吸道感染5例,尿路感染5例,带状疱疹病毒感染1例,肺部感染2例,给予对症治疗均好转。两组治疗期间无输液反应、肝功能异常、胃肠道症状和严重感染等不良事件发生。两组不良事件发生率比较,差异无统计学意义(P=0.793)。
3 讨 论
SLE是一种因免疫调节功能紊乱、产生多种自身抗体、进而引起全身多系统损害的自身免疫病。《2020中国系统性红斑狼疮诊疗指南》提出最新治疗目标,短期目标是控制疾病活动、改善临床症状,达到临床缓解或可能达到的最低疾病活动度;而长期目标则是预防和减少复发,减少药物不良反应,预防和控制疾病所致的器官损害,实现病情长期持续缓解,降低病死率,提高患者的生活质量[11]。激素在治疗SLE 中发挥着至关重要的作用,是 SLE 诱导缓解治疗最常用且国内外指南一致推荐的基础用药[12]。但是长期使用大剂量激素可导致器官损伤和一些并发症的发生,因此,SLE 中长期治疗应该将激素尽可能减量,甚至逐渐停用激素[13]。
贝利尤单抗与可溶性BLyS结合可抑制B细胞增殖、分化,诱导自身免疫性B细胞凋亡,从而减少自身抗体产生而发挥治疗SLE的作用[14]。王金润等[15]的研究表明,贝利尤单抗治疗SLE 3个月,患者的疾病活动度明显下降,同时能够协助糖皮质激素的常规减量。还有研究表明,对于 SLE 初诊疾病活动性评分较高、抗 ds-DNA 水平较高和补体下降明显的患者,贝利尤单抗可以明显降低SLE疾病活动度,降低SLEDAI评分、抗ds-DNA水平,提高补体水平,并减少糖皮质激素用量[16]。本研究旨在对贝利尤单抗治疗中、重度活动性SLE 12个月的临床疗效及安全性进行分析评价,并评估激素的减量情况。
此前,东北亚Ⅲ期临床试验研究结果表明,治疗52周,贝利尤单抗组的SRI-4应答率明显高于未用贝利尤单抗的对照组,贝利尤单抗显示出激素减量的明显优势,不良事件发生率与对照组相似[6]。本研究显示,常规治疗方案联合贝利尤单抗治疗中、重度活动性SLE 12个月,SRI-4应答率为60.00%,明显高于对照组;且在降低SLEDAI-2K评分,提高补体C3、C4、白蛋白水平,改善肾脏受累情况均较对照组更为有效,提示联合贝利尤单抗能更好地使中、重度活动性SLE达到疾病缓解,病情活动度下降,提高补体、白蛋白及改善患者肾脏受累情况。本研究结果还显示,常规治疗方案联合贝利尤单抗治疗从第3个月开始,甲泼尼龙片用量持续减少,与对照组比较,差异有统计学意义(P<0.05),提示贝利尤单抗对于激素减量有优势,这与国内外研究报道[6,17-20]一致。
本研究中,两组患者的不良事件发生率相差不大,以轻症感染为主,未出现真菌及卡氏肺孢子菌感染等严重不良事件,经对症治疗后病情均好转。因此,在常规治疗方案基础上联用贝利尤单抗治疗中、重度SLE,并不增加不良事件的发生,提示贝利尤单抗治疗SLE 的安全性、耐受性较好。
综上所述,在常规治疗背景下,联合贝利尤单抗治疗中、重度活动性SLE ,可明显提高患者SRI-4应答率,改善临床症状,提高补体、白蛋白水平,改善肾脏受累情况,降低疾病活动度,从而更好控制和稳定病情,并且更有助于激素减量,减少不良反应发生率。此外,贝利尤单抗的临床安全性较高,未出现重症感染患者。但由于本研究纳入样本量较少,研究观察时间较短,尚需更多时间、更大样本量的临床研究来评估贝利尤单抗对 SLE 患者的长期有效性及安全性。
