草酸与铬酸根形成配位络合物强化可见光还原六价铬的机理研究
2024-02-22关盈盈葛小明邓力恺邹建平
关盈盈, 王 浩, 葛小明, 邓力恺, 邓 斌, 穆 毅,*, 邹建平,*
(1. 南昌航空大学 江西省持久性污染物控制与资源化重点实验室,江西 南昌 630069; 2. 中国航发南方工业有限公司 安全保障部环境保护室,湖南 株洲 412002)
0 引 言
航空工业金属表面处理、皮革鞣制、印染等工业生产过程会产生大量含Cr(Ⅵ)废水[1]。由于早期环保意识欠缺、治理手段执行不到位,大量未经有效处理的含Cr(Ⅵ)废水直接排放到自然环境中,导致我国自然水体中出现Cr(Ⅵ)污染的现象[2]。相关研究表明,我国约有1 250万t土壤被Cr重度污染,Cr污染面积占土壤总面积的1.1%。Cr(Ⅵ)污染已成为我国5种最常见的重金属污染之一[3-4]。Cr(Ⅵ)具有高毒性,可以通过食物链的富集效应积累在人体内,而进入人体内的Cr(Ⅵ)很难自然排除。研究发现,当人体内Cr(Ⅵ)含量超过200 μg/L时会引起DNA变异以及组织器官癌变[5-6],对人体的伤害一般是终身不可逆的。基于此,国家制定了相关标准,规定Ⅰ、Ⅱ、Ⅲ类水体中Cr(Ⅵ)的最高允许浓度分别为0.005、0.010和0.050 mg/L (GB 14848—08)。因此,Cr(Ⅵ)污染的治理刻不容缓,其治理技术一直是环境保护领域的热点和难点。
通常主要通过生物炭吸附法、化学还原法和生物修复法等技术治理自然水体中的Cr(Ⅵ)污染[7-9],然而这些技术均存在一些问题。生物炭吸附法的运行成本高,对Cr(Ⅵ)的吸附容量有限[10];化学还原法是通过加入还原药剂(如硫酸亚铁、亚硫酸钠、硫化钠等)将高毒性的Cr(Ⅵ)还原为相对低毒性且稳定的Cr(Ⅲ),实现Cr(Ⅵ)的无害化处理,但大量使用化学药剂可能造成土壤板结、酸化和二次污染等问题[11];生物还原修复法的周期较长、时效性差[12]。因此,亟需开发一种低成本、高效且不产生二次污染的方法来解决自然环境中Cr(Ⅵ)污染问题。
草酸是自然水体中最常见的一种小分子酸,主要来自于大分子有机物的分解和植物根系的分泌,在水体中的浓度高达1 mmol/L[13-14]。通常认为草酸具有较强的还原性,能够充当电子供体将Cr(Ⅵ)还原成Cr(Ⅲ)[15]。然而,草酸直接还原Cr(Ⅵ)的速率十分缓慢,TESTA研究发现在200 μmol/L草酸还原20 μmol/L Cr(Ⅵ)的反应进程中,反应进行到400 d,Cr(Ⅵ)的浓度仍没有发生变化[16]。值得注意的是,自然界中存在的铁矿物(如赤铁矿、磁铁矿)是一种半导体物质,能够作为光催化剂诱导草酸还原Cr(Ⅵ)[17-21]。铁矿物在激发波长照射下能够生成电子-空穴对。草酸能够淬灭空穴,防止电子、空穴重新复合,进而促使电子还原Cr(Ⅵ)[22]。铁矿物的激发波长大多在紫外光区,因此光催化还原Cr(Ⅵ)过程通常需在紫外光照射下进行,限制了Cr(Ⅵ)的还原效率。
本文借助等温滴定微量热法(Isothermal Titration Calorimetry,ITC),电喷雾高分辨质谱(Electrospray Ionization High Resolution Mass Spectrometry,ESI-HRMS)等表征手段,结合理论计算探究草酸根和铬酸根形成配位络合物的反应机制,并得到配位络合物的具体结构式;通过理论计算研究草酸-铬酸配位络合物的光化学性质,通过分析草酸在可见光、单色光下还原Cr(Ⅵ)的动力学,揭示草酸根与铬酸根配位过程强化草酸可见光还原去除Cr(Ⅵ)的内在机制。随后,将继续分析草酸可见光还原Cr(Ⅵ)的中间产物,确定草酸可见光还原Cr(Ⅵ)的最终反应产物,推导Cr(Ⅵ)的光还原路径。本研究将为利用自然水体中常见的草酸在可见光照射下还原Cr(Ⅵ)技术提供理论依据。
1 材料与方法
1.1 实验仪器及试剂
实验仪器:微热等温滴定量热仪(ITC200,马尔文帕纳科,美国),高效液相色谱仪(HPLC,UltiMate 3000,赛默飞科技,美国),高分辨质谱仪(Dionex Ultimate 3000,赛默飞科技,德国)。
实验试剂:草酸(C2H2O4,分析纯,阿法埃莎(中国)化学有限公司),重铬酸钾(K2Cr2O7,分析纯,国药集团化学试剂有限公司),氢氧化钠(NaOH,分析纯,国药集团化学试剂有限公司),硫酸(H2SO4,国药集团化学试剂有限公司),1,5-二苯氨基卡巴肼(C13H14N4O,国药集团化学试剂有限公司)。
1.2 Cr(Ⅵ)光还原实验
配置100 mg/L Cr(Ⅵ)储备液:使用电子天平称取0.028 2 g K2Cr2O7固体溶于50 mL蒸馏水中,随后将溶液转移至100 mL容量瓶,加入蒸馏水定容至刻度线处,得到100 mg/L Cr(Ⅵ)储备液。
Cr(Ⅵ)光化学还原实验:在150 mL的光催化反应器中,使用300 W 泊菲莱氙灯作为光源,使用滤波片过滤420 nm以下的紫外光。反应条件为草酸初始浓度:5 mmol/L;Cr(Ⅵ)初始浓度:10 mg/L;反应体积:100 mL;溶液初始pH:3.0、4.0、5.0、6.0、7.0;取样时间:反应开始后每1 h取一次样;Cr(Ⅵ)浓度测试方法:1,5-二苯氨基卡巴肼显色法。
1.3 等温滴定量热法(ITC)
采用ITC研究Cr(Ⅵ)和草酸的配位络合能力。配置初始浓度分别为52 mg/L(1.0 mmol/L)和0.9 g/L(10.0 mmoL/L)的Cr(Ⅵ)和草酸溶液。利用H2SO4和NaOH分别调节Cr(Ⅵ)和草酸溶液的pH为3.0、4.0、5.0、和6.0。随后取200.0 μL的Cr(Ⅵ)到样品池中,每隔100 s滴入2.0 μL,同时监控释放的热量。随后以草酸与Cr(Ⅵ)的摩尔比为横坐标,体系释放的热量为纵坐标作图,得到等温滴定微量热曲线图。
1.4 电喷雾高分辨质谱(ESI-HRMS)
利用ESI-HRMS检测草酸和Cr(Ⅵ)形成的配位络合物以及草酸可见光还原Cr(Ⅵ)过程中的中间产物和最终反应产物。测试条件:进样体积为5 μL,喷雾电压为-3.2 kV,扫描模式为负离子模式,扫描范围m/z=100.0~500.0。利用Xcalibur 2.1软件分析质谱峰的归属,质谱峰对应物质的匹配精度≤5 mg/L。
1.5 DFT理论计算

2 结果与讨论
2.1 草酸根与铬酸根配位络合能力的研究
首先,利用ITC初步考察了在不同pH条件下,草酸和Cr(Ⅵ)形成络合物的能力。以草酸与Cr(Ⅵ)的摩尔比为纵坐标,体系释放的热量为横坐标作图。如图1所示,当溶液pH≤4,将草酸溶液滴入Cr(Ⅵ)溶液中,检测到释放的热能(ΔG)分别为-5.72 kJ/mol(pH=3.0)和-3.56 kJ/mol(pH=4.0)。值得注意的是,随着加入的草酸量逐步增加,释放的热量逐步减少。当样品池中草酸与Cr(Ⅵ)的摩尔比>1,释放的热量显著减少,表明草酸与Cr(Ⅵ)形成络合物的配位比是1。当溶液pH≥5,将草酸溶液滴入Cr(Ⅵ)溶液中,检测到少量的稀释热量,表明草酸根和Cr(Ⅵ)没有发生络合反应。ITC滴定实验结果表明,pH≤4.0时,草酸和Cr(Ⅵ)能够形成配位比为1∶1的络合物;而当pH≥5.0时,草酸和Cr(Ⅵ)不会发生配位络合反应。

图1 在不同初始pH条件下,与的等温滴定微量热曲线的积分热曲线Fig. 1 ITC analysis profile for Cr(Ⅵ)/oxalic acid at different pH

2.2 草酸-铬酸配位络合物光还原Cr(Ⅵ)的研究


图的表面静电势图和形成络合物过程中的 过渡态结构示意图形成过程中的能量变化图络合物的高分辨质谱图 (h)不同pH下,络合物的EIC图Fig. 2 Computer-generated structures and electrostatic potential maps of (a) (e) Basic geometrical parameters of the transition state structure for complexation of (f) IRC pathway for the formation of detected by high resolution mass spectra, and (h) The extracted ion chromatograms of complex (m/z=188.911 43~188.913 31) at different pH
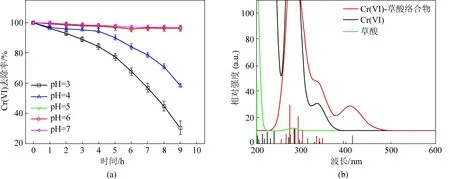
图3 (a)不同pH条件下草酸还原Cr(Ⅵ)的效果图 (b)理论计算模拟的络合物紫外-可见吸收光谱图Fig. 3 (a) Effect of different pH on Cr(Ⅵ) reduction by oxalic acid and (b) The simulated UV-vis absorption spectra of
2.3 理论计算
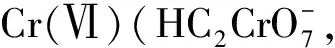
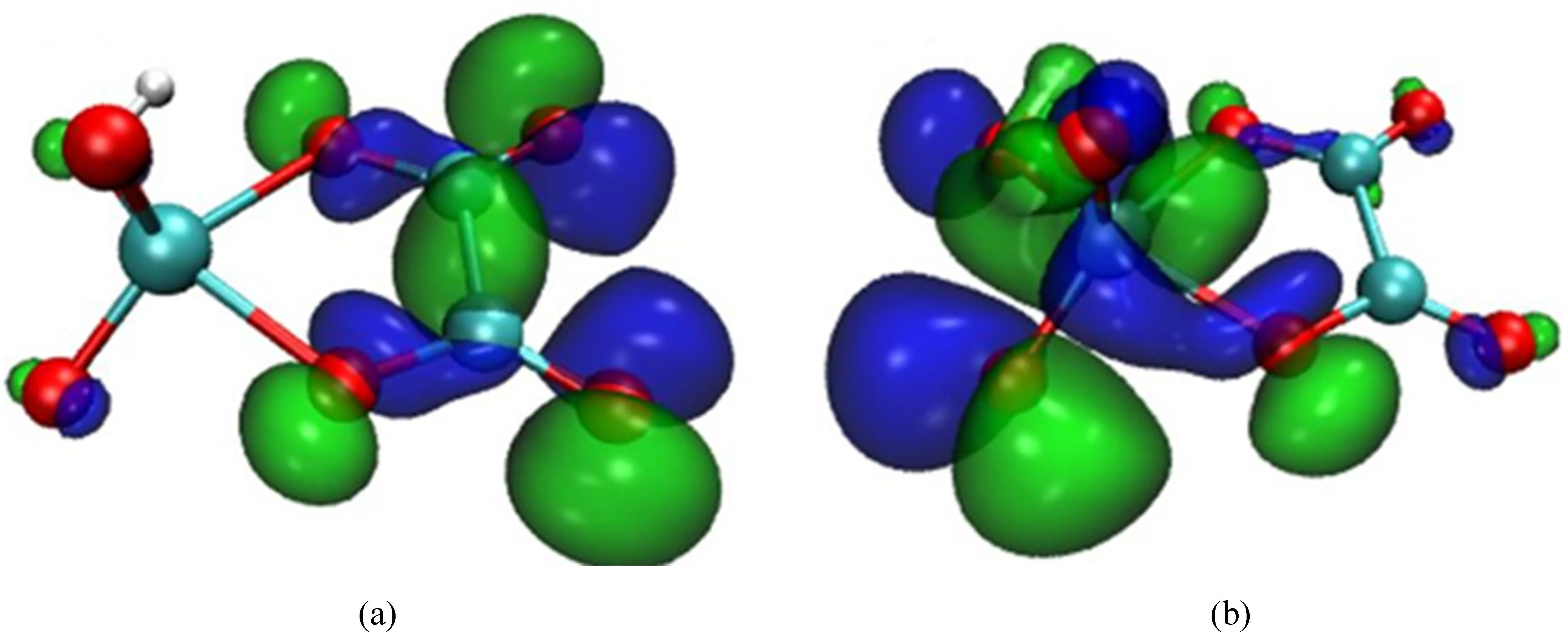
图的HOMO轨道的LUMO轨道Fig. 4 (a) The highest occupied molecular orbital (HOMO) and (b) The lowest unoccupied molecular orbital of complex

图5 电喷雾高分辨质谱检测草酸可见光还原Cr(Ⅵ)过程中的中间产物Fig. 5 The ESI-QTOF-MS spectra of Cr(Ⅵ) reduction intermediates in oxalic acid solution under visible light irradiation
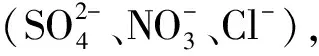


图6 草酸可见光还原Cr(Ⅵ)生成Cr(Ⅲ)的反应路径Fig. 6 Possible reduction pathway of Cr(Ⅵ) under visible light illumination with oxalic acid

图7 (a)水体中不同阴阳离子对草酸可见光还原Cr(Ⅵ)的影响(b)不同浓度的CaO对总Cr浓度的影响Fig. 7 (a) Effect of co-existed ions on reduction efficiency of Cr(Ⅵ) by oxalic acid under visible light illumination and (b) Effect of CaO with different concentrations on total Cr concentration
3 结论与展望

