活化过氧乙酸降解新污染物:过程、性能和机制
2024-02-22吴家宝刘艳彪
吴家宝, 刘艳彪, 2, *
(1. 东华大学 环境科学与工程学院, 上海 201620; 2. 上海污染控制与生态安全研究院, 上海 200092)
0 引 言
近年来,随着人口急剧增长以及工业化进程的加快,水资源短缺与水环境污染问题凸显[1]。目前,由新污染物导致的环境污染和生态毒害问题引起了广泛关注,亟待发现新原理,开发有针对性的新处理技术[2]。这是由于传统水处理技术在处理新污染物方面通常表现不佳,容易导致污染物的大量累积,甚至对生物处理系统造成冲击。
研究表明,H2O2、PMS/PDS与PI等氧化剂活化过程中易受溶液pH、共存有机质(NOM)和无机阴离子的影响,尤其是反应过程中极易产生有毒副产物。过氧乙酸(PAA)是一种新兴氧化剂,活化后可产生特殊的有机自由基如乙酰氧自由基(CH3C(O)O·)、过氧乙酰自由基(CH3C(O)OO·)与过氧烷基自由基(·OOCH3)等,具有较好的抗干扰性以及无有毒副产物等特点,是替代传统水处理氧化剂的理想选择[12-13]。
到目前为止,尽管已有通过活化PAA降解新污染物的相关报道,但仍然缺乏关于PAA活化的相关系统性综述。许多研究对活化PAA降解污染物过程中的活性物种来源、类型和局限性缺乏详细讨论。基于此,本文介绍了PAA的理化特性,总结了各种有效的PAA活化策略,讨论了PAA活化反应机理及相关影响因素;最后,综合比较了各种活化策略的优势和适用范围,并在此基础上分析了PAA活化水处理技术面临的问题,展望了基于PAA高级氧化技术未来的研究方向。
1 PAA的性质特征
PAA是一种过氧有机酸,由C、H、O三种元素组成,分子式为C2H4O3,分子结构如图1所示,具有与H2O2类似的O—O键,分子极性强,易断裂,具有较强的氧化性。PAA的O—O键键能为170 kJ/mol,稍弱于H2O2的210 kJ/mol。因此PAA活化相较于H2O2活化更具优势。PAA通常由乙酸(CH3COOH)和H2O2反应合成(见式(1))[14],是一种无色液体,有类似乙酸的刺激性气味。
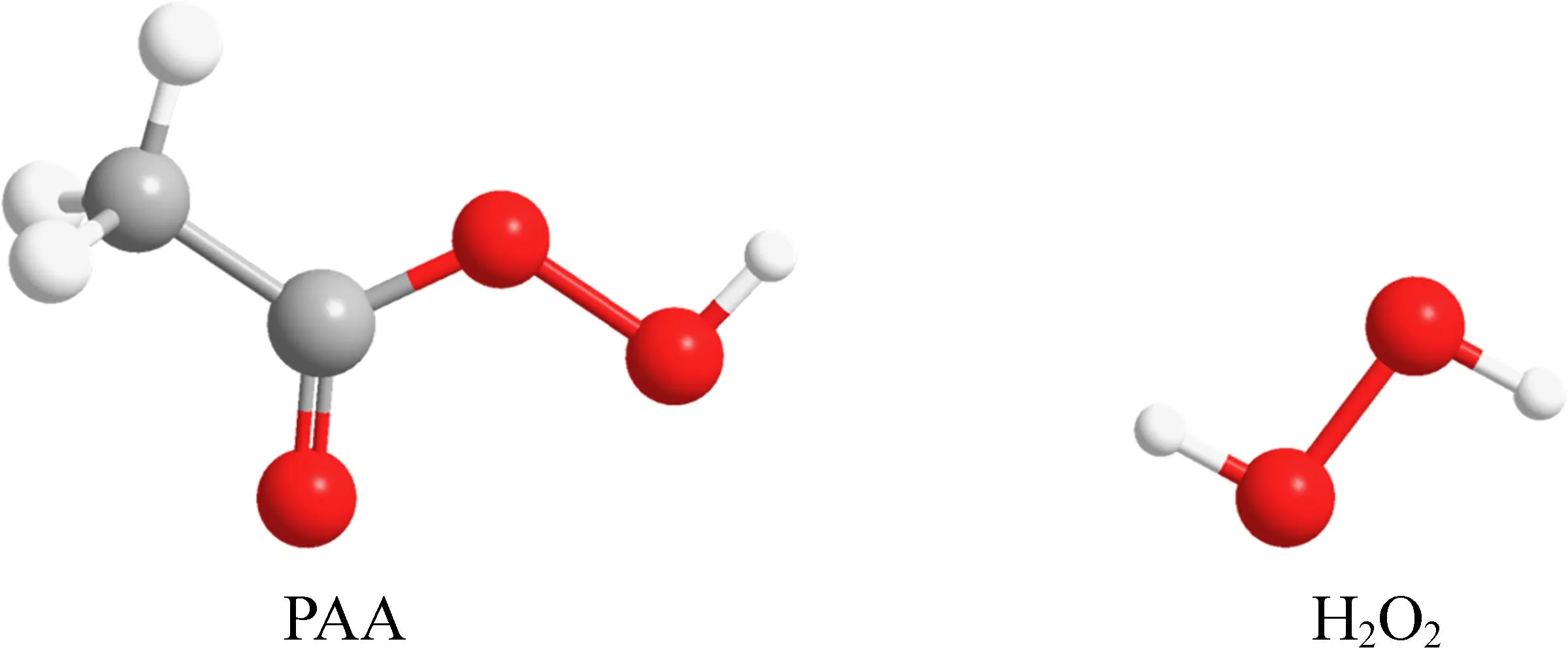
图1 PAA与H2O2结构模型对比 Fig. 1 The structural model of PAA and H2O2

(1)
此外,PAA的稳定性与溶液pH密切相关。研究表明,碱性条件易导致PAA分解失活。pH在5.5~8.2范围内,PAA会自发分解(见式(2)),此时水解程度较低;pH>8.2时,PAA同时发生分解和水解(见式(3)),产生乙酸和H2O2[15]。

(2)

(3)
由表1可知,PAA的沸点和熔点均较低,在水中易溶解,其水溶液pH通常小于1.5。PAA易挥发不稳定,当浓度大于15%时,有燃烧爆炸的危险。PAA的氧化还原电位在1.06~1.96 V之间,该电位随溶液pH增加而增大。长期暴露于高浓度PAA下会对眼睛、皮肤、粘膜和上呼吸道造成严重刺激[16]。

表1 PAA的物理化学性质
PAA具有较高的氧化还原电位,在漂白、消毒、杀菌、氧化以及催化聚合等方面均有应用,是一种极具发展潜力的新兴氧化剂[17]。然而PAA本身对有机污染物的降解能力有限,需要借助活化技术来增强其氧化能力。近年来的研究主要集中在研发各种高效的PAA活化策略(如直接活化[18-19]、均相活化[20-21]以及非均相活化[17, 22])产生HO·、CH3C(O)O·、CH3C(O)OO·、高价金属和1O2等氧化性物种来去除新污染物。
2 过氧乙酸活化策略
2.1 直接活化
2.1.1 紫外活化
紫外线(UV)可用于激活PMS、H2O2、PI与PAA等氧化剂,产生氧化性物种来灭活水中的细菌、病毒以及降解有机污染物[23]。在UV/PAA系统中通常采用波长为254 nm的紫外光来活化PAA,相关的紫外活化过程如式(4)~(7)[24-25]。

(4)

(5)

(6)

(7)
PAA受到紫外光照射后,可分解产生HO·和CH3C(O)O·。大量研究报道了UV/PAA在新污染物去除方面的进展。YAN等[26]采用UV/PAA技术可在45 min内将5 ppm土霉素完全去除,矿化率达到50.9%。UV和PAA联合使用对土霉素的去除和矿化具有协同作用,UV/PAA体系产生的HO·参与土霉素降解矿化的整个过程,副产物二甲基亚硝胺的浓度降低了65.8%,UV/PAA体系不仅可有效地去除难降解的抗生素,还可控制副产物的形成。
CAI等[24]评价了PAA在254 nm紫外线辐照下的光解作用和UV/PAA体系对抗生素的降解效能。在UV/PAA体系中,HO·是氧化降解布洛芬和卡马西平的主要活性物种。除HO·外,CH3C(O)O·和CH3C(O)OO·在降解萘普生(NPX)和2-萘氧基乙酸也有显著贡献,UV/PAA系统中产生的有机自由基对某些萘基化合物具有一定的氧化活性。
UV/PAA体系的主要影响因素是UV波长、辐照强度以及PAA投加量。UV波长对活性物质的产率具有显著影响,波长越短能量越高,越有利于活性物质的产生;当UV辐照强度增大时,反应速率常数呈线性增加;此外,UV/PAA体系中PAA剂量具有最佳值,PAA投加过少易造成活性物质产率不足,氧化能力弱;当PAA过量时,PAA会将HO·猝灭,降低污染物去除效果[27]。UV/PAA工艺简单、操作方便、可规模化操作,具有良好的可行性与适用性,应用前景良好。然而,目前相关研究主要集中在紫外光,其在太阳光谱中紫外光仅占其5%,因此反应主要依靠人造光源,这导致该技术处理成本较高。此外,有机废水一般具有较高的色度,会降低紫外光的透射率,从而影响UV/PAA体系的性能。
2.1.2 超声活化
超声波(US)是一种清洁安全的物理技术,逐渐被应用于水处理领域。超声作用主要通过空化产生,首先在水体中产生空腔,空腔逐渐生长,最后剧烈坍塌,空腔内部及其附近温度较高,空腔坍塌过程伴随着巨大的能量交换[28-29]。近年来一些研究将超声与氧化剂如PMS、O3、H2O2、PAA等结合用于水体新污染物治理,超声作用能够显著促进氧化剂活化产生高氧化性物种,从而提升对新污染物的去除效果[30-32]。在US/PAA体系中,PAA活化过程如式(8)~(10)[19]。超声作用可同时破坏PAA的O—H键和O—O键,产生HO·、CH3C(O)O·、CH3C(O)OO·与1O2等活性物种。

(8)

(9)

(10)
YAO等[19]利用超声活化PAA降解盐酸四环素,在US/PAA系统中超声活化PAA产生了大量1O2和CH3C(O)O·等有机基自由基,在30 min内四环素降解效率达到99.4%,超声作用将四环素的降解效率提升了4.88倍。此外,超声功率、溶液pH以及PAA剂量是影响US/PAA体系的主要因素。超声功率越高,越易形成空化气泡,并且超声作用能够显著增强机械冲击,加速传质过程,因此越有利于活化PAA产生大量的氧化性物种,从而提升水体污染物的去除效果。pH一方面会影响PAA的分解与水解,酸性条件下PAA较为稳定[15],另一方面是有机污染物在不同pH下可能会表现出不同的分子态和离子态,这将改变污染物与活性物种结合与相互作用方式[33]。US/PAA工艺操作简单,无二次污染产生,但超声处理过程需要持续向水体进行能量输送,这导致处理成本显著增加。
2.1.3 热活化
由于PAA中存在O—O键,其键能较弱,热量可加速O—O键断裂,产生CH3C(O)O·和HO·。此外,有研究报道PAA热活化过程存在两种途径[18, 34]:自由基途径与非自由基途径。自由基途径主要是PAA热活化生成HO·和CH3C(O)O·等,如式(11);非自由基途径是指PAA与CH3C(O)OO-在热能作用下,产生1O2,如式(12)。

(11)

(12)
WANG等[18]采用热活化策略活化PAA用于新污染物降解。在加热作用(60 ℃)下,PAA被活化产生HO·、CH3C(O)O·、CH3C(O)OO·与1O2等活性物种,可有效去除水中的磺胺甲噁唑(SMX)。热活化体系受温度影响显著。首先,温度升高,增加污染物在水中的溶解度,加速反应的动力学;其次,在温度较低时无法断裂O—O键,温度越高PAA活化效率越高,提供的活性氧物种将显著增多,促进污染物快速降解。
热活化作为PAA活化的有效策略之一,简便直接,不易造成水体污染,但需要加热设备,能耗高,通常自然水体温度较低,不能直接活化PAA产生活性物种,因此难以实现规模化操作。热活化PAA技术更适合处理某些高温的工业废水或冷却水,无需额外供给热量,利用废水余热直接活化PAA。
2.1.4 电场活化
电化学氧化技术具有操作简单、环保和高效等优势,是水处理领域的研究热点[35]。电活化是H2O2最常见的活化形式。近年来,利用电化学活化过硫酸盐的技术也受到关注[36]。目前,关于PAA电化学活化的报道较少。YUAN等[37]以铂片为阳极,石墨板为阴极,建立了一种电化学活化过氧乙酸(EC/PAA)协同体系用于有机污染物的降解,电场可以活化体系中的PAA产生HO·和有机自由基(RO·)。
如图2,在EC/PAA体系中,阳极将水氧化产生HO·,强化了体系的氧化性能。阴极则通过电子的还原作用,将PAA活化产生HO·,CH3(O)O·,CH3C(O)OO·等,主要反应过程如式(13)~(15)。

图2 EC/PAA体系的反应机制Fig. 2 The mechanism of EC/PAA system

(13)

(14)

(15)
LU等[38]利用掺硼金刚石(BDD)作为阳极,铁掺杂石墨烯为阴极构建了EC/PAA体系用于抗生素废水的处理,在EC/PAA的电化学体系中,BDD阳极主要产生HO·,阴极主要产生RO·,尤其是CH3C(O)OO·,EC与PAA的协同作用有效地去除了SMX等抗生素。除了PAA剂量和pH,电流密度是影响EC/PAA体系的主要因素,电流密度会直接影响电极电位,进而影响PAA电化学活化。通常电流密度越大,PAA活化效率越高,体系中生成的HO·和RO·越多,但是阳极可能发生析氧反应,阴极可能发生析氢反应,这些副反应将抑制PAA活化。电化学活化PAA是一种新兴的电类芬顿水处理技术,适用范围广,实用性强,该工艺易集成化与自动化,具有大规模应用的潜力。
2.2 均相活化
PAA常见的均相催化剂包括无机阴离子和金属离子。无机盐与金属离子便于运输和储存,具有成本低、相对稳定以及安全风险低等优点。其中,用于PAA活化的无机阴离子主要是氯离子(Cl-)和磷酸盐阴离子(PBS),金属离子主要是Fe2+、Cr3+、Cu2+、Co2+、Ru3+和Mn2+等,金属离子大多通过电子转移方式活化PAA,具有高活性、经济有效、环保的特性。
2.2.1 金属离子活化
(1)Fe2+活化
KIM等[39]构建了Fe(Ⅱ)/PAA体系降解NPX和BPA等新污染物,发现Fe(Ⅱ)与PAA的反应速度比H2O2快得多,提出了Fe(Ⅱ) 活化PAA化学机制,如式(16)~(19)。

(16)

(17)

(18)

(19)
Fe(Ⅱ)与PAA反应产生CH3C(O)O·与HO·,同时还形成了高价铁氧化性物种FeⅣO2+,由CH3C(O)O·引发的链式反应,进一步产生更多有机自由基,加速新污染物降解。
此外,YANG等[21]揭示了Fe(Ⅱ)/PAA体系氧化对砷酸的内在机制,在中性或酸性环境下,Fe(Ⅱ)/PAA体系可在20 s内快速降解对砷酸,远高于单独PAA氧化系统,在Fe(Ⅱ)/PAA体系中,HO·和RO·导致了对砷酸降解,在真实水体中,总砷去除率大于80%。然而,Fe2+与Fe3+遇碱后易发生沉淀,导致铁循环受阻,降低PAA的活化效率。因此,Fe(Ⅱ)/PAA体系更适合酸性条件下处理废水。
(2)Cr3+活化
BELL等[40]采用Cr(Ⅲ)活化PAA降解抗生素甲氧苄氨嘧啶(TMP),结果发现Cr(Ⅲ)/PAA体系在碱性条件下降解TMP的速率大于PAA和Cr(Ⅲ)/H2O2体系,同时提出了Cr(Ⅲ)活化PAA的机制,如图3所示,在PAA活化过程中,HO·是主要的自由基物种,Cr(Ⅳ)/Cr(Ⅴ)是额外的活性物质。

图3 Cr(Ⅲ)/PAA体系的反应机制[40]Fig. 3 The mechanism of Cr(Ⅲ)/PAA system[40]
Cr(Ⅲ)活化PAA主要的化学反应过程如式(20)~(23),可产生如Cr(Ⅳ)、Cr(Ⅴ)、Cr(Ⅵ)、·OH、CH3C(O)O·和CH3C(O)OO·等氧化性物种,有效地将TMP等新污染氧化去除。Cr(Ⅲ)/PAA体系在碱性条件下具有一定优势,但易导致高毒性的Cr(Ⅵ)在溶液中残留,引发二次污染,对生物、环境造成负面影响[41-42]。

(20)

(21)

(22)

(23)
(3)Co2+活化
WANG等[20]使用Co2+作为活化剂建立了均相PAA活化体系降解SMX,并提出了Co2+活化PAA反应机制,如式(24)(25),PAA与Co2+反应生成CH3C(O)O·与Co3+,随后Co3+与PAA反应生成CH3C(O)OO·与Co2+,Co2+与Co3+在活化PAA的过程中循环转化。

(24)

(25)
如图4所示,在Co2+/PAA体系中CH3C(O)OO·
是主要的活性物种,其次是CH3C(O)O·,由于Co3+与Co2+高效的氧化还原循环,即使Co添加剂量小于1 μmol/L也有良好的降解效率。Co2+/PAA体系最佳的反应pH接近中性,腐殖酸以及碳酸氢根会抑制SMX的降解。
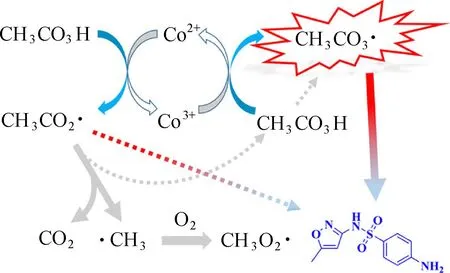
图4 Co2+/PAA体系的反应机制[20]Fig. 4 The mechanism of Co2+/PAA system[20]
DU等[43]同样以Co2+作为活化剂活化PAA,在中性条件下高效降解苯酚,Co(Ⅱ)/PAA体系中主要活性物质是CH3C(O)OO·,CH3C(O)OO·通过氢原子提取的方式氧化降解苯酚。
目前,普遍认为Co(Ⅱ)主要通过价态循环活化PAA产生RO·自由基(CH3C(O)O·和CH3C(O)OO·)来降解污染物[43-45],但关于活性Co物种对污染物的降解贡献仍不明确。ZHAO等[46]以BPA为目标污染物,证明了Co(Ⅱ)/PAA体系中RO·与Co(Ⅲ)均不是关键活性物种,利用拉曼光谱技术检测到Co(Ⅱ)-PAA络合物。因此,提出亚稳态的金属-过氧中间体Co(Ⅱ)-PAA才是该体系主要活性物种的新机制。
首先Co(Ⅱ)与PAA络合形成Co(Ⅱ)-PAA络合物,大部分Co(Ⅱ)-PAA络合物直接氧化有机污染物,少量Co(Ⅱ)-PAA络合物通过分子内O—O键断裂产生Co(Ⅲ)和RO·,它们作为次要活性物种参与污染物降解。
此外,Co(Ⅱ)/PAA体系受酸碱度影响较大,当pH在3.0~7.0范围内,污染物降解效率随pH增大而增加,这是因为pH的变化会改变Co(Ⅱ)-OO(O)CCH3物种质子化状态,并进一步影响Co(Ⅱ)-OO(O)CCH3物种的反应活性。当pH从7.0增加到9.0时,Co2+比例下降,在pH=11.0时溶液中不存在Co2+物种,碱性环境中产生的Co(OH)2无法与PAA形成Co(Ⅱ)-OO(O)CCH3物种,导致有机污染物去除效率下降[47]。因此该体系适合处理接近中性的废水,但需要考虑废水中NOM对降解的影响。
(4)Ru3+活化
在中性条件下Fe2+、Cu2+和Fe3+等离子易发生水解,因此中性条件下这些离子对PAA的活化效率较差,虽然Co2+在中性条件下可高效活化PAA,但是在磷酸盐缓冲溶液中Co2+易与磷酸盐形成复合物,这会抑制Co2+活化PAA的效率。LI等[48]探索了Fe2+、Mn2+、Ru3+、Co2+、Ni2+和Cu2+等离子在含10 mmol/L磷酸盐的体系中活化PAA降解磺胺类抗生素SMX,结果发现,Ru3+/PAA体系在2 min内将SMX完全降解,而相同条件下,以Fe2+、Mn2+、Co2+、Ni2+和Cu2+等离子活化PAA时,SMX仅降解20%左右。Ru3+/PAA体系在含磷酸盐条件下表现出远优于其他过渡金属离子的活化与降解性能。在Ru3+/PAA体系中,氧化降解SMX的主要活性物种是CH3C(O)O·与CH3C(O)OO·,Ru3+活化PAA与其他金属离子活化反应过程类似,如式(26)~(29)。

(26)

(27)

(28)

(29)
Ru3+/PAA体系中产生的Ru4+可与PAA反应产生额外的CH3C(O)OO·,进一步氧化SMX。此外,Ru3+/PAA体系的氧化过程除了受磷酸盐抑制小,也不受溶液中氯离子与碳酸盐离子影响,展现出良好的抗干扰性。
2.2.2 无机阴离子活化
(1)Cl-活化
除金属离子外,无机阴离子Cl-也可活化PAA。直接利用高盐废水中的Cl-活化PAA降解污染物,可减少化学品与能源消耗。SONG等[49]探究了Cl-对PAA的活化能力以及Cl-/PAA体系对新污染物BPA的降解性能与机制,通常PAA溶液含有大量H2O2,通过比较单独PAA、单独H2O2以及Cl-/H2O2体系,发现单独PAA和单独H2O2体系均无法降解BPA,Cl-不能活化H2O2产生活性物种,这可能是由于PAA中O—O键更易断裂。此外,Cl-活化PAA产生CH3C(O)O·是整个活化与降解过程的限速步骤,如式(30)(31)。

(30)

(31)
对比无活化剂的PAA体系发现,Cl-活化PAA分解速率是其常温下的107倍。如图5所示, Cl-/PAA体系化学反应较为复杂,活性物种类型多,其中有机自由基(CH3C(O)OO·、·CH3、CH3C(O)O·和CH3COO·)与游离氯(Cl2和HClO)是主要氧化物种,有机自由基对降解的贡献大于游离氯。此外,Cl2(l)的反应速率比HClO高得多,与BPA发生取代反应会生成氯代副产物。
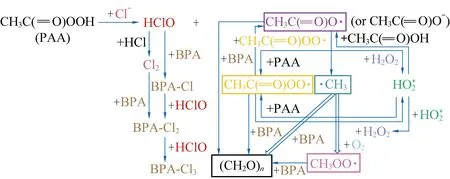
图5 Cl-/PAA体系降解BPA的反应原理[49]Fig. 5 The mechanism of Cl-/PAA system to degrade BPA[49]
Cl-/PAA体系的氧化性能受Cl-浓度影响较大,其氧化降解能力与Cl-浓度正相关。此外,体系pH会显著影响PAA、CH3COOH和HClO的形成,进一步影响BPA降解。在pH<3.4时,溶解的Cl2(l)是优势氧化物种,pH在3.4~7.7时,HClO是优势氧化物种,在中性条件pH<8.2时,PAA是优势氧化物种,中性形式的PAA具有更强的氧化能力[50]。Cl-/PAA体系以Cl-作为活化剂促进PAA活化,具有较宽的pH适用范围,在高盐废水有机污染治理方面展现出巨大的应用潜力。
(2)磷酸盐活化
DENG等[51]报道了一种采用PBS活化PAA的新策略,在PBS/PAA体系中,浓度为5 μmol/L的双氯芬酸(DCF)在45 min内被去除90%以上。在PBS/H2O2体系中,DCF几乎不降解。与H2O2不同的是,PAA具有不对称的结构,PBS易对PAA发起亲核攻击,导致O—O键断裂产生HO·和CH3C(O)O·,由CH3C(O)O·进一步转化形成更多的RO·与1O2,如式(32)~(34)。

(32)

(33)

(34)
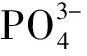

图6 PBS/PAA体系反应机制[51]Fig. 6 The mechanism of PBS/PAA system[51]
2.3 非均相活化
金属离子是一种高效的均相活化剂,被广泛用于PAA等氧化剂活化,但是金属离子本身具有毒性,均相催化剂分离回收困难,使用寿命短,这些一直是均相活化PAA技术在推广应用中面临的挑战[53-54]。因此研究者将注意力集中到非均相催化剂,研究和开发具有较高复用性的非均相催化剂用于PAA活化。目前,常用PAA非均相活化剂主要有金属催化剂如金属氧化物,非金属催化剂如活性炭与碳纳米管等。
2.3.1 金属催化剂
金属催化剂活化PAA的机制与金属离子活化PAA相似,PAA在金属催化剂表面发生反应,金属元素通过价态变化引发PAA活化,从而产生氧化性物种降解污染物。金属矿物种类非常丰富,但主要以Cu、Co、Mn和Fe等过渡金属为主。因此以氧化铜、钴锰尖晶石和氧基氯化铁这3种具有一定代表性的金属矿物为例,分析和归纳PAA活化机制与污染物降解性能。
(1)纳米氧化铜活化
ZHANG等[55]以纳米氧化铜(nCuO)作为催化剂在近中性条件下活化PAA,快速地降解了卡马西平(CBZ)。如图7所示,在nCuO/PAA体系中,PAA的催化分解是在nCuO表面发生的,Cu(Ⅱ)/Cu(Ⅰ)持续的氧化还原循环促进了PAA产生活性物质,体系中共存的H2O2对Cu(Ⅱ)/Cu(Ⅰ)循环起着重要作用。
如式(35)~(40)所示,nCuO与PAA接触后会形成表面Cu(Ⅱ)-过氧化物配合物,Cu(Ⅱ)与CH3C(O)OO-之间配位键拉伸促进了电子转移,进一步产生Cu(Ⅰ)和CH3C(O)OO·。此外,体系中共存的H2O2与nCuO表面形成Cu(Ⅱ)-过氧化物配合物,加速Cu(Ⅱ)与H2O2之间的电子转移[56],Cu(Ⅱ)有效地转化为Cu(Ⅰ),促进PAA分解,同时诱导产生Cu(Ⅱ)-OH配合物、CH3C(O)O·、CH3C(O)OO·和HO·,最终有效降解CBZ。CH3C(O)OO·是nCuO/PAA体系中主要活性物种,能选择性氧化具有丰富电子官能团的芳香族化合物,并且受实际废水基质影响较小,PAA分解形成的乙酸可作为后续生物处理的碳源,在水处理中具有良好的应用潜力。

(35)

(36)

(37)

(38)

(39)

(40)

图7 nCuO/PAA体系反应机制[55]Fig. 7 The mechanism of nCuO/PAA system[55]
在nCuO/PAA体系中,pH接近中性时降解效果最佳。pH除了影响PAA的分解与水解外,还会影响nCuO表面的电性,nCuO的等电点在3.0左右,在碱性条件下nCuO带负电荷,PAA-和nCuO之间的静电斥力会抑制PAA活化,并且碱性条件催化剂表面易形成非活性的氢氧化铜配合物,进一步降低nCuO的催化活性,因此该体系不适用于碱性条件。在酸性条件下,溶液中的优势物种是PAA,然而PAA中的O—O键长大于PAA-的O—O键长,PAA比PAA-更难活化[27]。酸性条件下,nCuO容易被腐蚀,导致金属离子浸出而使催化剂失活。此外,由于碳酸盐和碳酸氢盐会猝灭nCuO/PAA体系中的CH3C(O)OO·、CH3C(O)O·与HO·,因此碳酸盐和碳酸氢盐的存在会抑制污染物降解。
(2)Co-Mn尖晶石活化
尖晶石氧化物是一种双金属氧化物,因其制备简单、成本低和易回收,在多相催化高级氧化体系中应用广泛[57]。尖晶石结构氧化物内部存在较强的金属共价键,结构十分稳定,可有效防止金属离子浸出[58]。研究发现,锰(Mn)具有独特的Mn2+/Mn3+/Mn4+氧化还原特性,钴氧化物与Mn结合后呈多种价态,涉及复杂的电子转移路径,有利于氧化还原反应进行,因此在钴尖晶石结构中引入Mn可促进类芬顿反应的催化活性[59]。ZHANG等[60]制备了一系列不同金属比例的Co-Mn尖晶石氧化物(Co3-xMnxO4),其中Co1.1Mn1.9O4在PAA活化中表现出优异的性能,浓度为10 μmol/L的SMX在7 min内可被完全降解,超过了大多数报道的非均相催化剂。
在Co1.1Mn1.9O4/PAA体系中,CH3C(O)OO·是降解SMX的主要氧化性物种。Mn的存在不仅促进了电子转移过程,加速了Co(Ⅲ)到Co(Ⅱ)的还原,还降低了PAA活化的能垒,提高了PAA活化的动力学。
如式(41)~(48),在Co1.1Mn1.9O4的表面Co、Mn路易斯位点可分别与水分子反应形成Co(Ⅱ)-OH-和Mn(Ⅱ)-OH-物种,随后将吸附的PAA分子活化产生CH3C(O)O·与HO·,伴随生成Co(Ⅲ)与Mn(Ⅲ)和CH3C(O)OO·物种。其中,Mn(Ⅲ)有两种转化途径,分别是Mn(Ⅲ)-Mn(Ⅳ)-Mn(Ⅲ)-Mn(Ⅱ)和Mn(Ⅲ)-Mn(Ⅱ),而Co(Ⅲ)与PAA反应生成Co(Ⅱ),最终实现了Co(Ⅱ)与Mn(Ⅱ)在体系中的循环来高效活化PAA。此外,由于各种自由基与高浓度Cl-的连锁反应可产生大量HOCl,进一步促进SMX降解,因此,Co1.1Mn1.9O4/PAA体系中在模拟海水养殖废水中具有更高的SMX降解效率,在高盐度废水治理方面极具潜力。

(41)

(42)

(43)

(44)

(45)

(46)

(47)

(48)
(3)氧基氯化铁活化
氧基氯化铁(FeOCl)是一种具有斜立方晶体结构的层状金属[62],在层与层之间氯原子通过范德华力进行连接,特殊的线性结构(Cl-Fe-O和Fe-O-Fe)使其表面暴露大量的不饱和铁,这有利于电子转移同时将Fe(Ⅲ)还原为活性Fe(Ⅱ)[63-64]。CHENG等[61]以FeOCl作为活化剂活化PAA用于SMX降解,在中性条件下,SMX的去除率可达到90.37%。
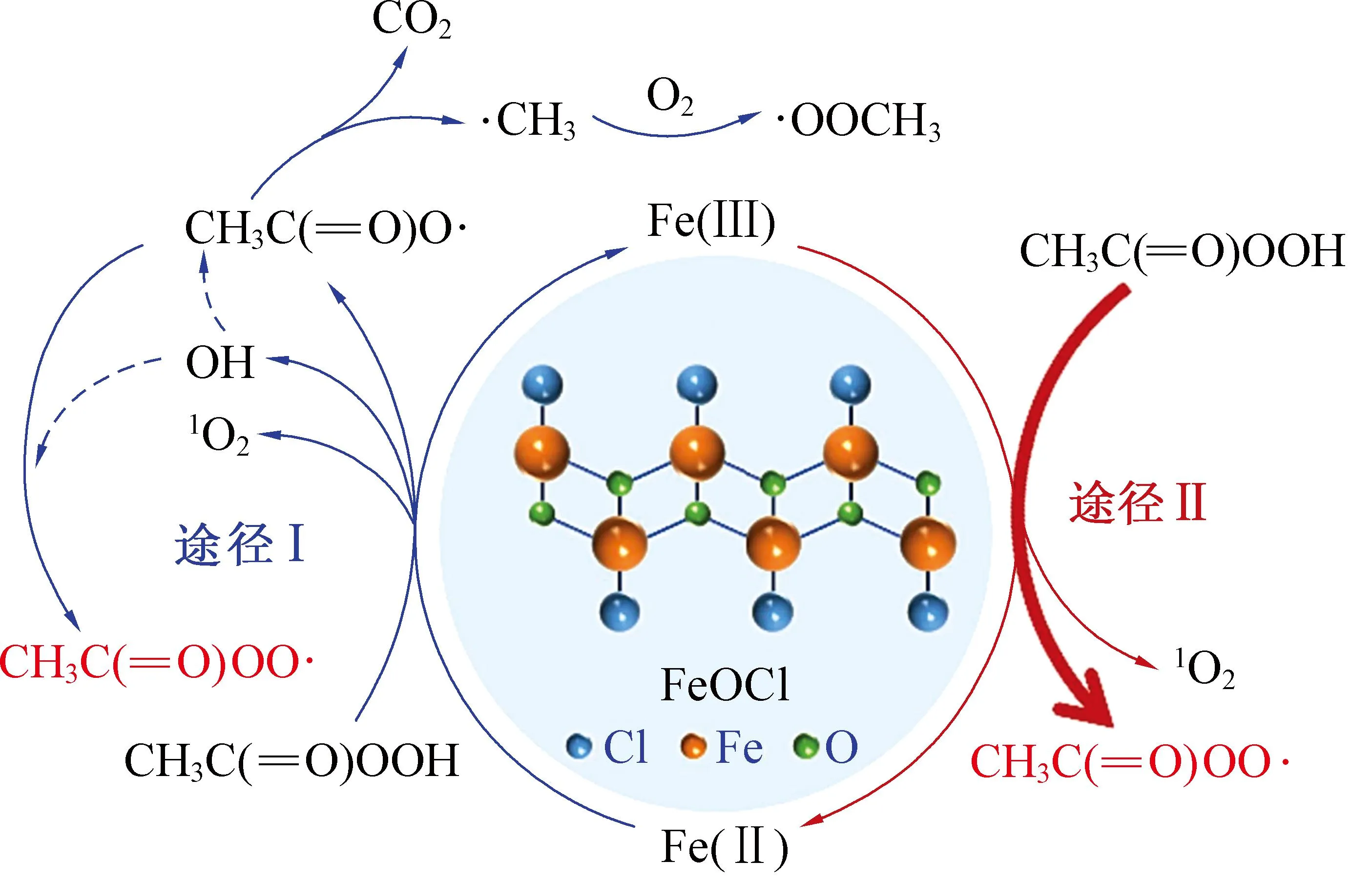
图8 FeOCl/PAA体系反应机制[61]Fig. 8 The mechanism of FeOCl/PAA system[61]
如图8所示,在FeOCl/PAA体系中,CH3C(O)OO·是降解SMX的主要活性物种。Fe(Ⅲ)/Fe(Ⅱ)的氧化还原循环是催化降解FeOCl的关键。PAA的活化过程涉及两条途径,途径I如式(49)(50),PAA与Fe(Ⅱ)反应生成CH3C(O)O·、HO·和Fe(Ⅲ),然后与PAA发生一系列的链式反应,产生CH3C(O)OO·、·CH3、·OOCH3和1O2。途径Ⅱ如式(51)(52),Fe(Ⅲ)被还原为Fe(Ⅱ),同时产生CH3C(O)OO·与1O2。

(49)

(50)

(51)

(52)
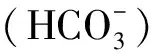
由表2可知,金属基催化剂在活化PAA时通常表现出较高的活性,能快速活化PAA产生HO·、CH3C(O)O·、CH3C(O)OO·和高价金属等活性物种降解水中的污染物。金属催化剂活化PAA原理清晰,改变催化剂种类可产生特定的活性物种,抗干扰能力较强,简便易操作,但是金属基催化剂的金属位点易中毒而丧失活化PAA的能力。此外,金属基催化剂在酸性条件下易被腐蚀,金属离子浸出后将导致二次污染。
2.3.2 非金属催化剂
非金属催化剂主要是碳催化剂,通常具有较大的比表面积、良好的电子转移性能、优异的化学和热稳定性,可避免金属浸出导致二次污染的问题。在PAA活化中常见碳催化剂主要是活性炭与碳纳米管[72-73]。与非均相金属催化剂通过表面氧化还原反应活化PAA不同的是,碳催化剂活化PAA是基于电子转移机制,碳催化剂材料表面的缺陷和富电子官能团如C—O、—OH和—OOH等可作为PAA的活化位点。
(1)活性炭活化
DAI等[74]对商用活性炭(Active Carbon,AC)进行热改性,制备了无原子掺杂和金属负载的AC600,将其用于PAA活化去除地下水中抗生素SMX,因具有丰富的结构缺陷和含氧官能团,表现出良好的氧化性能。在较低PAA剂量(0.24 mmol/L)下,可完全去除SMX,降解过程中整体毒性明显减弱。在AC600/PAA体系中,活化PAA降解污染物包括自由基和非自由基途径。自由基途径主要是AC600将PAA活化后产生HO·、CH3C(O)O·和CH3C(O)OO·等,如式(53)~(56),非自由基途径主要是1O2和电子转移。

(53)

表2 过渡金属材料/PAA体系去除水中新污染物

(54)

(55)

(56)
(2)碳纳米管活化
碳纳米管(Canbon Nanotubes,CNT)与AC不同的是,AC具有丰富的含氧官能团和较低的石墨化程度,而CNT官能团水平较低,sp2杂化碳含量高,这导致碳材料在活化PAA时产生的活性物种存在差异[75-76]。ZHANG等[77]以CNT作为催化剂活化PAA去除水体中的酚类污染物,研究了CNT表面化学性质与活性物种之间的关系。在CNT/PAA体系中主要活性物种是CNT-PAA*复合物,它直接夺取酚类污染物的电子实现高效氧化降解,体系中HO·起次要作用。在CNT/PAA体系中,CNT本体上sp2杂化碳是产生CNT-PAA*复合物的活性位点,CNT边缘的C—OH是产生HO·的活性位点。PAA分子首先吸附在CNT的sp2杂化碳上,形成亚稳态CNT-PAA*复合物,少部分CNT-PAA*复合物分解形成HO·和CH3C(O)O·,反应过程如式(57)(58),BPA在直接电子转移与HO·协同作用下被快速氧化降解。

(57)

(58)
碳材料具有复杂的结构和理化性质,明晰碳材料活化PAA的结构-活性关系,有利于通过调整碳材料结构性质主观调控PAA活化效率,加强PAA工艺氧化降解性能。KONG等[78]采用商用CNT为研究对象,利用热处理技术制备了一系列具有不同理化性质如比表面积、缺陷、石墨化、电导率以及氧含量的CNT,并研究了热处理后CNT活化PAA降解污染物的性能差异。

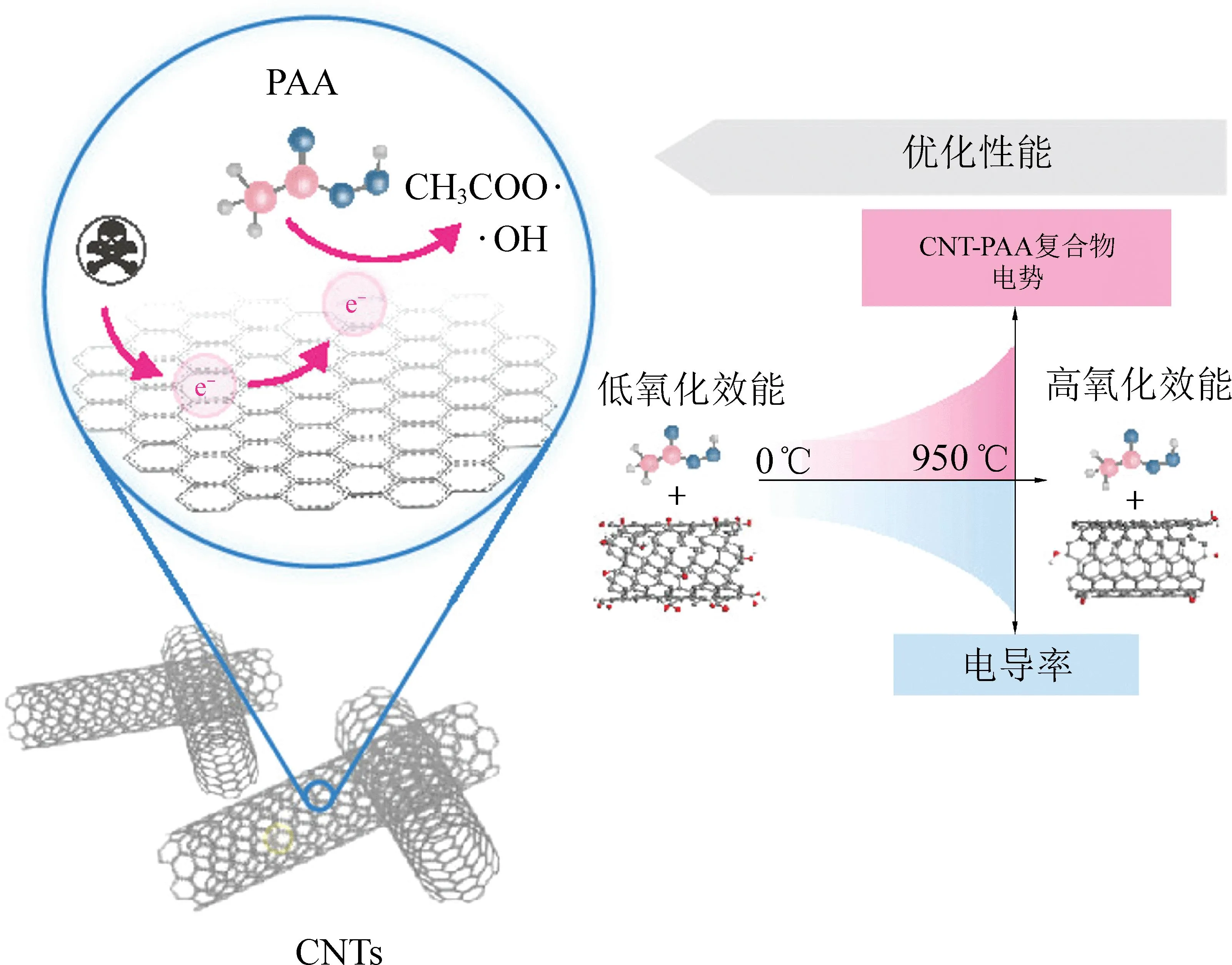
图9 CNT/PAA体系反应机制与CNT导电性 对氧化效率的影响[78]Fig. 9 The mechanism of CNT/PAA system and the influence of conductivity of CNT on the oxidation efficacy[78]
碳材料作为一种极具潜力的非金属PAA活化剂,目前的研究尚处于初始阶段。由于碳催化剂结构与理化性质复杂,相关的PAA活化机制尚不明晰。当前大多集中于对碳催化剂表面含氧官能团种类、石墨化与缺陷程度等调控,以改善PAA的活化效果。此外,有研究将碳材料与金属催化剂结合,从而获得更优异的PAA活化效率与污染物降解性能。碳催化剂通常能够以电子转移的非自由基途径降解污染物,受水质较小。碳材料制备成本较低、无金属浸出、经济环保,但该类催化剂的回收利用是扩大其应用范围的重要挑战。
3 总结与展望
本文综述了基于PAA活化降解新污染物方面的最新研究进展。基于PAA的高级氧化技术是一种高效水环境修复技术。在未来的研究中,首先仍然需要开发具有高PAA活化效率的催化材料,阐明催化剂与活化效能间的构效关系;其次,单一PAA活化技术可能对复杂废水的氧化能力有限,因此,可考虑多种PAA活化技术联用以提升PAA活化效率和污染物降解效率。目前大多数基于PAA活化的高级氧化技术主要集中在实验室规模的模拟废水,这无疑与真实废水环境存在较大差异。未来则应重点考察真实废水环境下的处理效果。此外,反应器的设计也是PAA活化技术走向规模化应用的关键。由于非均相催化剂在使用后仍需通过额外的操作步骤才能实现回收。将催化剂与膜技术结合,可简化催化剂回收过程。因此,研发面向PAA活化的催化膜反应器,制备具有高稳定性与高PAA活化效率的催化膜也是未来重要研发方向之一。
