氨分解催化剂研究进展
2024-02-20李世刚刘晓晖王艳芹
李世刚,李 冰,刘晓晖,郭 勇,王艳芹
(1.华东理工大学绿色化工与工业催化全国重点实验室,上海 200237;2.上海市质量监督检验技术研究院)
随着全球能源需求的持续增长,化石燃料的消耗量也在不断上升,这加剧了化石燃料的枯竭。同时化石燃料所产生的温室气体也对环境造成了负面影响[1]。为此,人们正在探索清洁可持续的能源,以缓解能源和环境问题。许多潜在的可再生能源(如风能与太阳能)可以实现未来社会的可持续发展[2-3]。然而,由于可再生能源的不可预测性和间歇性,需要将其产生的电力储存在载体中,以便在所需的地点使用。其中,氢因清洁无污染,被公认为是一种有前途的大型可再生能源载体。另外,由于氢与燃料电池结合使用时储存在氢分子中的电能可以有效地再生,所以引发了大量学者的关注。
目前储存氢的形式主要可以分为三大类:①以纯分子形式的气体或液体存储,不与任何材料存在物理或者化学结合;②氢分子以较弱的范德华力吸附在物质表面或者进入物质中,如利用金属有机框架(MOFs)[4]、多孔碳基材料[5]、多孔聚合材料[6]等作为吸附剂存储氢;③氢以化学键的形式存储在含氢化合物中[7]。虽然氢是一种理想的能源载体,但直接将氢以纯分子形式的气体或液体大量运输在经济上是不可行的,并且可能会引发严重的安全事故[8-9],主要是由于氢在材料中扩散的趋势会导致储存材料的弱化和脆化。其次对于将氢以物理方式存储在吸附剂中的研究目前还处于实验室规模,因为大多数应用的吸附剂的密度都很低,而且需要添加剂来提高有效的热传导性,因此储氢密度会受到影响[10]。所以使用可运输和通过化学反应在现场释放氢的含氢化合物来储氢被认为是一种实用的方法[8,11-12]。与其他储氢技术相比,含氢化合物通常是液体或者在较温和的情况下通过改变压力和温度以液体的形式存在,从而简化了它们的运输和储存以及脱氢过程中的热量和质量传递。目前常用的储氢化学氢化物,如甲醇、甲烷、氨和甲酸等,通常由天然气合成。这些化学品已经被广泛生产,并且其生产、处理和运输所需的许多必要的基础设施已经相当成熟。而在这些含氢化合物中大部分都含有碳元素,在利用的过程中不可避免地会加剧温室效应,为了减少碳排放[13-14],促使人们寻找一种更加环保无COx产生的储氢材料。
在众多的化合物中,氨引起了相当大的关注,首先,氨被认为是完美的储氢材料之一[7,15],因为利用氨制氢可以满足零碳的要求。其次,目前工业上利用Haber-Bosch法生产氨已经成为一项成熟的工艺,其生产规模已经达到上亿吨[16-18]。最后,与其他储氢材料相比,氨具有较高的氢含量(质量分数17.6%)和能量密度(3 000 W·h/kg),并且氨在室温和低压下(20 ℃,0.846 MPa)可以很容易地以液体形式储存。最重要的是其投入工业化所需的花费也是最小的。综合以上优点,氨分解制氢技术是一种极具应用价值、清洁、高效的原位制氢技术,可以有效解决传统高压储存氢的难题。
然而,现实情况中氨分解制氢很难在温和的条件下发生,其分解程度与氨接触的表面性质有关,即与催化剂有关,这就产生了开发高效氨分解催化剂的需求。传统上,氨分解制氢在600~850 ℃的高温下进行[15-16]。这种高温环境会造成严重的能源消耗,不利于工业化。正因为如此,人们才致力于开发具有应用前景的催化剂。早期的研究中,人们主要研究稀释氨气氛下的氨分解催化剂。近年来,更多的工作集中在纯氨分解的催化剂上[19-20]。
随着人们对氨脱氢反应研究的不断深入,国内外对氨分解反应的研究主要包括贵金属、非贵金属、双金属催化剂,过渡金属碳化物、氮化物,混合金属酰胺基催化剂,助剂,催化剂载体和脱氢反应器技术[21-25]。其中大量的研究成果表明,催化氨分解反应最活跃的活性金属是Ru[24]。有研究者测定了活性Al2O3负载的13种不同金属催化剂的氨分解率,发现活性由高到低依次为Ru>Ni>Rh>Co>Ir>Fe>>Pt>Cr>Pd>Cu>>Te,Se,Pb[2,24,26-31]。其中,Yin Shuangfeng等[32]在碳纳米管、活性炭(AC)、Al2O3、MgO、ZrO2和TiO2载体上负载Ru,Rh,Pt,Pd,Ni,Fe,发现碳纳米管负载Ru是最具活性的催化剂。尽管Ru比非贵金属昂贵,但在相同的空速和反应温度下,其显著优越的性能可以克服成本问题。当然除了Ru之外,Fe[33]、Ni[34]、Co[35]、CoMo[36]以及氮化物和碳化物[37-38]在氨分解方面显示出了很大的潜力。在非贵金属中,Ni基催化剂性能优于过渡金属Fe,Co,Mo。Ni基催化剂虽然在中温区(350~650 ℃)无法与贵金属Ru催化剂相比,但在高温(650~800 ℃)下可达到完全分解氨的效果,似乎可以作为颇有前景的催化剂替代贵金属催化剂[20,39-40]。由于Ni基催化剂是在高温强还原气氛下进行氨分解,不可避免地会导致活性物质烧结从而导致活性下降,所以目前关于优化催化剂活性和延长催化剂寿命的研究从未停止。基于此,本文主要围绕氨分解制氢的相关内容,对近年来相关催化剂的发展进行回顾,深入了解催化剂构效关系对氨分解制氢的影响,并为未来如何构建低温高效的催化剂提供见解与思路。
1 Ru基催化剂
Ru作为催化活性最高的金属,通常将其负载到多种材料(SiO2,Al2O3,MgO等)上,特别是负载到石墨化碳和碳纳米管上被认为是最有效的催化剂。其中活性组分的粒径和载体的电子导电性对实现高催化效率的重要性在很多研究中被提出。此外,碱金属、碱土或稀土金属离子作为促进剂对催化性能也有影响。所有这些事实使得新型催化剂的研究从表面性质的角度入手,以控制明确的活性位点的形成。就目前研究的内容来看,催化剂的设计主要从4个角度[41]去考虑:①粒径和结构控制;②双/多金属策略;③载体效应;④促进剂等(见图1)。比如,Fang Huihuang等[42]报道了在MgO极性(111)面负载原子分散的Ru显示出最高的氨分解速率,MgO的(111)面比(100)和(110)面的催化活性至少高4倍,是目前所有文献中报道最优异的催化剂,而这种高活性来源于强烈的金属与载体相互作用和高效的表面偶联反应。在此之前,将Ru负载到碳纳米管上是氨分解最活跃的催化剂之一,这种优异的催化性能是由于碳纳米管的导电性质使电子更容易转移到Ru上,并且Ru在碳纳米管上具有良好的分散性。此外,有学者报道在碳纳米管上进行氮改性将进一步提升催化活性[43-44],这是因为氮的掺杂增强了载体的碱性,从而对活性起到了促进作用。Borisov等[45]也得到相似的结论,他们研究了碳化和非碳化Al2O3纳米纤维(ANF)上氨分解活性,结果表明碳化载体(ANFC)催化剂的活性是非碳化载体催化剂活性的2~3倍,而这种催化剂活性的增加与活性组分分散程度和电子状态的变化相关。Ju Xiaohua等[30]利用沉积沉淀法制备了高活性稳定的介孔Ru/MgO催化剂,并且通过KOH进一步改善活性,其催化性能可以与Ru负载到碳纳米管上制备的催化剂相媲美,这主要是由于催化剂具有较大的比表面积与一定数量的介孔。为了减少催化剂在反应过程中引起的烧结,Kim等[46]将Ru纳米颗粒负载到垂直直立的二维结构中,有效地阻止了纳米颗粒的聚集,从而提高了催化剂的活性和寿命。
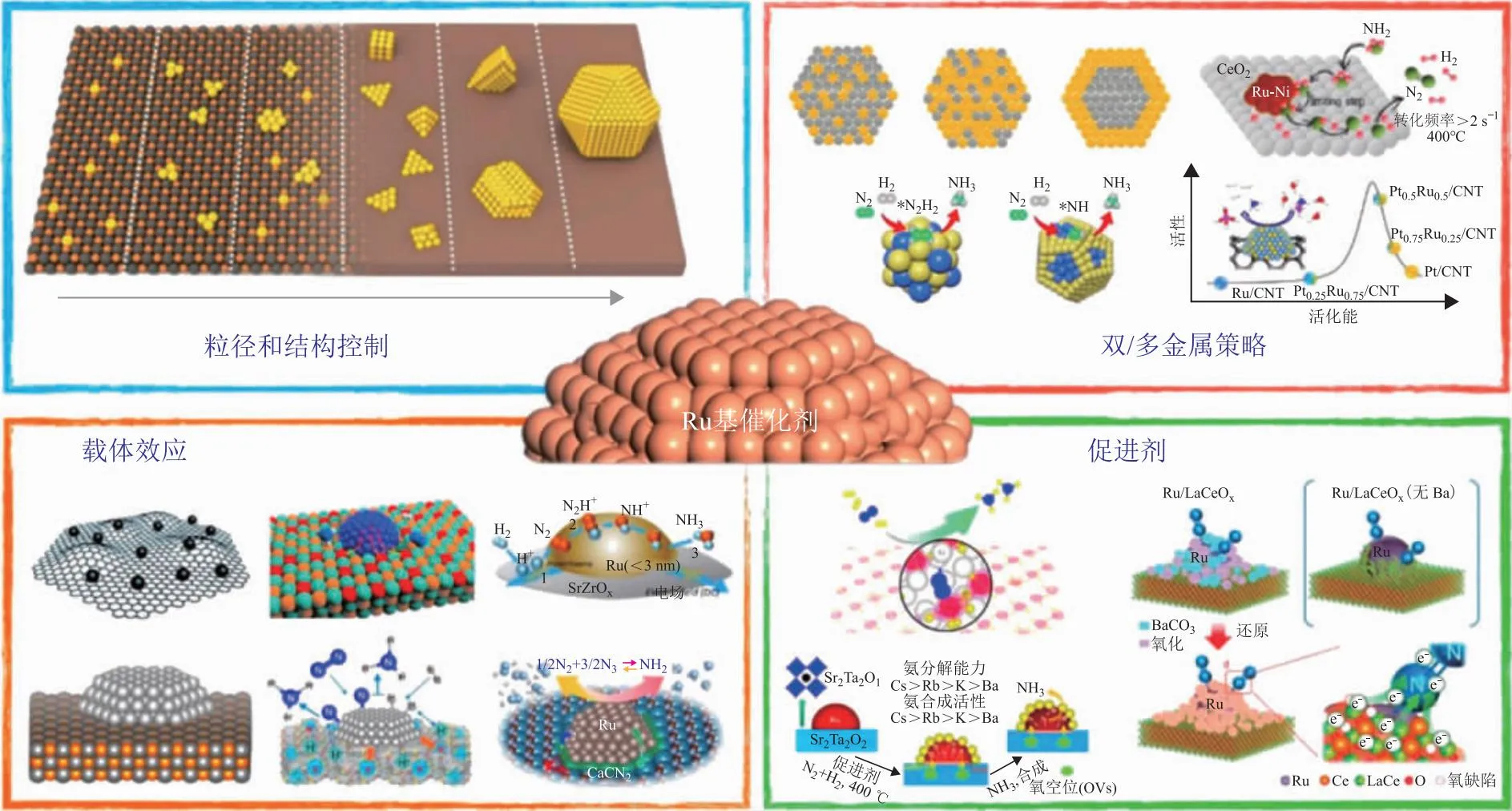
图1 Ru基催化剂的合理设计策略[41]
Lucentini等[47]将Ru负载到不同氧化物载体上,发现将Ru负载到CeO2上实现了优异的催化性能,而Ru与CeO2的相互作用是其活性优异的原因。另外,Zhang Jian等[48]通过在高比表面积MgO上负载2 nm左右的Ru粒子,证实了MgO负载Ru粒子的高活性,并且通过碱掺杂证明了Cs作为促进剂效果优于K,与早期Wang等[49]的研究结果相一致。综合相关的研究成果,Zhang Jian等[48]提出碱金属促进作用的顺序由高到低为K>Na>Li>Ba>Ca,Ce和La处于中间水平。热稳定性很好的MgAl2O4载体[50]也有类似的促进作用,比如在Cs和Ba的促进下,催化剂的活性提高了10倍,并且Cs的促进作用比Ba强。同样,Sayas等[51]利用K作为促进剂改善Ru/CaO的活性,发现可以通过K的促进作用降低Ru颗粒的尺寸来增加金属的分散,并且K和Ru之间的电子效应可以有效降低反应表观活化能。Shin等[52]通过不同的制备方法制备Ru/Ce/MgAl催化剂获得了较好的催化活性,并通过控制CeO2的浓度和煅烧温度调控表面的氧空位,首次提出CeO2作为促进剂可以有效提高N、H原子的复合/脱附。
Lorenzut等[53]报道了一种创新的合成方法,利用包埋策略将Ru纳米颗粒嵌入到La稳定的ZrO2(LSZ)载体中成功制备了Ru@LSZ催化剂,有效避免了金属的烧结以及反应过程中催化剂的失活。尽管金属负载量相对较低,但使用该方法制备的催化剂具有较高的金属分散性和良好的金属可及性,所以在400~600 ℃的温度范围内活性非常高。Fu Zhiqiang等[54]首次将一系列碱金属硅酸盐作为Ru纳米颗粒的载体,探讨了A2SiO3结构对催化活性的促进作用,发现碱金属硅酸盐的形成可以增加碱性的强度和数量,通过还原,A2SiO3结构中Ru粒子与氧空位之间会出现强电子金属-载体相互作用(EMSI),这种强相互作用的存在使Ru粒子在A2SiO3上的分散度提高,电子密度增大,极大地提高了氨分解的催化活性。表1为Ru基催化剂的氨分解活性汇总。

表1 Ru基催化剂的氨分解活性汇总
随着人们对Ru基催化剂研究的不断深入,Li Li和Zhu Mingyao等[63-64]制备了以不同的碳基作为载体负载Ru的催化剂,并且确定了载体的两个主要效应:①建立了载体的石墨化程度与催化活性之间的半定量关系,即石墨化程度最高的催化剂具有最高的转化频率(TOF),并解释这是由于导电载体材料更易传递电子所致;②提出了Ru颗粒的最佳粒径为3~4 nm。之后,Zheng Weiqing等[65]还报道了相同碳纳米管载体的分解活性与石墨化程度的相关性,发现碳纳米管外侧较大的Ru颗粒比管内小颗粒Ru更活跃,并初步将这种结果归因于碳纳米管载体在管状孔道的内外为Ru纳米颗粒提供了不同的位点,掩盖了高石墨化程度碳纳米管电子密度增强的有利影响。另外,Zheng Weiqing等[65]还观察到,平均粒径在2.2 nm左右时Ru/Al2O3催化剂的活性最高,当平均粒径低于2.2 nm时,Ru/Al2O3催化剂的反应速率明显降低,García-García等[66]也描述了类似的最佳Ru粒径范围。并且在这个粒径范围内,粒子的高活性是由于B5位(活性位点)的存在,因为他们观察到在3~5 nm的粒径范围内,B5位最丰富,并且这样的B5位点是由一层中3个Ru原子和在Ru(0001)晶面上的单原子台阶处上方层中的另外2个Ru原子组成。在此之前,人们认为B5位点是反应的关键位点,并推断为适应这些位点所需的最小尺寸约为2 nm。然而,这一说法必须在某种程度上加以修正,因为最近的研究表明,B5位点的出现不仅取决于颗粒大小,而且还取决于颗粒形状[67]。比如,对于半球形颗粒,在粒径1.8~3 nm之间观察到最大的TOF;对于扁平细长颗粒,在7 nm处观察到最大的TOF[68]。
目前的研究结果显示,载体上Ru颗粒的粒径、切面和形态对Ru基催化剂的催化性能有很大的影响。同时,Ru基催化剂的催化性能也可以由载体的特性调控。载体的作用不仅是分散和稳定Ru颗粒,还通过金属-载体的相互作用来调节Ru的电子和结构特性,这两者对Ru催化剂的性能至关重要。因此,探索合适的氧化物载体对于合理设计用于氨分解反应的高效催化剂是非常必要的。
2 Fe基催化剂
大量研究表明合成氨的高活性金属是Ru,但也有文献表明Fe可以作为合成氨的活性金属,并且Fe基催化剂是大多数合成氨工厂的主要催化剂。因此,人们对Fe基催化剂进行深入研究也就不足为奇了。
Fe元素可以形成稳定的氮化物(FexN),其中高温下的氨处理实际上是Fe的氮化。该反应大多需要500 ℃以上的温度,但对于纳米晶体表面的氮化,已有文献报道温度可低至300 ℃[69]。因此,在氨分解条件下,催化剂可能处于不同的状态,这取决于气相组成和温度。如果反应是在纯氨中进行的,人们可能会期望FexN作为活性物质存在。然而,Fe基催化剂转变为更活泼的FexN物种可能是缓慢的,存在一个较长的诱导期。Indriadi等[70]为了解决Fe基催化剂诱导期长的问题,他们尝试在Fe/SiO2上添加少量的Pt从而加速FexN的形成,结果发现加入少量的Pt使得FexN的生成速率增加了数倍,并且Pt可以通过反向溢出作用帮助氢从活性表面解吸,从而促使更多的活性位点暴露出来发生氮化,促使整个反应循环进行。Ji Jian等[71]利用催化化学气相沉积(CCVD)法制备了一系列Fe/CNFs(碳纳米纤维)催化剂,通过改变H2/CO原料气比例得到形状和位置不同的Fe纳米粒子,发现长多面体形状的纳米Fe颗粒在CNFs尖端或中部具有比短多面体形状和不规则形状的纳米Fe颗粒更强的氨分解活性,而活性优异的原因可能是活泼的活性表面更容易吸附氨。Li Lei等[72]采用水热和热处理相结合的方法将Fe纳米颗粒嵌入载体中,制备了具有独特纳米结构的介孔Fe@GC复合材料,由于金属和石墨化碳之间的相互作用,使得催化剂具有良好的活性和稳定性。表2为Fe基催化剂的氨分解活性汇总。

表2 Fe基催化剂的氨分解活性汇总
人们对制氢条件下Fe基催化剂的研究报道相对较少,其中一些研究主要是为了了解氨合成催化剂,而不是开发一种提供清洁氢气的催化剂。Kowalczyk等[76]利用氨合成催化剂去分解氨。在常压下,当氨体积分数超过20%时,反应速率明显增加,这是由于连续生成了具有较高催化活性的FexN相。在常压下也研究了Fe/CNT样品分解纯氨的性能,但这里使用的Fe催化剂是用于合成它们的工业碳纳米管中的残余催化剂,其中Fe未被活化,约占样品的2.3%。这些催化剂的活性较低,在较高的温度(700 ℃)下反应速率也较低,这与预期的结果一致。值得一提的是,FexN在反应中虽然占主导地位,但高温会导致碳纳米管与Fe颗粒发生强相互作用而失活。通过在云母上负载Fe/CNT样品可以防止这种情况的发生,因为该过程中会形成更小的、分离良好的Fe颗粒,在500 ℃下具有可观的活性。
综上所述,Fe基催化剂的活性按活性金属含量与Ru基催化剂相比要低很多,但如果按催化剂质量归一化,这种活性差异将大大减小。然而,Fe基催化剂想要完全取代昂贵的Ru基催化剂还存在很大困难。因此,在氨分解制氢领域,用Fe基催化剂来完全代替Ru催化剂还有待进一步研究。
3 Ni基催化剂
Ni是金属基催化剂中最常见的元素之一,由于具有相对较高的活性和低廉的价格,更有利于商业应用和推广,所以也成为近年来研究最为广泛的非贵金属催化剂。
Zhou Chen等[77]开发了一种CeO2和BN(氮化硼)混合负载Ni的催化剂(Ni/CeO2-BN)用于氨分解反应,通过在Ni/CeO2中添加BN,促进Ni纳米粒子的空间分布,从而减少了Ni在氧化物载体上的聚集。更重要的是,他们通过引入BN富集了氧空位,提高了Ce3+浓度,使电子从载体向Ni转移,使得Ni周围富集电子进而促进氨的活化,同时促进了表面氮原子的结合进行氮气分子的脱附,最终促进了氨的分解。Deng Qingfang等[78]以表面活性剂辅助法、共沉淀法和溶胶凝胶法合成了3种Ce0.8Zr0.2O2固溶体,然后采用浸渍法制备了Ni基催化剂。发现在Ni含量相同的条件下,用表面活性剂辅助合成的Ce0.8Zr0.2O2载体的促进效果优于其他方法制备的载体。同时Ni物种与Ce0.8Zr0.2O2载体之间的相互作用对催化剂的化学性质有很大的影响,并且Ce在催化剂中的促进作用表现在固溶体中出现大量的空位,从而获得了优异的催化活性。Im等[79]以碱土金属铝酸盐为载体合成了Ni/AM-Al-O催化剂(AM=Mg,Ca,Sr,Ba),发现强碱性会减弱催化剂对氢气的吸附,但对氮气的吸附略有增强,并且从动力学分析可知,氢气反应级数随催化剂碱性强度的增加而减小,表明催化剂的强碱性能缓解氢气对氨分解的抑制作用。Cao Jianliang等[80]采用酸消化、碱再沉淀法对赤泥(MRM)进行改性,得到了介孔改性赤泥,并将其作为载体通过浸渍法制备Ni/MRM催化剂,他们发现Ni物种与纳米结构MRM载体之间的协同效应、Ni物种的高度分散以及催化剂的高比表面积是催化剂具有较高催化活性和较快产氢速率的主要原因。Li Lei等[81]采用连续沉淀法制备了多孔硅包覆凹凸棒黏土(ATP)负载Ni催化剂,结果表明,ATP负载的Ni催化剂具有合适的比表面积、孔体积以及纳米核壳结构,可以有效包裹活性位点,从而使催化剂具有抗高温烧结性能。Muroyama等[29]进行了不同方法制备Ni/La2O3和Ni负载量对氨分解性能的研究,40%(w)Ni/La2O3催化剂在550 ℃时具有78.9%的氨转化率,这归因于在氢气还原过程中活性物质LaNiO3的形成,但是La2O3载体的比表面积(4.7 m2/g)有待进一步改善。
适宜碱性的MgO负载Ni后形成相似晶型结构的催化剂,已被广泛用于多种催化反应中,通过改变Ni和MgO之间相互交联作用使其形成抗还原的碱性固溶体NixMg(1-x)O作为高活性组分。Su Qin等[20]报道了高活性高稳定性的氨分解Nix(MgyAlzOn)催化剂,氧化物与Ni-Mg活性位点之间形成了协同效应。Podila等[82]考察了不同X-Mg(X为Al,Ce,La)混合氧化物载体负载Co的氨分解性能,发现在混合氧化物中La改性催化剂的活性最高,这归因于Mg和La的交联增强了碱度,而且MgO的含量增加使催化剂的比表面积、高活性表面积和高比表面晶格氧(O2-)也随之增加。由此可见,MgO的碱性对催化氨分解活性起着重要的作用。
目前改善Ni基催化剂催化氨分解活性的两种途径是:①通过添加氧化物来设计和改变载体的酸碱性;②减小活性组分Ni颗粒的粒径和分散度。改变载体的酸碱性一般是利用碱性氧化物(MxOy,其中M为Ce,Nd,Y,Zr,Mg)来调控。比如,目前有许多研究通过表面活性剂法制备多种混合氧化物XLa(X为Ce,Nd,Y,Zr,Mg)负载Ni基催化剂,研究其氨分解性能;另外还有制备不同摩尔比例的Ni/XMgLa催化剂研究其氨分解性能。同时结合氮气吸附-脱附、透射电子显微镜、X射线光电子能谱、X射线衍射、氢气程序升温还原和二氧化碳程序升温脱附等表征技术研究催化剂结构与活性之间的关系。
表3为Ni基催化剂的氨分解活性汇总。
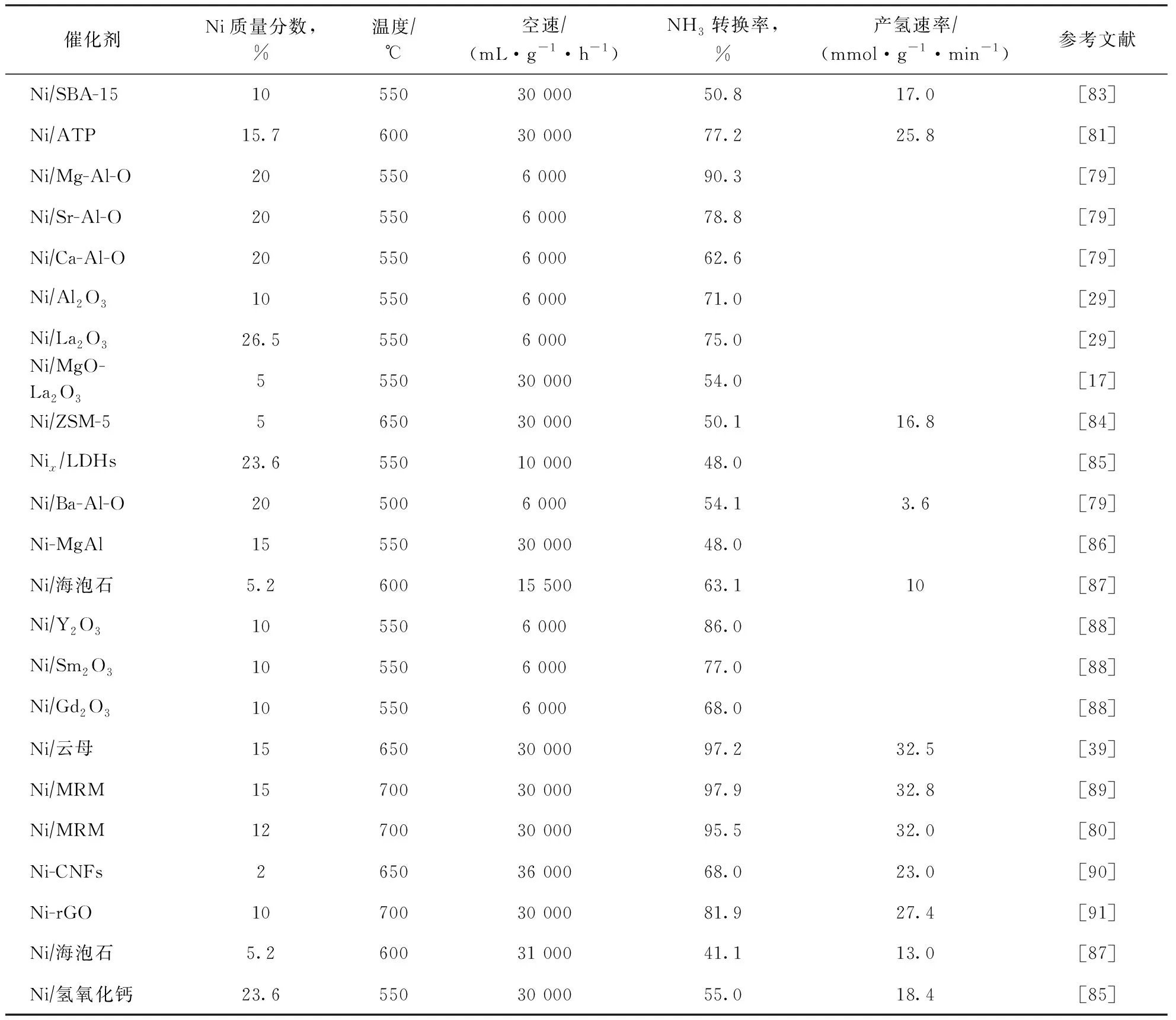
表3 Ni基催化剂的氨分解活性汇总
4 双金属催化剂
双金属催化剂是近年来发展起来的一种新型的多相催化材料,其目的是获得比单金属催化剂更好的活性、选择性和稳定性,这在很大程度上归因于双金属催化剂中金属-金属结合的协同效应。图2为金属基催化剂分解氨的表观活化能。

图2 金属基催化剂分解氨的表观活化能[92]
双金属催化剂的设计和开发主要依赖于氮原子与金属表面相互作用的结合能,然而,影响活性的因素如活性中心的性质等尚不明确,需要进一步去探讨[29]。此外,密度泛函理论(DFT)结合扫描隧道显微镜(STM)结果表明,催化剂表面缺陷、孤立金属原子和表面微观结构对氨分解反应有重要影响。双金属结构按金属-金属的分布可以分为不同的类别。两种金属的分布影响催化剂的表面性质,进而影响催化氨分解的性能。在双金属结构的各种类别中,以下着重对单层双金属和双金属合金两个分类进行简要讨论。
吸附金属在基质金属顶层的单层分布表现为单层双金属构型,合金和/或核壳双金属纳米颗粒的偏析表面模型表示可以使用单层双金属结构体系来实现。单层结构可以具有如图3所示的表面构型(在主体金属表面上存在吸附金属的情况下)或亚表面构型(主体金属下面是吸附金属)。通过DFT理论和试验分析,证明了这两种构型具有明显不同的特征,它们是单独的吸附金属和主体金属。基于构型的单层双金属表面的结合能不受母体金属结合能的影响。因此,用一种简单的方法合理地设计这些单层双金属催化剂是一项具有挑战性的任务。

图3 双金属单层表面和亚表面构型的示意[93]
均匀分布在表面和核心内部的原子构成合金层,这两种金属都以纯相组成存在于本体内和表面上。图4是双金属合金结构的图形表示,与单层双金属结构不同,合金表面特性是基体或母金属表面性质线性组合的函数。利用周期插值法,将低结合能金属与氮的高结合能混合,得到双金属合金的中等结合能。
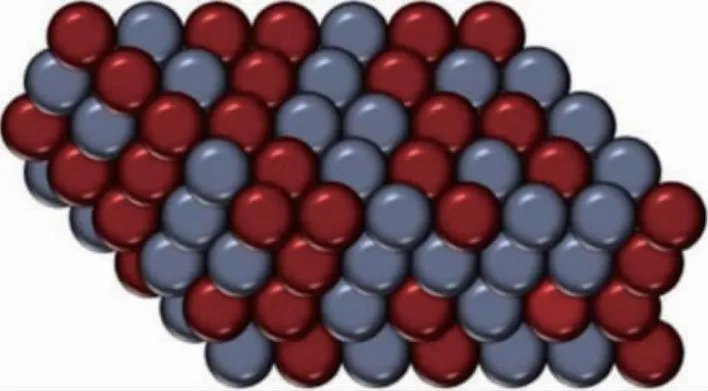
图4 一种双金属合金结构的示意[93]
近年来,研究开发高效、经济可行的氨分解双金属催化剂已成为国内外研究的热点。其中,Lucentini等[47]研究了以CeO2为载体的Ru-Ni双金属催化剂在氨分解中的作用。采用分浸法按先Ru后Ni的方式和采用共浸渍法制备了Ni-Ru两种催化剂,并与单金属催化剂进行比较。结果表明,合适的金属与载体相互作用起着重要作用,单金属催化剂活性优于双金属催化剂。在350~600 ℃温度范围内,两种双金属催化剂的氨转化率无明显差异,表明Ni-Ru双金属催化剂不能产生本质的协同作用。此外,不同的金属掺杂顺序和/或合成路线对活性的影响也不明显。
另外,不同催化剂的催化活性随温度和时间的变化而变化。与纳米粒子相比,Ru-Co纳米团簇具有优异的活性和TOF,其形成的不饱和低配位活性中心促进了氨的吸附和分解[94]。之后,有学者研究了碳纳米管负载的Ru-Fe双金属催化剂的氨分解性能[82],结果表明双金属催化剂的优异性能归因于其对活性金属表面氮物种的优化吸附和解吸。此外,较低的氮物种覆盖率和随后较快的吸附的氮原子的解吸有利于提高催化剂的活性。
近年来,双金属催化体系在氨分解制氢方面取得了重大进展,文献报道了几种贵金属-贵金属、贵金属-过渡金属、过渡金属-过渡金属的组合体系。可以看出,贵金属双金属催化剂在较低的反应温度下即表现出显著的活性,而过渡金属催化剂则需要较高的反应温度才能达到同样的活性水平。然而,这种趋势在一些过渡金属催化剂上并不相同,如Al2O3负载的Co-Fe催化剂即使在350 ℃下也达到了平衡转化率。因此,在未来的研究中需要着重阐明金属-金属界面的作用,以及金属-载体相互作用对氨分解反应催化性能的影响。综合目前对各种金属类型的研究结果:双金属合金或基体金属的改进与第二金属的加入对这些催化剂在氨分解反应中的性能有显著影响;氧化物载体材料的选择也对催化剂活性起着举足轻重的作用,这也是除了寻找合适的催化剂之外在未来的研究中所要探索的。
5 氨分解反应机理
众所周知,氨分解是通过氨逐步脱氢进行的,然后由脱附的两个氢原子或两个氮原子分别复合生成氢气和氮气。在氨分解过程中,人们普遍认为氮在金属表面的结合能是氨分解的一个很好的描述符[95-96]。而氨分解必须要满足两个基本条件,第一是氨分子中的氮原子与表面的结合能必须足够强,才能使*NHx物种脱氢,其次也要足够弱,才能使氮原子间重新结合,从表面解吸,以完成整个催化循环过程。综合这两个基本条件,确定氮结合能和氨分解活性之间的火山型关系。在过去的几十年里,人们努力探索高催化活性的新型氨分解催化剂,并针对催化剂提出了许多反应机理。其中大部分是基于氨分解生成纯氢的条件提出的。然而,不管催化材料是什么,目前主要认为有两种可能的速率控制步骤:N—H键的裂解形成吸附的*NH2和*H,或者吸附的氮原子的结合导致氮气分子的解吸。其中对于Ru,有学者提出了一个包括上述两个速控步骤的模型,氨的正反应级数约为0.75,而氢压的反应级数为强负[97]。最近的一项产品时间分析(TAP)研究显示,纯Ru和Na改性的Ru催化剂存在很大差异。但在这两个催化体系中,氮原子的重组均被认为是速控步骤[98]。在对更高压力下所用NiPt/Al2O3催化剂的研究中,认为氢气没有抑制作用,反应可以用氨气的简单一阶速率规律来描述,这表明氮的重组解吸是速控步骤。另外,在文献[98]中总结的大多数研究中,解吸被确定为速控步骤。然而,这似乎在一定程度上取决于所研究的催化材料和反应的确切条件。之后,一项研究证实了Ru基催化剂对于氨分解的动力学相关步骤[99]。最近,针对特定的催化剂,即Ni[100]和Ru/γ-Al2O3[101],开发了非常详细的动力学模型。这些模型包含了所有相关的步骤,还强调了吸附物之间横向相互作用的重要性。新的见解可能来自于对这一反应的计算研究,它能够很好地再现测量的反应速率。然而,DFT理论研究表明,对于Fe55团簇来说,第一个氢的吸附是速控步骤[102]。由此可见,对反应的机理途径问题没有得到结论性的回答。对于单一速控步骤的问题可能没有简单和普遍的答案,每个体系都需要进行详细的分析。
6 结论与展望
氨气作为能源系统的无碳能源载体,拥有高能量密度、成熟的合成工艺以及氢含量较高等优点,因此在未来人类社会的可持续发展中将发挥重要作用。对于氨分解反应,人们普遍认为活性相、载体和促进剂在反应中都起着关键作用。首先,对于活性金属而言,通过控制形状和尺寸可以最大限度地增加活性位点的数量。而如何以高效便捷的方法制备精确控制活性相的大小、形状、分散性和结构合理的催化剂仍然是氨分解领域的一个关键问题。其次,作为催化剂的载体需要比表面积较大,热稳定性优异。此外,催化剂表面酸碱性,尤其是碱性也是值得研究的。通常,催化剂的碱性是通过添加促进剂来调节的,这可以增加催化剂的给电子性,因为促进剂可以与载体产生间接的相互作用来诱导更强的碱度。而碱度一方面可能与活性金属的分散程度有关,另一方面对决速步骤氨脱氢和表面氮原子的重组解吸也有促进作用。从理论上讲,金属和氮的结合能与氨转化率之间的火山型分布曲线为催化剂的设计提供了有用的指导。所以对于氨在未来是否能够成功转化到氢能的工业化应用中,研究的关键点应该集中在以下几个方面:
(1)利用简单有效的方式合成新型催化剂。目前的研究表明,贵金属Ru在高温下可能会出现团聚或者挥发从而失活,非贵金属Ni在低温下活性较差而高温下又容易发生烧结。解决这些问题主要是通过活性组分的形貌、粒径和电子结构去调控催化剂的性能。在未来需要进一步结合理论计算,通过简单的策略设计新型材料,使其成为高效、可循环利用和成本较低的催化剂材料。
(2)进一步探索反应机理。对于氨分解的反应途径,不同的活性组分、载体以及促进剂对反应过程中出现的各种中间体(*NH3,*NH2,*NH,*N,*H)的吸附以及解吸都会产生不同程度的影响。所以在未来的研究中应将理论计算与试验结果进一步结合,深入揭示氨分解的反应机理,这将为新型催化剂的设计提供可预测性的指导。
