植物内生真菌中萜类化合物研究进展
2024-02-05刘明秀柴南南濮兴娜汪伟光李艳平
郭 晶,刘明秀,柴南南,濮兴娜,汪伟光,李艳平
(1.云南中医药大学 中药学院 云南省南药可持续利用重点实验室,云南 昆明 650500;2.云南民族大学 民族药资源化学国家民族事务委员会-教育部重点实验室,云南 昆明 650500)
植物内生真菌是寄生于健康植物体内的真菌,于其各组织、器官内或细胞间隙内完成它的生活周期[1].在与宿主植物进化过程中,它们之间建立互利共生的关系,特别是内生真菌会代谢出活性产物,增强了宿主植物的生长和竞争能力[2-4].目前研究表明,人们对植物内生真菌次生代谢产物总结得出以下几类化学成分:萜类,甾体类,黄酮类,肽类,脂肪族类,生物碱类,酯类和苯丙素类等,且大多具有广泛的药理活性,如抗炎、抗肿瘤、抗菌等[5].萜类化合物结构丰富,多具有较好的生物活性,近年来,从植物来源的内生真菌中获得的萜类化合物越来越多,本文将对该类成分进行综述,为植物内生真菌萜类化合物进一步研究提供借鉴.
1 化学成分
萜类化合物是由甲戊二羟酸衍生、且分子骨架以异戊二烯单元(C5单元)为基本结构单元的化合物及其衍生物.一般分为单萜、倍半萜、二萜、三萜、四萜等.下面将从单萜、倍半萜、二萜、二倍半萜、三萜等5个方面来介绍来源于植物内生真菌中的萜类成分.
1.1 单萜类化合物
从角果木内生青霉属内生真菌J54[6-7]中分离到单萜化合物citroside A (1),抗菌结果表明对大肠杆菌的MIC值是 25 μg/mL.Xu等[8]从内生真菌Pestalotiopsisfoedan分离得到1个新的单萜,命名为 (3R,4R,6R,7S)-7-hydroxyl-3,7-dimethyl-oxabicyclo [3.3.1] nonan-2-one (2).Liu等[9]从内生真菌Periconiasp.F-31分离出4个单萜,分别为 2-carene-5,8-diol-2-carene-8,10diol、 2-carene-8-acetamide、 8-hydroxy-1,7-expoxy-2-menthene (3~6).Qin等[10]从内生真菌UmbelopsisdimorphaSWUKD3.1410的发酵液中分离得到monoterpene (7).罗萍等[11]从旱生卷柏Selaginellastauntoniana内生真菌赭曲霉AspegillusochraceusSX-C7分离得到1个单萜6-hydroxy-p-menth-4(5)-en-3-one (8).见表1、图1所示.

表1 植物内生真菌中单萜类成分
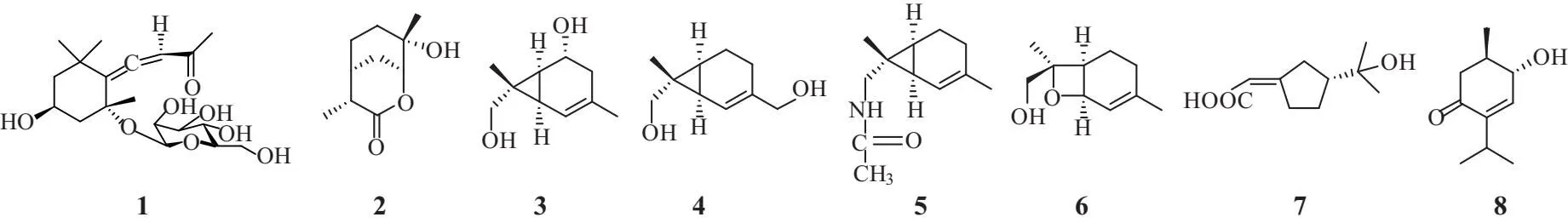
图1 植物内生真菌中单萜类成分
1.2 倍半萜类化合物
1.2.1 单环倍半萜
Zhang等[12-13]从红树林植物内生真菌Trichodermasp.Xy24中分离得到2个单环倍半烯二醇 cyclonerodiol B (9)、cyclonerodiol (10).贾林川等[14]从太子参中鉴定出一株内生真菌Penicilliumoxalicum,在其液体发酵后的次级代谢物种分离鉴定出 (7S,11S)-(+)-12-acetoxysydonic acid (11)、(S)-(+)-11-dehydrosydonic acid (12)、 sydonic acid (13)和1-hydroxy-boivinianin A (14)共4个倍半萜类化合物.余紫荆等[15]从植物杜英的叶片中分离得到一株内生真菌,经分子生物学方法鉴定为Aspergillusversi-color,在实验室中以大米麸皮培养基固体培养,经乙酸乙酯萃取、分离得到8个化合物,鉴定为(-)-hydroxysydonic acid (15)、12-acetoxysydonic acid (16)、10-hydroxysydowic acid (17)、sydowic acid (18)、sydonicavid (19)、(S)-(+)-11-dehydrosydonic acid (20)、Sydonollb (21)、(R)-hydroxyboivinianic acid (22).从Taxusbrevifolia[16-17]的内生真菌中得到倍半萜pestalotiopsin A~D(23~26)、7,14-diacetate (27)、pestalotiopsin E (28).在钩藤健康组织中的内生真菌ColletotrichumgloeosporioidesGT-7分离得到化合物colletotrichine B (29)[18].
1.2.2 双环倍半萜
在角果木 (Ceriopstagal)叶子中的内生真菌Penicilliumsp.J-54,发酵后分离鉴定出化合物penicieudesmol B (30)[19-20].Liu等[19,21]从黄草乌中鉴定出内生真菌Phomasp.YE 3135,从其发酵液中分离得到 phomanolide (31).化合物 annulohpoxylotol A (32)是Li等[22]在茭白 (Zizaniacaduciflora)叶子内生真菌Annulohypoxylontruncatum的发酵物中分离得到.Shi等[19,23]从青蒿的新鲜内部组织中分离得到内生真菌TrichodermavirensQA-8,大米固体发酵培养,在乙酸乙酯提取液中分离得到trichocadinins B~G (33~38).从内生真菌Eutypellasp.BBC 13199[24]分离得到ent-4-(15)-eudesmen-11-ol-1-one (39)、1-ent-4(15)-eudesmen-1α,11-diol (40).倍半萜irpexlacte A (41)是Duan等[19,25]在中华蚊母树(Distyliumchinense)鉴定出内生真菌IrpexlacteusDR10-1,在其发酵液乙酸乙酯萃取液中分离得到.Zhang等[12-13]从内生真菌Trichodermasp.Xy24中分离得到4个倍半萜,分别为trichoacorenols B~C,1α-isopropyl-4α,8-dimethylspiro[4.5]dec-8-ene-2β,7α-diol,1α-isopropyl-4α,8-dimethylspiro[4.5]dec-8-ene-3β,7α-diol (42~45).Wang等[26]对烟草内生菌的大米发酵产物进行分离,得到15个倍半萜类化合物,分别为rhizoperemophilane A~J (46~55)、guignarderemophilane D (56)、1α-hydroxyhydrosofukinon (57)[27]、2β-hydroxy-1,7(11),9-eremorphilatrien-8-one(58)[28]、guignarderemophilane B (59)、PR-toxin dimethyl acetal (60)[29].Chen等[30]对内生菌Phomopsissp.SYSU-QYP-23的马铃薯液体培养基分离得到13个倍半萜及其衍生物,分别为AA03390、eremofortin G、eremofortin F、eremofortin H~J、lithocarin A、petasol、isopetasan、Altiloxin C~E、Phomomane (61~73).Luo等[31]从诸葛菜Orychophrogmusviolaceus(L.)O.E.Schulz的植物内生真菌IrpexolacteusOV38培养基发酵液产物中分离鉴定8个倍半萜类化合物,分别为irpexolaceus A、tremulenolide D、irpexolaceus B、irpexolactin I~J、irpexolaceus D~F (74~81).
1.2.3 多环倍半萜
李薇[32]从马铃薯内生真菌Bipolariseleusines中分离鉴定出一系列多环倍半萜,例如Bipolenin G~N (82~89),Bipolenin D (90),Helminthosporol (91)、Drechslerine B (92)、Helminthosporic acid (93)、Drechslerine A (94)、9-Hydroxyhelminthosporol (95).
倍半萜类化合物见表2、图2所示.

表2 植物内生真菌中倍半萜类成分
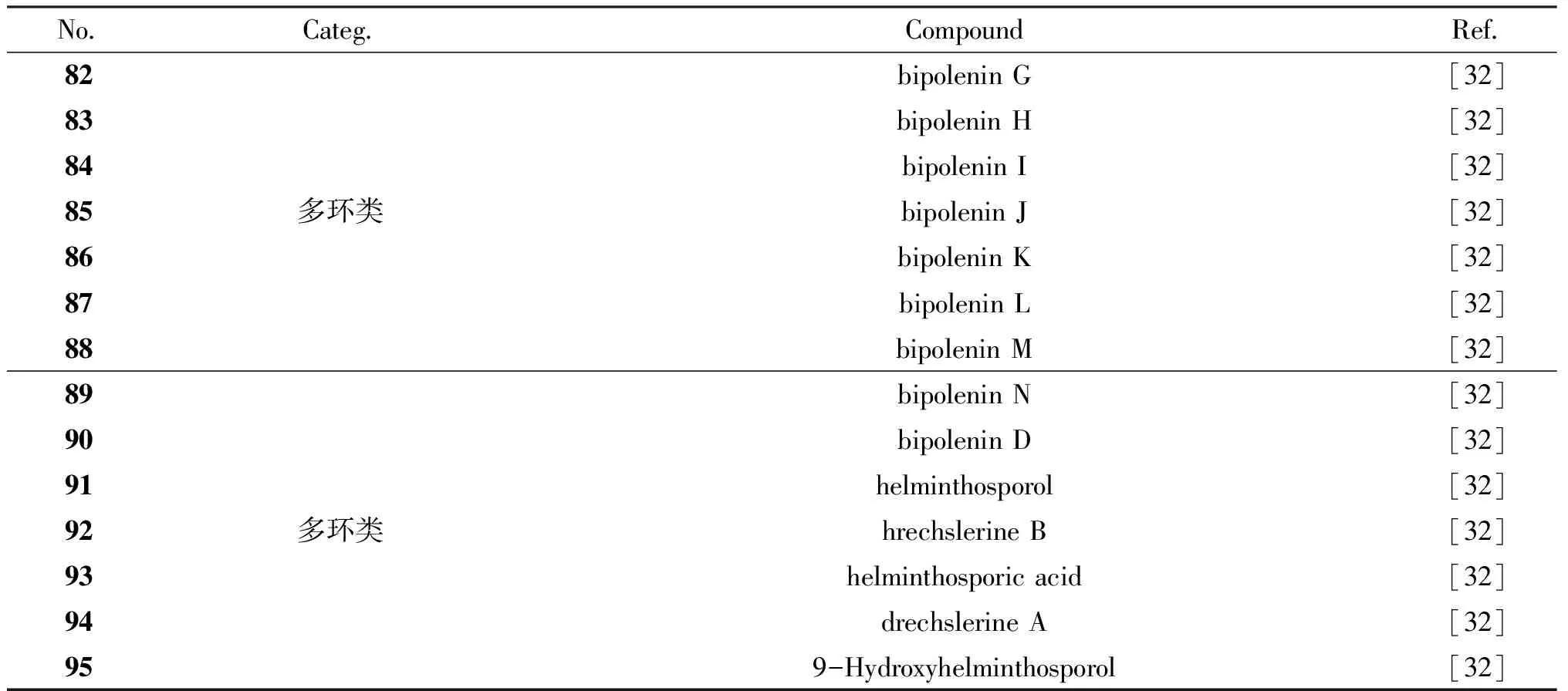
续表2

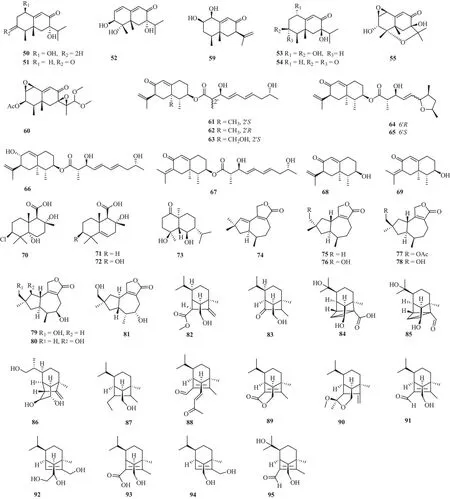
图2 植物内生真菌中倍半萜类成分
1.3 二萜类化合物
1.3.1 紫杉烷型
紫杉醇 (96)是Stierle等[3,33]在短叶红豆杉中一株安德紫杉菌Taxomycesandreanae中发现,具有较强的抗肿瘤活性.
1.3.2 半日花烷型
半日花烷型二萜类化合物在内生真菌中结构易发生变化,内酯、环氧、螺环、呋喃环等结构容易形成[3,34].如在雷公藤 (TripterygiumwilfordiiHook f.)中鉴定一株内生真菌Fusariumsubglutinans,分离得到化合物subglutinol A~B (97~98)[3],具有免疫抑制作用.从美登木 (Maytenushookeri)叶片组织分离鉴定出内生真菌Botryosphaeriasp.,固体发酵产物中分离得到12个二萜化合物[3,35],分别为botryosphaerins A~E (99~103), 13,14,15,16-tetranorlabd-7-ene-19,6β,12,17-diolide (104)、acrostalidic acid (105)、acrostalic acid (106)、agathic acid (107)、isocupressic acid (108)、LL-Z1271β(109)和 CJ-14445 (110).Yan 等[3,36]从蛇足石杉 (Huperziaserrata)鉴定出内生真菌Botryosphaeriasp.P483,在其发酵物中得到2个新化合物,命名为botryosphaerins G~H (111~112)以及7个已知的化合物13,14,15,16-tetranorlabden-19,6β,12,17-diolide (113)、Botryosphaerin A (114)、3α,10β-dimethyl-1,2,3,3α,5α,7,10β,10coctahydro-5,8-dioxa-8-acephenanthrylene-4,9-dione (115)、acrostalidicacid (116)、bortyosphaerin B (117)、LL-Z1271β(118)、acrostalic acid (119).
1.3.3 Harzianone型
Zhang等[37]从石榴木(Xylocarpusgranatum)内生真菌Trichodermasp.Xy24 发酵液的乙酸乙酯提取物中分离得到2个新的化合物,命名为 (9R,10R)-dihydroharzianone (120)、harzianelactone (121).
1.3.4 异海松烷型
异海松烷型二萜在的植物内生真菌代谢产物中普遍存在[3,38],Shiono 等[3,39]从欧洲山毛榉(Sylvaticalinnaeus)树干鉴定出内生真菌Paraconiothyriumsp.MY-42,在固体培养物中分离得到 6个化合物,即19-(α-D-glucopyranosyloxy)isopimara-7,15-dien-3β-ol (122)、19-(2-acetamido-2-deoxy-α-D-glucopyranosyloxy)isopimara-7,15-dien-3β-ol (123)、19-(α-D-glucopyranosyloxy)isopimara-7,15-dien3-one (124)、19-(2-acetamido-2-deoxy-α-D-Glucopyranosyloxy)isopimara-7,15-dien-3-one (125)、19-(α-D-gLucopyranosyloxy)-3β-hydroxyisopimara-8,15-dien-7-one (126)、19-(2-acetamido-2-deoxy-α-D-glucopyranosyloxy)-3β-hydroxyisopimara-8,15-dien-7-one (127).Wu等[3,40]在印楝中鉴定得到内生真菌Xylariasp.YM 311647,在其培养液中分离得到3个化合物,即14α,16-epo,xy-18-norisopimar-7-en-4α-ol (128)、16-O-sulfo-18-norisoimar-19-7-en-4α,16-diol (129)、9-deoxy-hymatoxin A (130).Yan 等[41]在银杏叶中分离得到内生真菌Aspergillussp.YXf 3,菌株发酵物中分离得到化合物aspergiloids E (131).Ye等[42]从白芨(BletillaStriata)根茎中分离得到一株内生真菌Ilyonectriarobusta,并对其进行液体发酵培养,分离鉴定5个新的异海松烷型二萜,为robustaditerpene A~E (132~136).
1.3.5 Guanacastane 型
Yu 等[3,43]在何首乌 (Fallopiajaponica)叶片内生真菌Cercosporasp.的发酵液中分离得到 1个化合物 cercosporene F (137),对人肿瘤细胞系 Hela有明显的细胞毒作用,IC50为 19.3 μmol/L.Chen 等[3,44]在巴戟天(Morindaofficinalis)内生真菌TrichodermakoningiopsisA729 中分离得到 2个化合物 koninginol A~B (138~139),具有Guanacastane 型骨架的二萜生物碱.
1.3.6 壳梭孢菌素型
Kim 等[3,45]从东北红豆杉(Taxuscuspidata)的小枝条分离出内生真菌Periconiasp.,菌株发酵物中分离鉴定2个新化合物,命名为 periconicins A~B (140~141).
1.3.7 吲哚二萜型
吲哚二萜型化合物是由香叶基香叶二磷酸 (GGPP)和吲哚-3-甘油磷酸酯转化而成[46-47].Gatenby 等[3,48]在内生真菌Neotyphodiumlolii发酵物中分离得到1个新化合物 14α-hydroxyterpendole C (142)为吲哚二萜型,和2个已知化合物 paspaline (143)、13-desoxypaxilline (144).从红树林植物海鞘根 (Rhizophorastylosa)新鲜组织分离出的内生真菌M.irregularisQEN189[3],发酵产物中鉴定出 6个新的吲哚二萜类化合物,命名为 rhizovarins A~F (145~150)和5个已知化合物[3,49],即 secopentrem D (151)、PC-M4 (152)、penitrem A~C (153~155).Zhao等[3,50]在三七根分离到内生真菌Drechmeriasp.,从Drechmeriasp.发酵液中分离得到 7个新化合物,命名为 drechmerins A~G (156~162)和4个已知化合物,即 drechmerins G (163)、terpendoles A (164)、terpendoles C (165)、terpendoles I (166)、dehydroxypaxillie (167).Zhang等[19,51]在木果楝 (XylocarpusgranatumKoenig)中鉴定出内生真菌Eupenicilliumsp.HJ002,菌株发酵产物中分离得到化合物 penicilindole A~B (168~169). Elsbaey 等[19,52]从白骨壤果实中分离得到内生真菌Aspergillusversicolor,菌株发酵液乙酸乙酯提取液中分离得到 anthcolorin H (170),对人肿瘤细胞系 Hela 有微弱的细胞毒作用.
1.3.8 银杏内酯型
Cui等[3,53]从银杏根皮内生真菌Fusariumoxysporum液体发酵代谢物中获得银杏内酯 B (171). 二萜类化合物见表3、图3所示.

表3 植物内生真菌中二萜类成分

续表3
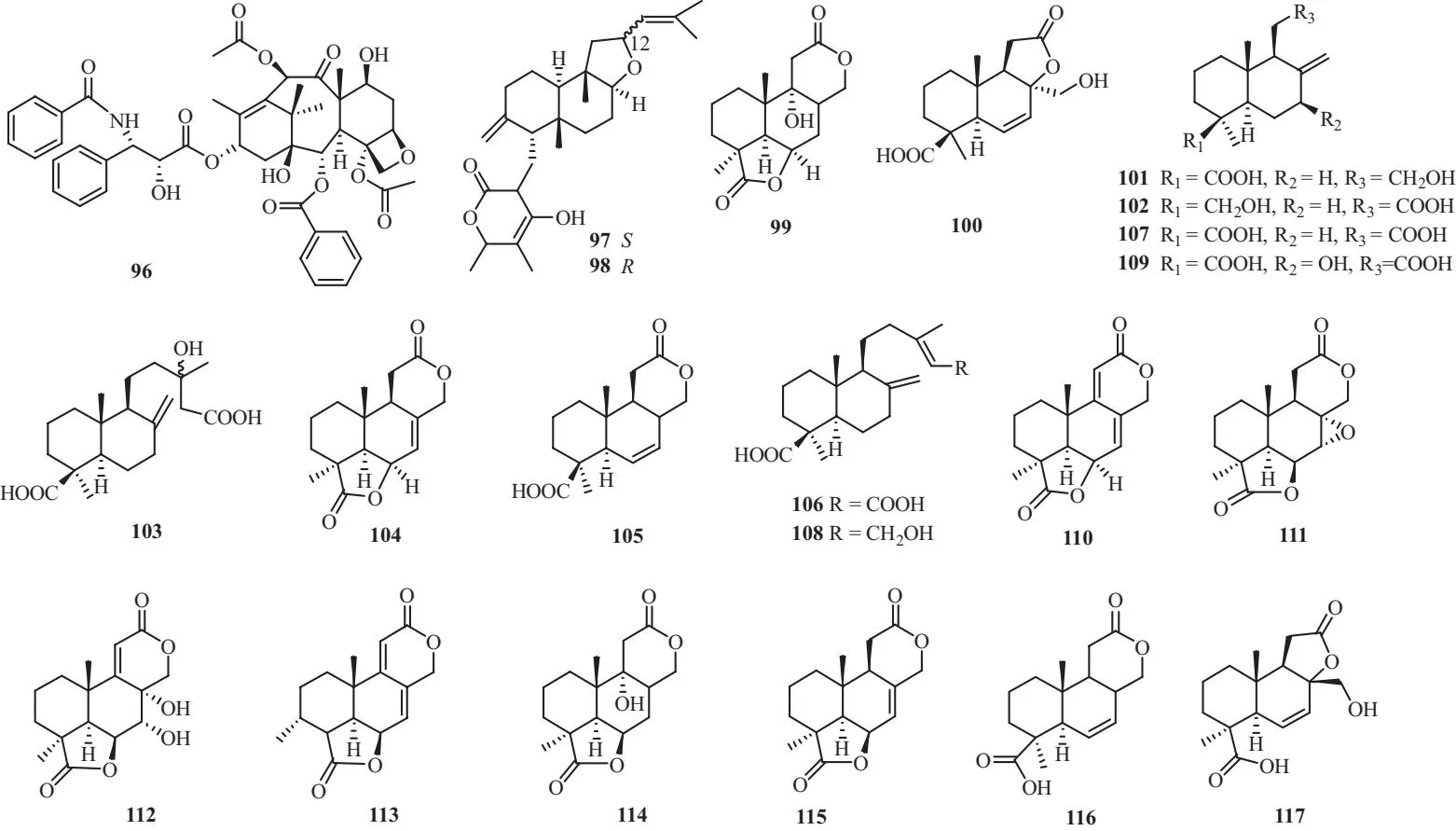

图3 植物内生真菌中二萜类成分
1.4 二倍半萜
Liu等[54]从内生真菌AspergillusterreusH010中分离得到2个新二倍半萜类化合物,命名为aspterpenacids A~B (172~173).Liu等[55]从内生真菌FusariumproliferatumMA-84分离得到4个二倍半萜类化合物,为 fusaprolifins A and B (174~175)、terpestacin (176)、 fusaproliferin (177).Zhu等[56]从红树林曲霉属真菌Aspergillusustus分离得到7个新的二倍半萜类化合物ophiobolins X~Z (178~179,181)、21-dehydroophiobolin U (180)、21-epiophiobolin Z (182)、21-epi-ophiobolin O (189)、deoxyophiobolin K (191),及11个已知化合物ophiobolin K (183)、 6-epi-ophiobolin K (184)、ophiobolin G (185)、6-epiophiobolin G (186)、ophiobolin P (187)、21,21-O-dihydro-6-epiophiobolin G (188)、ophiobolin O (190)、ophiobolin Q (192)、ophiobolin H (193)、5,6-diepiophiobolin H (194)、ophiobolin U (195).见表4、图4所示.
1.5 三萜类化合物
Qin[57]等从狭叶南五味子内生真菌PenicilliumochrochloronSWUKD4.1850中分离纯化得到5个新三萜类化合物,命名为为Kadanguslactone A~E (196~200),以及10个已知三萜类化合物nigranoic acid、henrischinin A-B、lancifodilactone C-D、schirubridilactone D、wuweizidilactone D、micrandilactone C、23α-hydroxynigranoic acid、7β-hydroxynigranoic acid (201~210).Liang等[58]从内生真菌Hypoxylonsp.6269分离得到化合物integracide A (211)、integracide E (212).陈亮亮等[59]从角果木内生革孔菌属真菌J5中分离到3个三萜类化合物14-acetoxy-15-hydroxyirpexan、15α-hydroxytrametenolic acid和3β-hydroxylanosta-8,24-dien-21-oic acid (213~215).见表5、图5所示.

表4 植物内生真菌中二倍半萜类成分

表5 植物内生真菌中三萜类成分

图4 植物内生真菌中二倍半萜类成分
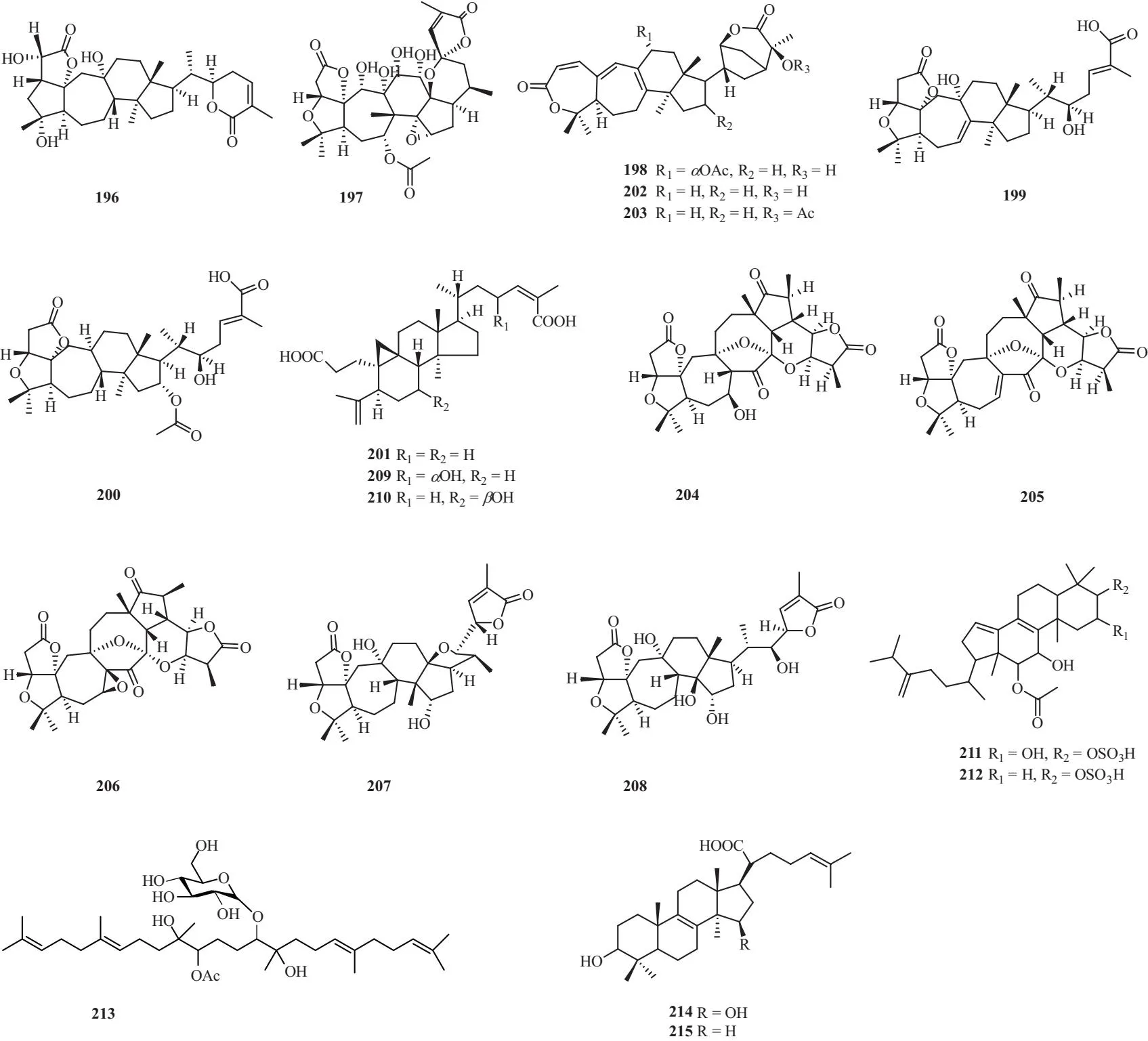
图5 植物内生真菌中三萜类化合物
2 生物活性
2.1 抗炎活性
Zhang等[12]在内生真菌分离得到的倍半萜化合物cyclonerodiol B (9)和化合物1α-isopropyl-4α,8-dimethylspiro[4.5]dec-8-ene-3β,7α-diol (45),通过抑制脂多糖诱导的BV2细胞NO产生,表现出显著的神经抗炎活性,0.1 μmol/L 时抑制率分别为75.0%、39.2%,比姜黄素更强,阳性对照,0.1 μmol/L 时抑制率为21.1%[12].红树林内生菌Phomopsissp.SYSU-QYP-23的马铃薯液体培养基分离鉴定倍半萜类化合物eremofortin I~J (64~65)对LPS诱导的RAW 264.7细胞NO的释放有较强的抑制活性,半抑制浓度值分别为8.6和 9.2 μmol/L.AA03390 (61)、eremofortin H (63)、lithocarin A (66)、petasol (67)表现出中等抑制活性(L-NMMA:15.0 μmol/L)[30].诸葛菜内生真菌IrpexolacteusOV38培养基发酵液产物中分离鉴定irpexolaceus D (79)、irpexolaceus F (81),在 50 μg/mL 浓度下,化合物81(50.2%)对NO生成的抑制作用强于化合物79(47.3%)[31].
2.2 抗菌活性
单萜类化合物(3R,4R,6R,7S)-7-hydroxyl-3,7-dimethyl-oxabicyclo[3.3.1]nonan-2-one (2)对灰酶霉和芝麻疫菌均具有较强的抗真菌活性,MIC值分别为 3.1 μg/mL[8].卫矛科美登木属美登木叶片组织内生真菌Botryosphaeriasp.固体培养物中分离得到化合物CJ-14445 (110)当浓度为 50 μg/disk 时,对白色念珠菌 (Canidiaalbicans)、酿酒酵 (Saccharomycescerevisiae)和Penicilliumavel-laneumUC-4376 存在抗真菌活性,抑菌圈分别为2.3、2.5、1.0 cm[35].石杉科中草药蛇足石杉分离得到葡萄孢霉Botryosphaeriasp.P483 发酵物中四降半日花烷型化合物botryosphaerins G~H (111~112)以及7个已知的化合物,即13,14,15,15-tetranorlabden-19,6β,12,17-diolide (113)、Botryosphaerin A (114)、3α,10β-dimethyl-1,2,3,3α,5α,7,10β,10coctahydro-5,8-dioxa-8-acephenanthrylene-4,9-dione (115)、acrostalidicacid (116)、bortyosphaerin B (117)、LL-Z1271β(118)、acrostalic acid (119),对禾谷镰刀菌 (Gaeumannomycesgraminis)、串珠镰刀菌(Fusariummoniliforme)、茄病镰刀菌(Fusariumsolani)、尖孢镰刀菌(Fusariumoxysporum)和稻瘟病菌 (Pyriculariaoryzae)等5种真菌有较强的抑菌活性[3,36].
2.3 抗肿瘤活性
Pulici等[3,16]在内生真菌Eupenicilliumsp.HJ002 分离得到的二萜类化合物 penicilindole A (23)和B (24),均对A549和HepG2 表现出不同程度的细胞毒性,与阳性对照5-氟烷 ( IC50=36.8,76.9 μmol/L)相比,化合物24对A549和HepG2 的抑制效果最好,其 IC50值分别为 5.5 和 1.5 μmol/L.
2.4 其它活性
余紫荆等[15]在内生真菌Aspergillusversicolor中分离得到倍半萜类化合物 phomanolide (22),其对抗甲型流感病毒效果 (IC50=(2.96±0.64) μg/mL)比阳性药剂阿比朵尔 (IC50=(0.15±0.04) μg/mL)稍弱[15].
3 结语与展望
植物内生真菌的发现已有 100 多年,活性成分研究较慢,尤其是诱导内生真菌活性物质的产生和富集的研究,是近年才被关注的领域.在分离鉴定菌种时,也应进一步研究植物内生真菌诱导萜类化合物的生成途径、生物活性与构效的关系,并找到其作用部位,这将为萜类化合物的应用提供理论基础[3].另外,需要优化培养内生真菌的条件,特别是真菌生长状态良好,未明显减弱,且容易产生次级代谢产物的条件.综上,将优化内生菌生长条件与所分离的活性化合物方法、构效关系共同考虑,对植物内生真菌萜类活性成分的开发利用具有深远意义.
