止得咳颗粒在大鼠体内的代谢产物研究 Δ
2024-02-02郑飘雪陈辉华黄春燕梁炎丽陆春莲谢晶晶马玉明彭嘉文赵立春陈日兰广西中医药大学药学院南宁3000广西高校中药提取纯化与质量分析重点实验室南宁3000中药固体制剂制造技术国家工程研究中心华南分中心南宁3000广西壮瑶药工程技术研究中心南宁3000钦州市检验检测中心广西钦州3000广西中医药大学附属瑞康医院药剂科南宁30011
梁 洁 ,郑飘雪 陈辉华 黄春燕 ,梁炎丽 陆春莲 谢晶晶 马玉明 彭嘉文 赵立春 ,陈日兰 (1.广西中医药大学药学院,南宁 3000;.广西高校中药提取纯化与质量分析重点实验室,南宁 3000;3.中药固体制剂制造技术国家工程研究中心华南分中心,南宁 3000;.广西壮瑶药工程技术研究中心,南宁 3000;.钦州市检验检测中心,广西 钦州 3000;.广西中医药大学附属瑞康医院药剂科,南宁 30011)
止得咳颗粒是在广西中医药大学附属瑞康医院临床经验方的基础上研制而成的中药复方制剂,由龙脷叶、射干、桔梗、白前、黄芩、柴胡、青天葵等10味药材配伍而成,现已获得药物临床试验批准。相关药理学研究表明,止得咳颗粒具有止咳、化痰和利咽等功效,常用于急、慢性支气管炎、肺炎的治疗[1]。但目前止得咳颗粒的研究仅限于质量控制、提取工艺和药效学研究[2―4],尚未有其体内代谢产物的相关研究。通过研究中药复方制剂代谢产物,鉴定其被吸收的活性成分,确定该复方制剂的药效活性成分,是阐明其药效物质基础和作用机制的重要环节。但中药复方成分的复杂性和体内代谢的多样性,导致其代谢产物的鉴定具有一定难度。超高效液相色谱-四极杆-静电场轨道阱高分辨质谱(UPLC-QExactive-MS)技术具有高灵敏度、高选择性和高分辨率的特点,能在复杂体系中快速识别与定量分析化学成分,现已成为中药代谢产物鉴定的重要手段。基于此,本研究采用UPLC-Q-Exactive-MS技术分析止得咳颗粒的化学成分,并对大鼠给予止得咳颗粒后的血清、尿液和粪便进行检测,分析其原型成分及可能的代谢产物,以期为阐明该制剂的药效物质基础和指导临床安全用药提供依据。
1 材料
1.1 主要仪器
Ultimate 3000型超高效液相色谱仪和Q-Exactive高分辨质谱仪均购自美国Thermo Fisher Scientific 公司;XW-80A 型涡旋仪购自上海沪西分析仪器厂有限公司;Milli-Q Gradient A10 型超纯水纯化系统购自美国Millipore 公司;5415R 型低温高速离心机购自艾本德中国有限公司;NDK200-2N 型氮吹仪购自杭州米欧仪器有限公司。
1.2 药品与试剂
止得咳颗粒由广西中医药大学附属瑞康医院自制(批号20210608);野鸢尾黄素、黄芩素、橙皮苷、黄芩苷、柠檬酸、右旋奎尼酸、柴胡皂苷C、D-(+)-蔗糖、尿苷、L-酪氨酸、芦荟大黄素、圣草酚-7-O-葡萄糖苷、山柰酚-3-O-芸香糖苷、汉黄芩苷、芹菜素-7-O-葡萄糖醛酸苷、绿原酸、咖啡酸、异鼠李素、山柰酚、木犀草素、柚皮素、香叶木素、黄芩新素、乔松素、次野鸢尾黄素、汉黄芩素(纯度均大于98%,批号分别为RP211021、RP220627、RP220321、RP220827、RP220527、RP200120、RP200604、RP210204、RP210525、RP200602、RP220614、RP220426、RP210827、RP221114、RP221223、RP210916、RP220610、RP211118、RP200312、RP210105、RP220113、RP210718、RP221129、RP211213、RP221130)对照品均购自成都麦德生科技有限公司;甲醇、乙腈为质谱纯,甲酸、甲酸铵为色谱纯,其他试剂均为分析纯,水为超纯水。
1.3 动物
本研究所用动物为雄性清洁级健康SD 大鼠,共24只,体重(220±20)g,购自湖南斯莱克景达实验动物有限公司,动物生产许可证号SCXK(湘)2019-0001。本文涉及的动物实验方案经广西中医药大学伦理委员会批准,批准号DW20220726-159。
2 方法
2.1 止得咳颗粒药液的制备
取止得咳颗粒500 g,研细,加入超纯水5 000 mL,搅拌至完全溶解,即得止得咳颗粒药液,于4 ℃保存备用。
2.2 动物分组及给药
将24 只雄性SD 大鼠随机分为空白组(n=6)、给药组(n=18)。实验前,所有大鼠均于SPF 级屏障环境中适应性喂养4 d,自由摄食、饮水;给药前禁食12 h(自由饮水),给药组大鼠按9.45 g/kg(临床等效剂量)灌胃止得咳颗粒药液,空白组大鼠灌胃等体积超纯水,每天2次,每次灌胃间隔6~8 h,连续3 d。
2.3 生物样品的收集与处理
末次给药后1 h,取给药组大鼠6 只,用戊巴比妥钠麻醉后行腹主动脉采血,于4 ℃下以3 000 r/min离心20 min,取上清液,得血清样品。将给药组剩余的12只大鼠均分后置于2个代谢笼中,其中一个代谢笼用于收集12 h 内尿液,另一个用于收集12 h 内粪便。将收集的尿液以3 500 r/min 离心10 min,取上清液,以氮气浓缩至2 mL,得尿液样品;将收集的粪便于50 ℃烘干,碾碎,得粪便样品。空白组大鼠同法收集血清、尿液及粪便样品。以上样品均置于-80 ℃冰箱中保存。
2.4 生物供试品溶液的制备
2.4.1 血清供试品溶液的制备
解冻血清样品,吸取100 μL,加入乙腈300 μL,涡旋30 s,于-20 ℃下超声(功率250 W,频率40 kHz,下同)提取20 min,于4 ℃下以13 000 r/min离心5 min;取上清液300 μL以氮气吹干,用超纯水100 μL复溶,涡旋振荡1 min,于4 ℃下以13 000 r/min 离心5 min,取全部上清液,即得。
2.4.2 尿液供试品溶液的制备
解冻尿液样品,涡旋1 min,取500 μL 置于1.5 mL离心管中,于4 ℃下以13 000 r/min离心5 min;取全部上清液,过0.22 μm水相滤膜,取滤液80 μL,即得。
2.4.3 粪便供试品溶液的制备
称取粪便样品10 mg,加入1%甲酸乙腈溶液1 mL,涡旋30 s,于-20 ℃下超声提取20 min,于4 ℃下以13 000 r/min 离心5 min;取上清液800 μL 以氮气吹干,用80%乙腈溶液(含1%甲酸)100 μL 复溶,于4 ℃下以13 000 r/min离心5 min,取全部上清液,即得。
2.5 对照品溶液的制备
分别精密称取“1.2”项下各对照品适量,置于10 mL容量瓶中,加甲醇溶解并定容,混匀,经0.22 μm 微孔滤膜滤过,取续滤液,即得适宜质量浓度的单一对照品溶液。
2.6 分析条件
2.6.1 色谱条件
以Waters HSS T3(100 mm×2.1 mm,1.8 μm)为色谱柱;正离子模式下流动相为0.1%甲酸溶液(A)和含0.1%甲酸的甲醇溶液(B),负离子模式下流动相为10 mmol/L 甲酸铵溶液(A)和含10 mmol/L 甲酸铵的95%甲醇溶液(B),进行梯度洗脱(0~1 min,90%A;1~13 min,90%A→2%A;13~18 min,2%A;18~18.5 min,2%A→90%A;18.5~20 min,90%A);流速为0.3 mL/min;柱温为35 ℃;进样量为2 μL。
2.6.2 质谱条件
采用电喷雾离子源(electron spray ionization,ESI),选择正、负离子模式分开检测,一级分辨率为70 000 FWHM,二级分辨率为17 500 FWHM;离子源喷雾电压分别为3.8、3.2 kV;毛细管温度为300 ℃;鞘气流速为40 Arb;雾化器温度为350 ℃。
2.7 分析方法
取血清供试品溶液、粪便供试品溶液、尿液供试品溶液、止得咳颗粒药液,按“2.6”项下分析条件进样。采用MS-DIAL 软件对实验数据进行分析处理,将得到的数据结果与MSBank、KEGG数据库比对,对各个色谱峰进行初步推测,得到化合物的准分子离子峰和二级碎片离子、分子式等信息,结合相关文献及质谱裂解规律,进一步对化合物进行推测及鉴定。
3 结果
正负离子模式下得到的总离子流图见图1、图2(正负离子模式下空白样品的总离子流图略)。通过与止得咳颗粒药液以及空白组样品进行对比,并结合对照品相关信息后发现,止得咳颗粒中共鉴定出31个化学成分,包含17个黄酮及其苷类化合物、7个有机酸类化合物、3个皂苷类化合物、4 个其他类化合物(表1)。大鼠的血清、尿液和粪便样品共鉴定出16 个原型成分和11 个代谢产物。其中,血清样品中鉴定出8 个原型成分和4 个代谢产物;尿液样品中鉴定出10个原型成分和7个代谢产物;粪便样品中鉴定出8 个原型成分和5 个代谢产物(表2)。
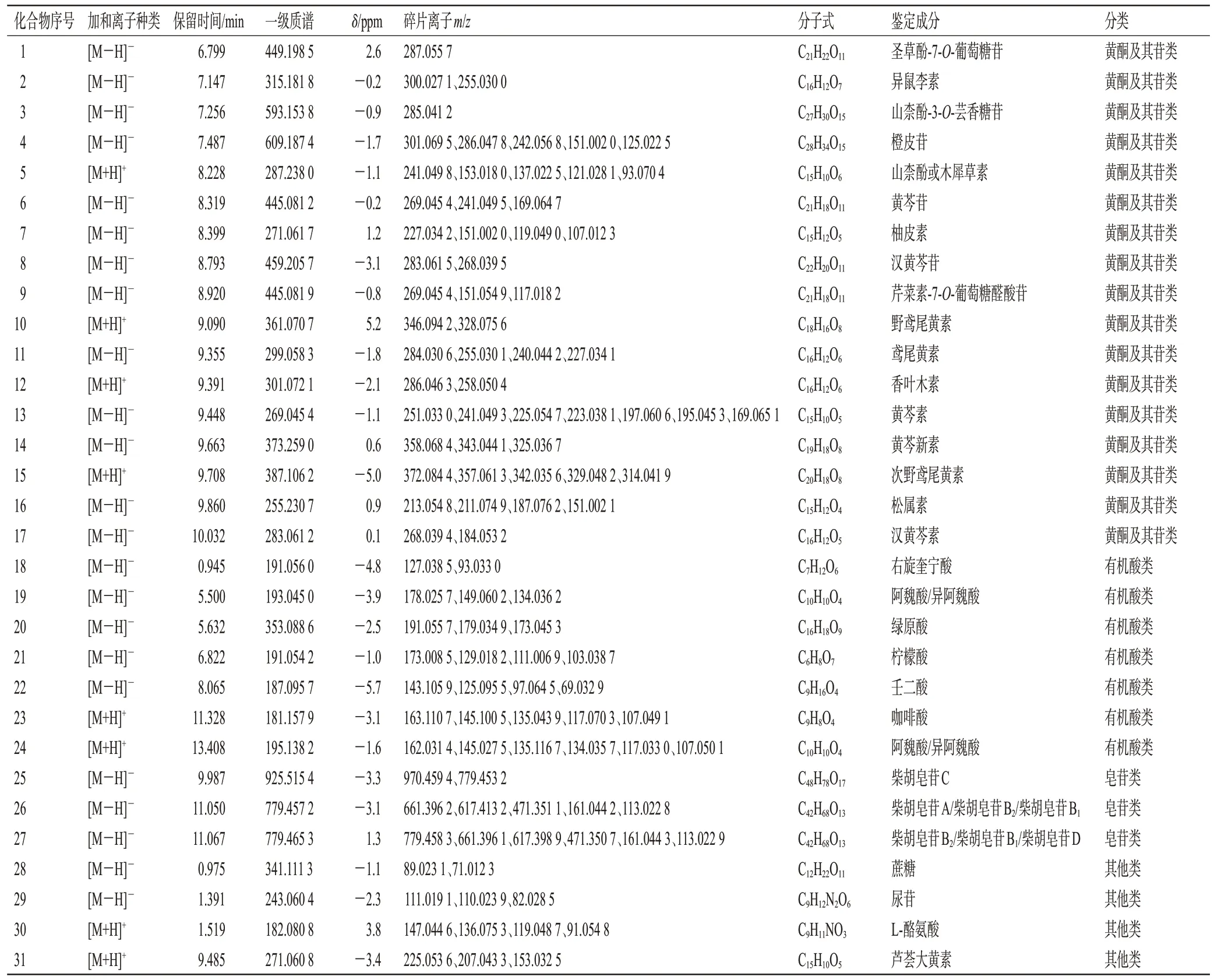
表1 止得咳颗粒中化学成分鉴定结果

表2 止得咳颗粒在大鼠血清、粪便、尿液中的主要原型成分和代谢产物
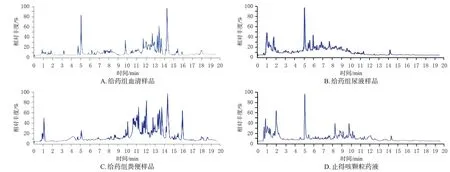
图1 正离子模式下给药组样品及止得咳颗粒药液的总离子流图

图2 负离子模式下给药组样品及止得咳颗粒药液的总离子流图
3.1 止得咳颗粒化学成分及原型成分的鉴定
3.1.1 黄酮及其苷类化合物
黄酮类化合物大部分以游离、与糖结合成苷类等形式存在,其裂解规律主要包括失去中性离子CH3、CO、CO2、H2O,糖苷键的断裂及发生逆狄尔斯-阿尔德裂解反应等[5]。
化合物13 的保留时间为9.448 min,准分子离子峰m/z269.045 4[M-H]-,分子式为C15H10O5。准分子离子峰m/z269.045 4[M-H]-的邻二羟基结构脱去H2O后生成m/z251.033 0[M-H-H2O]-,同时还失去了CO、CO2、H2O 等小分子,生成碎片离子m/z241.049 3[MH-CO]-、m/z225.054 7[M-H-CO2]-、m/z197.060 6[M-H-CO-CO2]-、m/z195.045 3[M-H-H2O-2CO]-、m/z169.065 1[M-H-2CO-CO2]-。这与文献报道的黄芩素裂解规律基本一致[5];此外,化合物13 的保留时间与黄芩素对照品一致,故推测其为黄芩素。
依据上述黄酮类成分的裂解规律,推测化合物2、5、7、10、11、12、14、15、16和17分别为异鼠李素、山柰酚或木犀草素、柚皮素、野鸢尾黄素、鸢尾黄素、香叶木素、黄芩新素、次野鸢尾黄素、松属素和汉黄芩素。
黄酮类化合物大多数以苷类形式存在于自然界,而糖苷键的断裂是黄酮苷类化合物的主要裂解途径。化合物4在负离子模式下的保留时间为7.487 min,由一级质谱得到准分子离子峰m/z609.187 4[M-H]-,分子式为C28H34O15。主要碎片离子包括m/z301.069 5[M-HRha-Glc]-、m/z286.047 8[M-H-Rha-Glc-CH3]-、m/z242.056 8[M-H-Rha-Glc-CH3-CO2]-、m/z151.020 0[M-H-Rha-Glc-C9H10O2]-、m/z125.022 5[M-HRha-Glc-C10H8O3]-。这与文献报道的橙皮苷裂解规律一致[5],经与对照品比对,确认该化合物为橙皮苷。
依据上述黄酮苷类成分的裂解规律,推测化合物1、3、6、8和9分别为圣草酚-7-O-葡萄糖苷、山柰酚-3-O-芸香糖苷、黄芩苷、汉黄芩苷和芹菜素-7-O-葡萄糖醛酸苷。
3.1.2 有机酸类化合物
有机酸是一类广泛存在于植物中的具有酸性的有机化合物,其裂解规律通常为失去CO、CO2、H2O等中性碎片。
化合物18 的保留时间为0.945 min,由一级质谱图得到准分子离子峰m/z191.056 [M-H]-,分子式为C7H12O6。准分子离子峰发生裂解,失去2 个H2O 和CO后得到碎片离子m/z127.038 5[M-H-2H2O-CO]-,或失去3 个H2O 和CO2后得到碎片离子m/z93.033 0[MH-3H2O-CO2]-。结合文献[5],经与对照品比对,确认该化合物为右旋奎宁酸。
依据上述有机酸类成分的裂解规律,推测化合物19和24均为阿魏酸/异阿魏酸,化合物20、21、22、23分别为绿原酸、柠檬酸、壬二酸、咖啡酸。
3.1.3 皂苷类化合物
止得咳颗粒中的皂苷类化合物主要来源于柴胡,该类化合物易失去母核上连接的葡萄糖、海藻糖基、CO2、H2O等中性分子。
化合物25 的保留时间为9.987 min,准分子离子峰m/z925.515 4[M-H]-,分子式为C48H78O17。准分子离子峰结合1 个羧基后得到碎片离子m/z970.459 4[M-H+COOH]+;准分子离子峰脱去1个海藻糖基(Fuc,146 Da)后产生碎片离子m/z779.453 2[M-H-Fuc]-,再脱去葡萄糖基(Glu,162 Da)后产生碎片离子m/z617.455 4[MH-Fuc-Glu]-。这与文献报道柴胡皂苷C的裂解规律一致[6],经与对照品比对,鉴定该化合物为柴胡皂苷C。其可能的裂解路径见图3。
3.1.4 其他类化合物
化合物28 的保留时间为0.975 min,准分子离子峰m/z341.111 3[M-H]-,分子式为C12H22O11。二级质谱中存在由准分子离子峰发生裂解失去C9H16O8后产生的碎片离子m/z89.023 1[M-H-C9H16O8]-,此碎片继续裂解失去1 个H2O 产生碎片离子m/z71.012 3[M-HC9H16O8-H2O]-。这与文献报道的蔗糖质谱信息相同[5],经与对照品比对,确认该化合物为蔗糖。
3.2 止得咳颗粒在大鼠体内的代谢产物鉴定
化合物M1 的保留时间为1.701 min,准分子离子峰m/z303.231 5[M-H]-,分子式为C15H12O7。二级质谱碎片离子有m/z285.043 8、m/z241.047 6、m/z169.061 5。碎片离子与山柰酚或木犀草素的特征碎片一致,预测该化合物的母核可能为山柰酚或木犀草素,且发现准分子离子峰m/z303.231 5[M-H]-比碎片离子m/z285.043 8多1 个H2O,因此推测该化合物可能为山柰酚或木犀草素水合产物[7]。
化合物M2 的保留时间为5.500 min,准分子离子峰m/z367.158 1[M-H]-,分子式为C17H20O9。二级质谱中存在碎片离子m/z193.050 3、m/z191.056 1、m/z173.045 4、m/z134.036 3,其中碎片离子m/z191.056 1、m/z134.036 3为绿原酸特征碎片,且准分子离子峰m/z368.158 1[MH]-比绿原酸m/z353.088 6[M-H]-多1 个CH2,因此预测该化合物可能为绿原酸甲基化产物[8]。
化合物M3 的保留时间为7.415 min,准分子离子峰m/z463.088 2[M+H]+,分子式为C21H18O12。二级质谱碎片离子有m/z287.053 6、m/z270.047 6、m/z169.011 8,与黄芩苷二级碎片离子相同,故预测该化合物的母核为黄芩苷;又因准分子离子峰比母核多1 个OH-,因此推测该化合物可能为黄芩苷羟基化产物[9]。
4 讨论
止得咳颗粒的化学成分及代谢的原型成分主要为黄酮及其苷类化合物、有机酸类化合物等。黄酮类成分包括野鸢尾黄素、黄芩素、黄芩苷等,具有抗菌、抗炎等活性[5,10―11];有机酸类化合物包括绿原酸、咖啡酸等,具有抗炎、止咳、平喘等功效[12―13]。这与本课题组前期研究发现止得咳颗粒具有止咳、抗炎的功效相一致[2],可为该制剂的药效物质基础提供理论依据。代谢产物的研究结果显示,本研究检测到黄芩苷原型及3个可能的代谢产物,因此笔者推断大鼠在给予止得咳颗粒后,黄芩苷在其体内主要发生了甲基化、羟基化和葡萄糖醛酸化,这与相关文献报道的黄芩苷代谢途径一致[7];另外,本研究还检测到鸢尾黄素原型及3个可能的代谢产物,因此笔者推断大鼠在给予止得咳颗粒后,鸢尾黄素在其体内主要发生了甲基化、去甲基化和去甲氧基化,这与相关文献报道的鸢尾黄素代谢途径一致[14]。本研究还发现,在大鼠的血清、尿液和粪便中能检测到黄芩苷、黄芩素、次野鸢尾黄素和绿原酸等原型成分,表明止得咳颗粒进入大鼠体内后,并不是完全经过代谢转化排出体外,还有一部分以原型成分直接排出体外。
从代谢产物的结果可知,鉴定出的成分大部分来源于射干、黄芩等药材,这可能与龙脷叶和青天葵等药材的化学成分研究较少,以及文献资料信息不足等有关。而且,仅从一级质谱、二级质谱和分子式等信息鉴定化学成分,对于具有相似结构的同分异构体无法区分。因此,若想明确化合物的具体结构,还需通过对照品比对,以及结合半制备液相色谱等技术进一步研究止得咳颗粒的化学成分。
综上所述,本研究通过UPLC-Q-Exactive-MS 技术对止得咳颗粒在大鼠血清、尿液和粪便中的代谢产物进行了分析,共鉴定出16个原型成分及11个代谢产物,主要涉及甲基化、羟基化、葡萄糖醛酸化等代谢途径。
