CNT/ZIF-67@ZIF-8/Ru-Cu催化剂的制备及催化性能研究
2024-01-30田进军
薛 艳,王 显,田进军
(南阳理工学院生物与化学工程学院 河南 南阳 473004)
燃烧化石能源所释放的气体带来温室效应,煤矿石油等能源物质过度开采也带来的一系列环境问题。为解决这些问题,需要寻找新型的可再生能源。氢气具有燃烧充分且能量利用率高的特点,是一种非常理想的新型能源[1]。氨硼烷(NH3BH3, AB)是一种简单的硼-氮化合物,具有分子量小(30.87 g/mol)、室温稳定、无毒等特点,尤其是AB含氢量高(约为19.6%),水解条件温和,分解产物中不含对环境有害的气体,是产氢材料的优选。根据氨硼烷的水解方程(公式1)可看出1 mol的氨硼烷理论上可水解产出3 mol的H2,事实上常温下氨硼烷分解十分缓慢,且氨硼烷的产氢率与催化剂有着莫大的关系,因此高效易制作的催化剂成为氨硼烷广泛使用的关键[2-3]。近几年研究表明,贵金属Pt、Pd、Ru等金属(0)催化剂[4-6]均表现出优异的催化氨硼烷分解制氢的能力,但这类催化剂成本较高,因此将成本较低的过渡金属与贵金属催化剂制备成合金催化剂则大大地降低了成本[7-9]。金属纳米粒子往往易团聚,将过渡金属纳米离子负载到合适载体上形成复合催化剂则可缓解这一缺陷,且能有效增大与氨硼烷(AB)的接触面积、增加活性位点,还可以显著增强催化活性和稳定性,是目前提升金属催化剂性能、促进氨硼烷(AB)水解制氢的研究方向之一。ZIFs是一类金属有机骨架的微孔材料,也称作MOFs材料,是一类多维网状结构的配位晶体材料[10-11]。ZIFs材料结构类沸石,都为孔状结构,且骨架十分柔软,也称作“软沸石”,可作为分散金属纳米粒子的载体。
(1)
本文利用ZIFs和碳纳米管作为载体制备了CNT/ZIF-67@ZIF-8金属有机骨架材料,将钌和铜按照不同的比例负载于其上形成负载型催化剂,并研究了金属钌(Ru)和金属铜(Cu)之间的协同效应以及金属和载体CNT/ZIF-67@ZIF-8之间的双功能机制,为研究氨硼烷这一储氢材料的制备以及氨硼烷水解产氢提供了一定的理论和实践参考。
1 实验部分
1.1 实验材料
2-甲基咪唑、六水硝酸钴、碳纳米管、三水硝酸铜、氯化钌氨硼烷等试剂均为分析纯。
1.2 催化剂材料的制备
1.2.1 CNT/ZIF-67@ZIF-8的制备
称取5.82 g的六水合硝酸钴[Co(NO3)2·6H2O]溶在150 mL的甲醇中制备成为A溶液,取0.212 g的碳纳米管(CNT)放入溶液A中,超声0.5 h。称取6.16 g的2-甲基咪唑溶解于150 mL的甲醇溶液中,制成溶液B。将B溶液在磁力搅拌下缓慢倒入A溶液中,再匀速搅拌1 h后,停止搅拌,将混合溶液常温放置24 h,于4000 r/min下离心10 min后得到的沉淀即为CNT/ZIF-67。向CNT/ZIF-67中加入80 mL含16 mmol 2-甲基咪唑的甲醇溶液,搅拌5 min以分散CNT/ZIF-67,再加入含有4 mmol乙酸锌的甲醇溶液20 mL,室温下搅拌1 h后,同样的过程静置老化24 h。老化后的混合溶液经同样的过程离心后得到的沉淀在70 ℃干燥12 h,即得到载体CNT/ZIF-67@ZIF-8。
1.2.2 CNT/ZIF-67@ZIF-8/Ru-Cu的制备
称取0.3 g CNT/ZIF-67@ZIF-8,并加入180 mL去离子水中,超声0.5 h。将硝酸铜、抗坏血酸、氢氧化钠按照摩尔比硝酸铜∶抗坏血酸∶氢氧化钠=1∶6∶2的比例加入上述溶液,所加硝酸铜的物质的量为0.4 mmol。将混合液转入圆底烧瓶,在80 ℃的恒温水浴锅中搅拌2 h后,用移液枪量取1.8 mL氯化钌溶液(10 g·L-1) 逐滴滴入以上反应液中,继续恒温搅拌1 h,冷却至室温后进行离心、干燥、研磨得到CNT/ZIF-67@ZIF-8/Ru-Cu纳米材料。
1.3 催化剂表征
日本 JEOL JEM 2100 透射电子显微镜 (TEM), 日 本 JEOL 公 司JSM-7900F的扫描电子显微镜(SEM)对催化剂样品的三维形貌进行观察和分析;Bruker D8 X射线衍射仪表征催化剂的晶型特征。
1.4 催化剂性能测试
氨硼烷水解制氢的反应过程如下:取一定量催化剂加入圆底烧瓶中,加入8 mL去离子水,超声10 s,设置不同的条件(改变催化剂用量、改变氨硼烷用量、改变温度,从而选出最佳条件),称量一定量氨硼烷溶于2 mL水中,将圆底烧瓶置于恒温磁力搅拌器中,将氨硼烷溶液迅速加入催化剂中,开始收集气体,每隔30 s观察收集气体的量,直至气体不再生成。根据实验数据测出催化剂的TOF值和产氢速率。
TOF值是单位时间单位质量目标反应物的转化量,可以用来衡量催化剂活性。
TOF值计算公式
TOF=(pV/RT)/(m·Δt)
(2)
反应速率计算公式
rB=V/(m·Δt)
(3)
活化能(Ea)计算公式
ln(TOF)=-Ea/RT+lnA
(4)
式中,V为产出氢气的体积(V=V2-V1),单位为mL;m为所用催化剂的质量,Δt为产生氢气体积从V1到V2,R为摩尔气体常量,T为热力学温度,Ea为表观活化能,A为指前因子(也称频率因子)。
1.4.1 AB水解反应速率的影响
制备出CNT/ZIF-67@ZIF-8/Ru-Cu催化剂,用于催化氨硼烷分解制氢的反应中,进而初步判断催化性能。考察了催化剂用量对AB水解反应的影响、反应底物氨硼烷用量对AB水解反应的影响、通过不同反应温度下的TOF值计算反应活化能。
1.4.2 回收测试
对使用过的催化剂进行回收干燥,回收的催化剂再次用于催化氨硼烷水解产氢,操作过程同上,记录实验数据。
2 结果与讨论
2.1 结构及形貌表征
CNT/ZIF-67@ZIF-8负载金属铜、钌3∶1的样品(即样品2)的结构表征如图1所示。

图1 CNT/ZIF-67@ZIF-8的结构表征
图1(a)是样品CNT/ZIF-67@ZIF-8/Ru-Cu的XRD谱图,从图中可看出样品的衍射峰较多,这些密集的衍射峰大多是ZIF的特征峰,从谱图中不能看到Cu和Ru的特征峰,可能是还原过程中产生的金属Cu和Ru被在此过程中由于结构不稳定而形成的ZIF-67和ZIF-8无定形物质覆盖。图1(b)是CNT/ZIF-67@ZIF-8/Ru-Cu样品的SEM,在还原过程中,Ru、Cu双金属颗粒附着在以CNT/ZIF-67@ZIF-8为载体的催化剂表面,通过图1(b)可以看出金属钌、金属铜颗粒分布在材料表面和孔道内,四万倍电镜下可看到ZIF结构不太稳定,有部分片状物质出现,碳纳米管和ZIF间相互交织也呈现多孔结构。载体CNTs、ZIFs具有大的比表面积和良好的稳定性,它们能提供较多的活性位点并且锚定金属纳米颗粒使其均匀稳定地在其表面上附着,不易团聚,从而使其活性更高。从TEM照片(图1(c))也可看出CNT/ZIF-67@ZIF-8/Ru-Cu样品由Ru、Cu双金属颗粒附着在CNT/ZIF-67@ZIF-8载体的表面,但由于结晶度较低不能捕捉到样品的晶格条纹。
2.2 催化剂的性能测试
以氨硼烷为反应底物,CNT/ZIF-67@ZIF-8/Ru-Cu为催化剂在一定条件下进行水解制氢反应,考察了催化剂用量对AB水解反应的影响、反应底物氨硼烷用量对AB水解反应的影响,通过不同反应温度下的TOF值计算反应活化能。
2.2.1 不同催化剂质量时的水解反应
CNT/ZIF-67@ZIF-8/Ru-Cu为催化剂,催化剂用量分别为15 mg、25 mg和30 mg时,底物氨硼烷的质量为45 mg,反应温度为室温时,考察催化剂用量对氨硼烷水解速率的影响。
由图2可知,当催化剂的质量为25 mg和35 mg时,反应基本上无明显变化,在反应开始0.5 min以后开始急剧上升,整个反应曲线疾速上升,约2 min左右产氢的体积可达到60 mL,曲线平缓,催化剂的质量为25 mg,在产氢体积20~60 mL时,每g催化剂(cat)的催化反应速率为1.4884 L/min,TOF值为0.0664 mol/min·g cat。当催化剂的质量为15 mg时,在最开始反应阶段,反应速率与25 mg时接近,随着反应的进行,虽然曲线略低于25 mg的曲线,但整体也呈现加速上升的状态,在产氢体积20~60 mL时,催化反应速率为1.775 L/min·g cat,TOF值为0.0792 mol/min·g cat。虽然在氨硼烷的质量为45 mg,室温下催化剂量为25 mg和35 mg时氨硼烷水解产氢的速率要略快于15 mg的催化剂速率,但15 mg的催化剂单位催化效率最优,所以当催化剂质量为15 mg时催化效果最好。

图2 催化剂质量对水解速率的影响
2.2.2 不同氨硼烷质量时的水解反应
CNT/ZIF-67@ZIF-8/Ru-Cu为催化剂,催化剂用量为15 mg,底物氨硼烷的质量分别为45 mg、60 mg、75 mg,反应温度为室温时,考察底物氨硼烷量不同,由于反应过程中加水的体积不变,即氨硼烷浓度不同时对水解速率的影响。
由图3可知,氨硼烷水解反应在产氢体积为20~60 mL时这一段反应相对稳定,且产氢体积的变化量和时间变化量基本为一定值,即单位时间内产氢体积的增加量是定值,表明氨硼烷的水解反应符合一级动力学反应。当氨硼烷的质量为45 mg时,水解反应速率最大,在产氢体积为20~60 mL这一阶段反应速率为1.824 L/min·g cat,TOF值为0.0814 mol/min·g cat,由于反应底物氨硼烷的初始浓度较低,产氢量最小约为73 mL。当氨硼烷质量为60 mg时,溶液中AB的浓度随之增加,水解反应速率依然较大,约3.5 min 收集到的氢气体积已过到60 mL。产氢体积为20~60 mL时,反应速率为1.635 L/min·g cat,TOF值为0.0730 mol/min·g cat。当氨硼烷的质量为75 mg时,溶液中AB的浓度进一步增加,反应速率明显小于前两组,反应速率和TOF值较低,但最终产氢量较大超过120 mL。当氨硼烷的质量为45 mg时反应最迅速,TOF值最高,但最终产氢量最低,当氨硼烷的质量为60 mg和75 mg时最终产氢量相差不大,但相对来说前者的反应速率和TOF值更高。因此反应底物氨硼烷的量为60 mg时,反应进行稳定,催化效率较高。
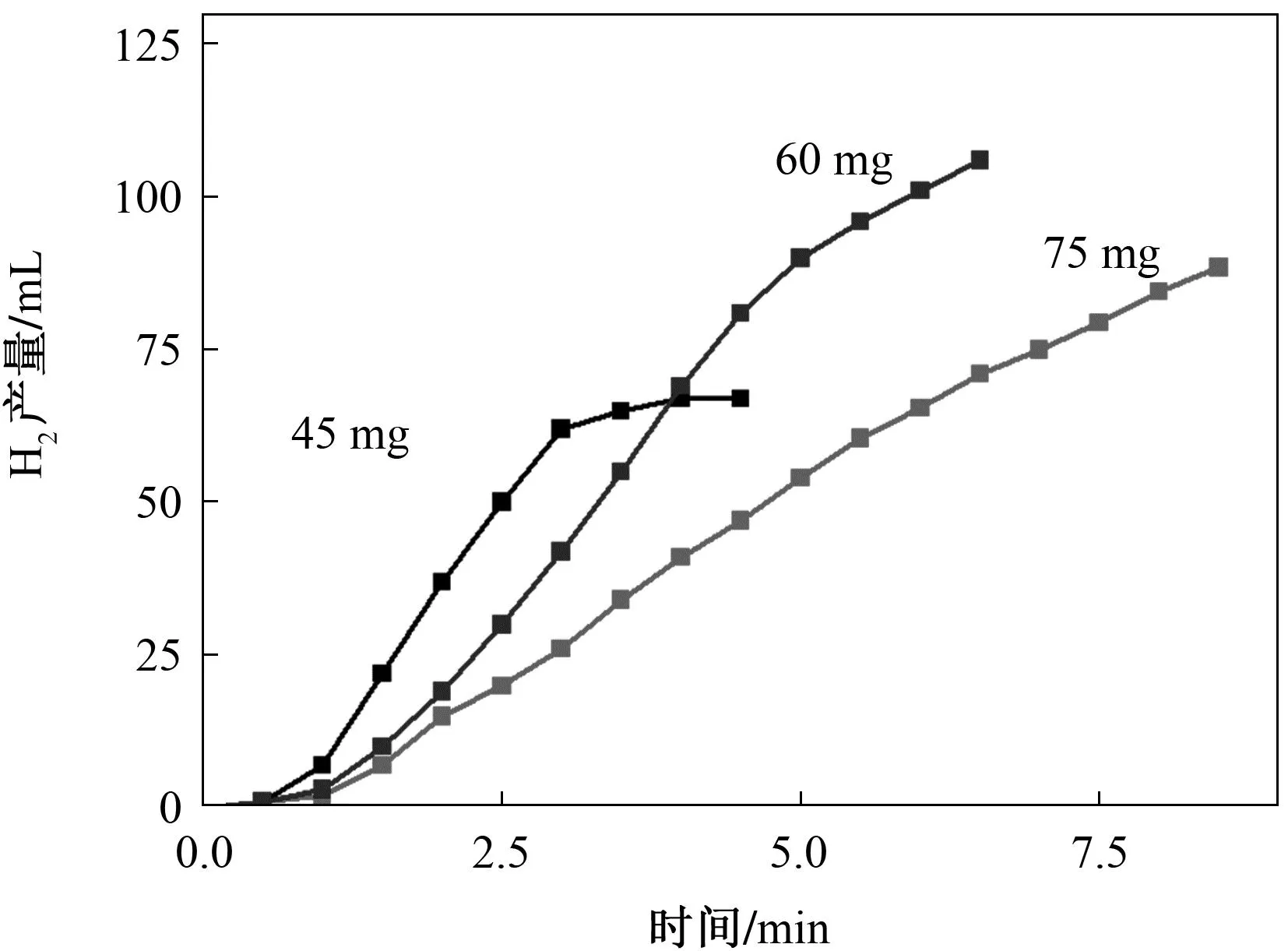
图3 氨硼烷质量对水解速率的影响
2.2.3 不同温度下的水解反应
设置恒温水浴锅温度分别为25 ℃、30 ℃、35 ℃、40 ℃。CNT/ZIF-67@ZIF-8/Ru-Cu为催化剂,催化剂用量为15 mg,底物氨硼烷的质量为75 mg时,考察温度和氨硼烷水解速率的有关系。
由图4可知,在温度为25 ℃、30 ℃、35 ℃、40 ℃时,反应均较快速进行,产氢体积从20 mL到时60 mL时各自的反应速率分别为0.889、0.882、0.889、1.104 L/min·g。随着温度的升高,催化剂分解氨硼烷的反应速率和TOF值也在逐渐升高,根据阿仑尼乌斯公式可计算出活化能Ea的数值为127.5 kJ/mol,活化能数值较大,超过其他负载型Ru基复合催化剂的活化能值[12]。较大的活化能值可能是ZIF结构不稳定引起,选择合适的改载体或将ZIF载体与其他能增加其稳定性的材料结合改善ZIF载体的稳定性,是提高ZIF基负载型双金属催化剂的有效方法。

图4 不同温度下的水解反应(a)和水解速率分析(b)
2.2.4 回收催化剂性能测试
使用过的催化剂进行离心与反应液分离后经过洗涤、干燥后回收,回收的催化剂再次用于催化氨硼烷水解产氢。
由图5可知,原催化剂的反应速率曲线陡峭上升,在2.5~6 min之内是明显加速反应阶段,6 min以后曲线出现拐点,反应速率略小于前6 min,但总体催化性能良好,第一次回收的催化剂催化性能略有下降,在反应前2 min初始阶段和原始催化剂相差几乎不大,随着反应的进行,第一次回收的催化剂没有加速反应阶段,一直处于缓慢上升的状态,11 min后催化反应速率变得更加缓慢,直至反应结束。第二次回收的催化剂相较于原催化剂,反应速率明显下降,整个反应过程耗时约是18 min,接近于原催化剂反应时间的两倍,反应速度非常缓慢,催化性能大幅下降。CNT/ZIF-67@ZIF-8/Ru-Cu催化剂经回收再利用后催化效率不佳可能主要由于其载体中的ZIF结构不稳定引起。在今后的研究中,应努力改善ZIF结构的稳定性,充分利用载体对过渡金属的分散作用及载体自身的特殊结构等优势,构建高效的负载型过渡金属催化剂。

图5 回收催化剂催化速率图
3 结论
采用多步制备法制备出一种新型高效双金属催化剂。以CNT/ZIF-67@ZIF-8为载体负载铜和钌双金属的催化剂CNT/ZIF-67@ZIF-8/Ru-Cu,成功促进氨硼烷水解制氢。催化剂CNT/ZIF-67@ZIF-8/Ru-Cu的形貌表征可知Ru、Cu双金属颗粒均匀地附着在以CNT/ZIF-67@ZIF-8为载体的催化剂表面,CNT/ZIF-67@ZIF-8载体能很好地分散Ru、Cu双金属颗粒避免其团聚。CNT/ZIF-67@ZIF-8/Ru-Cu催化剂在氨硼烷水解反应中表现出显著的产氢活性和催化效率。在室温下催化剂为15 mg,反应底物氨硼烷的量为45 mg时,反应速率和TOF值可达到最高值,分别为1.824 L/min·g cat,TOF值为0.0814 mol/min·g cat。反应底物氨硼烷的量增加到60 mg时,反应速率和TOF值稍有降低,分别为1.635 L/min·g cat,TOF值为0.0730 mol/min·g cat,且产氢量可增加至超过120 mL,催化性能最佳。CNT/ZIF-67@ZIF-8/Ru-Cu催化氨硼烷水解产氢反应的活化能为127.5 kJ/mol,催化剂经3次使用后仍有较佳的催化效果,但催化效果有待进一步提高。CNT/ZIF-67@ZIF-8/Ru-Cu催化剂的制备过程简单、催化活性高,对新型高效催化剂的制备研究具有一定的参考的价值。
