南丹参化学成分研究*
2024-01-27赵璐瑶陈心雨郑浩东张志君
赵璐瑶,陈心雨,郑浩东,边 樱,张志君
(湖北科技学院医学部药学院,湖北 咸宁 437100)
南丹参(SalviabowleyanaDunn)为唇形科鼠尾草属植物,多年生草本,高约1m。根茎粗短肥厚,外表红色,根数条,圆柱形,微卷曲,轮伞花序8至多花,组成14~30cm顶生总状花序或总状圆锥花序。通常生长在山地、山谷、路旁、林下或水边。主产于浙江、湖南、江西、福建、广东和广西等南部地区[1],具有活血化瘀和抗氧化作用[2]。南丹参的植株形态和丹参相似,不同之处是它的根部比丹参较细小,根系没丹参发达,南丹参与丹参为同属植物,它们在外观、成分、功效等方面相似,在浙江和江西等一些南方地区南丹参当作丹参药用[3]。但到现在为止,南丹参的研究还不够全面和深入。因此,本文对南丹参根90%乙醇提取物的乙酸乙酯萃取部位化学成分进行了研究,从中分离得到11个化合物,其中有6个化合物为首次从该植物中获得。
1 材料与方法
1.1 仪器
高效液相色谱仪LC300(北京清博华科技有限公司);电子天平FA2004(上海良平科学仪器有限公司);半制备液相色谱仪P230p(大连依利特分析仪器有限公司);RE-2000A型旋转蒸发仪(上海亚荣生化仪器厂);BRUKER 8040型核磁共振仪(瑞士Bruker公司)。
柱色谱硅胶和薄层硅胶板(青岛海洋化工厂);Sephadex LH-20(凝胶Pharmacia有限公司);甲醇、二氯甲烷等试剂(天津欧博凯化工有限公司)。
1.2 药品
实验样品南丹参的根,于2022年4月采集于湖北省咸宁市澄水洞附近,经湖北科技学院药学院张志君老师鉴定为唇形科鼠尾草属植物南丹参(Salviabowleyana)。
1.3 实验方法
将所采南丹参药材晒干、水洗和烘干,剪断叶和茎等其他部位得到其干燥根部4.0kg,用90%的乙醇浸泡48h后,加热回流提取3次(12L×3次),提取时间为5h、4h和2h,合并提取液经过滤并减压回收溶剂浓缩得到浸膏状样品0.502kg。总浸膏加水至3L成悬浮液,用等体积的有机溶剂对其进行三次萃取,依次是石油醚和乙酸乙酯,用旋转蒸发仪减压浓缩,回收溶剂,依次得乙酸乙酯部位浸膏57g。乙酸乙酯层总浸膏经硅胶柱层析(100-200目硅胶),以二氯甲烷/甲醇梯度(100∶0,100∶1,50∶1,20∶1,9∶1,8∶2,7∶3)洗脱,结合TLC薄层检测所得样品,得到馏分Fr.1-Fr.3。Fr.1(27g)经硅胶柱层析,以二氯甲烷/甲醇梯度(50∶1,9∶1,0∶1)洗脱,得到6个亚馏分Fr.1-1-Fr.1-6。所得馏分Fr.1-4(10.3g)经SephadexLH-20层析,以二氯甲烷/甲醇(1∶1)洗脱,得3个馏分。所得馏分Fr.1-4-2(1.5g)再经半制备型HPLC,33%甲醇/水为流动相,纯化得到A(9)(17.3mg,tR=20.89min)。Fr.1-2(1.9g)再经半制备型HPLC,66%甲醇/水为流动相,纯化得到E(3)(14.17mg,tR=21.26min),F(2)(39.1mg,tR=22.2min)。Fr.1-3(2.6g)再经半制备型HPLC,49%甲醇/水为流动相,纯化得到D(10)(11.52mg,tR=20.89min)。Fr.1-6(4.2g)再经半制备型HPLC,40%甲醇/水为流动相,纯化得到B(1)(44.21mg,tR=18.32min)。Fr.2(19g)经硅胶柱层析,以二氯甲烷/甲醇梯度(100∶0,100∶1,50∶1,20∶1,9∶1,8∶2,7∶3)洗脱,得到3个亚馏分Fr.2-1-Fr.2-3。所得馏分Fr.2-2(9.3g)经SephadexLH-20层析,以二氯甲烷/甲醇(1∶1)洗脱,得3个馏分Fr.2-1-Fr.2-3。所得馏分Fr.2-2-1(1.7g)再经制备型和半制备型HPLC,32%甲醇/水为流动相,纯化得到G(11)(59.72mg,tR=4.64min),H(7)(66.59mg,tR=6.71min),I(6)(9.97mg,tR=5.92min),J(5)(38.04mg,tR=7.31min)。所得馏分Fr.2-2-2(2.7g)再经制备型和半制备型HPLC,35%甲醇/水为流动相,纯化L(8)(15.2mg,tR=9.47min)。Fr.2-1(7.1g)再经制备型HPLC,22%甲醇/水为流动相,纯化得到M(4)(10.44mg,tR=10.17min)。南丹参乙酸乙酯部分化合物分离流程示意图见图1,化合物1-11结构式见图2。

图1 南丹参乙酸乙酯部分化合物分离流程示意图
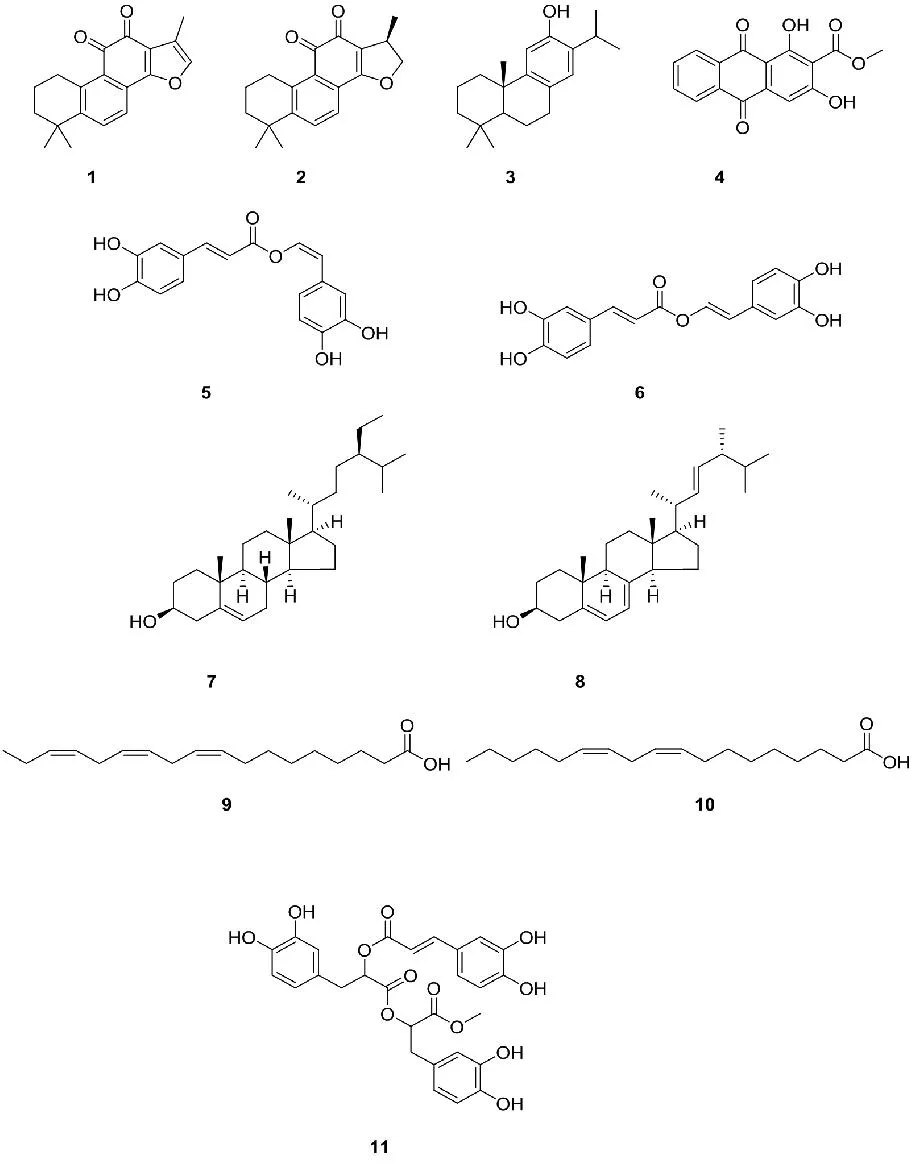
图2 南丹参中分离的化合物结构
2 结 果
化合物1:红色粉末(C19H18O3),易溶于氯仿、甲醇和丙酮等溶剂。ESI-MSm/z:295.3[M+H]+。在化合物1的1H-NMR(400MHz,CDCl3)谱中,呈现3个双键氢信号δH7.63(1H,d,J=8.1Hz,H-6),7.55(1H,d,J=8.1Hz,H-7),7.22(1H,s,H-16);3个亚甲基氢信号δH3.19(2H,t,J=6.4Hz,H-1),1.80(2H,m,H-2),1.67(2H,m,H-3);以及3个甲基氢信号δH2.26(3H,s,H-17),1.31(6H,s,H-18,19)。其13C-NMR谱中,共显示19个碳信号,包括2个羰基碳信号δC183.8(C-11),176.0(C-12),10个烯烃碳信号δC161.9(C-14),150.3(C-10),144.6(C-5),141.4(C-16),133.6(C-6),127.6(C-8),126.7(C-9),121.3(C-15),120.4(C-7),120.1(C-13);7个烷基碳信号δC38.0(C-3),34.8(C-4),32.0(C-18),32.0(C-19),30.0(C-1),19.3(C-2),9.0(C-17)。以上波谱数据与文献[4]基本一致,故鉴定化合物1为丹参酮ⅡA(tanshinone ⅡA)。化合物1的1H NMR(400MHz,CDCl3)谱图见图3,13C-NMR(100MHz,CDCl3)谱图见图4。

图3 化合物1的1H-NMR(400MHz,CDCl3)谱图
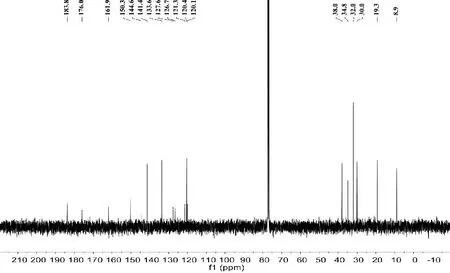
图4 化合物1的13C-NMR(100MHz,CDCl3)谱图
化合物2:红色粉末(C19H20O3),易溶于氯仿、甲醇和丙酮等溶剂。ESI-MSm/z:297.1[M+H]+。在1H-NMR(400MHz,CDCl3)谱中,呈现2个双键氢信号δH7.63(1H,d,J=8.1Hz,H-6),7.49(1H,d,J=8.1Hz,H-7);1组连氧亚甲基氢信号δH4.89(1H,dd,J=9.3,5.7Hz,H-16a),4.36(2H,t,J=9.3Hz,H-16b);4组烷基氢信号δH3.60(1H,m,H-15),3.21(2H,t,J=6.3Hz,H-1),1.79(2H,m,H-2),1.66(2H,m,H-3);以及3个甲基氢信号δH1.36(3H,d,J=6.5Hz,H-17),1.31(6H,s,H-18,19)。其13C-NMR谱中,共显示19个碳信号,包括2个羰基碳信号δC184.3(C-11),175.7(C-12),8个烯烃碳信号δC170.8(C-14),152.4(C-5),143.7(C-10),132.6(C-6),128.4(C-9),126.3(C-8),122.5(C-7),118.3(C-13);1个连氧烷基碳信号δC81.5(C-16);8个烷基碳信号δC37.8(C-3),34.9(C-4),34.6(C-15),31.9(C-18),31.9(C-19),29.7(C-1),19.1(C-2),18.8(C-17)。以上波谱数据与文献[5]基本一致,故鉴定化合物2为隐丹参酮(cryptotanshinone)。化合物2的1H-NMR(400MHz,CDCl3)谱图见图5,13C-NMR(100MHz,CDCl3)谱图见图6。

图5 化合物2的1H-NMR(400MHz,CDCl3)谱图

图6 化合物2的13C-NMR(100MHz,CDCl3)谱图
化合物3:黄色油状(C20H30O),易溶于氯仿、甲醇和丙酮等溶剂。ESI-MSm/z:286.1[M+H]+。在化合物3的1H-NMR(400MHz,CDCl3)谱中,呈现2个双键氢信号δH6.83(1H,s,H-14),6.63(1H,s,H-11);12组烷基氢信号δH3.11(1H,hept,J=7.0Hz,H-15),2.86(1H,ddd,J=16.9,7.1,1.9Hz,H-7a),2.77(1H,ddd,J=16.9,11.3,7.4Hz,H-7b),2.17(1H,m,H-1a),1.85(1H,ddt,J=11.9,7.4,1.9Hz,H-6a),1.70(1H,m,H-2a),1.60(1H,m,H-6b),1.46(1H,m,H-2b),1.39(1H,dd,J=13.0,3.8Hz,H-1b),1.33(1H,m,H-3a),1.31(1H,dd,J=12.4,2.3Hz,H-5),1.30(1H,m,H-3b);以及5个甲基氢信号δH1.23(3H,d,J=7.0Hz,H-17),1.20(3H,d,J=7.0Hz,H-16),1.17(3H,s,H-20),0.94(3H,s,H-19),0.91(3H,s,H-18)。其13C-NMR谱中,共显示20个碳信号,包括1组苯环碳信号δC150.8(C-12),148.8(C-9),131.5(C-13),127.4(C-8),126.8(C-14),111.1(C-11);14个烷基碳信号δC50.5(C-5),41.8(C-3),39.0(C-1),37.7(C-10),33.6(C-18),33.5(C-4),29.9(C-7),27.0(C-15),24.9(C-20),22.9(C-17),22.7(C-16),21.8(C-19),19.5(C-2),19.4(C-6)。以上波谱数据与文献[6]基本一致,故鉴定化合物3为弥罗松酚(ferruginol)。化合物3的1H-NMR(400MHz,CDCl3)谱图见图7,13C-NMR(100MHz,CDCl3)谱图见图8。

图8 化合物3的13C-NMR(100MHz,CDCl3)谱图
化合物4:黄色粉末(C16H10O6),易溶于氯仿、甲醇和丙酮等溶剂。ESI-MSm/z:298.2[M+H]+。在化合物4的1H-NMR(400MHz,CDCl3)谱中,呈现2个羟基氢信号δH14.81(br s,1H,1-OH),12.64(br s,1H,3-OH);5个双键氢信号δH8.34(m,1H,H-8),8.28(m,1H,H-5),7.82(m,2H,H-6,H-7);以及1个甲氧基氢信号δH4.08(s,3H,H-12)。其13C-NMR谱中,共显示16个碳信号,包括2个羰基碳信号δC186.9(C-9),181.9(C-10);2组苯环碳信号δC170.1(C-11),167.4(C-3),137.9(C-4a),134.8(C-7),134.6(C-6),133.6(C-10a),133.3(C-8a),127.7(C-8),127.2(C-5),109.8(C-4),109.5(C-2),105.6(C-9a);以及1个甲氧基碳信号δC53.3(C-12)。以上波谱数据与文献[7]基本一致,故鉴定化合物4为munjistin methyl ester。化合物4的1H-NMR(400MHz,CDCl3)谱图见图9,13C-NMR(100MHz,CDCl3)谱图见图10。
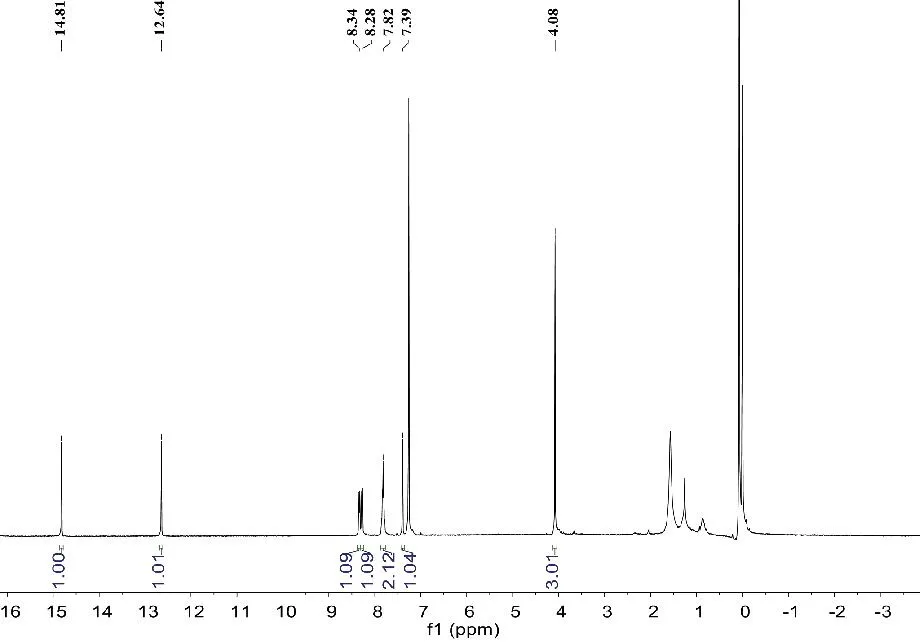
图9 化合物4的1H-NMR(400MHz,CDCl3)谱图

图10 化合物4的13C-NMR(100MHz,CDCl3)谱图
化合物5:黄色粉末(C17H14O6),易溶于氯仿、甲醇和丙酮等溶剂。ESI-MSm/z:315.2[M+H]+。在化合物5的1H-NMR(400MHz,CD3OD)谱中,呈现出10个双键氢信号δH7.73(d,J=15.9,1H,H-7),7.29(d,J=2.1,1H,H-2'),7.23(d,J=7.3,1H,H-7'),7.13(d,J=2.1,1H,H-2),7.05(dd,J=8.3,2.1,1H,H-6),6.91(dd,J=8.3,2.1,1H,H-6'),6.82(d,J=8.3,1H,H-5),6.75(d,J=8.3,1H,H-5'),6.46(d,J=15.9,1H,H-8),5.63(d,J=7.3,1H,H-8')。其13C-NMR(100MHz,CD3OD)谱中,共显示17个碳信号,包括1个羧基碳信号δC165.7(C-9);14个双键碳信号δC150.1(C-4),148.9(C-3'),148.9(C-4'),146.9(C-3),146.0(C-7),132.9(C-8'),127.8(C-1'),127.6(C-1),123.4(C-6),122.7(C-6'),117.3(C-2'),116.6(C-5),116.1(C-5'),115.5(C-2),113.7(C-8),113.2(C-7')。以上波谱数据与文献[8]基本一致,故鉴定化合物5为nepetoidin B。化合物5的1H-NMR(400MHz,CDCl3)谱图见图11,13C-NMR(100MHz,CDCl3)谱图见图12。

图11 化合物5的1H-NMR(400MHz,CD3OD)谱图

图12 化合物5的13C-NMR(100MHz,CD3OD)谱图
化合物6:黄色粉末(C17H14O6),易溶于氯仿、甲醇和丙酮等溶剂。ESI-MSm/z:315.2[M+H]+。在化合物61H-NMR(400MHz,CD3OD)谱中,呈现出10个双键氢信号δH7.80(d,J=12.8,1H,H-7'),7.67(d,J=15.8,1H,H-7),7.09(d,J=1.6,1H,H-2),7.00(dd,J=8.2,1.6,1H,H-6),6.83(d,J=1.6,1H,H-2'),6.80(d,J=8.2,1H,H-5),6.70(m,2H,H-5',H-6'),6.36(d,J=12.8,1H,H-8'),6.33(d,J=15.8,1H,H-8)。其13C-NMR(100MHz,CD3OD)谱中,共显示17个碳信号,包括1个羧基碳信号δC166.2(C-9);14个双键碳信号δC150.0(C-4),148.5(C-3'),148.5(C-4'),146.9(C-3),146.6(C-7),135.5(C-8'),127.6(C-1'),127.6(C-1),123.4(C-6),119.6(C-6'),117.3(C-2'),116.6(C-5),116.6(C-5'),115.3(C-2),113.7(C-8),113.6(C-7')。以上波谱数据与文献[9]基本一致,故鉴定化合物6为(E,E)-nepetoidinB。化合物6的1H-NMR(400MHz,CDCl3)谱图见图13,13C-NMR(100MHz,CDCl3)谱图见图14。

图13 化合物6的1H-NMR(400MHz,CD3OD)谱图
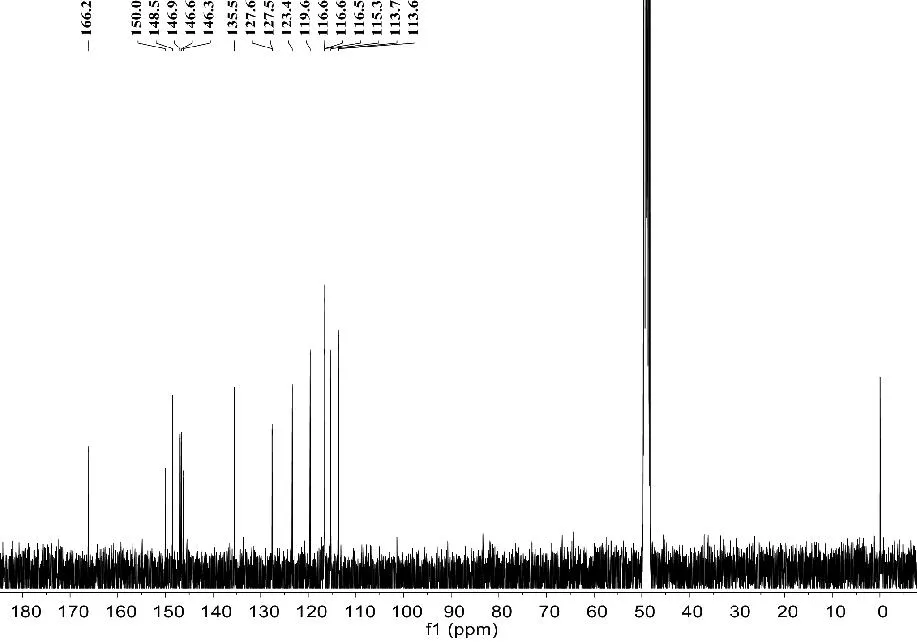
图14 化合物6的13C-NMR(100MHz,CD3OD)谱图
化合物7:无色针晶状(C29H44O),溶于氯仿。ESI-MSm/z:437.1[M+Na]+。在化合物7的1H-NMR(400MHz,CDCl3)谱中,呈现出甾醇特征性信号,包括2个角甲基单峰氢信号δH0.68,1.01;3个甲基双峰信号δH0.81,0.84,0.92;以及1个甲基三峰信号δ0.86。其13C-NMR谱中,共显示29个碳信号,进一步推断其为甾醇类化合物。详细碳谱数据如下δC37.5(C-1),31.9(C-2),72.0(C-3),46.1(C-4),140.9(C-5),121.9(C-6),34.2(C-7),31.8(C-8),50.4(C-9),36.3(C-10),21.2(C-11),40.0(C-12),42.5(C-13),57.0(C-14),24.5(C-15),28.4(C-16),56.3(C-17),12.0(C-18),20.0(C-19),36.1(C-20),19.6(C-21),32.1(C-22),19.0(C-23),29.4(C-24),26.3(C-25),19.2(C-26),23.3(C-27),26.3(C-28),12.2(C-29)。以上波谱数据与文献[6]基本一致,故鉴定化合物7为β-谷甾醇(β-sitosterol)。1H-NMR(400MHz,CDCl3)谱图见图15,13C-NMR(100MHz,CDCl3)谱图见图16。
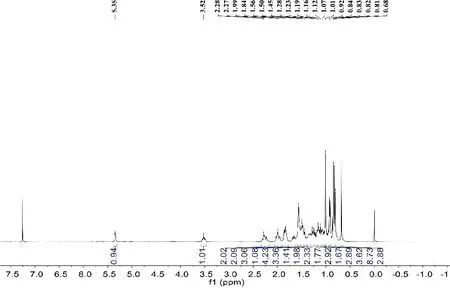
图15 化合物7的1H-NMR(400MHz,CDCl3)谱图

图16 化合物7的13C-NMR(100MHz,CDCl3)谱图
化合物8:无色针晶状(C28H50O),溶于氯仿。ESI-MSm/z:397[M+H]+。在化合物8的1H-NMR(400MHz,CDCl3)谱中,呈现出甾醇特征性信号,包括2个角甲基单峰氢信号δH0.62,0.94,3个甲基双峰信号δ:0.82,0.84,0.91,1.03。其13C-NMR谱中,共显示28个碳信号,进一步推断其为甾醇类化合物。δC141.5(C-8),139.9(C-5),135.7(C-22),132.1(C-23),119.7(C-6),116.4(C-7),70.6(C-3),55.9(C-17),54.7(C-14),46.4(C-9),43.0(C-13),41.0(C-4),40.6(C-20),39.2(C-12),38.5(C-1),37.2(C-10),33.2(C-25),32.2(C-2),28.5(C-16),23.2(C-15),21.3(C-11,21),20.1(C-27),19.8(C-26),17.8(C-19),16.4(C-28),12.2(C-18)。以上波谱数据与文献[10]基本一致,故鉴定化合物8为麦角甾醇(ergosterol)。化合物8的1H-NMR(400MHz,CDCl3)谱图见图17,13C-NMR(100MHz,CDCl3)谱图见图18。
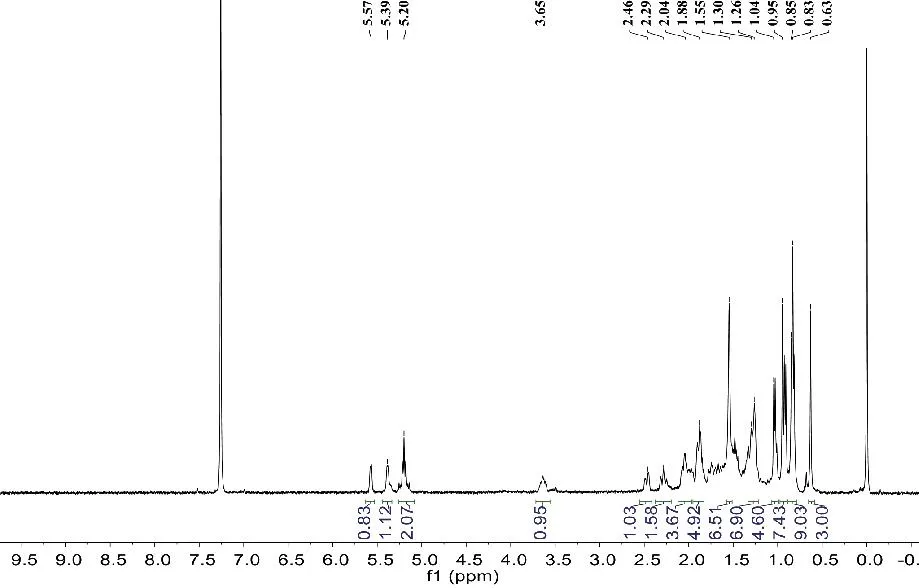
图17 化合物8的1H-NMR(400MHz,CD3Cl)谱图

图18 化合物8的13C-NMR(100MHz,CDCl3)谱图
化合物9:淡黄色油状(C18H30O2),溶于氯仿。ESI-MSm/z:279[M+H]+。在化合物9的1H-NMR(400MHz,CDCl3)谱中,呈现出6个双键氢信号δH5.36(6H,m,H-9,10,12,13,15,16);6组烷基氢信号δH2.81(4H,m,H-11,14),2.35(2H,t,J=7.2Hz,H-2),2.06(4H,m,H-8,17),1.63(2H,m,H-3),1.27~1.34(8H,m,H-4~7),0.97(3H,t,J=7.7Hz,H-18)其13C-NMR谱中,共显示18个碳信号,包括1个羧基碳信号δC176.5(C-1);6个双键碳信号δC132.1(C-9),130.4(C-16),128.4(C-12),128.4(C-13),127.9(C-15),127.2(C-10);以及11个烷基碳信号δC34.1(C-2),29.7(C-7),29.3(C-6),29.2(C-5),29.2(C-4),27.3(C-3),25.8(C-8),25.7(C-11),24.8(C-14),20.7(C-17),14.4(C-18)。以上波谱数据与文献[11]基本一致,故鉴定化合物9为亚麻酸(linolenicacid)。化合物9的1H-NMR(400MHz,CDCl3)谱图见图19,13C-NMR(100MHz,CDCl3)谱图见图20。
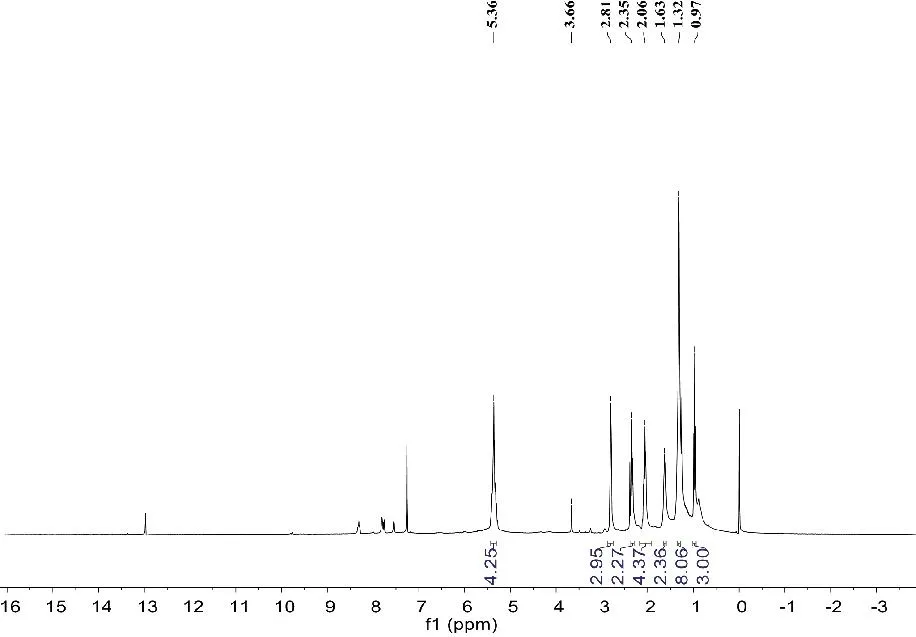
图19 化合物9的1H-NMR(400MHz,CDCl3)谱图

图20 化合物9的13C-NMR(100MHz,CDCl3)谱图
化合物10:淡黄色油状(C18H32O2),溶于氯仿。ESI-MSm/z:281[M+H]+。在化合物10的1H-NMR(400MHz,CDCl3)谱中,呈现出4个双键氢信号δH5.35(4H,m,H-9,10,12,13);6组烷基氢信号δH2.77(2H,t,J=6.8Hz,H-11),2.34(2H,m,H-2),2.04(4H,m,H-8,14),1.63(2H,m,H-3),1.31(14H,m,H-4,5,6,7,15,16,17),0.89(3Ht,J=7.0Hz,H-18)其13C-NMR谱中,共显示18个碳信号,包括1个羧基碳信号δC180.2(C-1);4个双键碳信号δC130.3(C-13),130.2(C-9),128.2(C-12),128.0(C-10);以及11个烷基碳信号δC34.2(C-2),31.7(C-16),29.7(C-7),29.5(C-15),29.3(C-6),29.2(C-5),29.2(C-4),27.3(C-8),27.3(C-14),25.8(C-11),24.8(C-3),22.7(C-17),14.2(C-18)。以上波谱数据与文献[12]基本一致,故鉴定化合物10为亚油酸(linoleicacid)。化合物10的1H-NMR(400MHz,CDCl3)谱图见图21,13C-NMR(100MHz,CDCl3)谱图见图22。

图21 化合物10的1H-NMR(400MHz,CDCl3)谱图

图22 化合物10的13C-NMR(100MHz,CDCl3)谱图
化合物11:棕色粉末(C28H26O12),易溶于氯仿、甲醇和丙酮等溶剂。ESI-MSm/z:553.2[M+H]+。在化合物11的1H-NMR(400MHz,CD3OD)谱中,呈现出多个双键氢信号δH7.53(1H,d,J=15.9,H-7'),7.03(1H,d,J=2.0,H-2'),6.93(1H,d,J=8.1,H-6'),6.77(1H,d,J=8.1,H-5'),6.74(1H,d,J=2.0,H-5'),6.69(1H,d,J=8.1,H-5'),6.59(1H,d,J=8.1,H-5'),6.25(1H,d,J=15.9,H-8');2个连氧次甲基氢信号5.17(1H,m,H-8),4.90(1H,m,H-8'');1个连氧甲基氢信号3.69(3H,s,OCH3);以及两个亚甲基氢信号3.04(2H,m,H-7),3.16(2H,m,H-7'').。其13C-NMR(100MHz,CD3OD)谱中,共显示28个碳信号,包括1个羧基碳信号δC173.6(C-9),172.2(C-9),168.5(C-9);20个双键碳信号δC149.8(C-4''),149.7(C-4'),148.0(C-4'),147.7(C-3''),146.8(C-7'),146.1(C-3'),145.2(C-3),129.3(C-1),128.7(C-1''),127.6(C-1'),123.2(C-6'),123.1(C-6''),121.8(C-6),117.6(C-5''),117.5(C-2''),117.5(C-2),116.5(C-5'),116.3(C-5),115.2(C-2'),114.4(C-8');1个连氧次甲基碳信号δC74.7(C-8''),74.7(C-8);1个连氧甲基碳信号δC52.7(-OCH3);2个烷基碳信号δC37.9(C-7),37.9(C-7'')。以上波谱数据与文献[13]基本一致,故鉴定化合物11为salpalaestinin。化合物11的1H-NMR(400MHz,CDCl3)谱图见图23,13C-NMR(100MHz,CDCl3)谱图见图24。

图23 化合物11的1H-NMR(400MHz,CD3OD)谱图

图24 化合物11的13C-NMR(100MHz,CD3OD)谱图
3 讨 论
南丹参和丹参这两种植物在化学成分和药理作用上存在着很多相似之处[14]。施天慧等[15]对云南丹参化学成分进行含量测定,结果显示南丹参中总酚酸和丹酚酸B与丹参中含的量接近。有研究[15]表明南丹参中丹酚酸B的含量不仅符合药典的规定,而且比丹参中丹酚酸B含量高,有可能成为丹参药材中的优良品种[15]。由此可见,南丹参中化学成分及活性测定有很大的研究潜力,南丹参可以成为丹参这一药用植物的优质替代资源。
本文主要对鼠尾草属中的南丹参展开了化学成分的研究。我们从南丹参90%乙醇提取物中分离纯化得到11个化合物,其中菲醌类化合物有两个(1、2),二萜类化合物一个(3),蒽醌类一个(4),有机酸类有三个(5、6、11),甾醇类有两个(7、8),不饱和脂肪酸类有两个(9、10)。从南丹参中首次分离出的化合物有6个,分别为:弥罗松酚(3)、munjistinmethylester(4)、(E,E)-nepetoidinB(6)、麦角甾醇(8)、亚麻酸(9)、salpalaestinin(11)。此次实验从南丹参首次分离得到的6个化合物,在丹参中也存在。根据丹参中活性成分与药效之间的作用关系,我们可以预测南丹参中存在的与丹参中相同的化学成分也具有相似的药理作用,为后期对南丹参中化合物的活性研究提供了新的思路和理论基础。此次实验对南丹参化学成分的研究进行了补充,为促进鼠尾草属植物的进一步开发利用提供参考。
