基于FAERS 的二肽基肽酶-Ⅳ抑制剂皮肤不良事件信号挖掘与评价*
2024-01-26幸婷婷陈光华李文东
幸婷婷,陈光华,李文东
(川北医学院附属医院,四川南充 637000)
二肽基肽酶-Ⅳ(DPP-4)抑制剂是治疗2 型糖尿病的新药,它通过抑制DPP - 4,提高肠促胰岛激素水平,促进胰岛素分泌,从而达到直接降血糖的目的[1-2]。DPP - 4 抑制剂已成为近年使用率增长最快的降糖药[3-4]。目前全球已上市的DPP-4 抑制剂包括西格列汀、维格列汀、沙格列汀、吉格列汀、奥格列汀、利格列汀、阿格列汀、替格列汀、曲格列汀、安奈格列汀、依格列汀[5-6],以西格列汀上市最早(2006年,美国)。然而,随着使用的增多,该类药的皮肤安全问题也日渐引起关注。有研究发现,使用利格列汀、维格列汀、阿格列汀治疗出现了红斑、大疱性类天疱疮(BP)[7]。还有研究发现,西格列汀与史蒂文斯— 约翰逊综合征、中毒性表皮坏死松解症及各种“大疱、脱屑、水疱、剥脱、荨麻疹或出汗反应”有关[8-9]。另有研究进行临床和组织病理学特征分析发现,使用替格列汀、西格列汀、维格列汀、沙格列汀、利格列汀的患者会发生BP、苔藓样皮炎、牛皮癣样皮炎、海绵状皮炎等相关皮肤病[10-11]。目前,DPP-4抑制剂的相关安全数据主要源于临床试验,少见药品不良事件(ADE)报告评价,也缺乏同类药物的数据对比。在此,检索美国食品和药物管理局不良事件报告系统(FAERS),对已上市的DDP-4抑制剂的皮肤ADE信号进行挖掘,以期为临床合理使用该类药物提供参考。现报道如下。
1 资料与方法
1.1 数据来源
选取2010年至2021年各季度FAERS 中的数据。该数据库主要采用监管活动医学词典(MedDRA)的首选语(PT)对ADE 进行编码[12]。选择药物信息(DRUG)、患者信息(DEMO)、不良事件(REAC)、事件结局(OUTC)4个子数据集的信息进行汇总与分析。
1.2 数据处理
依据FAERS 中附带的说明去除DEMO 中的重复报告,再通过“primary id”栏将4个子数据集的信息关联起来。利用“drugname”栏删除非药物的报告。纳入“role -cod”栏为首要怀疑(PS)药物且“drugname”栏分别为“sitagliptin”“vildagliptin”“saxagliptin”“alogliptin”“linagliptin”“gemigliptin”“teneligliptin”“trelagliptin”“anagliptin”“omarigliptin”“evogliptin”“zafatek”“metoana”“marizev”“sugarnon”“januvia”“galvus”“onglyza”“nesina”“trajenta”“zemiglo”“tenelia”的报告。
1.3 信号挖掘与整理
采用偏倚少、灵敏度高[13]的报告比值比(ROR)法分析,比例失衡法四格表见表1。计算公式为ROR=ad/bc;ROR95%置信区间(CI)=elnROR±1.961/a+1/b+1/c+1/d。ROR值越大,提示药品与ADE 的相关性越强[14]。a≥3 且ROR值的95%CI下限> 1,则提示生成1 个ADE 信号。将挖掘出的信号按MedDRA 的系统器官分类(SOC)整理,收集皮肤和皮下组织病症信号。

表1 比例失衡法四格表Tab.1 Fourfold table of disproportionality measure
1.4 统计学处理
采用χ2检验和秩和检验比较药物间的用药情况差异,两两比较采用Bonferroni 法进行校正。P<0.05 为差异有统计学意义。
2 结果
2.1 信号挖掘
以吉格列汀、奥格列汀、曲格列汀、安奈格列汀、依格列汀为PS药物的ADE 报告数均为0份,以西格列汀、维格列汀、沙格列汀、阿格列汀、利格列汀、替格列汀为PS 药物的ADE 报告数分别为192 131,2 034,6 787,3 635,4 532,2份,对应的ADE信号数依次为1 794,108,247,166,176,0 个,其中皮肤ADE 信号数依次为20,4,15,10,14,0个,且仅分别有2,2,8,1,6,0个信号在药品说明书中提及。详见表2至表6。
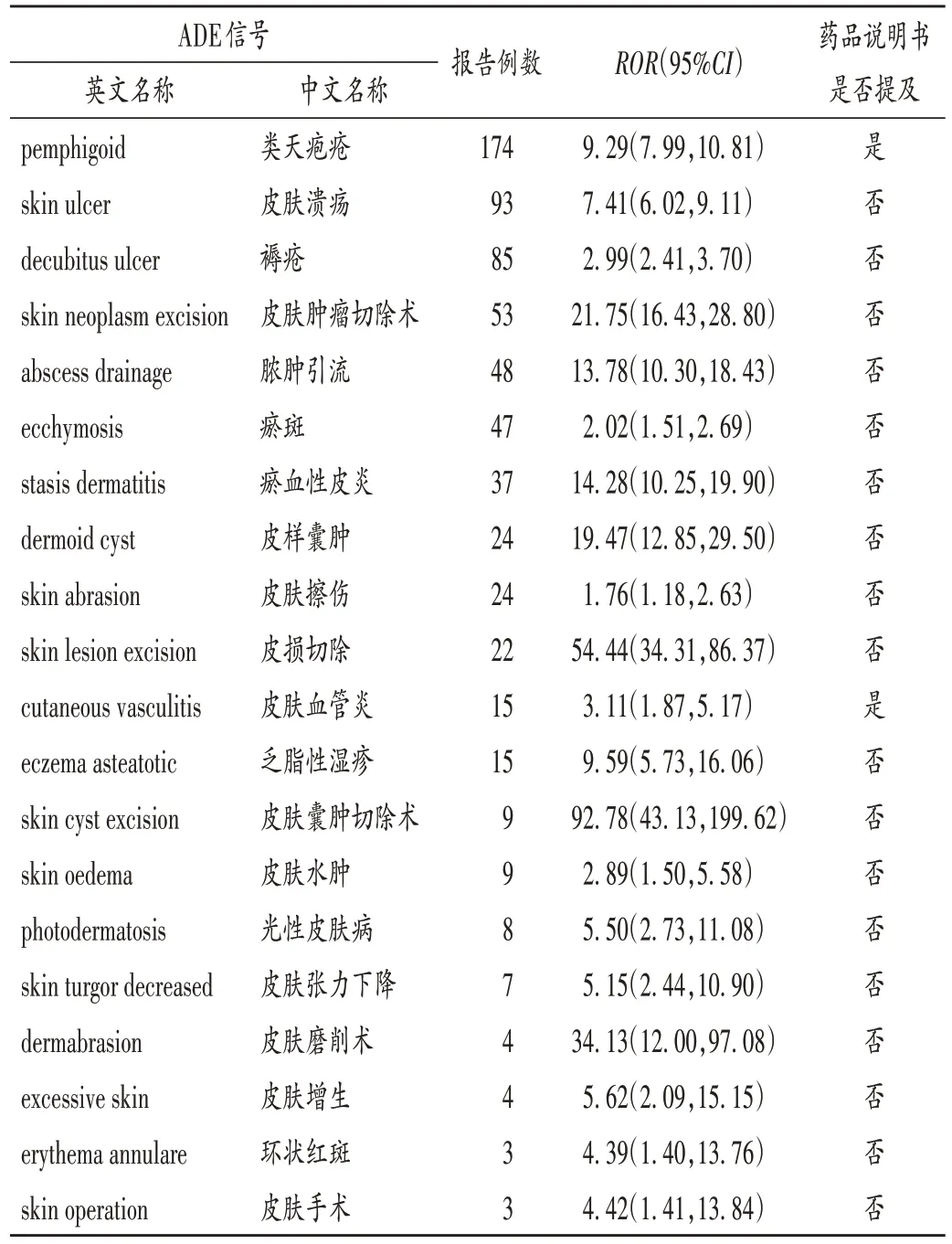
表2 西格列汀皮肤不良事件信号Tab.2 Skin ADE signals of sitagliptin
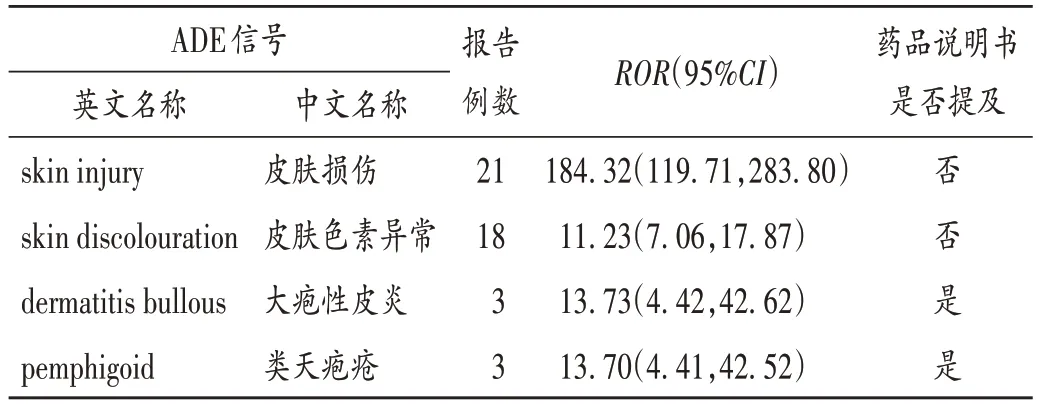
表3 维格列汀皮肤不良事件信号Tab.3 Skin ADE signals of vildagliptin
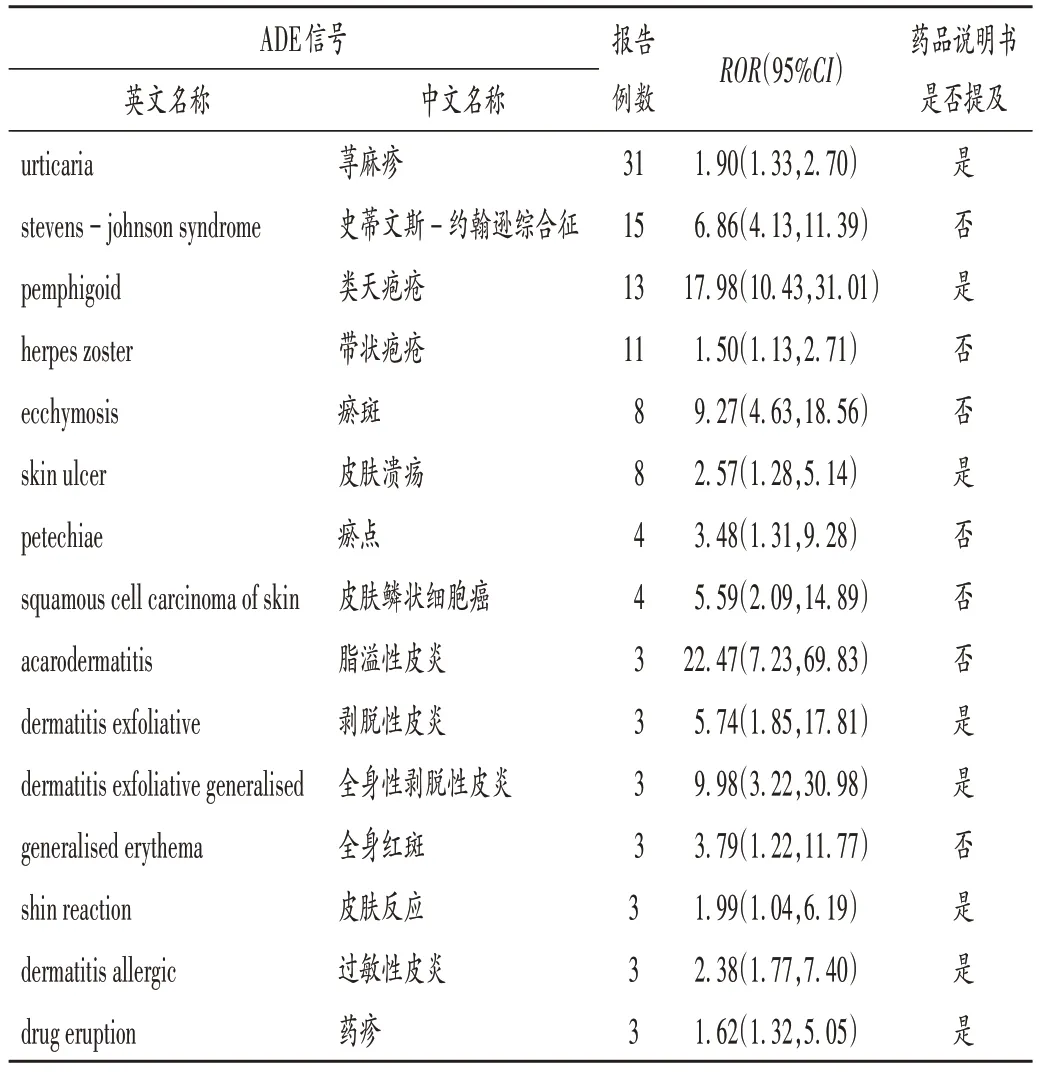
表4 沙格列汀皮肤不良事件信号Tab.4 Skin ADE signals of saxagliptin
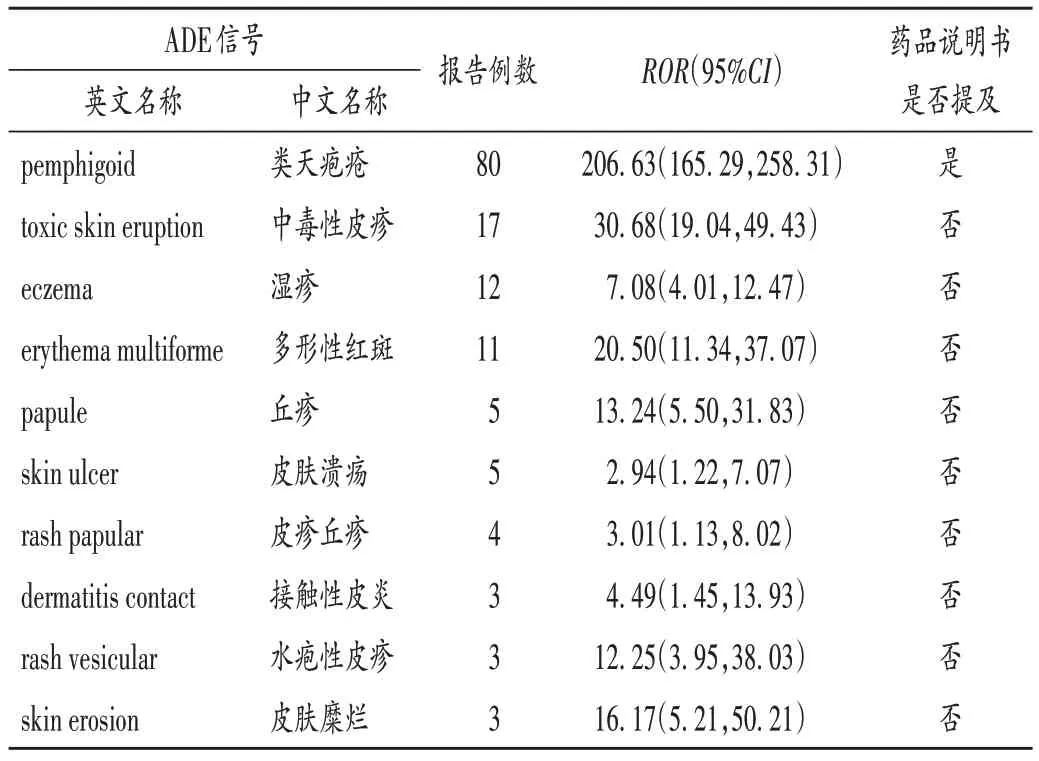
表5 阿格列汀皮肤不良事件信号Tab.5 Skin ADE signals of alogliptin

表6 利格列汀皮肤不良事件信号Tab.6 Skin ADE signals of linagliptin
2.2 用药信息
西格列汀、维格列汀、沙格列汀、阿格列汀、利格列汀皮肤ADE 涉及患者依次为684,45,115,143,167 例。患者中男多于女(除使用阿格列汀患者外),年龄多在65 岁以上;药物(除维格列汀外)疗程集中在半年内或1年以上;西格列汀、阿格列汀的临床结局多为住院,其余药物多为其他严重后果。详见表7 至表11(表10 中,在同一项目内,与西格列汀比较,*P< 0.05;与阿格列汀比较,#P<0.05;与维格列汀比较,△P<0.05)。

表7 皮肤不良事件报告用药信息统计[例(%)]Tab.7 Medication information of skin ADE reports[case(%)]
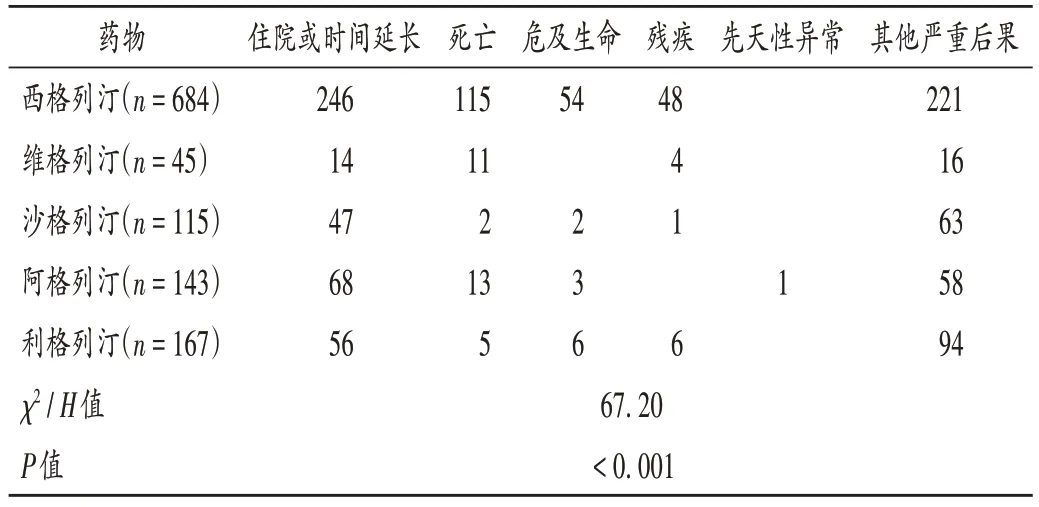
表8 皮肤不良事件报告临床结局Tab.8 Clinical outcomes in skin ADE reports

表9 皮肤不良事件报告上报国家(前5名)Tab.9 Top five countries reporting large quantity of skin ADE reports

表10 患者性别及临床结局两两比较结果Tab.10 Pairwise comparison of patients′genders and clinical outcomes

表11 患者年龄及用药时长两两比较结果Tab.11 Pairwise comparison of patients′ ages and duration of medication
3 讨论
已上市DPP-4 抑制剂中,吉格列汀、奥格列汀、曲格列汀、安奈格列汀、依格列汀、替格列汀均无皮肤ADE 报告,考虑可能与上述药物未在美国上市有关。西格列汀的报告数明显较其他DPP-4 抑制剂多,这可能与西格列汀上市时间最长,临床使用较多有关。西格列汀、维格列汀、沙格列汀、阿格列汀、利格列汀大多皮肤ADE 信号的ROR值较高,表明DPP-4抑制剂与这些皮肤ADE 关联较强,提醒医务工作者需留心观察患者用药期间的皮肤变化,避免严重ADE 的发生,已有严重皮肤病或易过敏体质者应谨慎用药。值得注意的是,本研究中挖掘出的多为新的ADE 信号,其中西格列汀包括脓肿引流、光性皮肤病、环状红斑等;维格列汀包括皮肤损伤、皮肤色素异常;沙格列汀包括皮肤鳞状细胞癌、脂溢性皮炎等;阿格列汀包括多形性红斑、中毒性皮疹、水疱性皮疹等;利格列汀包括福尼尔坏疽、大疱性皮炎、皮肤溃疡等,提示临床用药时若出现上述症状时,需考虑可能为DPP - 4 抑制剂所致,应评估病情并及时停药,减少患者伤害。
目前,DPP - 4 抑制剂致皮肤ADE 的机制仍未明确,NAKATANI 等[15]指出西格列汀的化学结构中具有苯环、羰基和显示3 个吸收峰的吸收光谱,它的光敏机制可能是皮疹、瘙痒、水肿发生的原因。FORSSMANN等[16]推测可能与DPP- 4 的抑制增加了嗜酸性粒细胞的动员和募集,从而促进体内由趋化因子配体11(CCL11)介导的过敏样反应有关。此外,现有研究表明,DPP - 4 抑制剂暴露增加了BP 的发生风险。BP 是常见的类天疱疮病,BENE等[17]通过挖掘法国药物警戒数据库首次提示DPP - 4 抑制剂与BP 存在关联。LEE 等[18]开展的病例对照研究发现DPP-4 抑制剂会增加BP 的风险,其中维格列汀的风险最高,其次是西格列汀、利格列汀,尤其是男性患者。BP180 作为存在于真表皮交界处的Ⅱ型跨膜蛋白,被认为是BP 致病自身抗体识别最主要的自身抗原[19],对于DPP - 4 抑制剂引发BP 的机制,有研究认为可能与DPP-4 抑制剂抑制BP180 的裂解,从而影响BP180 的功能和抗原性有关[20];也有研究认为可能与DPP - 4 抑制剂具有多种生物功能从而可改变表皮基底膜抗原性质和(或)调节免疫反应有关[21]。本研究中西格列汀、维格列汀、沙格列汀、阿格列汀、利格列汀均挖掘出类天疱疮ADE信号,且ROR值均较高,进一步证实DPP-4 抑制剂引起类天疱疮的可能性较大。
发生皮肤ADE 的患者中,年龄集中在65 岁以上,除使用阿格列汀患者为女性略多于男性外,其他药物为男性多于女性,用药剂量均处于药品说明书推荐范围内。在用药时长上,缺失数据较多,7 例使用维格列汀的患者用药时长为0.5~1年,其他药物多集中在半年内或1年以上。可见,DPP-4抑制剂导致皮肤ADE的涉及人群广泛,用药时应针对不同性别、年龄、用药剂量、用药时长给予同等关注,尤其注意65岁以上、用药半年内和1年以上人群。从临床结局来看,5种药物以患者需住院治疗或住院时间延长及其他严重后果为多,其次为死亡,危及生命、残疾等较少,表明DPP-4 抑制剂所致皮肤ADE 可对机体造成严重损害,临床应高度重视。目前,DPP-4 抑制剂所致皮肤ADE 的上报国家集中在欧美、日本等国,可能与药品主要在这些国家上市有关,是否存在地区和人种差异有待进一步研究。
需要指出的是,FAERS 中缺乏对患者病情的描述,故本研究中未考虑疾病本身对信号的影响,如患者原本可能患某种皮肤肿瘤或病变而行皮肤肿瘤切除术或皮肤手术,并非药物所致;FAERS 的漏报、报告偏倚等也可能会影响研究结果[22]。此外,数据挖掘出的信号是基于统计学特点而非生物学关联,不代表药物与ADE之间存在必然的因果联系,有待进一步分析[23]。
综上所述,本研究中利用数据挖掘方法对目前已上市的DPP-4 抑制剂进行了皮肤安全性问题的探讨,不仅可为DPP-4 抑制剂的合理使用提供数据支持,也可为进一步的安全性研究提供参考。
