脂肪乳氨基酸(17)葡萄糖(11%)注射液稳定性研究
2024-01-26杨培培张丽雯黄赵刚
杨培培,张丽雯,程 钢,黄赵刚
(安徽医科大学第一附属医院药剂科·国家中医药管理局中药化学三级实验室,安徽合肥 230022)
脂肪乳氨基酸(17)葡萄糖(11%)注射液(商品名卡文)为即用型预混式商品化肠外营养三腔袋[1],分别装有葡萄糖注射液、氨基酸注射液及脂肪乳注射液。使用前通过挤压混匀三者后,药品以胶体溶液、乳浊液的混合形式共存,属热力学不稳定体系,稳定性受电解质等添加物的影响[2-4]。由于处方中未添加维生素和微量元素,电解质含量也较少,故如长期给予卡文而不补充维生素,患者可能会因维生素B1缺乏而导致韦尼克脑病[5]。因此,临床使用过程中,医师常根据患者需要,在卡文中添加水溶性维生素、脂溶性维生素、氯化钾、浓氯化钠、多种微量元素等,但对卡文稳定性的影响尚未明晰。本研究中从pH、渗透压、微粒数、乳剂粒径等方面考察了卡文添加上述物质后的稳定性,为临床合理用药提供参考。现报道如下。
1 仪器与试药
1.1 仪器
Zetasizer Nano S90 激光纳米粒度分析仪(荷兰Malvern Panalytical 公司);GWF - 5JS 型微粒分析仪(天津天河分析仪器有限公司);SMC 30C 型渗透压摩尔浓度测定仪(天津斯格瑞科技有限公司);PHS-3E 型pH 计(上海仪电科学仪器有限公司)。
1.2 试药
脂肪乳氨基酸(17)葡萄糖(11%)注射液(国药准字J20130185,批号为10LI4747),注射用水溶性维生素(国药准字H32023002,批号为80MD50901),脂溶性维生素注射液(国药准字H32023138,批号为80MD56701),多种微量元素注射液(Ⅱ)(国药准字H32023907,批号为80LM557),均购自华瑞制药有限公司;氯化钾注射液(中国大冢制药有限公司,国药准字H20053710,批号为8G94K2);浓氯化钠注射液(湖北天圣康迪制药有限公司,国药准字H42020422,批号为20180608)。
2 方法与结果
2.1 待测样品制备
将卡文3 个腔室的液体混合,得样品S1;根据相容性等要求加入相应药品(其中加入氯化钾、氯化钠的量为依据卡文药品说明书可加入的最大量,多种微量元素量为该药品单日最大使用量;电解质加入时应及时分散,水溶性维生素与脂溶性维生素先混合),得样品S2-S5。待测样品信息见表1。

表1 待测样品信息Tab.1 Information of the samples to be tested
2.2 稳定性
各样品混匀,室温放置0,4,8,12 h 时肉眼观察均未见破乳、分层现象,表明混合液外观12 h内较稳定。
2.3 pH 及渗透压
取各样品适量,分别于室温下放置0,4,8,12 h 时测定pH及渗透压,详见表2(样品S1因在未加其他药品时很稳定,故未观察其4,8,12 h时的相应指标。
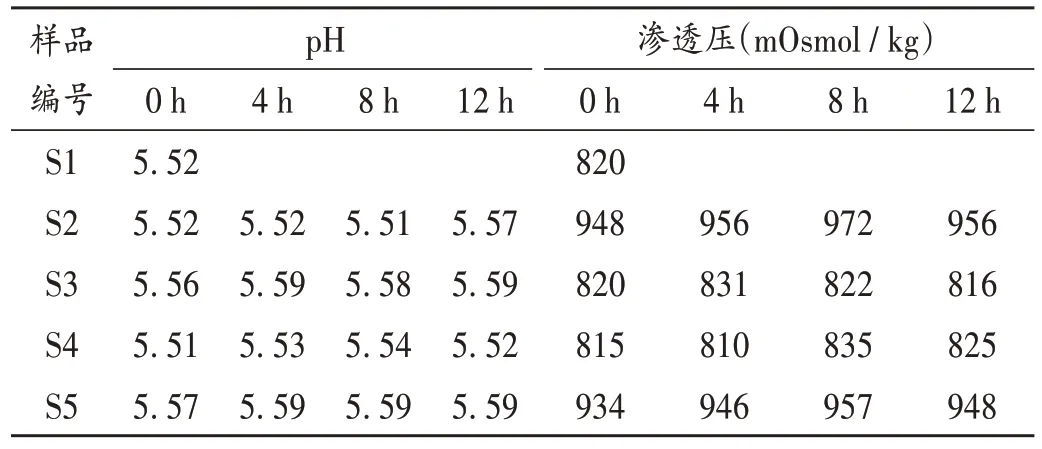
表2 样品室温放置12 h内的pH及渗透压(n=3)Tab.2 Results of pH and osmotic pressure determination of samples placed at room temperature for 12 h(n = 3)
2.4 微粒分析
分别于室温下放置0,4,8,12 h 时精密移取各样品10 mL,置100 mL 容量瓶中,用灭菌注射用水定容,混匀;取约50 mL,采用微粒分析仪分析(仪器自动测4次,取后3 次结果的平均值,且以1 mL 为单位计算),结果见表3。
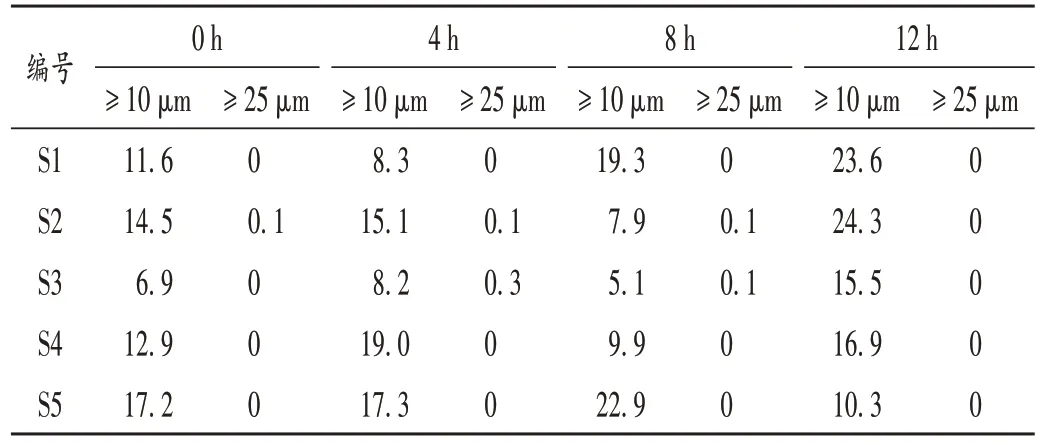
表3 样品室温放置12 h内微粒数(个,n=3)Tab.3 Results of particle number of samples placed at room temperature for 12 h(particle,n=3)
2.5 乳剂粒径分析
取样品S1和S5(因样品S5所加药品为S2-S4所加药品的总和,且实验条件有限,故认为样品S5的结果可反映S2 - S4 的结果)各约4 mL,分别于室温放置0,4,8,12 h 时以纳米粒度分析仪分析乳剂颗粒(见表4),结果粒径集中分布于1~10 nm,分布情况见图1。

图1 样品乳剂粒径分布图A.Sample S1 at 0 h B.Sample S1 at 12 h C.Sample S5 at 0 h D.Sample S5 at 12 hFig.1 Distribution of emulsion particle size of samples

表4 样品室温放置12 h内乳剂粒径(nm,n=3)Tab.4 Results of emulsion particle - size analysis of samples placed at room temperature for 12 h(nm,n=3)
3 讨论
实际应用中肠外营养液的pH 一般控制在5.4~6.5 之间[5-8],在此范围内肠外营养最稳定。本研究结果表明,各待测样品12 h 内pH 基本无变化,且均在要求范围内。肠外营养经外周静脉输入时,要求渗透压不大于900 mOsmol / kg;经中心静脉输入时,应不大于1 200 mOsmol / kg[9]。本研究结果显示,各待测样品12 h 内渗透压无明显变化,但电解质对渗透压影响较大,当加入电解质较多(氯化钠和氯化钾合计超过8 g)时,渗透压大于900 mOsmol / kg,建议经中心静脉输注。
不溶性微粒测定法有光阻法和显微计数法,光阻法较方便,但不适用于测定不澄明的液体[10]。有文献报道将肠外营养液用微粒检测用水稀释10 倍,用光阻法测定不溶性微粒[11]。因显微计数法操作烦琐,受主观影响较大,本研究中根据文献采用了稀释后光阻法。
脂肪乳颗粒的大小及分布是反映肠外营养液稳定性的重要指标,粒径大于5 µm 的脂肪颗粒对临床使用安全的影响较大[7,12],2020年版《中国药典(四部)》规定:静脉用乳状液型注射液中90%的乳滴粒径应小于1 μm,除另有规定外,不得有大于粒径5 μm 的乳滴。《美国药典》(USP)于2004年27 版起新增“静脉用脂肪乳粒径分布”规定:脂肪乳剂的平均粒径应小于0.5 μm,且粒径大于5 μm的百分比(PFAT5)应不超过0.05%。本研究结果显示,各待测样品的粒径集中分布在1~10 nm,分布范围较窄,说明样品粒径小且均一性好。文献报道依据个性化处方临时配制全合一肠外营养液的乳粒平均粒径约为300 nm[13-14],与本研究结果有较大差异,具体原因有待进一步研究。
综上所述,在卡文中加入规定限度内的电解质、维生素和多种微量元素,对其pH、微粒数、稳定性影响较小,但电解质对其渗透压影响较大,应予以重视。
