不同剂量利伐沙班在心房颤动导管消融术围手术期抗凝治疗中的应用观察
2024-01-17刘冰凌孙敬敏
刘冰凌,孙敬敏
心房颤动是临床常见的心血管疾病,主要表现为心率快而不规律,患者通常会出现眩晕、心悸、气短、胸部不适等症状。若不及时治疗会出现脑栓塞、心力衰竭等并发症,从而危及患者的生命安全[1]。相关流行病学调查显示[2],我国心房颤动的发病率约为0.77%,且随着年龄的增加而不断增加,这不仅对患者的生命安全造成了极大的威胁,也给患者家庭及社会造成了经济负担,因此如何有效防治其发生与发展已成为医学领域研究的重点课题之一。目前,临床上治疗心房颤动主要有药物治疗与非药物治疗。药物治疗并不能根治心房颤动,只能控制患者病情,但治疗效果不太理想。非药物治疗可达到根治的效果,故其为目前临床治疗心房颤动的首选方法[3]。导管消融术是近年来新兴的一种非药物治疗方式,治疗效果理想,且随着该术的不断发展及完善,其治疗心房颤动的成功率逐渐升高,在提高患者心功能、改善患者临床症状及生活质量、促进患者生存方面发挥了重要作用[4]。导管消融术的成功率较高,但作为有创治疗手段,其所引发的围手术期出血和栓塞等并发症并不能完全避免。相关数据显示[5],行导管消融术治疗的患者血栓栓塞的发生率为0.5%,由其引发的并发症发生率为0.5%,脑卒中的发生率为0.5%,这在一定程度上严重影响了患者的预后,故如何避免发生并发症是其面临的一大难题。近年来,相关研究发现[6],有效的抗凝治疗不仅可以提高导管消融术的治疗效果,还可最大限度地避免出血和栓塞风险,因此选择合理、有效的抗凝方案至关重要。目前,对于行导管消融术的患者,常用的抗凝药物为华法林,但其需要反复检测凝血指标,安全范围较小,且易与食物、药物等发生相互作用。不同于华法林,利伐沙班作为新型口服抗凝药物,其具有显著的抗凝作用。大量研究已证实[7-8],利伐沙班在防治血栓性疾病方面具有安全、有效等优势,故其越来越受到临床的关注及重视。但目前关于利伐沙班围手术期的用药策略尚无统一意见。基于此,本研究就不同剂量利伐沙班在心房颤动行导管消融术患者围手术期抗凝治疗中的临床疗效进行了研究与探讨,以期为临床治疗心房颤动提供参考。现报道如下。
1 资料和方法
1.1 一般资料
选取2019 年9 月~2022 年12 月期间于某院就诊的300 例心房颤动并行导管消融术的患者作为研究对象,按照随机数字表法分为利伐沙班低剂量组(LR 组)、中剂量组(MR 组)和高剂量组(HR组),每组100 例。LR 组:男性56 例,女性44 例;年龄46~74 岁,平均年龄(60.12±13.89)岁;病程51~119 个月,平均病程(85.12±33.89)个月;MR组:男性55 例,女性45 例;年龄45~75 岁,平均年龄(60.07±14.65)岁;病程55~123 个月,平均病程(88.47±33.95)个月;HR 组:男性54 例,女性46 例;年龄47~75 岁,平均年龄(60.91±13.96)岁;病程52~120 个月,平均病程(86.58±33.92)个月。三组患者一般资料比较均无统计学差异(P>0.05),具有可比性(表1)。本研究经医院伦理委员会审批通过,所有患者均知情并签署知情同意书。
表1 两组患者一般资料比较 n=100,±s,n(%)
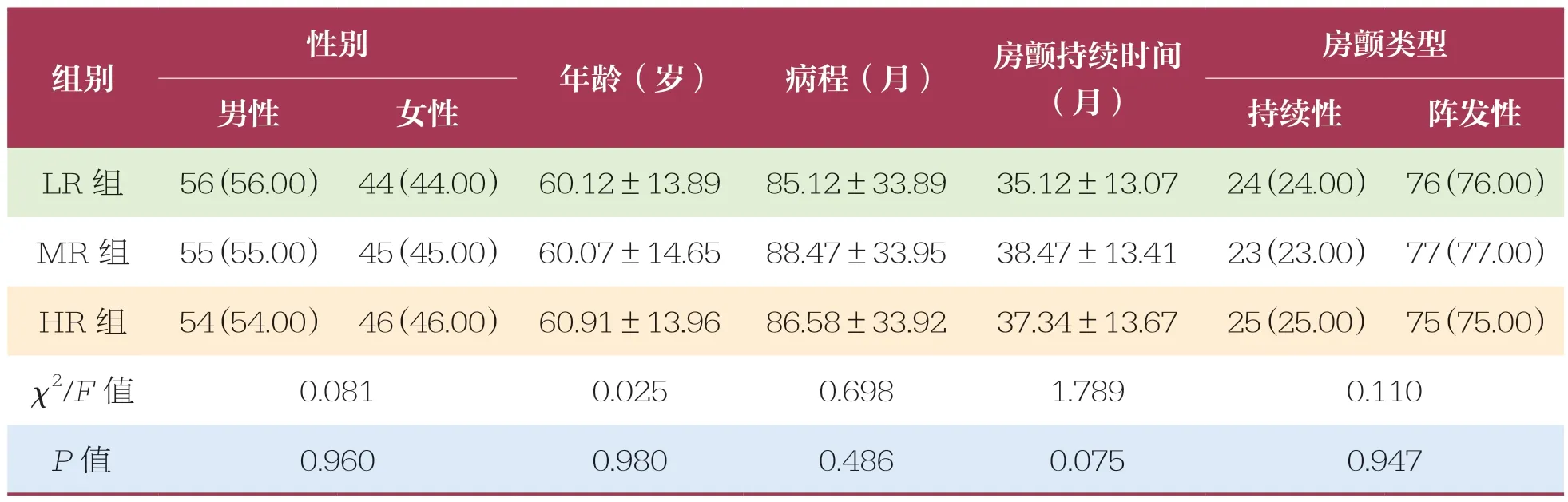
表1 两组患者一般资料比较 n=100,±s,n(%)
房颤类型男性女性持续性阵发性LR 组56(56.00) 44(44.00) 60.12±13.89 85.12±33.8935.12±13.0724(24.00) 76(76.00)MR 组55(55.00) 45(45.00) 60.07±14.65 88.47±33.9538.47±13.4123(23.00) 77(77.00)HR 组54(54.00) 46(46.00) 60.91±13.96 86.58±33.9237.34±13.6725(25.00) 75(75.00)χ2/F 值0.0810.0250.6981.7890.110 P 值0.9600.9800.4860.0750.947性别组别年龄(岁)病程(月)房颤持续时间(月)
纳入标准:①经心脏彩色多普勒超声检查确诊为心房颤动且行导管消融术者。②临床资料完整者。③年龄18~80 岁者。④无治疗禁忌症者。
排除标准:①严重心、肝、肾、消化功能不全者。②合并恶性肿瘤者。③导管消融术后未转复为窦性心律者。④合并精神性疾病或表达能力欠缺者。⑤合并心脏瓣膜病史或左心房血栓者。⑥哺乳期、妊娠期妇女。
1.2 治疗方法
三组患者均行导管消融术治疗。患者入院后,首先皮下注射低分子量肝素钙注射液(河北常山生化药业股份有限公司,国药准字H20063910,规格0.4ml∶4100AXaIU)5~10 天,注射剂量为0.5mg/kg,qd,术前8~12h 停用。当国际标准化比值(intemational normalized ration,INR)<1.5 时行导管消融术治疗,术前1~2 天行经食道心脏超声检查排除心房及心耳内血栓。消融参数:消融预设温度为43℃,冷盐水流速17~30ml/min,功率35~50W,10s 内室速/室早消失为有效消融。巩固消融60~90s 后观察3min,如果上述部位均消融无效,且冠状静脉窦内激动标测满意,则在冠状静脉窦内试消融,消融预设温度为43℃,功率10~25W,冷盐水流速30ml/min。术后,LR 组口服利伐沙班片(Bayer AG,国药准字HJ20181081,规格10mg)10mg,qd;MR 组口服利伐沙班片20mg,qd;HR 组口服利伐沙班片15mg,bid,三组均连续治疗6 个月。
1.3 观察指标
(1)INR 比较:分别于治疗前后采集患者静脉血3ml,采用Coatron 5000 全自动凝血分析仪(北京美德美康生物技术有限公司)检测患者INR 水平。
(2)出血情况比较:观察并记录三组患者治疗后的出血情况。①轻度出血:出血量<750ml。②中度出血:出血量750~1500ml。③重度出血:出血量>1500ml。
(3)出血事件发生情况:观察并记录三组患者鼻出血、牙龈出血及结膜出血等出血事件的发生情况。
(4)血栓栓塞事件发生情况:观察并记录三组患者死亡、脑栓塞、肺栓塞、体循环栓塞等血栓栓塞事件的发生情况。
(5)不良反应发生情况:观察并记录三组患者治疗期间头晕、短暂性缺血、缺血性肠病、缺血性脑病等不良反应的发生情况。
1.4 统计学方法
应用GraphPad Prism 8.0 软件对数据进行统计分析。计量资料以±s表示,多组间比较采用单因素方差分析,两两比较采用LSD-t检验;计数资料以n(%)表示,采用χ2检验。P<0.05 为具有统计学差异。
2 结果
2.1 治疗前后三组患者INR 比较
治疗前,三组患者INR 比较无统计学差异(P>0.05);治疗后,三组患者INR 均升高(P<0.05),且HR 组高于LR 组和MR 组(P<0.05)(表2)。
表2 治疗前后三组患者INR 比较 n=100,±s

表2 治疗前后三组患者INR 比较 n=100,±s
与同组治疗前比较,a:P﹤0.05;与LR 组比较,b:P﹤0.05;与MR 组比较,c:P﹤0.05
组别INR治疗前治疗后LR 组1.51±0.151.82±0.22a MR 组1.48±0.132.14±0.28ab HR 组1.50±0.142.49±0.33abc F 值1.5118.986 P 值0.132<0.001
2.2 三组患者出血情况结果比较
HR 组患者总出血率低于LR 组和MR 组(P<0.05)(表3)。

表3 三组患者出血情况比较 n=100,n(%)
2.3 三组患者出血事件发生情况比较
HR 组患者出血事件总发生率低于LR 组和MR 组(P<0.05)(表4)。
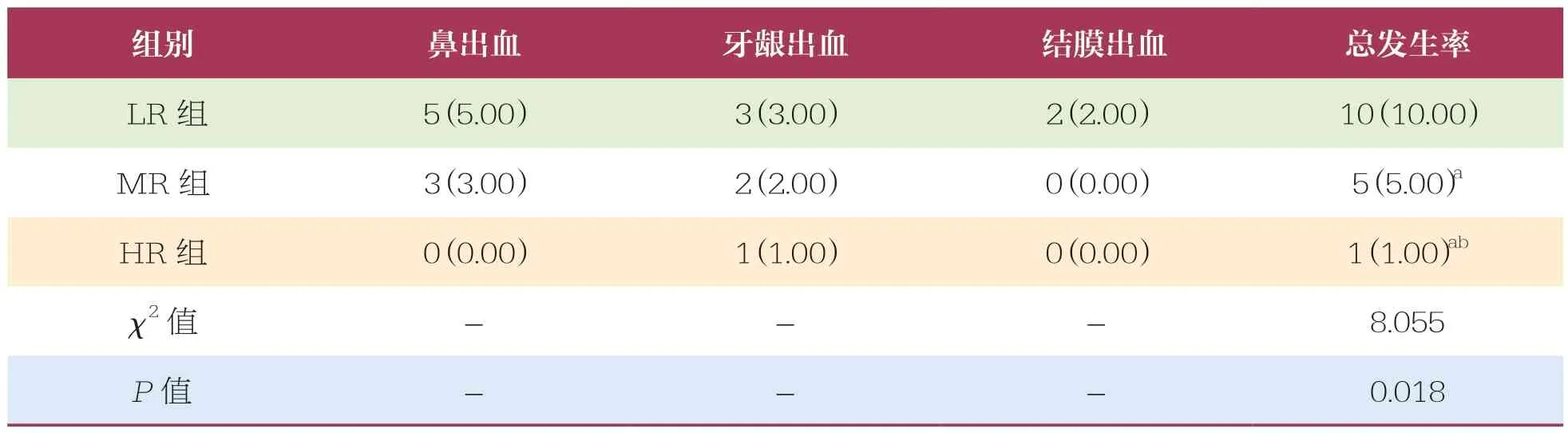
表4 三组患者出血事件发生情况比较 n=100,n(%)
2.4 三组患者血栓栓塞事件发生情况比较
HR 组患者血栓栓塞事件总发生率低于LR 组和MR 组(P<0.05)(表5)。

表5 三组患者血栓栓塞事件发生情况比较 n=100,n(%)
2.5 三组患者不良反应发生情况比较
HR 组患者不良反应总发生率低于LR 组和MR 组,无统计学差异(P>0.05)(表6)。

表6 三组患者不良反应发生情况比较 n=100,n(%)
3 讨论
心房颤动是一种临床常见的心律失常,已成为影响患者生命安全的公共健康问题[9]。心房颤动不仅严重影响了患者的生活质量,其所引发的脑卒中及血栓栓塞等并发症更是导致患者残疾、死亡的主要原因,因此对其开展及时有效的治疗尤为重要[10]。目前,临床对于心房颤动患者主要给予导管消融术治疗,其具有良好的治愈率,但术后患者可能会出现出血或血栓栓塞事件,故抗凝治疗成为导管消融术的重要环节。对于心房颤动行导管消融术的患者,目前国内外心房颤动诊治指南均主张术后一定时间内或者长期进行抗凝治疗[11]。
2012 年美国心律学会/欧洲心律学会/欧洲心律失常学会关于经导管消融术治疗心房颤动的专家共识推荐[12],所有患者在导管消融术后需要常规使用华法林至少2 个月。华法林是一种双香豆素类抗凝剂,具有良好的抗凝作用,但其在使用过程中需要监测INR,使其控制在2.0~3.0,这就导致患者的依从性较差,从而影响了导管消融术的治疗效果[13]。因此,探寻一种新型、有效且患者依从性良好的抗凝药物是目前临床关注的焦点之一,这对患者的疾病治疗以及术后康复效果均具有重要意义[14]。利伐沙班是一种新型抗凝药物,具有高选择性,可通过特异性抑制凝血因子Xa 阻断内源性及外源性凝血途径,并抑制凝血酶的产生、形成和凝血级联反应,进而发挥抗凝作用。此外,使用利伐沙班过程中不需要抗凝血酶Ⅱ/Ⅲ等辅助治疗,故无需监测凝血指标,也不需要频繁调整用药剂量,临床应用较为方便,且患者用药依从性也较好[15]。利伐沙班起效较快、吸收良好、生物利用度较高,与食物、药物几乎不发生相互作用,且安全性较高,近年来已逐渐应用于临床[16]。而在心房颤动行导管消融术患者围手术期抗凝治疗中,选择利伐沙班合适的剂量对于保证患者的安全和临床疗效至关重要。基于此,本研究就不同剂量利伐沙班在心房颤动行导管消融术患者围手术期抗凝治疗中的临床疗效进行观察探讨。利伐沙班安全使用范围为10~30mg/d,且呈剂量依赖性。因此,本研究以利伐沙班剂量10~30mg/d 进行研究探讨,结果显示,治疗后三组患者INR 均升高(P<0.05),且HR组高于LR组和MR组(P<0.05);HR 组患者总出血率、出血事件总发生率、血栓栓塞事件总发生率均低于LR 组和HR 组(P<0.05);HR 组患者不良反应总发生率低于LR 组和MR 组,但三组比较无统计学差异(P>0.05)。本研究结果提示利伐沙班具有良好的有效性及安全性,且药效呈剂量依赖性,利伐沙班30mg/d 剂量组的抗凝效果较10mg/d 和20mg/d 剂量组更佳,在临床抗凝治疗中具有一定优势。此外,相关研究显示[17],对于心房颤动行导管消融术患者,术后接受利伐沙班抗凝治疗可显著改善患者出血及血栓栓塞情况,并降低不良反应发生率;另一研究显示[18],利伐沙班具有显著的抗凝有效性及安全性,心房颤动行导管消融术患者围手术期服用利伐沙班,可有效降低患者出血及并发症的发生风险,可作为围手术期华法林抗凝治疗的替代选择,这与本研究结果相符。
心房颤动行导管消融术的患者在围手术期发生血栓栓塞的风险较高,推测原因为:①消融设备会与血液发生异物接触。②在导管消融术的过程中会有血栓性成分释放,如血小板聚集或纤维蛋白形成。③消融热量会在一定程度上导致左心房内皮损伤及炎症反应。④心房颤动转换为窦性心律后血流动力学出现改变。这些原因都会激活内源性及外源性凝血系统,从而导致凝血及抗凝失衡,引发血栓[19]。相关研究表明[20],在围手术期对行导管消融术的心房颤动患者进行抗凝治疗可降低血栓栓塞等并发症的发生风险,且不会增加出血风险。利伐沙班主要通过选择性抑制凝血因子Xa 来发挥抗凝效果,这一机制使得利伐沙班较华法林使用更加方便和可控,且具有更稳定的抗凝效果[21]。本研究结果提示高剂量利伐沙班较中剂量和低剂量可更有效地发挥抗凝作用,推测利伐沙班呈剂量依赖性的原因为:①利伐沙班与凝血因子Xa 结合后,可长时间抑制其活性,而利伐沙班30mg/d 剂量的抑制作用更强,从而产生更强的抗凝效果。②根据药动学研究,利伐沙班的吸收、分布和消除过程呈剂量依赖性,30mg/d剂量的利伐沙班可提供更高的药物浓度,使得抗凝效果更明显。③应用30mg/d 剂量的利伐沙班,可降低血栓形成的风险,特别是在围手术期。但需要注意的是,剂量选择应考虑患者的个体特征、手术类型和风险评估结果。过高的剂量可能会增加患者出血风险,而过低的剂量可能无法达到预期的抗凝效果。因此,在实际应用中,还需综合考虑多种因素来确定利伐沙班的最佳使用剂量。
综上所述,利伐沙班对心房颤动行导管消融术围手术期的患者具有显著的抗凝效果,且呈剂量依赖性,可有效减少患者出血情况及不良反应的发生情况。然而,本研究仍存在一定局限性,如纳入的样本量较少且为单中心研究,今后将开展多中心、大样本的研究以进一步为临床治疗心房颤动提供更多、更有利的依据。
