碳氢燃料热解气再燃还原NO的化学动力学研究
2024-01-16王明睿沈天祺李东升陆海洋贾鑫
王明睿,沈天祺,李东升,陆海洋,贾鑫
(沈阳化工大学 资源化工与材料教育部重点实验室,辽宁 沈阳 110142)
目前随着环境污染愈加严重,污染物的排放标准也随之愈加严格,并成为亟待解决的问题,而氮氧化物(NOx)作为大气污染物之一,主要来源于人类的工业生产活动。与SO2的减排情况相比,NOx的排放量改善状况较差,“十三五”期间,我国大气中的NO2降低速率与大气中SO2浓度的改善速度差异明显[1-2]。因此,应给予氮氧化物减排问题足够的关注和重视。
选择性催化还原(SCR)技术是目前技术最成熟且被世界各国广泛应用的脱硝手段[3],但也存在催化剂中毒等限制因素[4]。因此,在碳氢燃料燃烧过程中产生的H2、CO、CH4和NH3等还原气体的脱硝也是研究热点之一。ALZUETA 等[5]采用柱塞流反应器研究了碳氢类气体再燃还原NO 的反应特性,发现温度及过量空气系数是影响NOx还原的主要因素。FAN[6]等研究了生物质中再燃的热解气对NO的还原特性,发现热解气中较高比例的CH4有利于降低NO 的还原效率,而较高比例的H2和CO 则不利于NO 的还原。王义德[7]等采用CHEMKIN-PRO和Leeds 综合机理模拟研究了含硫天然气还原NO的反应特性,发现CH4浓度的增加会使NO 还原率升高,且停留时间对反应进行程度会造成较大影响。
本文采用化学动力学软件CHEMKIN-PRO 和Shrestha 综合机理[8],模拟研究了反应温度、还原气体体积分数、过量空气系数和停留时间对还原性气体H2、CO、CH4和NH3还原NO 的影响规律,能够为碳氢燃料再燃脱硝的工业应用提供一定参考。
1 计算模型与理论
1.1 数值计算模型
在还原性气体再燃还原NO 的研究过程中,选择CHEMKIN-PRO 中自带的柱塞流模型进行计算。图1 为模拟过程中所建立的反应模型。
图1 反应模型示意图
PFR 模型用于模拟绝热封闭系统下的化学反应,其主要控制方程如下[7]。
质量方程:
动量方程:
气体组分方程:
气体状态方程:
式中:u—气体在反应器中的纵向速度,m·s-1;
A—垂直流动方向的横截面积,m2;
p—气体绝对压力,Pa;
F—反应器内壁和气体间的摩擦阻力,N;
Yk—组分k 的质量分数,%;

W¯—气体平均相对分子质量。
1.2 化学反应机理
还原性气体H2、CO、CH4和NH3还原NO 过程涉及碳氢类化合物、含氮物质及中间活性自由基的相互反应。为准确模拟该过程,采用SHRESTHA[8-10]等提出的SHRESTHA 综合机理,该机理含有C、H、O、N 元素,含有135 种组分和1 127 种基元反应。
根据学者研究[11-12],一般认为在无氧条件下NO在中等温度下与H2通过以下反应途径被去除:
在有氧气存在的情况下,自由基池会积累到更高的水平,使得速率较慢的反应(5)和反应(6)变得不再是主要脱硝途径,而是通过以下的途径:
所以,在考虑反应速率的情况下,H2还原NO的主要途径为:H+NO→HNO→NH→N2。
在一定的高温条件下,NO 也可能与H 自由基或者H2直接反应而被还原,但速率较为缓慢。
一般来说,在没有H 自由基参与的情况下,CO还原NO 的途径如下[13-14]:
提高温度有助于增强反应(12)和反应(13)的正向反应,然而反应(14)十分缓慢,在没有H自由基参与时,可能会重新产生NO,导致NO 的还原速率降低。
与H2类似,在一定条件的高温下,NO 可以被CO 直接还原,从而产生NO→N→N2的反应途径。
在对于CH4还原NO 的机理研究中,普遍认为CH4不直接与NO 反应,而是先通过氧化反应生成活性较高的CH3、CH2和CH 自由基[6,15],然后通过以下途径还原NO。
根据梁秀进[16-18]等的研究表明,在NH3为还原剂的脱硝过程中,主要反应如下:
NH3也会和H、OH 和O 等自由基反应生成NH2以实现对NO 的还原。
1.3 数值计算工况
本文柱塞流模型尺寸与ALZUETA[5]等在试验和数值模拟中所用相同,长度和内径分别为19 cm(模拟停留时间的影响时会适当增长)和9 mm。反应组分包括还原性气体(H2、CO、CH4和NH3)、氧化剂(O2)和载气(Ar)。在所有模拟工况中,保持反应气流量为1 200 mL·min-1(标态1.01×105Pa、273.15 K)不变,反应气的停留时间取决于反应温度,具体模拟工况详见表1。在停留时间的研究中,保持反应气流量和温度不变,在反应器长度方向不同位置采样,由位置计算得出相应的停留时间。
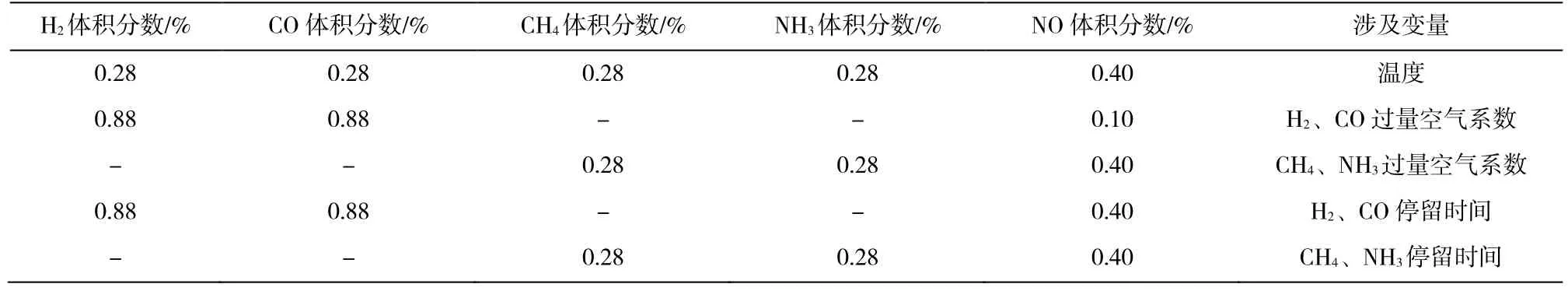
表1 数值模拟基础工况
2 结果与分析
2.1 温度对还原性气体还原NO 的影响
反应温度是影响还原性气体脱硝效率的重要影响因素之一,不同的还原性气体在不同的温度区间,其脱硝效率并不相同,即存在最佳的反应温度区间,使其能耗比最大化。图2 为H2、CO、CH4、NH3体积分数都为0.28%、NO 体积分数为0.40%时,温度在600~1 600 ℃区间内,反应器出口的NO还原率。
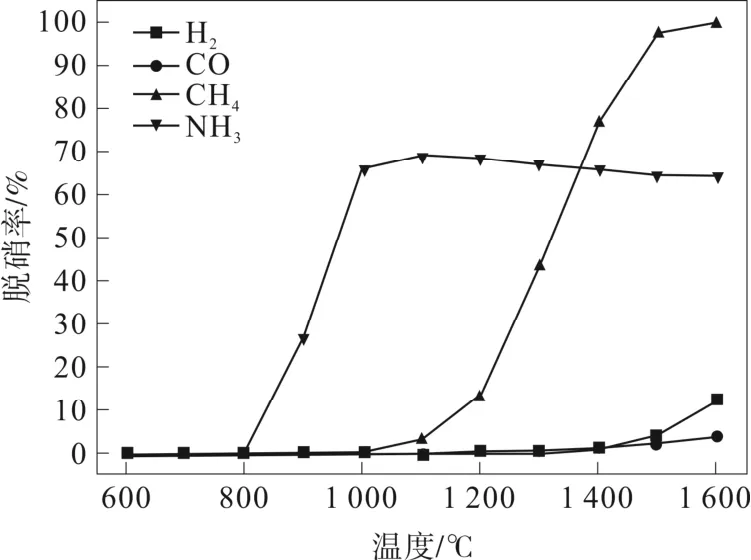
图2 温度对还原性气体还原NO 的影响
由图2 可知,在当前工况下,600~800 ℃时,各种还原性气体只发生微弱的还原反应。而在反应温度900~1 000 ℃时,NH3对NO 的还原率迅速增加,并随着温度的增加趋于平缓,最高值为69.28%,这说明NH3相较于H2、CO、CH4进行NO 还原反应时所需的反应温度相对较低,且过高的反应温度并不能增加NH3的脱硝率。而在1 100 ℃和更高温度时,CH4对NO 的还原率开始迅速增加,最高值为99.09%,且在1 350 ℃附近,其脱硝率高于NH3,说明在较高温度下,CH4对NO 的还原率与NH3相近甚至更高。在600~1 400 ℃时,H2和CO 脱硝效率相近,而在更高温度时,H2的脱硝率要高于CO,两者在当前工况下 NO 还原率的最高值分别为12.34%和3.79%,即H2和CO 对NO 的还原率要低于CH4和NH3。
2.2 体积分数对还原性气体还原NO 的影响
还原性气体的体积分数也是对NO 还原率的重要影响因素之一,但是由于反应速率的不同,不同还原性气体体积分数的增加对脱硝效率的影响也不相同。图3(a)为H2和CO 在1 600 ℃下体积分数在0.04%~0.88%以及NO 体积分数为0.40%时,NO还原率的变化。图3(b)为CH4和NH3在1 200 ℃下体积分数在0.04%~0.88%以及NO 体积分数为0.40%时,NO 还原率的变化。
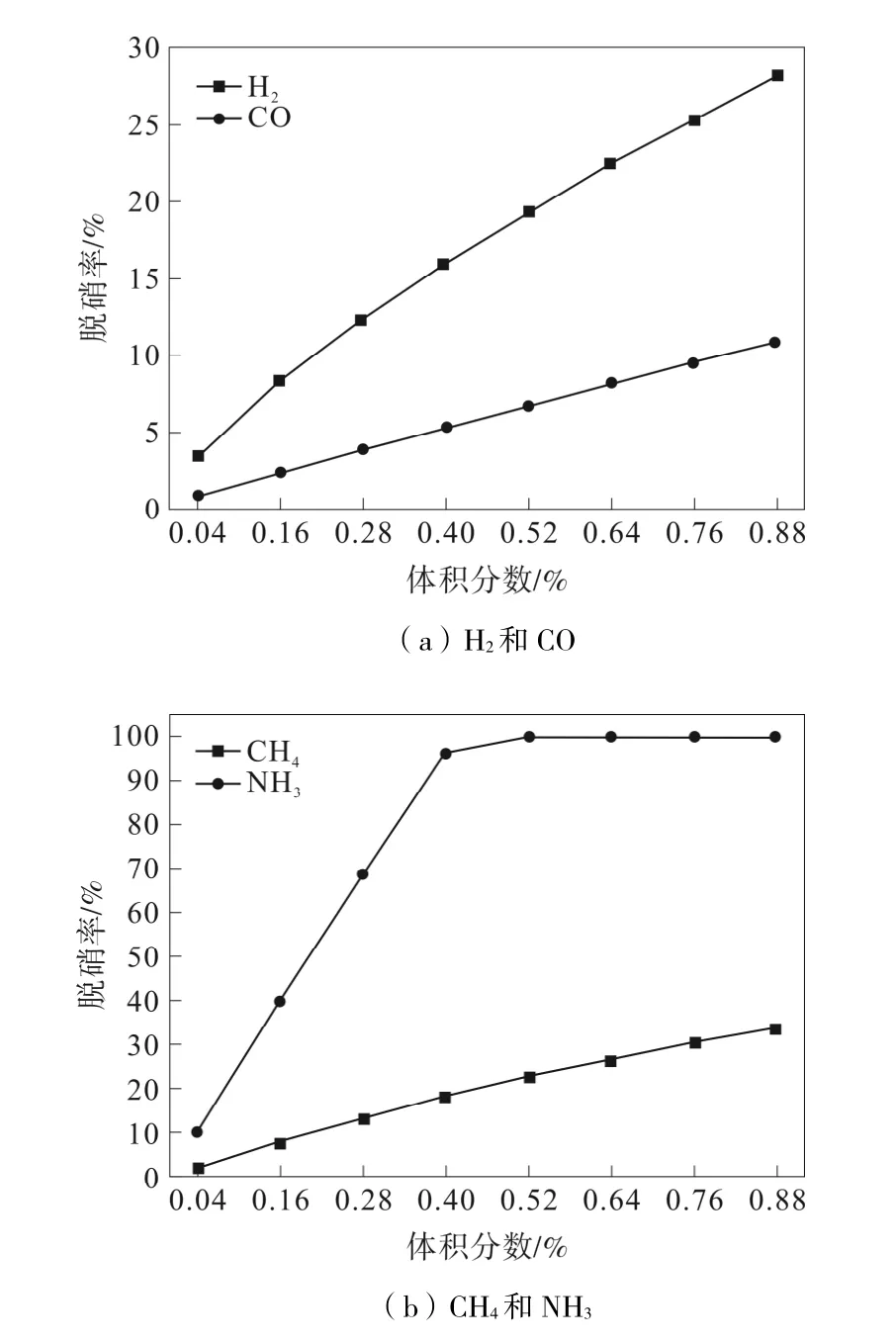
图3 体积分数对还原性气体还原NO 的影响
由图3 可知,随着还原性气体体积分数的增加,NO 还原率也在逐渐增加,这是由于还原性气体体积分数的增加可以生成更多的还原性基团。随着H2和CO 体积分数的增加,NO 的还原率逐渐增加,H2对NO 的还原率随着其体积分数的增加相对CO增加较快,说明在较高温度下,H2体积分数对NO还原率的影响比CO 更大。
随着CH4和NH3体积分数的增加,NO 的还原率逐渐增加,NH3对NO 的还原率随着其体积分数的增加相对CH4增加较快,说明在当前温度下,NH3体积分数对NO 还原率的影响比CH4更大。
2.3 过量空气系数对还原性气体还原NO 的影响
当还原性气体体积分数保持不变时,过量空气系数的改变直接反映为O2的浓度值,O2对还原性分子及基团的转化有较大影响,进而影响NO 的还原效率。图4(a)为H2和CO 在1 200 ℃下,过量空气系数为0~1.2、NO 体积分数为0.10%时,NO 还原率的变化。图4(b)为CH4和NH3在1 200 ℃下,过量空气系数为0~1.2、NO 体积分数为0.40%时,NO 还原率的变化。
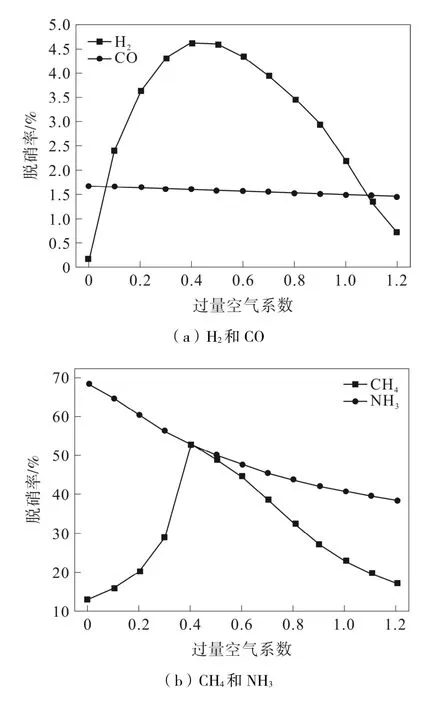
图4 过量空气系数对还原性气体还原NO 的影响
由图4(a)可知,随着过量空气系数的增加,H2对NO 的还原率先增加后降低,并在过量空气系数为0.4 时达到最高值4.62%,说明在不同的工况下,存在最佳当量比使H2对NO 的还原率达到最高,即一定量的O2对H2还原NO 的反应具有促进作用。而随着过量空气系数的增加,CO 对NO 的还原率则逐渐降低,可能是O2与CO 生成CO2的反应与CO还原NO 的反应存在竞争关系,且CO2可能会抑制CO 对NO 的还原[19]。
由图4(b)可知,随着过量空气系数的增加,CH4对NO 的还原率先增加后降低,并在过量空气系数为0.4 时达到最高值53.09%,说明在不同的工况下,存在最佳当量比使CH4对NO 的还原率达到最高,即一定量的O2对CH4还原NO 的反应具有促进作用。而随着过量空气系数的增加,NH3对NO的还原率则逐渐降低,可能是O2与NH3生成H2O的反应与NH3还原NO 的反应存在竞争关系,且O2与NH3反应也会重新生成一部分NO,导致脱硝效率的降低。
2.4 停留时间对还原性气体还原NO 的影响
不同的化学反应需要不同的反应时间,不同气体在反应器中的停留时间是决定反应进行程度的重要因素,要保证反应气充分反应就需要有足够的停留时间。为了探究停留时间对还原性气体还原NO的影响,本文统计了在不同温度的工况下,还原性气体H2、CO、CH4、NH3对NO 还原率随停留时间变化的数据,具体结果如图5 所示。

图5 停留时间对还原性气体还原NO 的影响
气体在反应器内的停留时间与反应器长度有关,为了更直观地观察到停留时间对反应进行程度的影响,将反应器加长以增加停留时间(模拟H2和CO与NO 的反应时增长至500 cm,模拟CH4和NH3与NO 的反应时增长至120 cm)。图5(a)为H2体积分数0.88%、NO 体积分数0.40%、1 400~1 600 ℃时NO 还原率随停留时间的变化。随着停留时间的增加,NO 还原率逐渐升高,在1 400 ℃升高速率较为缓慢,而温度提高后H2对NO 的还原速率也迅速增加。在1 600 ℃时,NO 还原率在0~1.2 s 内迅速增加,之后曲线则趋于平缓。这说明充足的停留时间可以增加H2对NO 的还原率,温度越高时反应完全发生所需的停留时间越短,而当达到一定温度后,过长的停留时间并不能明显增加H2对NO 的还原率。同时,由于气体体积随温度膨胀,温度越高时在相同长度的反应器中气体的停留时间越短。
图5(b)为CO 体积分数0.88%、NO 体积分数0.40%、14 00~1 600 ℃时NO 还原率随停留时间的变化。
与H2类似,随着停留时间的增加,NO 还原率逐渐升高,而温度提高后CO 对NO 的还原速率也迅速增加。但相较于H2,反应温度的增加并没有明显提升CO 的脱硝效率。
图5(c)为CH4体积分数0.28%、NO 体积分数0.40%、1 200~1 400 ℃时NO 还原率随停留时间的变化。同样,随着停留时间的增加,NO 还原率逐渐升高,在还原率达到一定程度后逐渐平缓,温度越高时曲线达到平缓所需的停留时间逐渐减少,且在1 200 ℃提升至1 300 ℃时较为明显。这说明反应温度由1 200 ℃提升至1 300 ℃时,CH4对NO的还原速率提升明显。
图5(d)为NH3体积分数0.28%、NO 体积分数0.40%、900 ℃和1 000 ℃时NO 还原率随停留时间的变化。与CH4类似,随着停留时间的增加,NO 还原率逐渐升高,在还原率达到一定程度后逐渐平缓,在反应温度由900 ℃提升至1 000 ℃时,曲线达到平缓所需的停留时间明显减少。这说明反应温度由900 ℃提升至1 000 ℃时,NH3对NO 的还原速率提升明显。
3 结 论
采用化学动力学软件 CHEMKIN-PRO 和Shrestha 综合机理,模拟研究了反应温度、还原气体体积分数、过量空气系数和停留时间对还原性气体H2、CO、CH4和NH3还原NO 的影响规律,得到主要结论如下:
1)随着反应温度的增加,H2、CO、CH4和NH3对NO 的还原率升高。在模拟工况中,较高温度下,相同体积分数的H2对NO 的还原率要高于CO、低于CH4和NH3。
2)随着H2、CO、CH4和NH3体积分数的增加,对NO 的还原率也随之升高。在模拟工况中脱硝效率越高的气体,其受到体积分数增加所提升的对NO还原率也越高。
3)适当的增加过量空气系数可以对H2和CH4还原NO 起到促进作用,即存在最佳当量比使H2和CH4对NO 的还原率达到最高。但是过量空气系数的增加可能会对CO 和NH3还原NO 的反应起到抑制效果。
4)适当的增加停留时间,可以使反应更加完全以增加H2、CO、CH4和NH3对NO 还原率,温度越高时反应完全发生所需的停留时间越短。
