高锰酸钾改性秸秆生物质炭及对氨氮的吸附研究
2024-01-16李佳利解鹤晁婧马有良
李佳利,解鹤,晁婧,马有良
(宁夏理工学院 理学与化学工程学院,宁夏 石嘴山 753000)
目前处理水体中的氨氮方法有很多,比如生物法、化学沉淀法、吸附法等。与其他方法相比吸附法具有操作简单,不会带来二次污染等优点而被广泛研究[1]。生物质资源具有来源广泛、价格低廉、可再生等优势,但大部分的生物质资源只是被简单的掩埋或焚烧,未能实现废弃生物质的有效资源化利用[2]。而将生物质缺氧热解得到生物质炭由于其孔隙结构丰富,比表面积较大,含氧官能团较多,对污染物的吸附十分有利。生物质原料的不同使得生物炭的元素组成、比表面积,孔结构和官能团也会不同,影响生物炭的吸附性能[3]。一般情况下,结构致密的生物质前体,不利于孔径结构的有效调控,而对于含碳量较高的生物质前体,在碳化/活化过程中非常有利于形成相互连接的微/介孔结构或含N/S/O 的表面官能团,这将大大增强生物炭材料的吸附性能[4]。生物炭的主要来源是生物质热解。热解是将生物质转化为多孔碳材料等增值产品的整个过程的核心,是生物炭制备的常用方法[5]。随着温度的升高,生物炭产量降低,合成气产量增加[6]。生物炭材料表面含氧官能团的增加可增强电子给体-受体相互作用,进而有利于含有氨基、双碳键、苯环或其他可作为电子供体基团的PPCPs的吸附[7]。本文使用玉米秸秆为生物质原料,采用高锰酸钾为改性剂制备改性生物质炭,用于水体中氨氮的吸附性能研究。
1 材料与方法
1.1 试剂与仪器
玉米秸秆,宁夏石嘴山市某农场;氯化铵(AR)、氢氧化钠(AR)、高锰酸钾(AR)、双氧水(AR)、酒石酸钾钠(AR)、二氯化汞(AR)、碘化钾(AR)、盐酸(AR)。
管式炉(OTF-1200X),合肥科晶材料技术有限公司;紫外-可见分光光度计(UV775B 型),上海佑科仪器仪表有限公司;傅里叶红外光谱仪(Thermo Scientific Nicolet iS50)美国赛默飞科技有限公司;扫描电子显微镜(Zeiss Sigma 300),卡尔蔡司管理有限公司(上海);BET 比表面积仪(ASAP2020),麦克莫瑞提克仪器有限公司(上海)。
1.2 KMnO4改性生物质炭的制备
1.2.1 生物质浸渍改性
将采集来的新鲜玉米秸秆和叶片分离,清洗、干燥、粉碎过60 目(250μm)筛备用。分别称量两份10 g KMnO4于250 mL 烧杯中,加入去离子水搅拌溶解,配置成质量分数为5%的高锰酸钾水溶液;再分别称取20 g 上述处理好的玉米秸秆粉末和玉米叶片粉末,加入高锰酸钾溶液中,在室温下浸渍24 h。将浸渍好的样品抽滤后,置于表面皿上,在鼓风干燥箱中100 ℃进行干燥8 h,取出、研磨备用。
1.2.2 生物质炭的制备
将浸渍改性处理好的两个样品粉末分别置于石英瓷舟内,在管式炉N2氛围中,按照5 ℃/min 的升温速率,升温至500 ℃,保温时间为3 h。再将得到的碳化物置于马弗炉中,400 ℃空气中加热15 min,以去除热解过程中产生的滞留沉积物,从而产生“扩孔”的效果[8]。将加热后的生物质炭用30%H2O2进行清洗,去除生物质表面的灰分后,置于烘箱中80℃干燥12 h。将处理好的改性玉米秸秆生物质炭命名为Mn-BC-1,将处理好的改性玉米叶片生物质炭命名Mn-BC-2。
1.3 生物质炭的表征
微观结构表征采用扫描电子显微镜(Zeiss Sigma 300)测定;生物质炭表面官能团分布采用傅里叶红外光谱仪(Thermo Scientific Nicolet iS50);比表面积和孔隙结构的测定采用比表面积、孔径分析仪(ASAP2460)测定。
1.4 吸附实验
1.4.1 吸附动力学实验
将上述制备的两种生物质炭样品分别称取0.5 g 至1 L 烧杯中,加入500 mL 氨氮浓度为50 mg/L的NH4Cl 溶液中。在25 ℃的水浴中,恒温避光振荡,分别在0、5、10、20、30、40、50、60、70、80、90 和100 min 时取上清液,用0.45 μm 滤膜过滤,用纳氏分光光度法测量氨氮吸光度。
1.4.2 等温吸附实验
将上述制备的两种生物质炭样品分别称取0.05 g 至100 mL 锥形瓶中,加入氨氮质量浓度分别为0、5、10、20、30、40、50 和60 mg/L 的NH4Cl 溶液,在25 ℃的水浴中,恒温避光振荡24 h,待达到吸附平衡后取上清液,用0.45μm 滤膜过滤,用纳氏分光光度法测量氨氮吸光度。
1.5 数据处理
氨氮吸附量计算:
吸附动力学数据分别用准一级动力学模型(2)和准二级动力学模型(3)进行拟合。
等温吸附数据分别用Langmuir 等温吸附模型(4)和Freundlich 等温吸附模型(5)进行拟合。
式中:qe—吸附达平衡时的吸附量,mg·g-1;
qt—t时刻的吸附量,mg·g-1;
c0、ct—分别为初始时刻和t时刻氨氮的浓度,mg·L-1;
V—溶液的体积,L;
m—吸附剂Mn-BC 的质量,g;
k1—准一级动力学吸附速率常数,min-1;
k2—准二级动力学吸附速率常数,g·(mg·min)-1;
t—吸附时间,min。
qm—单层理论极限吸附量,mg·g-1;
kL—Langmuir 吸附常数;
Ce—吸附平衡时的浓度,mg·L-1;
kF—Freundlich 常数,g·(mg·min)-1;
n—组分因子。
2 结果与讨论
2.1 Mn-BC 的表征分析
2.1.1 扫描电镜分析
图1 为Mn-BC-1(a)、(b),Mn-BC-2(c)、(d)的SEM 图。

图1 Mn-BC-1(a)、(b),Mn-BC-2(c)、(d)的SEM 图
从图1 中可以看出使用玉米秸秆为原料的生物质炭和使用玉米叶片为原料的生物质炭的形貌有很大的差距。玉米秸秆生物质炭木质素较多,微观结构以长孔道为主,高温煅烧使KMnO4改性致使孔道部分坍塌,改性粒子主要附着在孔道外壁。玉米叶片生物质炭纤维素较多,其微观结构出现平面蜂窝状,且大量改性粒子分散在蜂窝结构内外。改性面积较大,生物质炭孔隙度增加,改性粒子分布广泛且均匀,呈现出疏松多孔的海绵状。
2.1.2 红外光谱分析
图2 为Mn-BC-1 和Mn-BC-2 的红外光谱图。

图2 Mn-BC-1 和Mn-BC-2 的红外光谱图
Mn-BC-1 和Mn-BC-2 在3 423 cm-1和3 325 cm-1处的宽频峰对应缔合-OH 伸缩振动峰[9],振动幅度Mn-BC-2 比Mn-BC-1 明显,说明两种改性生物质炭表面含有缔合-OH 基团,且Mn-BC-2 比Mn-BC-1表面缔合-OH 基团多。2 924 cm-1和2 945 cm-1的特征峰为脂肪族或者芳香族的C-H 振动[10]。1 050 cm-1和1 009 cm-1附近的特征峰为C-O-C对称伸缩振动和反对称伸缩振动[11]。然而,Mn-BC-2 在1 650 cm-1处的峰值与-COOH 伸缩振动有关[12],表明Mn-BC-2 表面含有大量的-COOH,在1 405 cm-1附近的特征峰是Ar-OH 类结构[13]。900 cm-1以内为苯的指纹区。
2.1.3 比表面积分析
对Mn-BC-1 和Mn-BC-2 的进行BET 测试。在77 K 下,对氮气等温吸附-脱附曲线进行测试。图3为样品Mn-BC-1 和Mn-BC-2 对N2吸附-解吸等温线及孔径分布图。样品的孔结构特性在表1 中列出。由图3 和表1 数据可以看出,Mn-BC-2 对N2的吸附量大于Mn-BC-1,Mn-BC-1 的比表面积为17.266 3 m2/g,Mn-BC-2 的比表面积为49.412 0 m2/g,说明同样用高锰酸钾改性,玉米叶子的孔隙结构比玉米秸秆的丰富。同时,从孔径分布图(内插图)上可以看出,Mn-BC-1(改性玉米秸秆)的孔径主要集中在20 nm 左右,Mn-BC-2(改性玉米秸秆叶子)的孔径主要集中在7 nm 左右,以介孔为主,有利于比表面积的增加和吸附位点的增加。当相对压力(p/p0)大于0.9 时,Mn-BC-1 和Mn-BC-2 的吸附曲线又急剧上升,根据IUPAC 吸附曲线分类,Mn-BC-1和Mn-BC-2 的吸附曲线属于Ⅱ型吸附曲线。
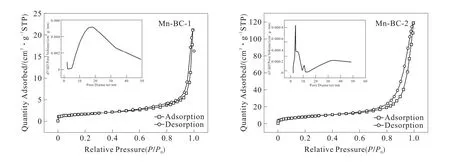
图3 Mn-BC-1 和Mn-BC-2 对N2吸附-解吸等温线图及孔径分布图(内插图)

表1 Mn-BC-1 和Mn-BC-2 的孔结构特性
2.2 Mn-BC-1 和Mn-BC-2 对氨氮的吸附模型分析
2.2.1 Mn-BC-1 和Mn-BC-2 对氨氮的吸附动力学模型
Mn-BC-1 和Mn-BC-2 对氨氮的吸附量随时间的变化如图4 所示。可以看出,Mn-BC-1 和Mn-BC-2对氨氮的吸附量随着吸附的进行逐渐增加,最后趋于饱和,达到吸附平衡;Mn-BC-1 对氨氮的吸附在初始30 min 内,吸附速度很快,30 min 后达到吸附平衡;Mn-BC-2 对氨氮的吸附在50 min 后才达到平衡。这主要是由于吸附开始时,生物质炭表面有大量吸附位点,随着吸附的进行,位点逐渐减少,最后达到饱和。同时,Mn-BC-1 和Mn-BC-2 对氨氮的饱和吸附量分别为14.23 mg/g 和36.78 mg/g,说明Mn-BC-2 比Mn-BC-1 具有更多的吸附位点和更大的比表面积。分别对二者进行准一级和准二级动力学模型拟合,Mn-BC-1 和Mn-BC-2 更好的符合准二级动力学模型(R2分别为0.991 和0.992),对氨氮的最大吸附量分别为13.998 mg/g 和36.996 mg/g 较为符合实验测定结果,且说明Mn-BC-1 和Mn-BC-2 对氨氮的吸附是多因素共同作用的结果,这表明限速步骤可能是化学吸附或离子交换[14]。
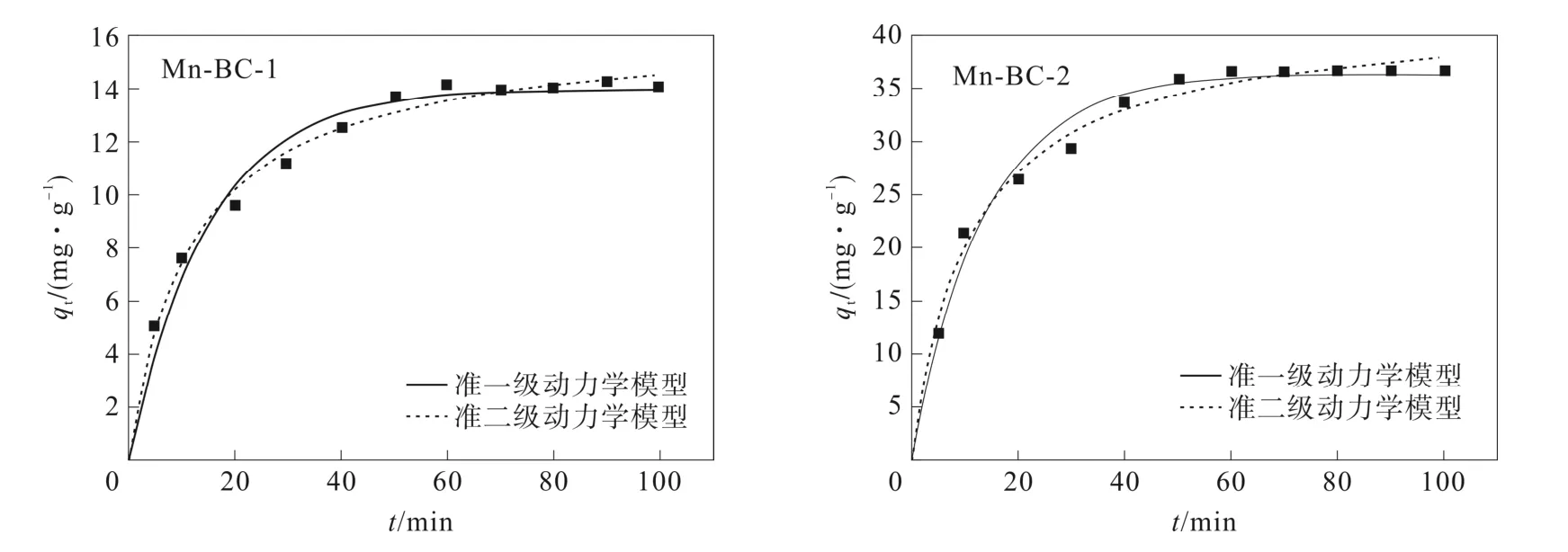
图4 Mn-BC-1 和Mn-BC-2 吸附氨氮的准一级动力学模型和准二级动力学模型
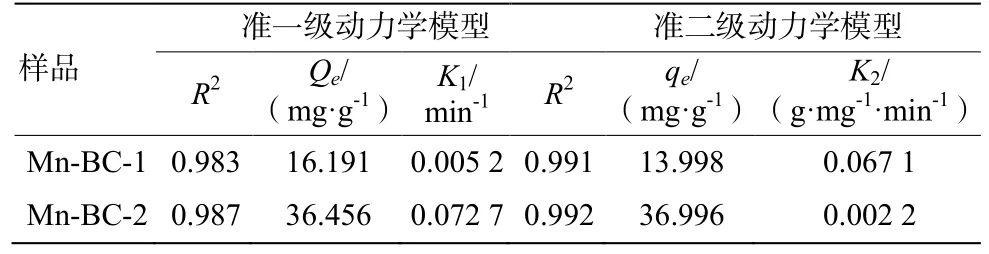
表2 Mn-BC-1 和Mn-BC-2 吸附氨氮的动力学模型拟合参数
2.2.2 Mn-BC-1 和Mn-BC-2 对氨氮的等温吸附模型
为了进一步分析Mn-BC-1 和Mn-BC-2 对氨氮吸附的机理,对浓度范围在0~60 mg/L 的氨氮溶液的吸附数据采用Langmuir 和Freundlich 等温吸附模型进行拟合,结果如图5 所示,相关参数见表3。可以看出,Mn-BC-1 和Mn-BC-2 吸附氨氮都更符合Langmuir 等温吸附模型(R2分别为0.977 91 和0.988 19),说明吸附更倾向于单层吸附,且以化学吸附为主。Langmuir 等温吸附模型拟合吸附容量分别为17.770 5 mg/g 和36.551 07 mg/g,与实验测定值基本相近。
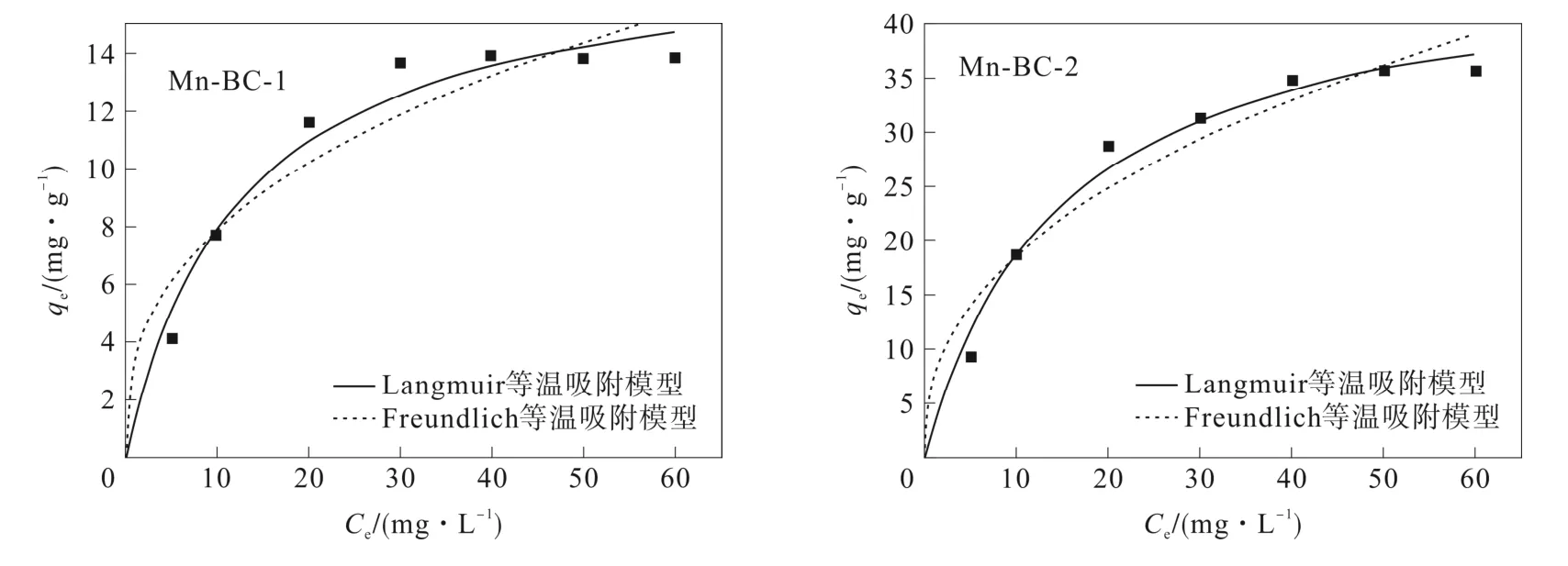
图5 Mn-BC-1 和Mn-BC-2 吸附氨氮的Langmuir 等温吸附模型和Freundlich 等温吸附模型

表3 Mn-BC-1 和Mn-BC-2 吸附氨氮的等温吸附模型拟合参数
3 结论
1)制备了用高锰酸钾改性的玉米秸秆生物质炭(Mn-BC-1)和玉米叶片生物质炭(Mn-BC-2),经过材料表征发现,后者具有更大的比表面积,样品表面呈现平面蜂窝状,并含有大量的羟基和羧基等含氧官能团,为氨氮的提供了更多的吸附位点。
2)Mn-BC-1 和Mn-BC-2 对氨氮的平衡吸附量分别为 14.12 mg/g 和 36.68 mg/g,对比看出Mn-BC-2 对氨氮具有更高的吸附量,且分别在吸附时间为30 min 和50 min 时达到吸附平衡。
3)Mn-BC-1 和Mn-BC-2 对氨氮的吸附均符合准二级动力学模型,表明吸附是由多种因素共同作用的结果;均符合Langmuir 等温吸附模型,表明吸附主要以化学吸附为主。
