奥美拉唑杂质毒性预测及细胞毒性研究
2024-01-10刘荷英刘波郑洋滨陈涛刘宁
刘荷英,刘波,郑洋滨,陈涛,刘宁
1.江西省药品检验检测研究院,国家药品监督管理局中成药质量评价重点实验室,江西省药品与医疗器械质量工程技术研究中心,江西 南昌 330029;2.上海凡默谷信息技术有限公司,上海 200127
药品中不可避免地存在或多或少的杂质,杂质的毒性直接影响到药品的安全性,因此对药物杂质的毒性研究非常重要。目前药物杂质的毒性研究方法较多,传统方法主要为各种体内外动物试验和细胞试验,动物试验是毒性研究中最准确直观的方法,但考虑到动物伦理和“3R”原则的要求,加之动物试验的成本较高,试验周期较长,越来越多种体外毒性研究方法用于替代动物试验研究。细胞试验一定程度上弥补了上述动物试验的缺陷,且更能研究出药物作用机制,近年来在毒性研究领域应用广泛[1-3],但细胞试验只能反映某一方面的潜在毒性,存在片面性。随着计算机技术的飞速发展,计算机辅助预测化合物毒性方面的应用越来越多,其具有快速、经济、环保、易实现等优点,一定程度上弥补了动物试验和细胞试验的局限性。定量结构-性质/活性关系(QSPR/QSAR)模型是指通过数学方法建立化合物的分子描述符与其生物性质/活性之间的线性或非线性关系模型[4],近年来在化合物毒性预测方面应用广泛[5-11],许多国际组织和监管机构都支持和推动QSPR/QSAR 的运用,并认为其可以作为动物实验的替代方法[12]。
奥美拉唑是一种能够有效抑制胃酸分泌的质子泵抑制剂,用于治疗十二指肠溃疡,胃溃疡、反流性食管炎及 Zollinger-Ellison 综合征等[13-14],临床上应用的奥美拉唑系列药物有很多,包括注射用奥美拉唑钠、注射用艾司奥美拉唑钠、奥美拉唑肠溶胶囊、奥美拉唑肠溶片、奥美拉唑钠肠溶片、奥美拉唑镁肠溶片和艾司奥美拉唑镁肠溶片等。《中国药典》[15]、《英国药典》[16]、《欧洲药典》[17]、《美国药典》[18]和《日本药典》[19]均收载了奥美拉唑的杂质结构,其中《英国药典》《欧洲药典》和《美国药典》中收载的杂质最多,共9 个杂质(杂质A~I),此外《中国药典》艾司奥美拉唑钠(S 型奥美拉唑钠)质量标准[15]中收载了5 个杂质(杂质I~V),其中杂质I 和杂质V 分别为国外药典中的杂质D 和杂质A,其他3 个杂质结构与国外药典不同,本课题组前期研究了注射用奥美拉唑钠的有关物质,除各国药典收载的12 个已知杂质外,还推测了4 个未知杂质的结构[20]。奥美拉唑药物在生产和贮存过程中易降解产生杂质[21],更需关注其杂质安全性问题。奥美拉唑毒理学研究发现大鼠长期服药导致的高胃泌素血症能引发胃癌,人类的慢性高胃泌素血症可导致肠嗜铬细胞样细胞增生和胃体内的类癌肿瘤,尽管概率很小[22],但至今未发现奥美拉唑相关杂质的毒理学方面报道。
ADMET Predictor 软件可基于化合物的结构预测其吸收、分布、代谢、排泄和毒性,并综合判断化合物的成药性。本研究采用该软件基于QSPR 模型对奥美拉唑及16 个杂质进行毒性预测,再采用MTT法结合细胞形态学观察对奥美拉唑钠及7 种杂质进行L-929 细胞毒性试验研究,杂质毒性研究数据可为奥美拉唑系列药物的质量安全性评价提供参考。
1 材料与方法
1.1 仪器与软件
酶标仪(美国Thermo 公司,型号:MULTISKAN GO);二氧化碳培养箱(美国Thermo 公司,型号:HERACELL150i);倒置显微镜(重庆光学仪器有限公司,型号:XDS-1B);自动细胞计数仪(上海睿钰生物科技有限公司,型号:IC1000);涡旋混合器(意大利VELP 公司,型号:VORTEX WX);ADMET PredictorTM 软件(美国Simulations Plus 公司,版本:9.5.0.16);ChemOffice 2010(美国CambridgeSoft 公司)。
1.2 对照品与试剂
奥美拉唑钠对照品(中国食品药品检定研究院,批号:100760-201504,含量:95.2%);杂质A(东京化成工业株式会社,批号:N5R3G-RK,HPLC 纯度:99.9%);杂质B(山东博洛德生物科技有限公司,批号:AML ZZZ20170501,纯度:98.36%);杂质C[徐希爱(上海)化成工业发展有限公司,批号:FRIFI-LL,HPLC 纯度:99.9%];杂质D(EDQM CS,批号:3.0);杂质E(北京百灵威科技有限公司,批号:LF30Q06,HPLC 纯度:98.60%);杂质J(江苏奥赛康药业有限公司,批号:S18012901,纯度:94.2%);杂质K(Comprison 公司,批号:31171,纯度:98.06%)。
小鼠成纤维细胞(L-929,武汉大学中国科学院典型培养物保藏中心)。RPMI 完全1640basic(1×)培养基(含10%杭州四季清新生牛血清)(上海语纯生物科技有限公司)、磷酸缓冲液(上海语纯生物科技有限公司)、二甲基亚砜(DMSO,Sigma 公司,细胞培养级)、噻唑蓝(MTT,Sigma 公司)。
1.3 方法
1.3.1 ADMET Predictor 软件方法 采用ChemOffice 2010 软件分别绘制奥美拉唑及其16 个杂质的结构,其中杂质K 为《中国药典》中艾司奥美拉唑钠的杂质Ⅲ,为一对同分异构体的混合物,此文中分别命名为杂质K1 和K2,奥美拉唑及其各杂质的结构见图1。将各化合物的结构图导出为MOL 格式文件,然后导入ADMET Predictor 软件中,进行心脏毒性、大鼠急性毒性、致癌性、肝脏不良反应毒性和致突变性的预测,再综合计算出毒性风险系数。ADMET Predictor 软件分析大部分上市药物的毒性风险系数预测结果≤3.3;且毒性风险系数越大,说明毒性越大。心脏毒性通过预测化合物对hERG 钾离子通道的半抑制浓度的log 值(pIC50)来评估,pIC50≤[5.5,6]mol/L 时,说明心脏毒性小或无;大鼠急性毒性通过预测大鼠口服给药模型的半数致死量(LD50)来评估,预测结果≥[200,320]mg/kg 时,说明产生的毒性小或无;致癌性是通过预测大鼠及小鼠口服给药模型的半数中毒剂量(TD50)来评估,大鼠的TD50值≥[4,6.5]mg·kg-1·d-1时,说明化合物对大鼠的致癌性小或无,小鼠的TD50值≥[20,35]mg·kg-1·d-1时,认为化合物对小鼠的致癌性小或无;肝脏不良反应是通过预测化合物是否会导致肝脏碱性磷酸酶(AlkPhos)、γ-谷氨酰转肽酶(GGT)、乳酸脱氢酶(LDH)、血清谷草转氨酶(AST)和血清谷丙转氨酶(ALT)这5 种肝酶水平升高来评估,肝酶水平升高表示该化合物可能产生肝脏不良反应,当化合物同时导致AST、ALT 和LDH 升高时,认为化合物具有肝脏毒性;致突变性是通过预测不同沙门氏菌属(共10 株)Ames 试验中的致突变可能性,得出致突变性风险系数,大部分上市药物的致突变性风险系数预测结果≤1,当突变性风险系数>1 时,表明化合物产生致突变性的可能性较大。

图1 奥美拉唑及其各杂质结构
1.3.2 细胞毒性试验方法 取奥美拉唑钠和杂质J、K 分别用培养基溶解,取杂质A、B、C、D、E 分别用含0.5% DMSO 的培养基溶解,过滤除菌,按2倍系列梯度稀释成不同浓度,作为供试品溶液。以最高浓度下多数细胞被杀死,而最低浓度时不会杀死细胞为标准,选择各化合物的最终浓度区间,奥美拉唑钠浓度为25~400 μg/mL、杂质A、D 浓度为125~2 000 μg/mL、杂质B 浓度为9.375~300 μg/mL、杂质C、K 浓度为250~4 000 μg/mL、杂质E 浓度为36.25~1 160 μg/mL、杂质J浓度为62.5~1 000 μg/mL。同时分别取培养基和含0.5% DMSO 的培养基,作为阴性对照溶液;取含5% DMSO 的培养基,作为阳性对照溶液。取对数生长期的L-929 细胞消化吹打计数,稀释细胞浓度至1×104个/mL 的细胞悬液。取细胞悬液接种于96 孔培养板,每孔接种100 μL 细胞悬液,置CO2培养箱(含体积分数5%二氧化碳气体)37 ℃培养。培养24 h 后,弃去原培养液。取阴性对照溶液、阳性对照溶液和供试品溶液,各设至少6 孔,每孔100 μL,置CO2培养箱继续培养72 h。于更换培养液后的72 h,置显微镜下观察细胞形态。每孔加入20 μL 5 g/L 的MTT溶液(取0.5 g 噻唑蓝,用100 mL 磷酸缓冲液溶解,过滤除菌),继续培养4 h。弃去孔内液体,加入150 μL DMSO,置振荡器上振荡10 min,以570 nm为测定波长,630 nm 为参比波长,在酶标仪下测定吸光度,以加药组与阴性对照组的吸光度比值计算相对增殖率(RGR),以100%减去RGR 即得抑制率,再运用SPSS 19.0 软件使用Logit 模型进行probit 回归分析,计算得到各化合物的半抑制浓度IC50值。
2 结果
2.1 毒性预测结果
奥美拉唑及其杂质的毒性预测结果见表1。心脏毒性预测结果表明,奥美拉唑及其杂质的hERG钾离子通道的pIC50值均<5.5 mol/L,说明无明显心脏毒性;大鼠急性毒性预测结果表明,奥美拉唑及其杂质的LD50值均>320 mg/kg,说明产生大鼠急性毒性的可能性较小;致癌性预测结果表明,奥美拉唑和杂质B、C、D、E、H、I、L、O、P 的大鼠TD50值均<4 mg·kg-1·d-1,说明产生大鼠致癌性的风险较高,杂质C 的小鼠TD50值<20 mg·kg-1·d-1,说明其产生小鼠致癌性的风险较高,杂质C 可能同时具有大小鼠致癌性,毒性较大;肝脏不良反应预测结果表明,杂质A可能同时引起AST、ALT 和LDH 升高,产生肝脏毒性的可能性较大,其他化合物产生肝脏毒性的可能性较小;致突变性预测结果表明,杂质A、F、G 的致突变性风险系数>1,产生致突变毒性的可能性高。奥美拉唑及其杂质的综合的毒性风险系数均<3.3,在上市药物毒性范围内,其中杂质A、C、F、G 的毒性风险系数高于奥美拉唑,说明其毒性比奥美拉唑大,杂质A 的主要毒性是致突变性和肝脏毒性,杂质C的主要毒性是大、小鼠致癌性,杂质F、G 的主要毒性是致突变性。
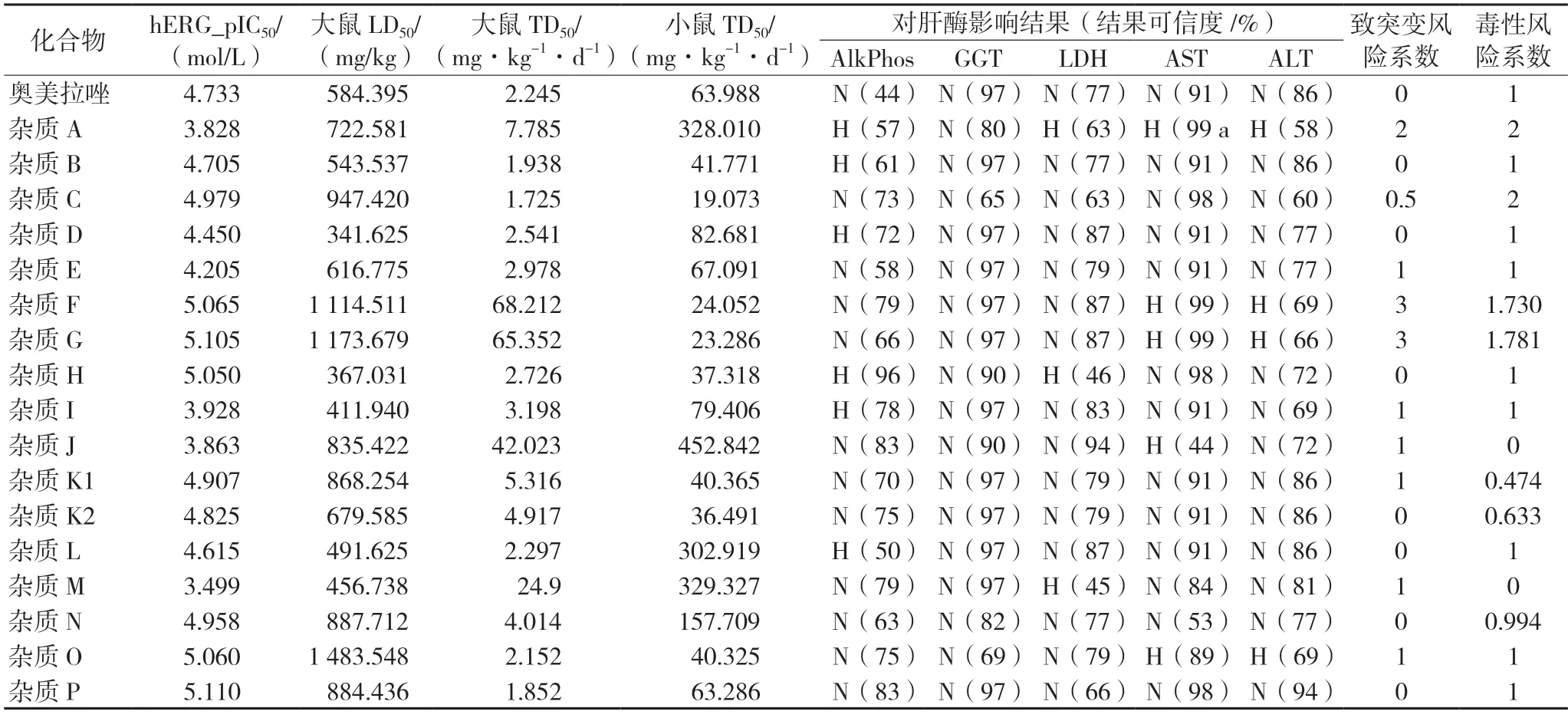
表1 ADMET Predictor软件对奥美拉唑及其杂质的毒性预测结果
2.2 细胞毒性试验结果
阳性对照组细胞层完全破坏,重度抑制细胞增殖。奥美拉唑钠及杂质A、B、C、D、E、J、K 在不同浓度下对细胞增殖的抑制率见图2,计算的IC50值见表2,从图表结果可知,杂质B 对细胞增殖的抑制作用最强,IC50值最小,细胞毒性最大,杂质C的细胞毒性最小,各化合物细胞毒性大小为杂质B>奥美拉唑钠>杂质E>杂质J>杂质A>杂质K>杂质D>杂质C,仅杂质B 的细胞毒性大于奥美拉唑钠。

表2 奥美拉唑钠及其杂质的IC50测得值 μg/mL
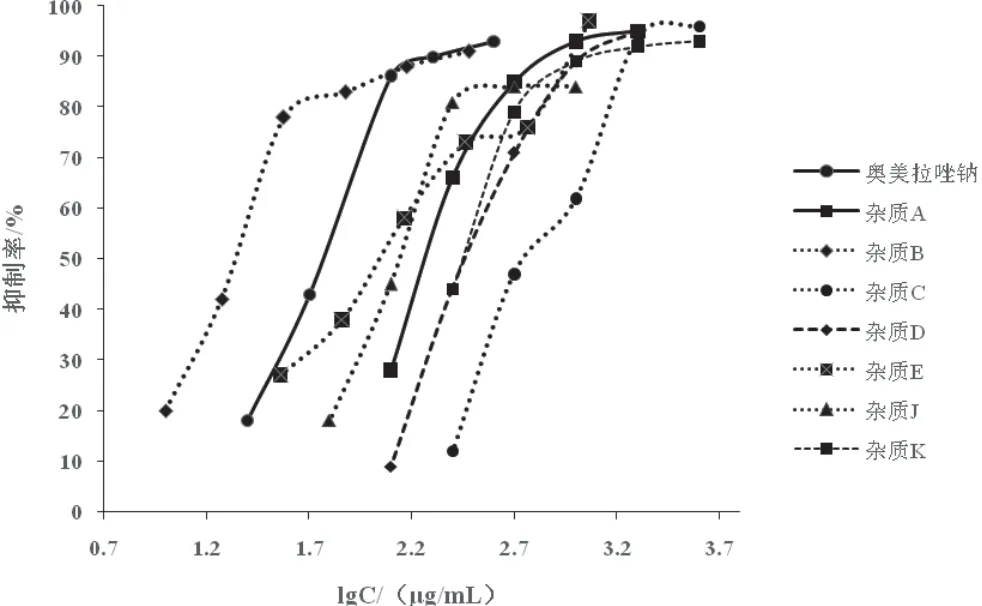
图2 奥美拉唑钠及其杂质在不同浓度下的细胞抑制率
3 讨论
本研究采用ADMET Predictor 软件进行毒性风险系数评估是基于统计来自全球药物索引(WDI)中的2 270 个药物分子的预测结果总结出的打分规则。打分规则里的中括号[ ]表示“软”阈值,85%的上市药物不违反打分规则,10%的上市药物违反打分规则,中括号[ ]中的数据可以理解为5%的上市药物在中括号[ ]的范围内。以LD50值的阈值[200,320]mg/kg 为例,若LD50值<200 mg/kg,说明违反该打分规则,存在毒性;若LD50值在200~320 mg/kg 之间,也违反该打分规则,同样存在毒性,但毒性更小;若LD50值>320 mg/kg,说明不违反该打分规则,产生毒性的可能性小。该软件可预测35 项毒性参数,但仅将主要的5 项参数(心脏毒性、大鼠急性毒性、致癌性、肝脏毒性和致突变性)纳入毒性风险系数的打分。肝脏毒性预测了化合物对5 种肝酶水平变化的影响,虽然仅将主要的3 种肝酶纳入打分规则,但其他2 种肝酶的影响结果仍值得关注。
奥美拉唑毒性预测结果表明其可能具有大鼠致癌性,这与文献[22]报道的大鼠长期服用奥美拉唑导致的高胃泌素血症引发胃癌结果相符。奥美拉唑预测的大鼠LD50值为584.395 mg/kg,比文献[23]报道的实验值(>4 g/kg)更小,但根据软件打分规则,预测的LD50值>320 mg/kg 时,认为产生大鼠急性毒性的可能性较小,因此本次预测的结果与文献基本一致。杂质K1 和K2 为一对同分异构体,市场上仅能购买到它们的混合物,通过软件毒性预测可分别研究其毒性,预测结果表明二者均未发现明显毒性,毒性风险系数均低于奥美拉唑。奥美拉唑及其杂质的综合毒性风险系数均不高,在上市药物毒性范围内,但有4 个杂质的毒性风险高于奥美拉唑,需警惕杂质A 的致突变性和肝脏毒性、杂质C 的大小鼠致癌性和杂质F、G 的致突变性。
目前化学药品的细胞毒性研究还没有相关的检测标准或指导原则,大多参照GB/T 16886.5-2017/ISO 10993-5:2009[24]和GB/T 14233.2-2005[25]进行研究。本研究采用以上2 个国标中共同收载的方法,也是最常用的MTT 法,以小鼠成纤维细胞(L-929)进行杂质的细胞毒性研究。目前报道的奥美拉唑相关杂质共16 个,但仅7 个杂质能购买到纯品,因此本研究仅对这7 个杂质进行了研究。杂质B 的细胞毒性约为奥美拉唑钠的2 倍,其预测的大鼠LD50值与奥美拉唑接近,但该杂质在药品中的含量极低,因此杂质B 的毒性风险不高。由于药品中的杂质含量极低,杂质纯品较难获得,在进行毒性实验研究时会受到限制,而采用软件进行毒性预测仅需明确杂质结构。通过软件毒性预测结合细胞毒性研究可快速筛查药品中微量杂质的毒性,但需注意将杂质的毒性与主药同步研究进行对比才能更准确地评价药品安全性。
