放疗联合卡瑞利珠单抗或替吉奥治疗局部晚期食管癌的疗效
2024-01-10朱梅程旭钱晓涛
朱梅, 程旭, 钱晓涛
食管癌是消化系统恶性肿瘤之一,早期患者治疗首选手术[1-2]。中晚期患者多数已经错过手术治疗最佳时期,临床治疗以放化疗为主[3]。局部晚期食管癌是指食管癌变浸润食管及其周围组织,但未浸润重要脏器,无远处转移[4]。在局部晚期食管癌的治疗中,放疗可以控制肿瘤扩散、减小肿瘤体积,但单独放疗疗效不佳[5]。替吉奥是临床较为常用的一种抗肿瘤化疗药物[6],但由于不良反应多,用药时间长,且治疗期间容易出现耐药性,临床疗效有限[7]。近年来,免疫治疗治疗逐渐应用于临床多种肿瘤的治疗中,疗效显著[8]。卡瑞利珠单抗是一种PD-1单抗药物,通过抑制程序性死亡受体-1(PD-1)通路,提升机体免疫功能,促进肿瘤细胞死亡,临床在治疗多种恶性肿瘤中均取得较好疗效[9-10]。本研究对比局部晚期食管癌行放疗联合替吉奥化疗和放疗联合卡瑞利珠单抗治疗两种方案的疗效,以期为局部晚期食管癌治疗方案的选择提供依据。
1 资料与方法
1.1 一般资料
选取可国科学院合肥肿瘤医院在2020年1月至2022年12月间收治的80例局部晚期食管癌患者,依据患者临床治疗方法将其分为对照组(40例)和观察组(40例)。两组基本资料比较差异无统计学意义(P>0.05),表1。本院医学伦理委员会同意开展本项研究。

表1 对照组和观察组基本资料比较
1.2 纳入及排除标准
纳入标准:①经影像学检查符合局部晚期食管癌相关诊断标准[11-12];②临床相关资料准确完整;③生命体征平稳,生存期预计在3个月以上;④患者知情同意并自愿参与研究;⑤符合放疗指征。排除标准:①合并其他恶性肿瘤疾病;②合并严重肝肾脏器损伤;③入组前进行过相关治疗;④对研究所用药物过敏或不耐受;⑤出现远处器官转移。
1.3 方法
对照组行放疗联合口服替吉奥化疗方案治疗。患者进行CT扫描、食管镜检查、食管造影检查,综合检查结果勾画出肿瘤靶区(GTV),病灶总体积包括原发病灶组织、淋巴结转移病灶组织,然后在GTV区域上勾画出临床靶区(CTV),上下外扩3~5 cm,四周外扩 0.5~0.8 cm,包括转移淋巴结区域,按解剖结构修改。然后在CTV区域上勾画出计划靶区(PTV),四周外扩0.5~1.0 cm。使用美国ELEKTA-AXESSE机器,在Monaco治疗计划系统内进行放疗计划设计,使用VMAT容积调强计划,射野中心为PTV的空间几何中心,将该点规定为剂量归一标准点,要求95%的GTV处方为60 Gy;95%的PTV剂量为54~60 Gy,每周放疗5次,共6周。同时联用替吉奥(江苏恒瑞医药股份有限公司,国药准字H20100135,20 mg/粒,)每天2次,每次40 mg,21 d为1个治疗周期,每个周期内连续用药14 d,停药7 d。持续用药3个治疗周期。
观察组行放疗联合卡瑞利珠单抗治疗,放疗操作同对照组一致,同时联用卡瑞利珠单抗(苏州盛迪亚生物医药有限公司,国药准字S20190027,200 mg/支)治疗,以21 d为1个治疗周期,患者在每个治疗周期的第1天予以200 mg静脉注射,持续用药3个治疗周期。
1.4 观察指标
1.4.1 临床疗效 ①完全缓解(CR):病灶组织完全消失,维持至少1个月未复发;②部分缓解(PR):基线病灶组织最大径之和下降在30%以上,维持至少1个月为复发;③疾病稳定(SD):最大径之和降低在30%以下,或增加在20%以下;④疾病进展(PD):最大径之和增加在20%以上或出现新的病灶组织[13]。客观缓解率(ORR)=CR+PR;疾病控制率(DCR)=CR+PR+SD。在患者用药3个治疗周期后进行评估。
1.4.2 免疫功能 治疗前后24 h抽取患者空腹静脉血3 mL,用EXFLOW-206型流式细胞仪(深圳市达科为生物技术股份有限公司)测定患者T淋巴细胞亚群CD3+、CD4+、CD8+水平。
1.4.3 肿瘤标志物 治疗前后24 h内采用酶联免疫吸附法(试剂盒购自上海瓦兰生物科技有限公司)测定血清中癌胚抗原(CEA)、糖类抗原724(CA724)水平。
1.4.4 用药安全性 记录两组血小板减少、胃肠道反应、白细胞降低、肝肾功能异常、甲状腺功能减退、发热、乏力等不良反应发生情况。
1.4.5生存质量 用KPS评分[14]评估生存质量,KPS总评分为0~100分,分值越高,生存质量越好;用食管癌患者补充量表(QLQ-OES18)[15]评分评估生活质量,量表共18个条目,每个条目评分为1~4分,其中有1个条目为反向计分,量表总评分为21~69分,分值越高,生活质量越差。
1.5 统计学方法
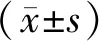
2 结果
2.1 对照组和观察组临床疗效比较
观察组ORR和DCR均高于对照组,差异有统计学意义(P<0.05),表2。
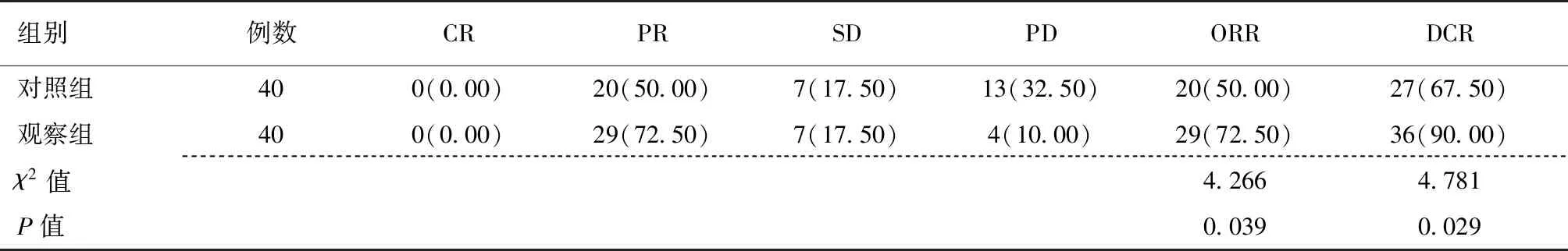
表2 对照组和观察组临床疗效比较 [例(%)]
2.2 对照组和观察组免疫功能比较
两组CD3+、CD4+/CD8+水平均高于治疗前,观察组CD3+、CD4+/CD8+水平高于对照组,差异有统计学意义(P<0.05),表3。
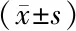
表3 对照组和观察组免疫功能比较
2.3 对照组和观察组肿瘤标志物水平比较
两组CEA、CA724水平均低于治疗前,观察CEA、CA724水平低于对照组,差异有统计学意义(P<0.05),表4。
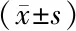
表4 对照组和观察组标志物水平比较
2.4 对照组和观察组用药安全性比较
对照组行放疗联合替吉奥化疗方案,观察组行放疗联合卡瑞利珠单抗方案治疗,两组不良反应比较差异无统计学意义(P>0.05),表5。
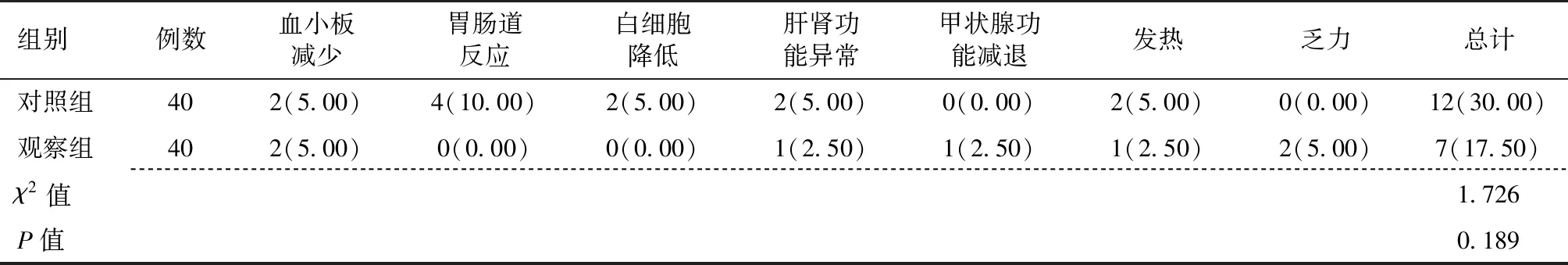
表5 对照组和观察组不良反应比较 [例(%)]
2.5 对照组和观察组生存质量比较
治疗后,两组KPS评分均高于治疗前,观察组高于对照组(P<0.05),两组QLQ-OES18评分均低于治疗前,观察组低于对照组(P<0.05),表6。

表6 比较两组生存质量(分,
3 讨论
食管癌病因尚不明确,遗传、长期饮酒吸烟、饮食习惯不良等都可能诱发该病[16-17]。PD-1是一种可抑制免疫应答激活的蛋白,可表达于活化T细胞、B细胞、NK细胞、单核细胞等细胞表面;PD-L1是PD-1配体,与PD-1结合可有效抑制T细胞活化、增殖,发挥免疫应答抑制作用,促进肿瘤细胞免疫逃逸[18]。卡瑞利珠单抗是PD-1抑制剂,通过抑制PD-1与其配体结合,促进免疫应答作用,增强免疫功能,从而促进T细胞对肿瘤细胞杀伤作用[19]。
本研究结果显示,局部晚期食管癌患者放疗联合卡瑞利珠单抗方案(观察组)ORR和DCR均高于放疗联合替吉奥化疗方案(对照组),两组不良反应差异无统计学意义;治疗后,两组KPS评分均高于治疗前,观察组高于对照组,两组QLQ-OES18评分均低于治疗前,观察组低于对照组;提示放疗联合卡瑞利珠单抗可提升患者疗效及生存质量,且用药安全。替吉奥是由替加氟、吉美嘧啶和奥替拉西钾制成的复方制剂,药物进入体内后,替加氟会转变为5氟尿嘧啶(5-FU)发挥抗肿瘤作用,吉美嘧啶可抑制5-FU分解代谢酶活性,增加5-FU浓度,增强抗肿瘤作用,奥替拉西钾可减少药物对消化道的不良反应,减轻药物不良反应[20]。卡瑞利珠单抗可通过抑制PD-1,增强免疫功能,发挥抗肿瘤作用。本研究中二者临床药物不良反应差异无统计学意义,但卡瑞利珠单抗疗效高于替吉奥,从而能提升患者生存质量。CD3+是T淋巴细胞总值,CD4+、CD8+是T淋巴细胞亚群,CD4+可诱导B细胞分化,CD8+可抑制B细胞合成 和T淋巴细胞增殖,CD4+/CD8+平衡在维持机体正常免疫应答中有重要作用[21]。CEA是一种糖蛋白复合物,属于广谱肿瘤标志物,在多种肿瘤中均异常高表达,临床可用于辅助肿瘤诊断、预后评估、疗效监测等[22]。CA724也是临床一种肿瘤标志物,对消化道肿瘤敏感度较高[23]。本研究显示,治疗后,两组CD3+、CD4+/CD8+水平均高于治疗前,研究组高于对照组;两组CEA、CA724水平均低于治疗前,观察组低于对照组;提示放疗联合卡瑞利珠单抗可明显改善患者免疫功能,下调肿瘤标志物。卡瑞利珠单抗可通过抑制PD-1通路,增强免疫应答反应,提升免疫功能,促进T淋巴细胞活化、增殖,有效杀灭肿瘤细胞,降低肿瘤标志物水平。
综上所述,与放疗联合替吉奥化疗相比,放疗联合卡瑞利珠单抗在局部晚期食管癌的临床治疗中应用效果较好,患者临床疗效有明显提升,免疫功能及肿瘤标志物水平有明显改善,患者生存质量有明显提升,值得临床推广。
