肝硬化合并急性胆囊炎患者手术风险评估*
2024-01-07王东君张春岩晁祥嵩王兴权
王东君,张春岩,晁祥嵩,李 志,王兴权
急性胆囊炎(acute cholecystitis,AC)是临床常见的外科急腹症之一。与非结石源性AC相比,胆囊结石导致的胆囊管梗阻和胆汁排出受阻是引发AC的主要原因,占疾病总发生率的90%~95%[1]。1985年,德国Erich Miihe首次开展了腹腔镜下胆囊切除术(laparoscopic cholecystectomy,LC)。此后,LC逐步成为治疗胆囊结石和胆囊炎的首选方法。随着腹腔镜技术的发展,手术的安全性也得到了大幅度的提升[2]。在肝硬化患者,因脾功能亢进症、免疫性溶血和胆囊排空障碍等因素的存在,胆囊结石发生率达到非肝硬化人群的2倍[3]。因此,临床上肝硬化患者出现AC并不少见[4]。AC患者胆囊壁及其周围组织水肿、粘连,再加上肝硬化本身解剖和病理学改变,两种疾病的叠加不仅使得疾病本身的复杂程度增加,同时也导致手术难度增大,使LC中转开腹率和手术并发症发生风险升高[5]。一般,按照疾病严重程度将AC分为Ⅰ级、Ⅱ级和Ⅲ级[6]。终末期肝病模型(model for end-stage liver disease,MELD)是评估晚期肝病病情的方法,参数简单,在评估肝胆病病情和判断预后方面具有较高的应用价值[7]。本研究分析了不同胆囊炎严重程度分级和MELD评分的肝硬化患者合并AC的手术治疗风险,现报道如下。
1 资料与方法
1.1 病例来源 2021年2月~2022年12月我院诊治的肝硬化合并AC患者92例,男性49例,女性43例;年龄为40~71岁,平均年龄为(57.7±6.8)岁。符合《肝硬化诊治指南》[8]和2018年东京指南有关急性结石性胆囊炎的诊断标准[9],其中乙型肝炎肝硬化78例,丙型肝炎肝硬化8例,乙型肝炎合并丙型肝炎肝硬化4例,原发性胆汁性肝硬化2例。排除标准:合并其它脏器疾病;合并严重的出血性疾病或凝血功能障碍;合并恶性肿瘤;急性胰腺炎;慢性结石性胆囊炎;既往有腹部手术史。本研究经我院医学伦理委员会审核、通过,患者及其家属签署知情同意书。
1.2 LC手术方法 患者入院后完善相关检查,评估肝脏贮备功能和手术耐受程度。术前,禁饮食,补液、维持水电解质和酸碱平衡,预防性应用抗生素,护肝治疗,给予白蛋白、冷冻血浆、注射维生素K1和利尿。清洁肠道。全身麻醉,气管插管。采用“三孔法”或 “四孔法”LC术,在脐旁作10 mm切口,建立气腹,维持腹压为12~14 mmHg。置入10 mm Trocar和腔镜。在剑突下、右肋弓下或锁骨中线上分别作10 mm和5 mm切口,置入Trocar和相关器械。在行四孔法手术时,则于右肋弓下与腋前线交界处再作5 mm切口。采用顺行或逆行切除法,以Hem-o-lok夹闭胆囊管和胆囊动脉、切断,以电灼法止血。切除胆囊后,置入取物袋,经剑突下切口取出,术后留置腹腔引流管。对于中转开腹手术者,采用右侧肋缘下斜切口,顺行或逆行切除胆囊。
1.3 胆囊炎严重程度分级与MELD评分 参照《东京指南(2018年)》[8]行胆囊炎严重程度分级。Ⅲ级:满足下列任一器官或系统功能障碍者,包括心血管、呼吸、神经、肝功能、肾功能、血液系统功能障碍;Ⅱ级:出现下列任一情况:白细胞计数升高(>18.0×109/L)、右上腹出现压痛性肿块、症状持续72 h以上、存在明显的局部感染表现;Ⅰ级:不具备Ⅱ级或Ⅲ级标准,无器官功能障碍,仅存在轻度的胆囊炎症。按如下公式计算MELD评分,即MELD 评分=3.8×lg(胆红素×0.058)+11.2×lg(国际标准化比值)+9.6×lg(肌酐×0.011)+6.4×(酒精型肝硬化×0,其他原因×1)。其中,低危:≤14分;中危:15~18分;高危:>18分。

2 结果
2.1 不同胆囊炎严重程度分级和MELD评分患者围术期指标比较 各种分级或评分患者中转开腹率比较,差异无显著性统计学意义(P>0.05);Ⅱ/Ⅲ级患者手术时间显著长于Ⅰ级患者,术中出血量和腹腔引流量显著大于Ⅰ级患者(P<0.05);低危与中高危MELD评分患者手术时间、术中出血量和腹腔引流量比较,差异无显著性统计学意义(P>0.05,表1)。
2.2 不同胆囊炎严重程度分级和MELD评分患者术后并发症发生率比较 Ⅱ级或Ⅲ级胆囊炎严重程度患者术后并发症发生率显著高于Ⅰ级患者,中高危MELD评分患者术后并发症发生率显著高于低危患者(P<0.05,表2)。
2.3 影响肝硬化合并AC患者LC手术风险的单因素分析 以中转开腹以及术后发生腹腔出血、腹水、腹腔感染、肠梗阻和胆瘘并发症为存在手术风险,结果发现风险组胆囊炎Ⅱ/Ⅲ级和MELD评分中高危比例显著高于非风险组(P<0.05,表3)。
2.4 影响肝硬化合并AC患者LC手术风险的Logistic多因素分析 对两组之间有统计学差异的指标赋值,即胆囊炎分级(Ⅰ级=0,Ⅱ/Ⅲ级=1)和MELD评分(低危=0,中高危=1),经Logistic多因素分析结果显示胆囊炎Ⅱ/Ⅲ级和MELD评分为中高危是肝硬化合并AC患者LC手术高风险的独立危险因素(P<0.05,表4)。
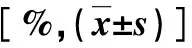
表1 不同胆囊炎严重程度和MELD评分患者围术期指标比较
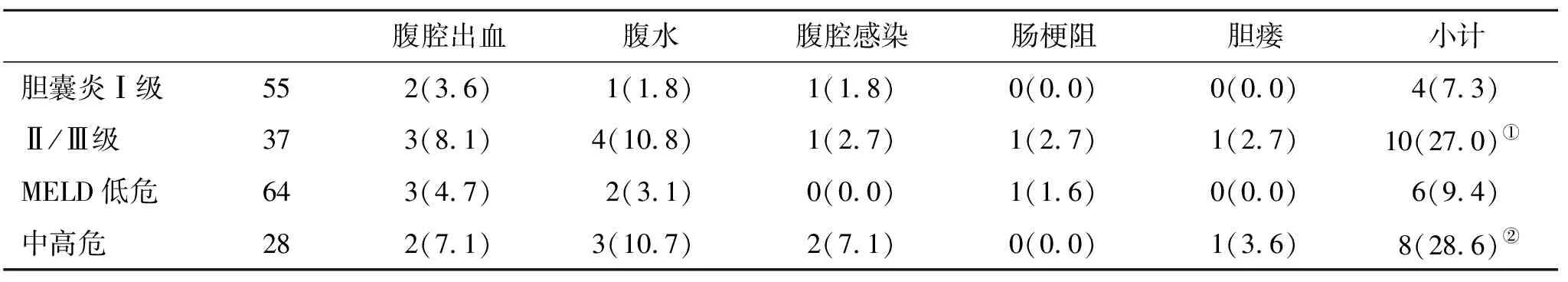
表2 不同胆囊炎严重程度和MELD评分患者术后并发症发生率(%)比较
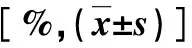
表3 影响肝硬化合并AC患者LC手术风险的单因素分析

表4 影响肝硬化合并AC患者LC手术风险的Logistic多因素分析
3 讨论
《东京指南(2018年)》是目前AC严重程度分级的标准。该标准综合临床表现、生化指标、影像学结果等多种因素,将疾病严重程度分为Ⅰ级、Ⅱ级和Ⅲ级,能客观反映疾病状态[10-14]。本研究对比不同分级患者围术期指标和术后并发症发生情况,结果显示随着胆囊炎严重程度分级增加,术中出血量和腹腔引流量也增加,术后并发症发生率升高,AC严重程度分级进展是导致合并肝硬化的AC患者LC手术风险增加的影响因素。AC进展到严重阶段,可能会由于粘连、炎症、坏疽、穿孔等而对外科手术造成严重干扰,甚至引起出血、组织损伤、胆瘘等严重并发症[15]。
本研究经MELD评分,将患者分为低危、中危和高危组,结果显示中高危患者术后并发症发生风险显著高于低危患者。多因素Logistic回归分析结果显示高MELD评分是肝硬化合并AC患者LC手术风险增加的影响因素。肝硬化合并AC患者往往存在肝损害、门脉高压伴侧支循环形成、凝血功能异常。由于胆囊位置改变,胆囊壁多伴水肿或萎缩,使手术复杂程度增加,并发症发生率随之升高。MELD评分反映了肝硬化病情,可在术前对肝功能储备做出客观评估,在指导手术方案选择和预测预后等方面具有重要的意义[16-18]。
腹腔镜手术常需考虑中转开腹的问题。相关研究显示[19],肝硬化合并症状性胆石病患者行LC手术中转开腹发生率达到非肝硬化者的1倍。在术后并发症方面,如胸腹水和腹腔出血发生率均较高。术后腹水的发生可能是由于手术和炎症使得患者肝功能损害加重所。此外,胆囊局部炎症引起的膈下感染和手术耗时长使得补液过多等因素均可能导致腹水的发生。腹腔出血则可能是由于肝硬化患者凝血功能障碍以及术区血管解剖变异导致[20]。本研究显示,随着胆囊炎严重程度加重和MELD评分升高,肝硬化合并AC患者LC手术风险随之增加。外科医生在术前,必须对胆囊炎严重程度进行分级和对肝功能进行MELD评分,这些指标在一定程度上可指导临床选择合理的手术方案,评估手术风险,预防术后并发症的发生。
