苦黄注射液预防抗结核药物导致的药物性肝损伤患者疗效研究*
2024-01-07刘力伟吴于青
任 浩,刘力伟,施 维,刘 波,吴于青,吕 芹
结核病(tuberculosis,TB)是临床常见的慢性传染病,是全球关注的严重公共卫生和社会问题[1]。临床上,常以异烟肼、利福平、吡嗪酰胺和乙胺丁醇等药物联合应用作为治疗TB的标准一线抗结核药物 (anti-tuberculosis drugs,ATD)。肝毒性是ATD常见且严重的不良反应,可能需要中断或修改抗结核治疗方案,导致治疗失败、复发和耐药,且多数患者因肝功能受损导致治疗依从性变差,从而显著降低了对TB的控制率[2]。ATD是引起我国急性药物性肝损伤(drug-induced liver injury,DILI)的主要病因,约占全部病例的21.2%[3]。根据目前的建议,只要肝损伤达到安全阈值,即需要中断抗结核治疗,以避免严重的DILI发生[4]。然而,并不是所有转氨酶升高都提示真正的DILI,同时存在药物性肝损伤适应现象(phenomenon of adaptation to drug-induced liver injury),是指一些能够诱发严重特异质性药物性肝损伤的药物,可引起短暂的、无症状的肝脏生化指标升高,继续使用相同药物和剂量时,升高的血清肝脏生化指标会恢复正常,称之为对肝损伤的适应现象[5]。认识药物性肝损伤适应现象的意义在于有可能减少或避免不必要的停药,以免失去控制重要临床疾病的手段。据报道,ATD引起的药物性肝损伤适应现象发生在20%或更多的抗结核药物治疗患者[6],但我们目前的检测不能正确区分药物性肝损伤适应现象与DILI,大多数因丙氨酸氨基转移酶(alanine aminotransferase,ALT)升高而中断治疗的患者可以耐受重新开始的标准抗结核方案,提示是肝损伤适应现象而不是 DILI,但导致过早的中断治疗可能影响了抗结核治疗的疗效。因此,控制抗结核治疗过程中的肝损伤适应现象也是一项必要的举措[7]。本研究进行了一项前瞻性、随机、临床对照试验,以评估苦黄注射液预防性治疗抗结核药物性肝损伤的安全性和有效性。
1 资料与方法
1.1 临床资料 该研究已获得我院医学伦理委员会批准,并符合《赫尔辛基宣言》的要求。 患者充分了解研究的性质、疾病、药物特征、治疗方法和参与研究所涉及的义务。每个参与者都给出知情同意书。2022年3月~2022年11月我院收治的肝功能正常的初治肺结核患者102例,符合《肺结核基层诊疗指南(2018年)》[8]初治肺结核的诊断标准,且经胸部DR检查发现肺部有活动性结核病和痰菌检查阳性。排除5例不能接受静脉输液治疗患者,将97例(男53例,女44例,年龄为27~64岁,平均年龄为46.44±7.66岁)患者纳入研究,随机将患者分为试验组50例和对照组47例,两组性别、年龄和病情差异无统计学意义(P>0.05)。参考《抗结核药物所致药物性肝损伤诊断与处理专家建议》[9]标准诊断DILI,适应性肝损伤是指轻中度血清ALT升高[4]。排除标准:伴有严重的肝、肾功能障碍、合并其他严重的基础疾病、既往存在肝损害史、合并结核性脑膜炎、肠结核等肺外结核、妊娠或哺乳期妇女。
1.2 治疗方法 给予所有患者乙胺吡嗪/利福霉素/异烟肼(沈阳红旗制药有限公司,国药准字H20051903)口服治疗,即乙胺吡嗪利福异烟片(Ⅱ,含利福平150 mg,异烟肼75 mg,吡嗪酰胺400 mg,盐酸乙胺丁醇275 mg),1次/d。对于体质量为38~54 kg的患者,每日3片,对于体质量为55~70 kg的患者,每日4片,对于71 kg以上的患者每日5片。试验组在此抗痨的基础上联合苦黄注射液(常熟雷允上制药有限公司,国药准字 Z10960004)3支,加入5%葡萄糖溶液250 mL中静脉滴注,1次/d。治疗观察8周。
1.3 观察指标 常规检测血生化指标(杭州艾康生物技术有限公司);采用双抗体夹心 ELISA 法检测血清白介素 6(interleukin-6,IL-6)和肿瘤坏死因子-α(tumor necrosis factor- α,TNF-α)水平(上海恒远生物科技有限公司);采用放射免疫法检测血清血红素加氧酶(heme oxygenase,HO-1)和超氧化物歧化酶(superoxide dismutase,SOD)水平(武汉默沙克生物科技有限公司)。

2 结果
2.1 两组肝损伤发生率比较 在治疗8周末,试验组适应性肝损伤和DILI发生率显著低于对照组(P<0.05,表1)。
2.2 两组肝功能指标比较 治疗前,两组各项肝功能指标水平比较均无统计学差异(P>0.05);在治疗8周末,试验组血清ALT、AST和TBIL水平显著低于对照组(P<0.05,表2)。
2.3 两组血清氧化应激和炎症因子水平比较 在治疗8周末,试验组血清HO-1和SOD水平显著高于(P<0.05),而血清IL-6和TNF-α水平显著低于对照组(P<0.05,表3)。
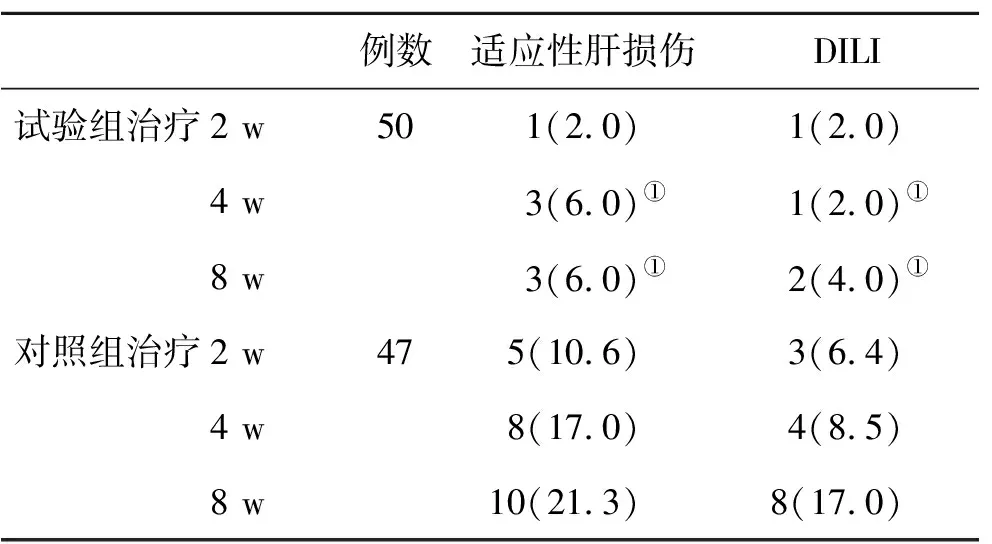
表1 两组肝损伤发生率(%)比较

表2 两组血生化指标比较

表3 两组血清氧化应激和炎性细胞因子水平比较
3 讨论
抗结核药物性肝损伤是指由ATD通过直接肝毒性或代谢产生的有毒或免疫原性中间体引起的肝脏损伤,可以表现为无症状转氨酶升高,也可呈急性肝炎,甚至是急性肝坏死,严重影响肺结核病患者治疗效果和预后[9]。ATD对肝脏的损伤机制至少包括:(1)直接肝损伤:研究发现异烟肼在体内可代谢为有毒的乙酰肼或肼,吡嗪酰胺在体内可代谢为有毒的吡嗪酸和5-羟基吡嗪酸,这些产物与肝损伤有直接的关系[10];(2)细胞代谢紊乱与肝损伤:近年研究发现利福平可干扰胆汁酸和胆红素代谢,异烟肼和利福平联用可干扰血红素生成途径,而异烟肼、利福平和吡嗪酰胺联用对三羧酸循环、精氨酸和脯氨酸代谢以及嘌呤代谢途径均有不利的影响[11,12];(3)应激反应与肝损伤:体内研究发现大剂量的异烟肼长时间服用可导致线粒体功能受损,包括三羧酸循环中的能量代谢和葡萄糖代谢,降低线粒体膜电位。超微结构研究表明大剂量的利福平可导致线粒体肿胀。体外研究发现吡嗪酰胺可降低细胞三磷酸腺苷(adenosine-triphosphate,ATP)和线粒体膜电位水平,并能抑制线粒体复合物 Ⅰ 活性,对线粒体形态也有一定程度的损伤。此外,内质网应激研究结果表明异烟肼、吡嗪酰胺和利福平均可能通过细胞凋亡介导肝损伤[13-15];(4)免疫反应与肝损伤:结核病患者在接受异烟肼、利福平和吡嗪酰胺联合治疗后会出现淋巴细胞转化试验(LTTs)呈阳性的结果,其损伤机制还不明[16]。
研究证实,在抗结核治疗期间,肺结核患者DILI发生率超过30%,其中因严重DILI致死率约为4.7%[9]。在ATD诱发的肝毒性方面,并非所有ALT升高都提示真正的DILI, 肝适应现象发生在20%或更多的ATD治疗患者[17]。本组资料显示,大部分(11/16,68.8%)肝功能异常患者为轻度损伤,应归为适应现象,但适应现象背后的机制尚不清楚。无法适应可能涉及环境或遗传因素,或两者兼而有之。有假说认为抗炎细胞因子或氧化应激蛋白的多态性可能使某些个体无法适应和控制轻微的组织损伤[18]。TNF-α是在损伤性免疫反应过程中突出的细胞因子,也可以促进细胞死亡[19]。应用适应性应激通路预测DILI发生研究显示,氧化应激通路SRXN1有重要意义,Srxn1和Foxo3α的上调可能通过增加抗氧化系统HO-1和SOD改善氧化应激诱导的细胞死亡[20]。
本研究观察了应用苦黄注射液预防性治疗抗结核药物性肝损伤发生的安全性和有效性。苦黄注射液主要成分包括苦参、大黄、茵陈、春柴胡、大青叶等五味中药。近年来的研究发现,苦黄注射液可用于酒精性脂肪肝和药物性肝损伤等疾病的治疗,具有降低血清ALT、AST和TBIL水平,缓解肝区疼痛及延缓肝纤维化进程等优势。本研究结果显示,在治疗8周末,试验组血清ALT、AST和TBIL等指标和肝损伤发生率均优于对照组(P<0.05)。进一步研究发现,试验组患者治疗后血清HO-1和SOD水平升高及IL-6和TNF-α水平降低非常明显,提示在接受抗结核药物治疗的基础上联用苦黄注射液有利于机体炎症氧化应激的调节,对肝脏的保护可能起到关键作用。苦黄注射液安全性良好,能有效预防ATD诱导的肝损伤。
