共存阳离子对含锰酸性矿山废水化学中和处理过程的影响
2024-01-06岳正波许庆升王绍平王广成
杨 程, 岳正波, 许庆升, 王绍平, 王广成, 王 进
(1.合肥工业大学 资源与环境工程学院,安徽 合肥 230009; 2.安徽马钢矿业资源集团南山矿业有限责任公司,安徽 马鞍山 243000)
近年来,随着我国工业化进程不断推进,冶炼、矿山等行业迅速发展,在消耗大量水资源的同时,也造成了大量含锰酸性矿山废水(acid mine drainage,AMD)的排放[1]。AMD对环境危害巨大,若不经处理直接排入自然水体,则会导致植物的枯萎、死亡以及土壤的酸化、毒化,还会对鱼类、水藻等水生生物构成极大威胁,甚至会通过食物链的富集最终危害人类健康[2-5]。因此,含锰AMD的高效处理方法与机理逐渐成为研究热点。
目前,主要的处理方法有化学中和法、硫化物沉淀法、人工湿地法及生物吸附法。其中化学中和法具有成本低、工艺流程相对简单的特点,是目前主流的去除工艺[6-7]。对于共存阳离子对锰离子去除的影响,已有一些研究报道。文献[8]研究表明,当共存Fe2+时,在w(Fe2+)/w(Mn2+)>4下,会发生Fe2+氧化成Fe3+,而Mn则被重新溶解并以Mn(Ⅱ)重新引入溶液中,从而抑制Mn的沉淀;文献[9]研究发现,Al3+的中和产物Al(OH)3对锰离子有较强的吸附作用,且随着pH值的增大,吸附效果增强;文献[10]指出,Fe的产物铁氢化物表面在Mn(Ⅱ)氧化过程中也可能起着重要而特殊的作用。但是对于含锰AMD中和固相产物中锰的形态,相关研究很少。
本文通过配制模拟AMD并采用化学中和法进行处理,研究曝气搅拌和机械搅拌2种条件下,常见共存离子Mg2+、Al3+和Fe2+对锰离子去除的影响,并对固相产物中锰的平均价态及物相进行解析。
1 实验材料与方法
1.1 主要试剂
本实验使用MnSO4溶液配制600 mg/L模拟AMD,配制1 mol/L NaOH溶液中和处理模拟AMD,主要试剂有MnSO4·H2O、NaOH、MgSO4·7H2O、Al2(SO4)3·18H2O、FeSO4·7H2O、草酸钠、过硫酸铵等,均为分析纯。
1.2 实验设计
室温条件下进行4组实验,即分别添加Mg2+、Fe2+、 Al3+模拟AMD组(共存Mg2+组、共存Fe2+组、共存Al3+组)及空白对照组,外加离子质量浓度均为1 000 mg/L,体系均为3 L,初始pH=3.0。每组实验分别采用曝气搅拌和机械搅拌2种处理工艺(曝气量为23.3 L/min),同时以222 mL/h匀速添加1 mol/L NaOH溶液,调节pH=9.5,记录各阶段碱液消耗量、溶解氧(dissolved oxygen,DO)和锰离子的变化情况。
对最终的中和产物进行锰的平均氧化态(average oxidation state of manganese,MnAOS)分析测定和X射线衍射(X-ray diffraction,XRD)分析。根据实验结果,分析不同ρ(Al3+)对化学中和法处理AMD的影响。
1.3 测定分析方法
采用pH-501工业pH计(济南研华分析仪器有限公司)和DO601溶解氧仪(济南研华分析仪器有限公司),实时监测pH值及DO变化;金属离子采用WYS2200火焰型原子吸收光谱仪(安徽皖仪科技股份有限公司)测定,锰离子去除率η计算公式为:
(1)
其中:ρ0为锰离子初始质量浓度;ρ为处理后锰离子质量浓度。
中和固相产物组成成分采用D/MAX-2500 X射线衍射仪(日本理学株式会社)测定,扫描范围为10°~70°;中和固相产物锰的平均价态采用高锰酸钾光度法测定[11]。
2 实验结果与讨论
2.1 不同金属离子对锰去除率的影响
2种搅拌条件、不同共存金属离子下锰离子去除率随pH值变化如图1所示。从图1可以看出,尽管搅拌条件不同,随着pH值增大,ρ锰离子均逐渐下降,其中对照组、共存Mg2+组和共存Fe2+组在pH=8.0后,锰离子去除率显著提高。值得注意的是,Al3+存在下,体系pH>6.0时ρ锰离子开始迅速下降,且最终出水ρ锰离子低于其他实验组,这表明Al3+对锰离子的去除效果最佳。这主要是由于在强碱作用下,共存Al3+组生成比表面积较大、孔隙度较高的絮状Al(OH)3沉淀[12],对锰离子具有较强的吸附能力。进一步分析可知,Al(OH)3的溶度积Ksp=4.57×10-33,根据溶度积公式,Al3+在pH=6.0已经完全沉淀,故当pH>6.0时,体系中产生大量的絮状Al(OH)3,其对废水中的锰离子具有良好的吸附性能。这种吸附过程伴随着表面羟基的参与,因而具有较强的pH值效应,pH≤6.0时H+较多,影响吸附性能,进而抑制锰离子的去除效果[9]。
对比图1a、图1b可知:共存Al3+组在pH=9.5时,机械搅拌和曝气搅拌2种处理工艺对出水中ρ锰离子无显著影响;而在对照组、共存Fe2+组、共存Mg2+组中,曝气搅拌提高了锰离子的去除率。在氧化条件下,Mn2O3和MnOOH等锰氧化物生成,而MnCO3在pH值为7.0~11.0时,在碳酸根离子存在下自然沉淀[13]。曝气搅拌同时引入空气中的CO2和O2,导致水中游离Mn2+更容易被氧化或是以碳酸盐形式沉淀去除。其中,在共存Mg2+组中,当pH≥9.0时,会产生大量具有絮凝作用的Mg(OH)2沉淀,从而促进Mn2+的去除[14]。在机械搅拌下溶液pH≥8.5时,相比于对照组,共存Fe2+组中锰的去除率更高,这是由于机械搅拌提供的DO不足,导致大量Fe2+和Fe3+共同存在,形成具有絮凝作用的铁氧体、Fe(OH)2和Fe(OH)3沉淀,从而促进锰离子的吸附去除[15-17]。而在曝气搅拌条件下,Fe2+几乎被完全氧化为Fe3+,形成Fe(OH)3沉淀。
综上可知,当Al3+存在时,锰离子的去除效果最佳,下面进一步分析对比曝气搅拌条件下不同ρ(Al3+)对锰离子去除效果的影响。曝气搅拌下不同ρ(Al3+)时锰离子去除效果对比如图2所示。
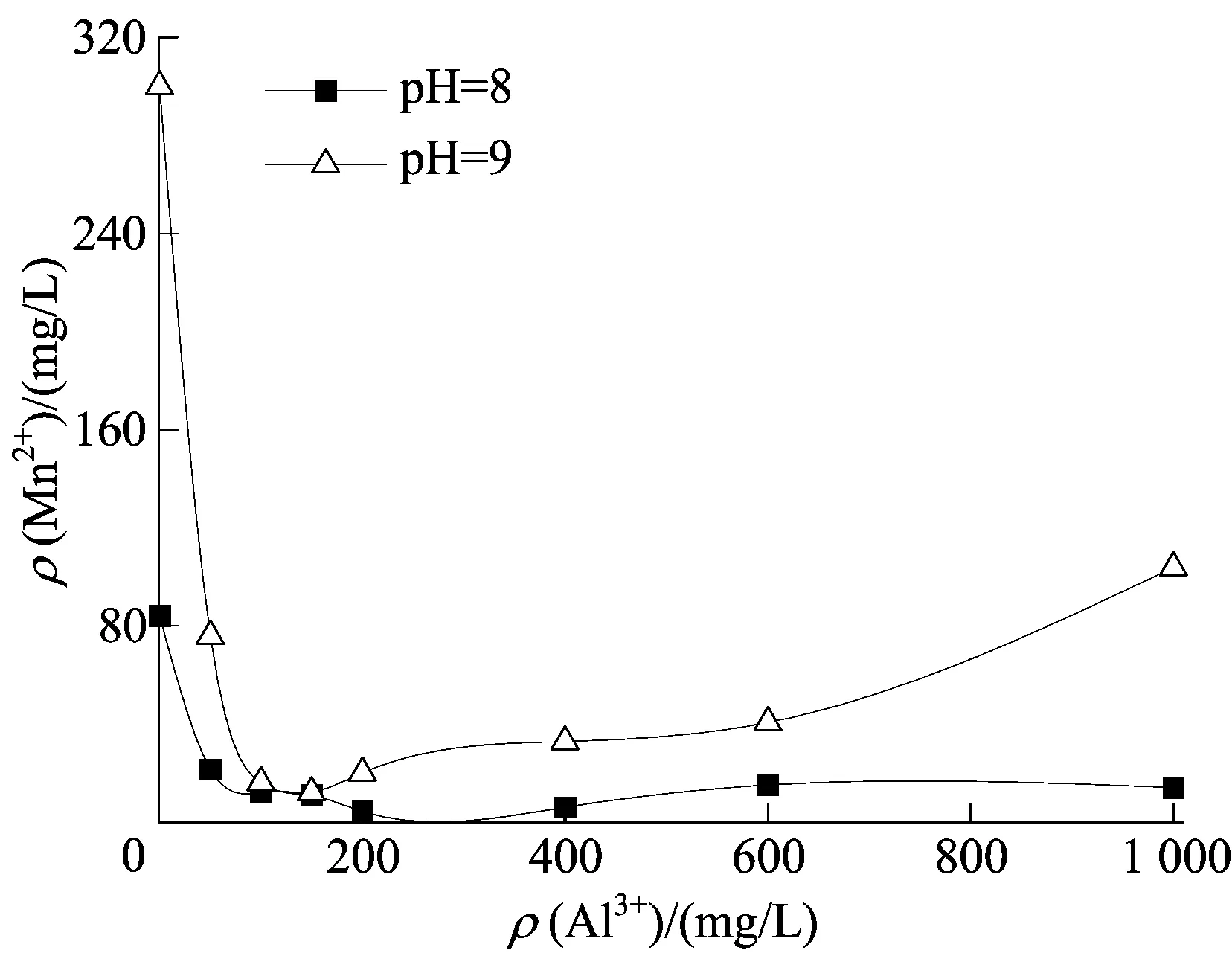
图2 曝气搅拌下不同ρ(Al3+)时锰离子去除效果对比
从图2可以看出:当pH=9.0、ρ(Al3+)为0~200 mg/L时,锰离子的去除率呈明显递增趋势,这是由于随着ρ(Al3+)增大,产生的具有吸附作用的絮状Al(OH)3沉淀增多,大量的锰离子被吸附去除;随着ρ(Al3+)继续增大,最终剩余锰离子的质量浓度却缓慢增加。这是由于Al3+及其产物对锰离子的氧化具有抑制作用,而在0~200 mg/L内,Al(OH)3的吸附点位渐趋饱和,对锰的吸附效果接近阈值吸附量。若此时Al3+及其产物在体系中过量存在,则会导致抑制作用更显著。
2.2 不同共存金属离子对DO的影响
在曝气搅拌条件提供相对稳定的氧化环境下,各组实验中ρDO一直维持在8.5~9.0 mg/L之间,没有明显变化;但在机械搅拌条件下,ρDO变化显著。机械搅拌、不同共存离子下ρDO随pH值的变化如图3所示。

图3 机械搅拌、不同共存离子下ρDO随pH值的变化
从图3可以看出,在机械搅拌条件下,各组实验中ρDO随pH值变化均呈递减趋势。其中共存Al3+组DO的主要消耗在pH值为3.5~4.5之间,此时Al3+沉淀使DO减少,pH>4.5后,ρDO无明显变化。
2种搅拌条件、不同共存离子下中和产物锰的平均价态对比如图4所示。

图4 2种搅拌条件、不同共存离子下中和产物锰的平均价态
由图3、图4可知,在机械搅拌条件下,共存Al3+组锰的平均价态最低,抑制锰离子的氧化过程,相对于对照组中和过程耗氧量减少。
共存Mg2+组与对照组的ρDO变化趋势相同,这是由于在pH=8.7左右ρDO降至0 mg/L,而Mg2+的反应主要在此之后,共存Mg2+组在中和过程中基本是锰离子反应消耗DO[18]。
而机械搅拌条件下,共存Fe2+组DO的消耗主要发生在pH=5.5之前,随后ρDO维持在4.1 mg/L左右。由图4可知,共存Fe2+组有利于锰离子的氧化,其中和过程产生的具有半导体性质的铁氧化物有利于电子转移,减少了DO消耗,因而ρDO不会降低至4.0 mg/L甚至更低水平。
2.3 不同金属离子对锰离子氧化程度的影响
在一般环境pH值和Eh条件下,均相体系中Mn(Ⅱ)到Mn(Ⅲ/Ⅳ)氧化物的非生物氧化速率在动力学上非常缓慢,除非pH>8.0。有研究表明,锰以锰(Ⅱ)的形式存在于溶液中,以锰(Ⅲ)和锰(Ⅳ)的氧化物形式存在于固体中[19]。
由图4可知,2种搅拌条件下,锰中和产物的平均价态差异不明显。
2种搅拌条件、不同共存离子下中和产物XRD分析结果如图5所示。
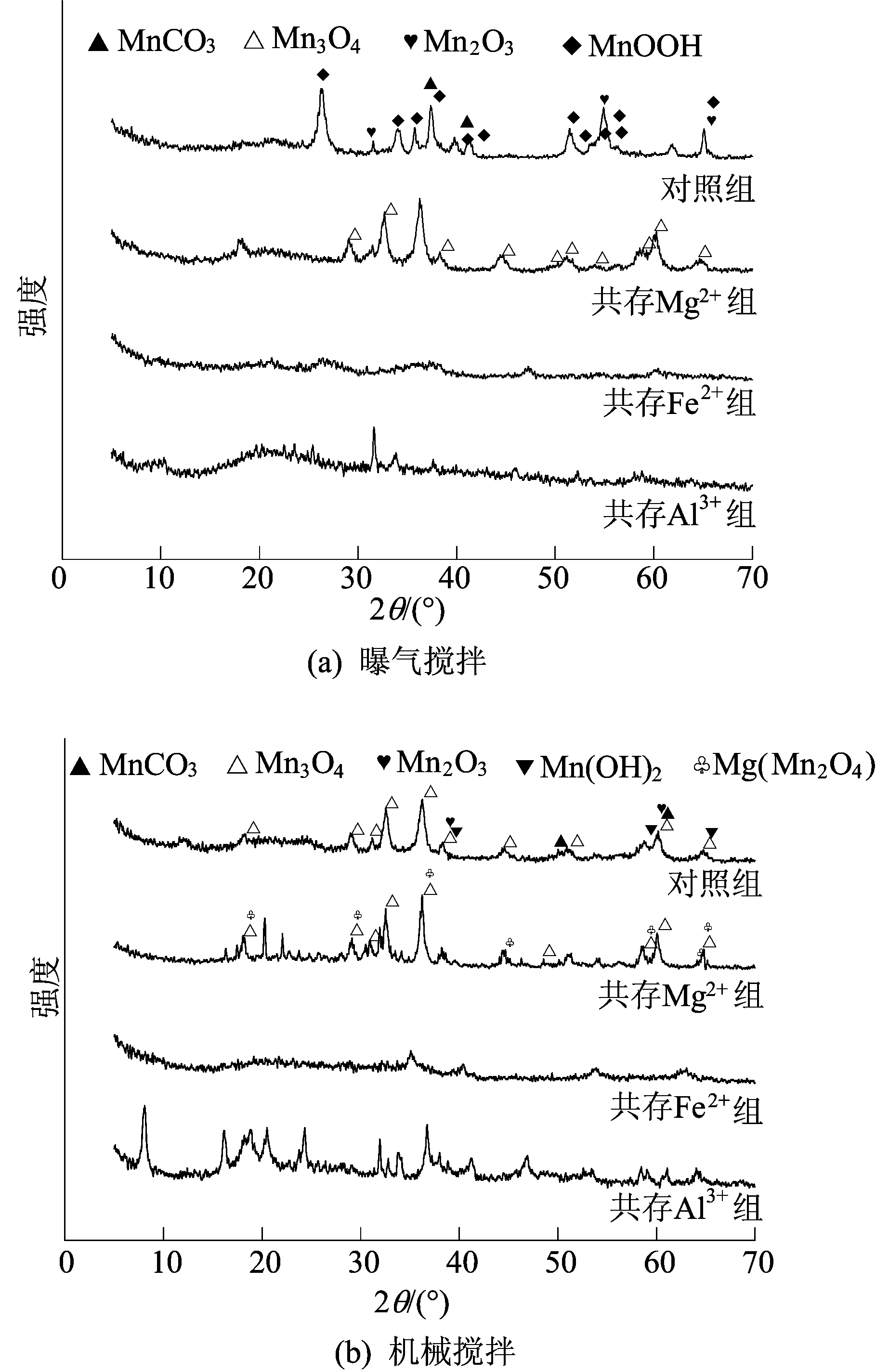
图5 2种搅拌条件、不同共存离子下中和产物XRD分析结果
由图5可知,曝气搅拌生成氧化物沉淀的同时,还生成大量MnCO3沉淀,MnCO3沉淀可以覆盖已经形成的(自催化活性)MnOx,通过延迟和干扰自催化吸附和氧化反应来阻碍成熟过程。因此,MnCO3的可能形成及其在过滤介质上的保留将不利于过滤介质的成熟过程[20]。
氧化铁能通过界面效应催化锰离子的氧化,在所有的铁(氧合物)氧化物中,水铁矿具有最小的晶体尺寸和最差的结晶度,因此显示出最强的表面活性[10]。水铁矿表面促进Mn(Ⅱ)氧化,从而导致形成水锰矿、水钠锰矿和黑锰矿(Mn3O4)[21]。铁氢化物表面在Mn(Ⅱ)氧化过程中也可能起着重要而特殊的作用。共存Fe2+组由于产生Fe3O4等具有半导体特性的铁氧体物质,会促进Mn(Ⅱ)的氧化,但曝气搅拌下形成的产物主要以Fe(OH)2、Fe(OH)3为主,因此相对于对照组,提高Mn(Ⅱ)氧化的效果并不显著。
在具有相同的总表面积时,晶态Al(OH)3对Mn(Ⅱ)氧化的催化活性强于非晶态的Al(OH)3。尽管非晶态Al(OH)3表面上的表面官能团与水铁矿表面相似,但非晶态Al(OH)3表面对Mn(Ⅱ)的催化活性非常弱。强碱作用下,Al3+产生的非晶态Al(OH)3是一种具有吸附性能的绝缘体材料,虽然能吸附去除锰离子,但不利于电子的传递和传输,从而抑制Mn(Ⅱ)氧化,因此共存Al3+组的中和产物锰的平均价态均低于其他组[22]。
共存Mg2+组的中和产物锰平均价态接近于对照组,说明Mg2+对于锰离子的氧化影响并不明显。
2.4 不同金属离子对含锰废水中和产物的影响
由图5可知,中和产物中含锰物质主要包括黑锰矿(Mn3O4)、菱锰矿(MnCO3)、Mn(OH)2、水锰矿(MnOOH)和Mn2O3。曝气搅拌相对于机械搅拌,中和产物中含有较多的MnCO3、MnOOH和Mn2O3,这是由于曝气搅拌充入大量空气,而空气中含有O2、CO2等,CO2溶于体系中,形成的CO32-与Mn(Ⅱ)结合生成MnCO3[23],充沛的O2在提供充足的氧化还原电位后,Mn(OH)2易被氧化成MnOOH、Mn2O3等物质。在机械搅拌下,由图3可知,在pH=8.7后ρDO=0 mg/L,Mn(OH)2能在体系中稳定存在[24]。
在共存Al3+组、共存Fe2+组,中和过程中形成大量絮状无定形沉淀,抑制晶体衍射峰的形成,无法准确地判断出主要生成的含锰中和产物。而在共存Mg2+组,由于锰镁的共沉淀作用生成Mg(Mn2O4),有利于锰的去除。
2种搅拌条件、不同共存离子下中和产物锰质量比的对比如图6所示。

图6 2种搅拌条件、不同共存离子下中和产物锰质量比的对比
由图6可知:机械搅拌下中和产物中锰的质量比低于曝气搅拌,而曝气搅拌能够加强Mn2+的氧化程度;外加金属离子显著影响锰在中和产物中的质量比。其中共存Mg2+组2种搅拌条件下的差异显著,这是由于镁锰形成共沉淀物质Mg(Mn2O4),镁在中和产物中的质量比增加,导致锰质量比降低;在共存Al3+组、共存Fe2+组,中和产物中锰的质量比较低,可能不利于锰的回收利用,且铝、铁对中和产物物相组成的影响更显著[25]。
3 结 论
曝气搅拌条件下由于锰的氧化程度更高,去除效果优于机械搅拌。Fe2+、Mg2+、Al3+3种金属离子会在中和过程中形成絮凝沉淀,从而促进对锰离子的吸附。Al3+的强化去除效果最佳,但Al3+及其产物对Mn(Ⅱ)的氧化有抑制作用。Fe2+存在下,生成的半导体特性的铁氧体物质会促进Mn(Ⅱ)的氧化。与机械搅拌相比,曝气搅拌过程中产生较多氧化物沉淀和MnCO3沉淀。当共存Mg2+时,生成的Mg(Mn2O4)共沉淀物质促进锰的去除。而高质量浓度Al3+、Fe2+的存在会显著影响中和产物物相组成;Al3+存在时,锰在中和产物中的质量比最低;而Al3+、Fe2+存在时,锰在中和产物中的质量比较低,不利于锰的回收利用。
