物理回收下再生聚对苯二甲酸乙二醇酯的物理表征及挥发性有机化合物监测
2024-01-03金莉莉吴永宁罗世鹏商贵芹王志伟刘桂华胡长鹰
曾 严,金莉莉,朱 蕾,吴永宁,罗世鹏,商贵芹,王志伟,刘桂华,,胡长鹰,,
(1.暨南大学理工学院食品科学与工程系,广东 广州 510632;2.常州工业及消费品检验有限公司,江苏 常州 213017;3.国家食品安全风险评估中心,北京 100022;4.南京海关危险货物与包装检测中心,江苏 常州 213000;5.暨南大学包装工程学院,广东 珠海 519070)
聚对苯二甲酸乙二醇酯(polyethylene terephthalate,PET)是公认的优良材料[1-3],广泛应用于软饮料、矿泉水、果汁、啤酒等食品包装。PET消费量的不断增长,如不合理处置将会对资源浪费、人类健康和生态环境造成严重影响[4]。由于PET具有相对于其他塑料更低的吸收消费后污染物的能力,被认为是最可能实现回收并同级使用的食品包装塑料,并且已在欧美推广使用[5-7]。食品用PET瓶的理想回收方式是“瓶到瓶”之间的回收利用[6]。
PET瓶的回收利用方法可主要分为物理回收法和化学回收法[8-9]。物理回收法是将PET经脱标、分选、破碎、清洗、熔融挤出等工艺过程后,通过固相增黏(solid state polycondensation,SSP)再加工成新制品[10-11]。在回收PET(rPET)物理表征方面,较多集中在熔融挤出工艺上的热降解研究[12-15],而缺乏对各个阶段下rPET的基础表征。表征可以帮助跟踪并判断各工艺过程对回收后材料性能以及对小分子污染物的产生和消除效果的影响。而回收过程中小分子污染物的存在,严重影响PET的同级回收利用[6]。回收材料中的小分子污染物主要是挥发性有机化合物(volatile organic compounds,VOCs),其主要是聚合物在再生过程中热氧化和热降解的结果[16]。rPET中经常存在的VOCs如乙醛[17-18]、苯乙烯[19]等物质,不仅具有令人不适的特殊气味,还常常伴随着刺激性、毒性、致癌性和致畸性不良作用。此外,柠檬烯在消费后PET瓶中普遍存在,是回收后清洁程度的重要指标[20-22]。了解物理回收工艺过程中的rPET材料和rPET瓶中VOCs的种类和含量变化,对评判rPET瓶作为食品接触材料的安全性起着重要作用。
早在十几年前,欧盟[23]和美国[24]便建立了rPET的工艺安全性评估,允许受批准的rPET作为食品接触材料。在最近几年,日本、韩国等国家也纷纷出台了相关政策将rPET纳入到允许使用的食品接触材料范围内。在“可持续发展”“碳达峰、碳中和”的大背景之下,中国作为一个PET生产和消费大国,至今还未允许将rPET作为食品接触用。本实验主要有以下两个目的:其一,对来自目前国内物理回收工艺下的rPET样品以及制成不同回收料含量的rPET瓶进行基础物理表征,以了解rPET的热性能、基团结构、形貌、颜色变化;其二,优化顶空-气相色谱-质谱(headspace gas chromatography-mass spectrometry,HS-GC-MS)条件,对VOCs进行检测,监测VOCs种类和含量的变化。最后对物理回收工艺下的rPET瓶用于食品接触进行初步安全评估。以上研究旨在为中国建立相关标准和法规提供支持。
1 材料与方法
1.1 材料与试剂
从国内企业取同一批次下不同工艺过程的rPET材料,命名为S1系列。其中rPET材料的原料瓶来源于该企业自建回收体系下的饮料瓶;制得回收料含量不同的rPET成品瓶,命名为S2系列。原生PET(vPET)、rPET母粒原料的特性黏度分别为0.776、0.877 dL/g,密度分别为1.382、1.386 g/cm2。具体rPET材料信息见表1。
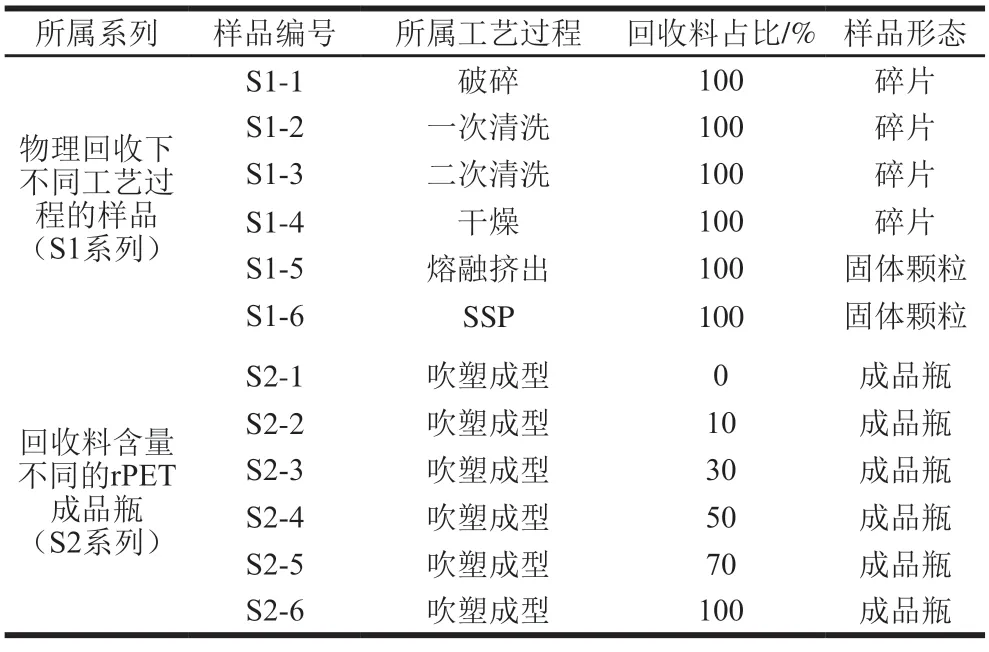
表1 材料的相关信息Table 1 Information about the materials investigated in this study
C7~C40正构烷烃(纯度≥98%)上海安谱实验科技股份有限公司;异丙醇-D8(22739-76-0,纯度≥99%)上海阿拉丁生化科技股份有限公司;氘代甲苯(2037-26-5,纯品型)上海泰坦科技股份有限公司;N,N-二甲乙酰胺(127-19-5,纯度≥99.8%)上海萨恩化学技术有限公司。
1.2 仪器与设备
Ultra-55型场发射扫描电子显微镜 蔡司光学仪器(上海)国际贸易有限公司;TGA/DSC 3+型热重及同步热分析仪 梅特勒-托利多仪器(瑞士)有限公司;Nicolet iS50+iN10型傅里叶变换红外光谱仪 赛默飞世尔(上海)仪器有限公司;UltraScan PRO型分光测试仪美国HunterLab公司;7697A/8890/5977B型HS-GC-MS联用仪、DB-WAX色谱柱(30 m×250 μm,0.5 μm)美国Agilent公司;EL 104型电子天平 梅特勒-托利多仪器(上海)有限公司;MM400型冷冻混合球磨仪弗尔德(上海)仪器设备有限公司。
1.3 方法
1.3.1 热重(thermal gravity,TG)分析
将样品放入液氮中进行充分冷却后,边加液氮边用球磨仪粉碎形成粉末,用电子天平称取粉碎样品约10 mg左右置于坩埚中。用热重及同步热分析仪对粉碎样品进行测试。在氮气(流速(50±5)mL/min)保护下,以10 ℃/min速率由25 ℃升温至600 ℃,记录TG和微分热重(derivative thermogravimetry,DTG)数据。
1.3.2 差示扫描量热分析
用电子天平称取粉碎样品约6~8 mg左右置于铝制坩埚中,采用差示扫描量热仪对样品进行测试。温度扫描程序:1)在氮气的保护下,样品以20 ℃/min的速率从30 ℃加热到300 ℃,以消除热历史;2)300 ℃保持5 min后,以20 ℃/min降温速率降至30 ℃;3)30 ℃保持5 min后,再以20 ℃/min升温速率升至300 ℃。用空的坩埚作为参考,记录相关数据。S1系列样品选取第1次升温数据以研究其在回收再生过程中所受到的热影响,S2系列样品选取第2次升温数据以研究其熔融焓、结晶度等差异性。结晶度按式(1)计算:
式中:ΔHm、ΔHc分别为测试样品的熔融焓和结晶焓;为100%结晶的PET样品的熔融焓(140 J/g)。
1.3.3 傅里叶变换红外光谱
对S 2 系列样品选取相同中间的部位剪裁成2 cm×2 cm大小,把样品分别放在红外光谱附件晶体表面,调整压力板使样品和晶体表面贴紧,进行数据采集,扫描范围为800~4 000 cm-1,扫描次数为32,分辨率为4 cm-1。
1.3.4 形貌特征
表面形貌:对S2系列样品选取相同中间的部位剪裁成1 cm×1 cm型,样品充分干燥后用导电双面胶黏贴安装在青铜载物台上进行喷金处理,采用扫描电子显微镜观察样品表面的微观结构。电压为20 kV,放大倍数为1 000。
横截面形貌:将S2系列样品置于液氮中充分冷却后,选取相同部位使其发生冲击断裂,样品充分干燥后用导电双面胶黏贴安装在青铜载物台上进行喷金处理,采用扫描电子显微镜观察样品横截面的微观结构。电压为15 kV,放大倍数为100 000。
1.3.5 颜色、色差测定
采用分光测色仪对S2系列样品瓶进行颜色测定,得到L*、a*、b*值。以S2-1 vPET瓶为对照样品,计算相关样品的总色差ΔE。计算如式(2)所示:
式中:ΔL*、Δa*、Δb*分别表示不同回收含量的rPET瓶与vPET瓶L*、a*、b*值的差值。
1.3.6 VOCs检测分析
1.3.6.1 样品前处理
将样品放入液氮中进行充分冷却后,边加液氮边用球磨仪粉碎形成粉末。将粉碎的样品称取1.00 g置于洁净的顶空瓶中,加入混合内标后立即盖上盖子,后经过HSGC-MS上机分析。
1.3.6.2 HS-GC-MS分析条件
HS条件:平衡温度:120 ℃;平衡时间:45 min;定量环温度:130 ℃;传输线温度:140 ℃;进样量:1 mL。
GC条件:色谱柱:DB-WAX(30 m×250 μm,0.5 μm);进样口温度:200 ℃;分流比:3∶1;进样量:10 μL;升温程序:初始温度为40 ℃,保持3 min,再以15 ℃/min升至240 ℃,保持15 min,后运行温度为240 ℃,保持2 min。载气为氦气,载气流速为1.0 mL/min。
MS条件:电子能量:70 eV;离子源温度:230 ℃;四极杆温度:150 ℃;溶剂延迟时间:0 min;扫描方式:全扫描模式;质量扫描范围:30~900 Da;扫描速率:1.7 spectra/s。
1.3.6.3 化合物的定性与定量分析
检出的未知化合物使用NIST 20.L数据库和实验室自建的内部数据库对目标物质进行检索,结合保留指数定性,统计匹配度大于80%的VOCs。检出的含硅化合物均被排除在外(如硅氧烷、硅烷等),因为它们极有可能是来自色谱柱、隔膜、顶空瓶密封盖,并不能算作为样品中的检出化合物[21]。
采用半定量方式对检出物质定量[25-26]。采用异丙醇-D8、氘代甲苯、N,N-二甲乙酰胺作为半定量内标。化合物含量的计算如式(3)所示:
式中:Cx为目标化合物的含量/(mg/kg);Ax和Ai分别为目标化合物和内标物质的峰面积;Ci为加入的内标物质的质量浓度/(mg/L);Vi为加入内标物质的体积/µL;M为加入样品质量/g;1 000为单位换算。
1.4 数据处理
2 结果与分析
2.1 TG分析
采用TG分析法研究氮气氛围下rPET的热降解和热稳定性(图1、2)。S1、S2系列样品的TG和DTG曲线相互重叠,样品分解温度在350~500 ℃范围内,主要是由聚酯大分子链的断裂,产生乙烯基酯和羧酸等初级产物[29-31]。显著质量损失(即5%的质量损失)在400 ℃之后才逐渐呈现出大分子链的分解断链,而当温度超过500 ℃以后,TG和DTG曲线趋于平缓,最后形成碳化残余。S1系列形成的碳化残余物在14.2%~17.5%之间,而S2系列vPET/rPET瓶集中在13.6%左右。DTG表明所有样品的最大分解速率均处于在440 ℃左右。物理回收过程中的rPET样品和rPET成品瓶都表现出与vPET相似的热稳定性,说明物理回收并没有明显影响rPET的热稳定性。
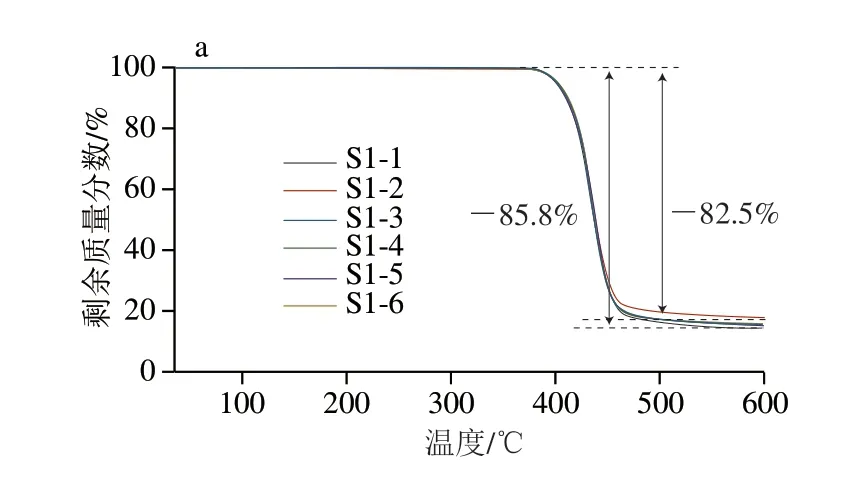
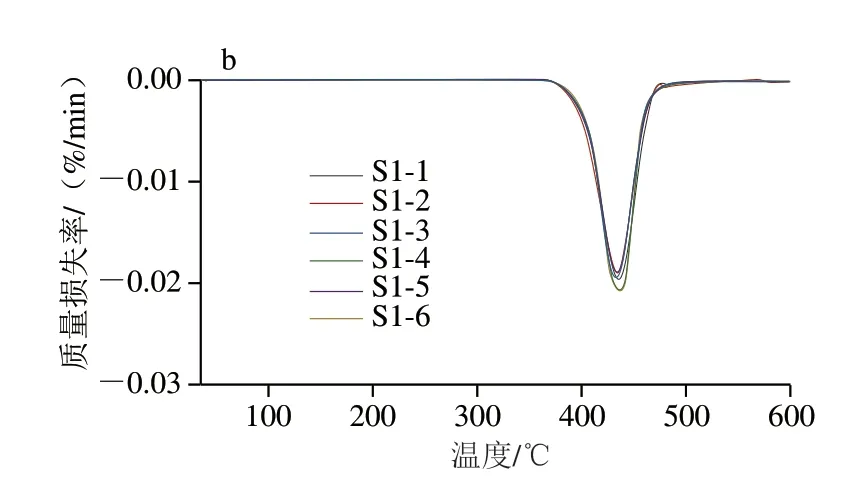
图1 S1系列rPET的TG和DTG曲线Fig.1 TG and DTG curves of S1 series of rPET
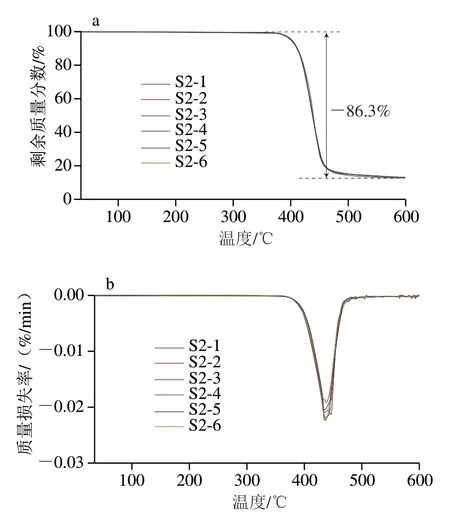
图2 S2系列rPET瓶的TG和DTG曲线Fig.2 TG and DTG curves of S2 series of rPET bottles
2.2 熔融及结晶行为分析
PET通常是一种半结晶聚合物,具有低结晶速率的特征[32]。但无定形PET的透明性对其在饮料工业中的应用非常有吸引力,而PET的结晶度越高,渗透性越低,越有利于保存易于氧化的食品和饮料[33]。从DSC曲线中可以了解到rPET的结晶和融化行为。
2.2.1 物理回收过程中rPET的熔融及结晶行为
绝大多数PET材料的玻璃化转变温度(Tg)都是处于67~140 ℃[34],物理回收过程中的rPET的Tg在72.6 ℃左右(图3),说明物理回收过程中rPET呈现出较好的分子柔韧性。只有在熔融挤出后的rPET(S1~5)出现了冷结晶峰,结晶温度(Tc)为121.6 ℃。说明熔融挤出后没有足够的时间使rPET完全结晶,从而在升温当中使得分子链进一步排入晶格。物理回收中的样品的熔融温度(Tm)大多集中在248.5~253.0 ℃左右,这与商业用PET的Tm(255~265 ℃)相近[34],但SSP后的样品出现了Tm(239.1 ℃)向低温偏移的现象,且熔融焓相对于其他样品有所增大,可能的原因是SSP过程发生了缩聚反应,使得聚合物的聚合度增大,从而改变了聚合物的分子链,进一步限制了分子链的运动。
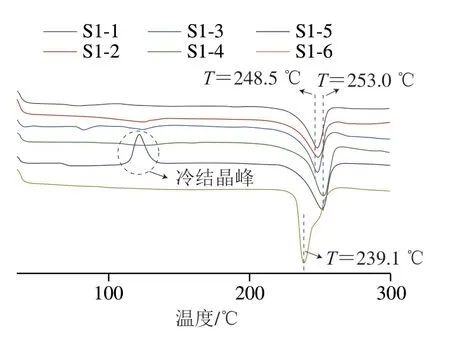
图3 S1系列样品的DSC曲线Fig.3 DSC curves of S1 series of samples
2.2.2 vPET/rPET瓶的熔融及结晶行为
如表2所示,不同回收料含量的rPET瓶和vPET瓶的Tg、Tm和结晶度之间并没有显著差异。其中Tg、Tm分别集中在77、247 ℃左右,而Tc位于134~137 ℃之间,结晶度位于22%~25%之间。表明回收料含量不同的rPET瓶具有与vPET瓶相似的结晶和熔融行为,且回收料含量对rPET瓶的结晶度影响并不显著。
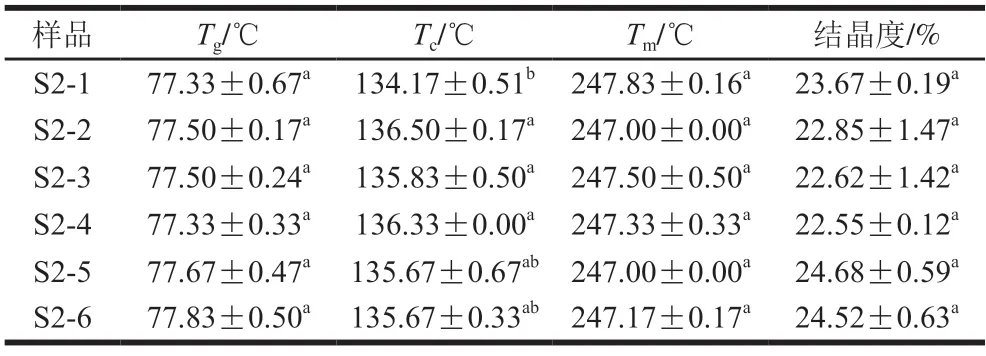
表2 S2系列vPET/rPET瓶的DSC结果Table 2 DSC properties of S2 series of vPET and rPET bottles
2.3 傅里叶变换红外光谱分析
红外吸收光谱有助于分析vPET和rPET瓶的基团及结构的变化(图4)。位于2 963 cm-1和2 902 cm-1附近的吸收峰对应于乙二醇(ethylene glycol,EG)结构中CH2的拉伸振动。如果主链中存在二甘醇(diethylene glycol,DEG)结构,这些振动带将会转移到2 918 cm-1和2 854 cm-1左右[13]。位于1 750~1 700 cm-1处的羰基(C=O)吸收峰是受降解影响的主峰[35-36],随着回收料含量的增加,峰高有所降低,但趋势并不明显。其他两个位于1 250 cm-1和1 100 cm-1附近的较大吸收峰分别对应于酯基((C=O)—O)[37]和(C—O—C)[38]振动。另外一个在700~750 cm-1区域的吸收峰显示了聚合物主链中亚甲基部分的摇摆振动,较大的吸收表明其晶体结构更好[39]。70% rPET瓶样品(S2-5)中主链的亚甲基吸收峰最弱。
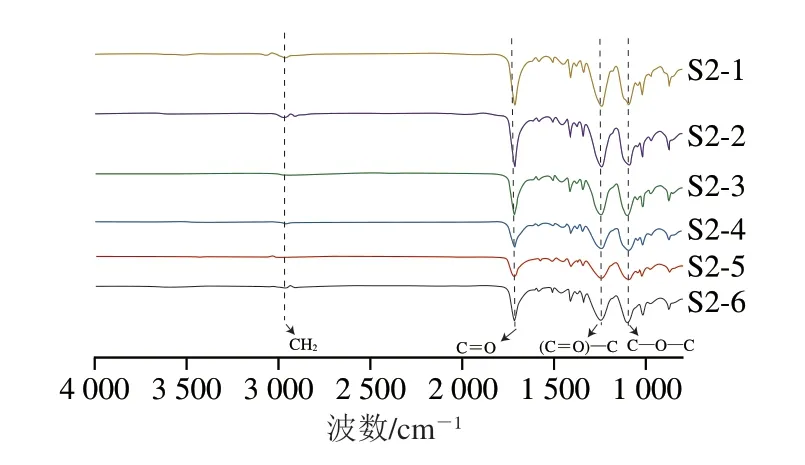
图4 S2系列vPET/rPET瓶的红外光谱图Fig.4 Infrared spectra of S2 series of vPET and rPET bottles
同时还存在一些微弱的峰如:1 440~1 330 cm-1处属于苯环骨架的拉伸振动带;1 020 cm-1的吸收峰对应苯环中C—H的面内弯曲振动[37];870 cm-1处是C—H的面外弯曲振动[36]。可以发现,rPET瓶存在着与vPET瓶一样的红外特征吸收峰,不存在新的吸收峰出现和旧吸收峰消失。这表明PET在物理回收工艺下制成的rPET成品瓶并未产生基团和结构上的明显变化,即化学结构较稳定。
2.4 形貌分析
2.4.1 表面形貌
对vPET瓶和rPET瓶的表面形貌进行观察(图5)。不管是vPET瓶还是rPET瓶的表面都呈现出致密、稳定的状态。但随着回收料添加量的增加,rPET瓶的表面粗糙程度有所差异,这主要体现在更容易被机械划伤[13]。这种细微机械划伤是否会影响rPET瓶内部物质的迁移从而影响包装食品的安全值得进一步考虑。类似的形态缺陷也在其他回收塑料中(如聚烯烃[40]、聚苯乙烯[41])有所体现。

图5 S2系列vPET/rPET瓶的表面形貌图Fig.5 Surface morphology of S2 series of vPET and rPET bottles
2.4.2 横截面形貌
如图6所示,6 种样品的断裂面均表现平滑、完整的状态,表明不同回收料含量的rPET瓶中vPET和rPET两相成分都能够很好地结合,其他vPET[42]、rPET[43-44]研究当中也呈现出相似的截面形貌。并且,均未观察到有任何杂质或异物的存在,这也证明了物理回收对杂质去除能力较为显著。但在S2-6 100% rPET瓶中出现了较大面积的细微裂缝,在S2-4、S2-5中也有轻微存在(蓝色曲线标注),可能是由于受到冲击应力导致,这表明高比例回收料含量的rPET瓶承受冲击应力的能力较差,从而易导致应力开裂。
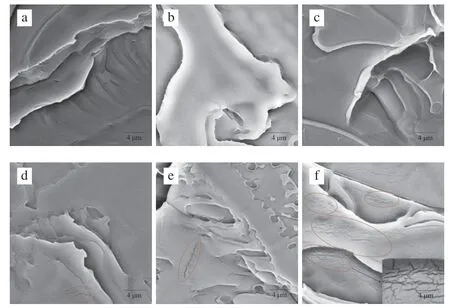
图6 S2系列vPET/rPET瓶的横截面形貌图Fig.6 Cross-sectional morphology of S2 series vPET and rPET bottles
2.5 颜色、色差分析
如表3所示,不同回收料含量的rPET瓶和vPET瓶的L*、a*、b*值存在显著差异(P<0.05)。随着回收料含量的增加,L*、a*值存在减小的趋势,b*值则存在增大的趋势,表明回收量含量越高的rPET瓶中,其颜色更深(暗)、更绿和更黄。rPET瓶更绿的原因可能是在回收过程中掺杂了一些绿色或者蓝色瓶片,使得由此类原料制成的rPET瓶的a*值更低[45]。rPET瓶更黄的原因与热降解有关,当在回收再生工艺中的温度高于熔融温度时,rPET中的酯键会发生热裂解形成羧基端和乙烯基酯基端,而羧基端会进一步促进rPET的氧化。因此,在经历过回收工艺的rPET相对于vPET存在着更多的羧基端,并且氧化程度更大,从而引起rPET瓶的黄变[46]。不同回收料含量的rPET瓶与vPET瓶的色差值(ΔE)在1.0~3.2之间,存在着颜色差异,且当回收料含量达到了100%时的rPET瓶ΔE值最大,在一定程度上会影响其外观。
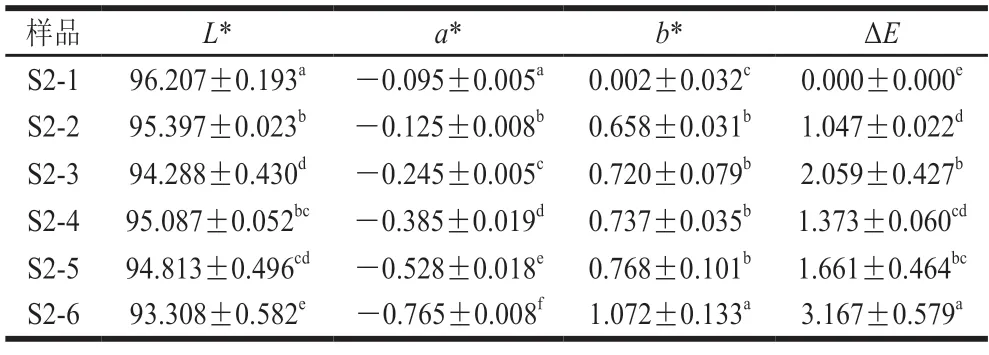
表3 S2系列vPET/rPET瓶的颜色变化Table 3 Color parameters of S2 series of vPET and rPET bottles
2.6 挥发性物质分析
2.6.1 前处理及顶空条件优化
Franz[20,22]、Nerìn[47]等提出,在对rPET材料进行VOCs筛查时不采用研磨、粉碎等前处理方法,因为此类方式会造成交叉污染的风险以及挥发性很强的物质损失。但也有许多vPET、rPET的VOCs研究中依旧采用研磨、粉碎的方式。图7a结果表明,随着rPET样品粒度的减小,总峰面积增大,但未造成VOCs的损失。表明在粉碎前用液氮浸泡和边加液氮边粉碎保证了低温,是可以避免交叉污染的风险和VOCs的损失。
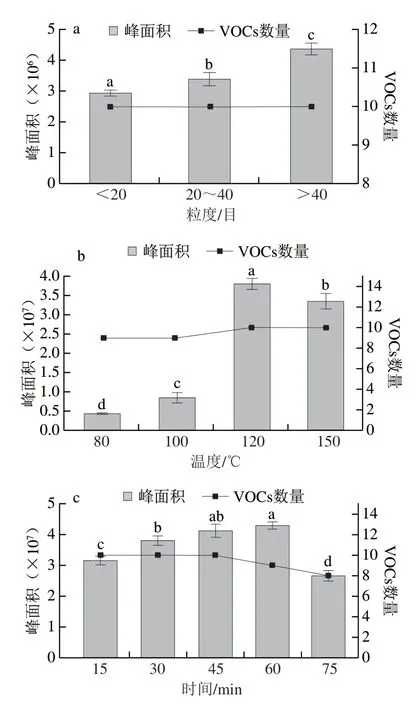
图7 不同前处理和顶空条件下的色谱峰总面积和VOCs数量Fig.7 Total peak areas and numbers of VOCs under different pretreatment and headspace conditions
样品顶空进样时的平衡温度取决于被测组分分子从样品基质扩散到GC的速率[48]。研究结果表明随着顶空平衡温度的升高,检出物质的总峰面积增大,检出物质个数也相应增多(图7b)。但温度达到120 ℃时,总峰面积达到峰值,且平衡温度继续升高时,相应的检出物质个数并未增多,反而会影响气液平衡效果。最后选择120 ℃作为顶空条件的平衡温度。
平衡时间与样品量、平衡温度及样品的挥发性有着密切的联系。当平衡时间在60 min以下时,随着时间延长,VOCs的总峰面积逐渐增加(图7c)。而当平衡温度达到60 min以上时,造成VOCs检出数量下降,可能是由于平衡时间过长,使GC中的水蒸气含量增加,导致目标物数量下降[49]。综合考虑后取45 min作为顶空条件的平衡时间。
2.6.2 VOCs的定性及来源分析
rPET材料中的VOCs主要是醛、醇、烯类物质。其中,乙醛、2-甲基-1,3-二氧戊环(2-methyl-1,3-dioxacyclopentane,2-MD)、EG、柠檬烯是高频检出物质。详细物质信息及含量见表4。
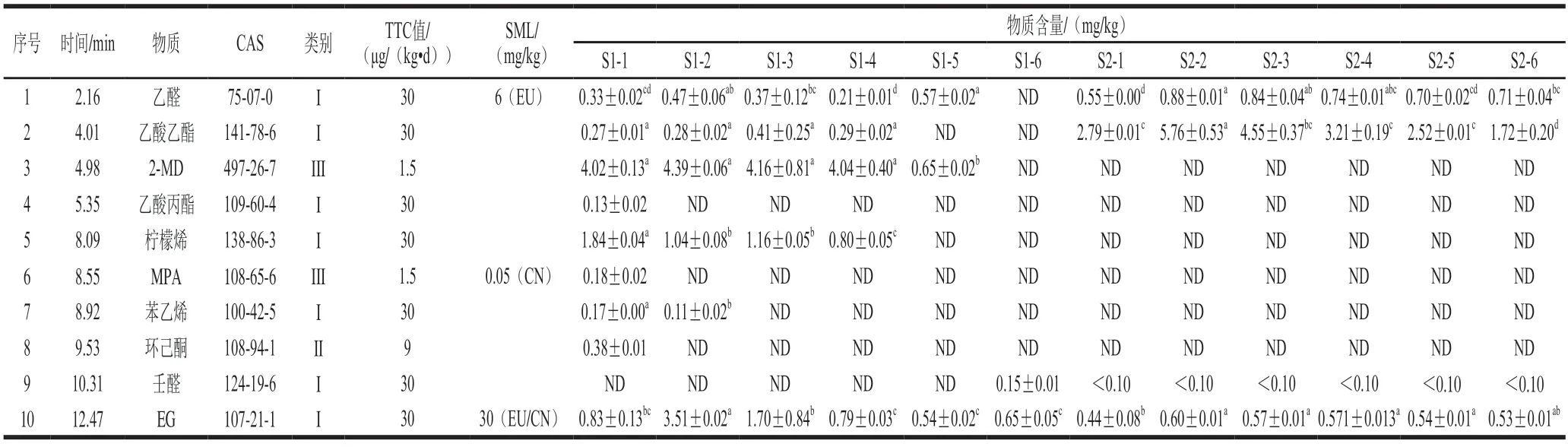
表4 S1和S2系列样品中VOCs的相关信息和定量结果Table 4 Information and quantitative results of VOCs in S1 and S2 series of samples
当PET处于高温条件时(如在熔融挤出、吹塑、注塑等工艺),热降解反应会使得主链内酯基团的随机断链,从而形成羰基和乙烯基酯。之后通过乙烯基酯的酯交换反应生成乙烯醇,最后通过互变异构转化为乙醛[50]。而乙醛的残留及迁移是瓶装水行业的一个关键问题,因为当它扩散到相关食品中时,会改变食品(主要是水)的味道[51]。EG作为最简单的二元醇,不仅是PET的组成单体,也是降解产物之一[6]。2-MD是EG和乙醛的缩合产物,因此它的浓度取决于这两种前体的浓度[19]。壬醛[52]、丙烯醛[53]、2-乙基己醇、环己酮等物质可能是PET相关物质的热降解产物[20]。不仅一些典型的VOCs可以作为rPET热降解产物的代表,一些非挥发性物质如环状、线性寡聚物同样也扮演着重要的角色[54]。rPET材料中柠檬烯(1-甲基-4-(1-甲基乙烯基)环已烯)的存在方式主要以D-柠檬烯为主。柠檬烯是典型的食品残留物之一,可作为区别rPET和vPET的标志物[22]。rPET中的苯乙烯可能来自于某些聚合物的降解,在一些质量低的rPET材料中可能存在着聚苯乙烯污染物,从而降解产生了苯乙烯[50]。乙酸乙酯、乙酸丙酯是应用最为广泛的两种脂肪酸酯,因其拥有良好的性能,广泛应用于香料香精、涂料、油墨等[55]。丙二醇甲醚醋酸酯(1-methoxy-2-propyl acetate,MPA)具有多种官能团,常作为油墨、油漆等的非公害溶剂。有些研究还发现,rPET材料中可能还存在着其他VOCs(如苯[7]、甲醛[53]、β-红没药烯[21]等),或许是由于样品来源的复杂性造成。
rPET中的残留物质是否存在潜在风险,需进行科学评估。表2也提供了rPET材料中主要VOCs的SML、Cramer分类、TTC。SML只适用于在食品模拟物的迁移限值,而对于打算用于食品接触用的rPET瓶,欧洲食品安全局建议在进行超清洁工艺SSP前的rPET材料中的残留物质污染水平控制在3 mg/kg范围内[56]。从现有评估结果看,大部分检出物质的毒性都并不强,且满足上述欧洲食品安全局的建议,但MPA和2-MD作为仅有的两种Cramer III类物质,其安全性需要重点关注。
2.6.3 VOCs含量分析
物理回收过程中的VOCs(除PET自身存在的乙醛、2-MD、EG等),总体上会呈现出随着工艺进程含量逐渐减小直到完全去除的趋势(图8a)。破碎工艺作为物理回收过程的前端,呈现出绝大部分的VOCs,含量在0.13~4.02 mg/kg范围内。它们不只是PET材质本身含有的VOCs,更多的是使用过程中的食品残留物和其他污染物。苯乙烯、乙酸丙酯、MPA等物质在经过清洗工艺后便不复存在,表明了清洗工艺在一定程度上对VOCs的去除起重要作用。柠檬烯作为rPET中的代表物质,由于其沸点高达176 ℃,前期的清洗工艺是完全达不到此温度,所以在熔融挤出工艺中才能完全去除。SSP作为超清洁工艺,不仅能实现rPET主链的延长,还能够有效地去除乙醛和2-MD,但仍然有微量的EG残留((0.65±0.05)mg/kg)。此外,在前端工艺中从未出现的壬醛在SSP工艺中却有微量检出((0.15±0.01)mg/kg),可能是由于高温下的热反应生成。经过物理回收后的rPET呈现出极少的VOCs残留,表明了消费后PET中的食品残留和油墨等污染物能够通过物理回收工艺基本去除。
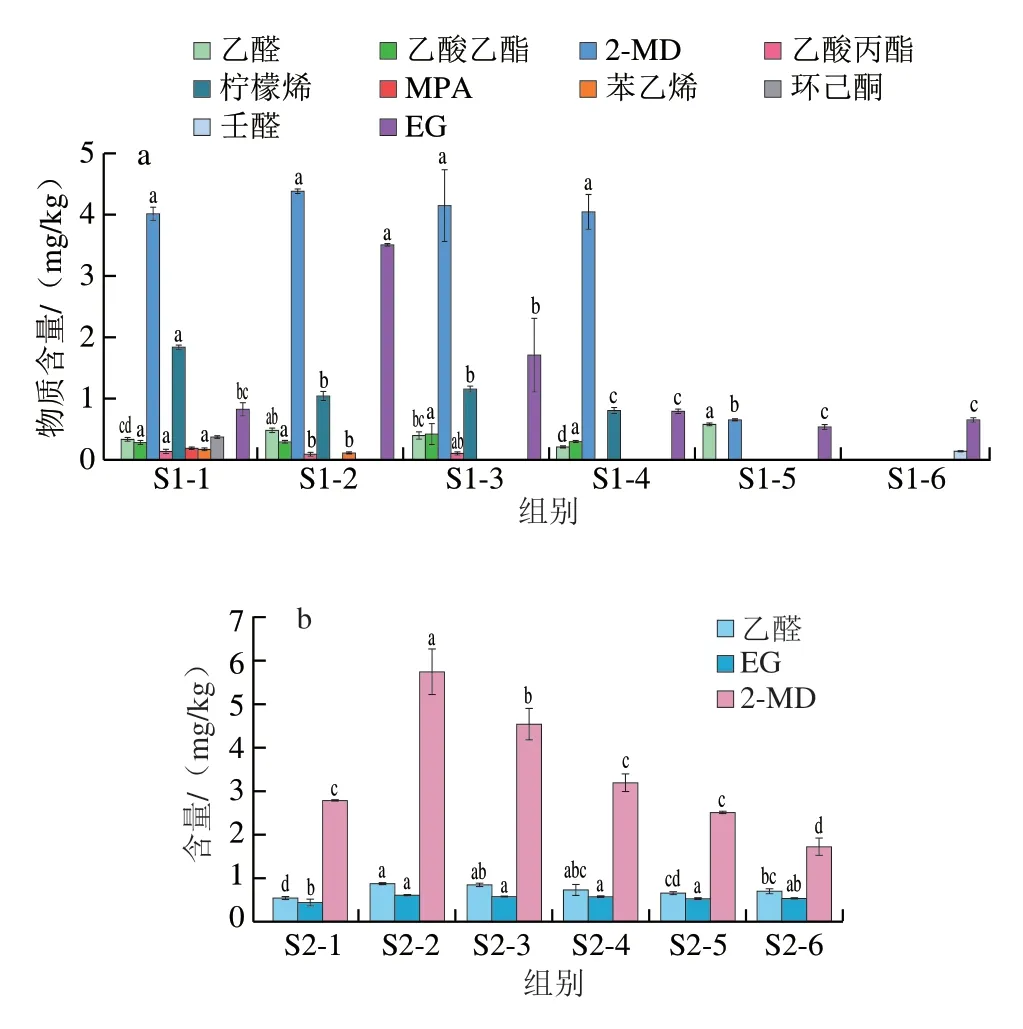
图8 S1、S2系列样品中VOCs的含量变化Fig.8 Changes in the contents of VOCs in S1 and S2 series of samples
对于rPET瓶和vPET瓶中的VOCs,种类一致,但含量存在显著差异(P<0.05)(图8b)。经过SSP工艺后的rPET母粒通过注塑、吹塑等工艺形成制品,在此过程中存在的高温环境容易导致热降解,所以在rPET/vPET瓶中又会形成乙醛、2-MD等物质。乙醛和EG的SML分别为6 mg/kg(EU No.10/2011)和30 mg/kg(EU No.10/2011、GB 9685—2016),壬醛、2-MD不在清单中。壬醛、乙醛和EG在vPET和 rPET瓶中含量都较低(<1.00 mg/kg),而2-MD含量则呈现出稍高状态(1.72~5.76 mg/kg),在10% rPET瓶样品中达到峰值。rPET瓶中2-MD含量与回收料含量的多少并无关系,而取决于回收过程中存在的扩散现象以及其他一些化学反应[52,57]。值得庆幸的是在rPET瓶中并未出现MPA残留,而作为PET材料自身便存在的2-MD是不可避免的。从rPET瓶中所检出的VOCs种类和含量来看,经历过超清洁工艺(SSP)的物理回收法制成的rPET瓶能够作为食品接触用。
3 讨论与结论
采用TG分析、差示扫描量热、傅里叶变换红外光谱、扫描电镜等方法对物理回收下的rPET材料以及制成不同回收料含量的rPET瓶进行热稳定性、熔融和结晶行为、形貌、颜色等物理表征。同时优化了HS-GC-MS的前处理和顶空条件,对rPET中的VOCs进行检测。
不论是rPET过程样品还是回收料含量不同的rPET瓶,物理回收工艺都没有显著影响其热稳定性。rPET瓶具有与vPET瓶相似的结晶和熔融行为,也并未产生基团和结构上的明显变化。但rPET瓶的表面微观形貌出现了细微的机械划伤。同时,经过物理回收后的rPET呈现出极少的VOCs残留,表明了含有SSP等超清洁工艺的物理回收法能够把消费后PET中的食品残留和油墨等化学品去除。在rPET瓶中检出4 种VOCs(乙醛、EG、壬醛均低于1.00 mg/kg;2-MD为1.72~5.76 mg/kg),与vPET瓶中的VOCs种类一致,但含量有所差异。
虽然随着回收料含量的增加,rPET瓶颜色变得更深(暗)、更绿和更黄,但在热稳定性、熔融及结晶行为、结构、形貌等方面的表现,具备了再次用于食品接触的物理条件。在VOCs去污效率的评估上,欧、美、日、韩等国家中,均都采用“挑战性实验”作为回收工艺中VOCs污染物清除效率的手段,即对终端工艺中特定污染物含量的把控。对于现阶段以至未来rPET作为食品接触材料来看,需要选择合适的替代污染物评估我国物理回收工艺过程中的去污效率。此外,严格的回收体系、监管体系也是去污效率好坏的重要因素。
