紫外线活化过一硫酸盐工艺对水中苯脲类除草剂Chlortoluron的去除特性研究*
2024-01-02莫晨骋母兴艳李珍珍田富箱
莫晨骋 赖 璠 母兴艳 陈 晨 李珍珍 田富箱
(上海应用技术大学化学与环境工程学院,上海 201418)
绿麦隆(Chlortoluron)是一种低毒的防治禾本科和阔叶杂草的常见苯脲类除草剂,其性质非常稳定,在水中的降解十分缓慢,半衰期可达几个月甚至几年,这使其在地表水和饮用水中的检出浓度达μg/L水平[1]。我国是农业大国,农药使用量大,农药在田间水体和土壤中的残留量使得这类污染物及其代谢产物对人体带来的健康风险备受关注[2]。已有研究表明,Chlortoluron可能引起动物和人类的代谢紊乱,甚至具有致癌风险和细胞遗传效应[3]。此外,Chlortoluron对水生生物具有毒性,会对水体环境构成严重威胁[4]。因此,世界卫生组织将饮用水中的Chlortoluron最高质量浓度定为30 μg/L[5]。
基于此,本研究分析了UV/PMS工艺对Chlortoluron的去除特性,系统考察了不同水质参数和常见水体背景离子对Chlortoluron降解速率的影响,进而量化评估了不同工况条件下UV/PMS工艺去除Chlortoluron的能耗情况,从而为水处理中UV/PMS工艺对典型苯脲类除草剂Chlortoluron的去除提供理论参考和技术支持。
1 材料与方法
1.1 实验试剂
Chlortoluron(纯度>99%)、过一硫酸钾三盐(2KHSO5·KHSO4·K2SO4)、KH2PO4和乙腈等试剂均为优级纯;NaOH、Na2CO3、NaHCO3、H2SO4、Na2S2O3·5H2O、Na2SO4和乙醇等试剂均为分析纯。实验用水由Milli-Q超纯水机制备。
1.2 分析方法
使用高效液相色谱仪(岛津TC-20A)对Chlortoluron浓度进行测定。色谱柱为XTerra©MS C18色谱柱(4.6 mm×250 mm,5 μm,Waters),测定条件为:流动相由乙腈和水(体积比50∶50)组成,检测波长为241 nm,流速为1.0 mL/min,分析时间为9 min。
1.3 实验方法
配置初始摩尔浓度为20 μmol/L的Chlortoluron储备液,经稀释后为8 μmol/L。使用磷酸盐缓冲溶液调节体系pH。尽管有研究表明磷酸盐的加入对PMS体系有促进作用[13],但课题组实验发现,10 mmol/L磷酸盐存在对Chlortoluron降解无显著性影响。反应开始前加入10 mmol/L的磷酸盐缓冲溶液,对UV/PMS体系中污染物的降解没有显著影响[14]。然后添加一定浓度的PMS溶液。将溶液整体转移至石英管中,放入光反应装置进行UV照射,反应的同时进行搅拌,并开始计时。在反应的不同时刻取样1 mL反应液于液相分析样品瓶中,并用50 μmol/L乙醇淬灭样品中的自由基物种,待实验结束后立即用液相色谱仪测定Chlortoluron浓度,平行实验同时进行。
2 结果与讨论
2.1 UV/PMS工艺对Chlortoluron的降解效能
已有研究表明UV/PMS工艺对很多污染物的降解过程都符合拟一级动力学模型,因此可通过式(1)、式(2)来描述UV/PMS工艺对Chlortoluron的降解[15]4,[16]。
(1)
ln(C0/Ct)=kobst
(2)
式中:kobs为拟一级速率常数,s-1;t为反应时间,s;C为污染物摩尔浓度,μmol/L;C0为污染物的初始摩尔浓度,8 μmol/L;Ct为污染物的瞬时摩尔浓度,μmol/L。
Chlortoluron的降解可分别归因于UV辐射(速率常数kUV,s-1)、PMS的氧化(速率常数kPMS,s-1)和相关活性自由基的降解(速率常数kradicals,s-1)贡献,如式(3)所示。而由图1可知,300 s内单独PMS对Chlortoluron几乎无氧化降解效果,因此可以忽略体系中kPMS的存在。故kobs可以简化为式(4)所示。
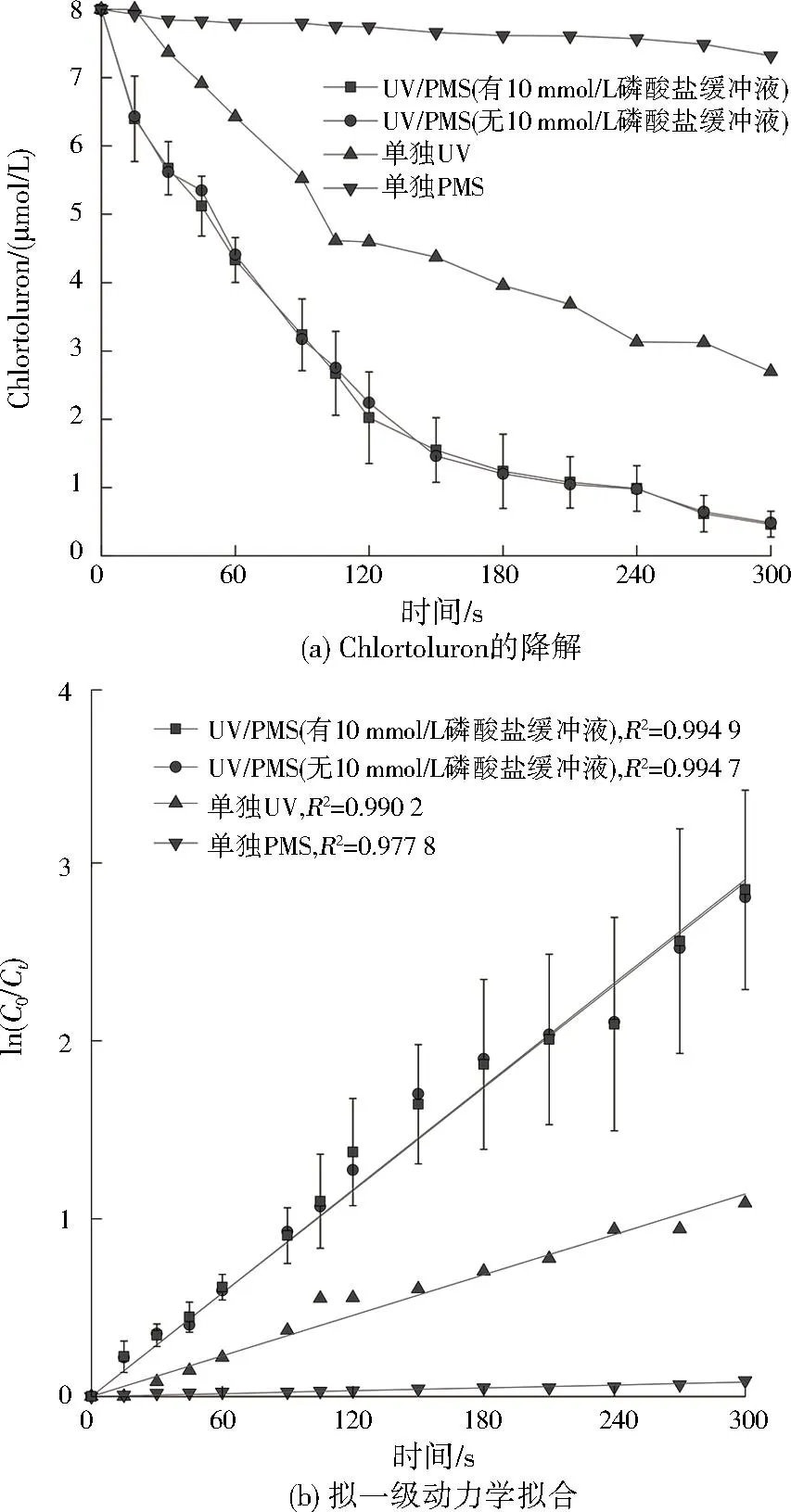
注:实验条件为Chlortoluron初始摩尔浓度8 μmol/L,磷酸盐缓冲液摩尔浓度10 mmol/L,pH=7,PMS初始摩尔浓度160 μmol/L,UV强度2.43 mW/cm2。
kobs=kUV+kPMS+kradicals
(3)
kobs=kUV+kradicals
(4)

(5)
2.2 UV/PMS工艺降解Chlortoluron的影响因素探究
2.2.1 不同工艺参数对Chlortoluron降解的影响
1) 不同PMS投加量的影响


注:实验条件为Chlortoluron初始摩尔浓度8 μmol/L,磷酸盐缓冲液摩尔浓度10 mmol/L,pH=7,UV强度2.43 mW/cm2。
2) 不同UV强度的影响


注:实验条件为Chlortoluron初始摩尔浓度8 μmol/L,磷酸盐缓冲液摩尔浓度10 mmol/L,pH=7,PMS初始摩尔浓度160 μmol/L。
3) 不同pH的影响
溶液pH会直接影响水中污染物降解过程中氧化剂的氧化性和相关次生自由基的形成与转化。控制溶液pH为5~9时实验结果如图4所示。在pH为5~7时,Chlortoluron降解时的kobs几乎保持不变,然而当pH从7增加到9时,kobs从0.008 03 s-1显著增加到0.013 90 s-1,这表明碱性pH环境比酸性pH更有利于Chlortoluron降解。
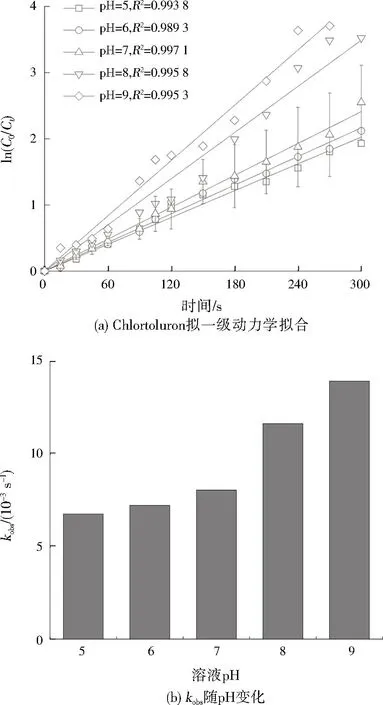
注:实验条件为Chlortoluron初始摩尔浓度8 μmol/L,磷酸盐缓冲液摩尔浓度10 mmol/L,PMS初始摩尔浓度160 μmol/L,UV强度2.43 mW/cm2。
(6)
(7)
2.2.2 水体背景离子对Chlortoluron降解的影响


(8)

注:实验条件为Chlortoluron初始摩尔浓度8 μmol/L,磷酸盐缓冲液摩尔浓度10 mmol/L,pH=7,PMS初始摩尔浓度160 μmol/L,UV强度2.43 mW/cm2。
(9)
(10)
(11)
NH3+HO·→NH2·+H2O
(12)
NH2·+O2→NH2O2·
(13)
NH2O2·→NO·+H2O
(14)
NO·+HO·→HNO2
(15)
(16)
(17)

(18)
(19)
(20)
(21)
(22)
(23)
2.3 UV/PMS工艺降解Chlortoluron的能耗计算
在本研究中,整个UV/PMS工艺的成本效益适用性通过单位电能消耗量(EE/O,kW·h/m3)来估计,这一参数常被用于评估AOP的可行性[30]634。EE/O为在1 m3水中去除90%目标污染物时所消耗的电量[33],其总量由电能费用(EE/OUV,kW·h/m3)和氧化剂成本(EE/Ooxidant,kW·h/m3)组成,可通过式(24)至式(26)计算[30]634。
EE/O=EE/OUV+EE/Ooxidant
(24)
(25)
(26)
式中:V为氧化样品的平均体积,L;P为UV照射的输入功率,kW;T为照射时间,h;O为所用PMS摩尔浓度,0.16×10-3mol/L;Eqoxidant为每使用1 mol PMS转换成的等效电能,kW·h/ mol。
Eqoxidant的计算如式(27)所示:
(27)
式中:Pprice为PMS的平均价格,15 595.71元/t;Mmass为PMS的摩尔质量,307.38 g/mol;Ppurity为PMS的纯度,49.5%;EC为平均电费,0.668元/(kW·h)。
通过式(27)计算得到Eqoxidant=14.497 7 kW·h/mol。在此基础上,计算不同条件下UV/PMS工艺降解Chlortoluron的EE/O及EE/OUV和EE/Ooxidant(见表1、表2)。

表1 不同水质参数下UV/PMS工艺降解Chlortoluron的EE/O计算Table 1 EE/O calculation of Chlortoluron by UV/PMS process under different water quality parameters

表2 不同背景离子下UV/PMS工艺降解Chlortoluron的EE/O计算Table 2 EE/O calculation of Chlortoluron degradation by UV/PMS process under different background ions


3 结 论
1) UV/PMS工艺、单独UV和单独PMS对Chlortoluron降解效果比较,UV/PMS工艺的降解效果最为显著,在300 s内的降解率达到94.21%。


