水痘-带状疱疹病毒高效价中和抗体的制备及应用
2024-01-02邵宏秋魏巍黄晓娜李景新魏国良张芸畅修华谦刘婷婷王宇迪孙博卢井才石亮
邵宏秋,魏巍,黄晓娜,李景新,魏国良,张芸畅,修华谦,刘婷婷,王宇迪,孙博,卢井才,石亮
1.吉林农业大学生命科学学院,吉林 长春 130018;2.长春百克生物科技股份公司,吉林 长春 130013;3.长春生物制品研究所有限责任公司,吉林 长春 130062;4.吉林省药品监督管理局长春检查分局,吉林 长春 130000;5.吉林大学生命科学学院,吉林 长春 130000
水痘-带状疱疹病毒(varicella-herpes zoster virus,VZV)是一种可引起水痘和带状疱疹的病原体,属人类疱疹病毒α 亚科,具有嗜神经性,在人群中可通过呼吸道及密切接触进行传播,能够引发水痘和带状疱疹两种不同临床症状的疾病[1-3]。初次感染VZV可引起水痘,宿主免疫力低下时,病毒可再次激活引起带状疱疹[4-5]。人类对该病毒易感,目前,接种水痘减毒活疫苗和带状疱疹减毒活疫苗是最有效的预防方式[6-11]。各国生产水痘疫苗均采用人二倍体细胞,根据WHO 关于疫苗生产中用于病毒检定等的抗血清的要求,免疫用病毒的毒株和培养用细胞应不同于疫苗生产所用毒株和细胞系[12-16]。
VZV 具有嗜神经性,可潜伏在神经系统,部分人群不能完全清除,当再次激活时可随神经节传导引发带状疱疹等表面皮肤病,常伴随神经疼痛的症状,可持续数月或数年,给患者生活带来极大困扰。在VZV 包膜表面,有gE、gB、gH、gI、gK、gN、gC 和gL 等8种糖蛋白,这些糖蛋白在病毒成熟及包装方面发挥重要作用。其中,gE蛋白因其完整的结构,病毒表面表达最丰富,在病毒传播中发挥重要作用[17-18],同时也是诱导宿主体液免疫和细胞免疫的主要抗原之一。因此,gE 蛋白成为水痘疫苗和带状疱疹疫苗的核心蛋白[19]。
在水痘减毒活疫苗生产过程中,需对毒种进行严格的外源病毒因子检查,确保无外源病毒污染,并且需对毒种及成品进行鉴别试验。在进行外源病毒因子检查及鉴别试验时,需对样品中VZV进行中和,但国内至今尚无VZV 中和抗体标准品[19-20]。目前大多数厂家采用自制抗体,免疫原多为VZV,制备过程中使用动物源性细胞且纯度不高,因此,采用高度纯化的抗原进行动物免疫制备高效价中和抗体,是保证产品安全至关重要的因素[21]。
gE 糖蛋白是VZV 抗原性最强、含量最丰富的外膜蛋白,是目前制备带状疱疹亚单位疫苗重要的候选蛋白。VZV 的gE 糖蛋白具有高度保守性,目前已应用于重组带状疱疹疫苗中[22-25]。本研究以纯化的重组gE 蛋白为免疫原制备高效价中和抗体,并将其应用于水痘减毒活疫苗质量控制中。
1 材料与方法
1.1 疫苗、细胞及毒株 重组带状疱疹疫苗(CHO 细胞),0.5 mL/剂,批号:AM4NS,购自葛兰素史克(GSK)公司;VZV(Oka 株)工作种子批毒种(批号:91001)、Vero细胞、MRC-5细胞、WI-38细胞、水痘减毒活疫苗(参考品,批号:201903026-1)、牛副流感病毒由长春百克生物科技股份公司制备并提供。
1.2 主要试剂 弗氏完全佐剂(10 mL/支,批号:SLCD6299)、弗氏不完全佐剂(10 mL/支,批号:SLCB8702)购自美国Sigma 公司;水痘病毒特异性免疫血清、gE糖蛋白、氢氧化铝佐剂及MF59佐剂由长春百克生物科技股份公司制备,考马斯亮蓝R250染色液、0.94%MEM 溶液、0.25%胰蛋白酶溶液由该公司质量控制部提供;新生牛血清(批号:20171111)购自兰州荣晔生物科技有限责任公司。
1.3 实验动物 SPF级新西兰兔,雄性,11周龄,体质量2.0 ~ 2.5 kg,购自青岛康大生物科技有限公司,动物许可证号:SCXK(鲁)20210003,实验动物福利伦理审查号:BCHT-AEEI-2022-001。本实验均以科研为目的进行新西兰兔的养殖和使用,并按照实验动物福利伦理审查指南的相关规定进行(GB/T 35892-2018)。
1.4 VZV特异性免疫血清的制备
1.4.1 动物分组及免疫 为探讨gE 蛋白制备高效价中和抗体的可行性,采用多种免疫组合方式进行分组。免疫1 组:重组带状疱疹疫苗(CHO 细胞)。免疫2 组:gE 糖蛋白+弗氏佐剂。将gE 糖蛋白用PBS稀释至2 mg/mL,与弗氏佐剂按1∶1 混合乳化,备用;初次免疫使用弗氏完全佐剂,第2 次及以后免疫使用弗氏不完全佐剂,免疫剂量为1.0 mL/只。免疫3 组:gE 糖蛋白+氢氧化铝佐剂。将gE 糖蛋白稀释至2 mg/mL,与氢氧化铝佐剂(2.5 mg/mL)按1∶1混合,2~8 ℃振荡混匀,每10 min混匀1次,时长1 h,备用;免疫剂量为1.0 mL/只。免疫4组:gE糖蛋白+ MF59 佐剂。将gE 糖蛋白稀释至2 mg/mL,与MF59佐剂按1∶1混合,备用;免疫剂量为1.0 mL/只。免疫1 和4 组兔经后腿肌内免疫,每只注射1 点,共2点/次;免疫2和3组经背部皮下免疫,0.1~0.3mL/点,每只至少注射5 个点(应在30 min 内完成)。每组免疫2只兔。除免疫1组进行2次免疫外,其余3组均进行4 次免疫,免疫间隔14 d。试验设免疫5 组(VZV对照组):皮下免疫VZV,1.0 mL/只。
1.4.2 采血 免疫前每只兔经耳静脉采血1.0 mL,离心分离血清作为免疫前对照血清。免疫1 组于免疫后14 d,每只采血1.0 mL,离心分离血清;免疫后第28 天每只均最大量采血(心脏或颈动脉),室温静止1 h 后,离心分离血清。免疫2、3、4 组于免疫后第14、28、42 天每只采血1.0 mL,室温静止1 h 后,离心分离血清;免疫后第56 天每只最大量采血(心脏或颈动脉),室温静止1 h 后,离心分离血清。免疫5 组免疫后第56 天每只最大量采血(心脏或颈动脉),室温静止1 h后,离心分离血清。
1.5 血清中和抗体效价检测 将免疫1~5组免疫后(分别第28、56、56、56、56天)血清进行2倍系列稀释(1∶16~1∶1 024),与水痘病毒等量混合,(37±1)℃培养进行中和反应;中和结束后接种至长满单层MRC-5 株人二倍体细胞的6 孔板中,100 μL/孔,(37 ± 1)℃孵育7 d;PBS 缓冲液洗涤,每次3 mL,共1~3次,加入考马斯亮蓝R250染色液,1 mL/孔,室温5 ~ 10 min;吸弃染色液,流水冲净,晾干,计数蚀斑数(PFU)。
1.6 血清中和病毒能力检测 将VZV 减毒活疫苗原液稀释至40 000、80 000、160 000、240 000 PFU/mL,分别与免疫血清等量混合孵育,进行中和反应;中和结束后接种至长满单层MRC-5 株人二倍体细胞的6 孔板中,100 μL/孔,同时设病毒对照组(病毒稀释至800 ~ 1 000 PFU/mL,取0.1 mL 加入稀释液0.1 mL)、细胞对照组(稀释液0.2 mL)和血清对照组(免疫血清0.1 mL + 稀释液0.1 mL),(37 ± 1)℃孵育7 d;PBS 缓冲液洗涤,每次3 mL,共1~3 次,加入考马斯亮蓝R250染色液,1 mL/孔,室温5~10 min;吸弃染色液,流水冲净,晾干,计数蚀斑数(PFU)。试验重复2次。
1.7 外源病毒因子检查 将VZV 特异性免疫血清56 ℃灭活30 min,与稀释液1∶1 混匀。将VZV(Oka株)工作种子批毒种稀释至88 889 PFU/mL 作为供试品,与稀释后VZV 特异性免疫血清按1∶1 进行中和,置(37 ± 1)℃水浴60 min;取中和后供试品接种Vero、MRC-5和WI-38细胞,同时设阴性对照(不加病毒)及阳性对照(接种牛副流感病毒),(36±1)℃吸附1 h;换液继续培养14 d,观察细胞病变。
1.8 鉴别试验 将VZV(Oka 株)工作种子批毒种稀释至1 000 PFU/mL。稀释后病毒液与稀释液1∶1混合作为病毒对照组,稀释后病毒液与免疫血清1∶1 混合作为实验组,免疫血清与稀释液1∶1 混合作为血清对照组,单独稀释液作为细胞对照组。各组接种2 孔MRC-5 株人二倍体细胞,0.1 mL/孔,置(37 ± 1)℃,5% CO2培养箱吸附60 min,每隔20 min轻轻摇板1 次;补加维持液后继续培养7 d;弃培养液,PBS缓冲液洗涤,加入考马斯亮蓝溶液,室温5 min;流水冲洗,晾干。计数每孔10 ~ 50 个以内的蚀斑数,得出该稀释度平均蚀斑数,并按下式计算病毒滴度。试验重复2次。

1.9 数据采集及分析 使用Graphpad 8.0.2软件进行数据采集及分析。
2 结果
2.1 血清中和抗体效价免疫2组血清中和抗体效价最高,为1∶512,显著高于对照组。见图1。
2.2 血清中和病毒能力 细胞对照组无蚀斑,病毒对照组有蚀斑(43 PFU/孔),证明试验成立。免疫2 组血清对病毒中和能力最强,可达240 000 PFU/mL,且高于免疫5组。见图2。

图2 各组中和抗体中和病毒能力Fig.2 Virus neutralizing ability of neutralizing antibody in various groups
2.3 外源病毒因子 3 种细胞的培养物均未见细胞病变,且阴性和阳性对照也均未见细胞病变,试验成立,表明稀释后的特异性免疫血清可完全中和稀释后VZV。
2.4 鉴别试验 制备的VZV 特异性免疫血清可完全中和稀释后VZV,血清及细胞对照均为阴性。见表1。
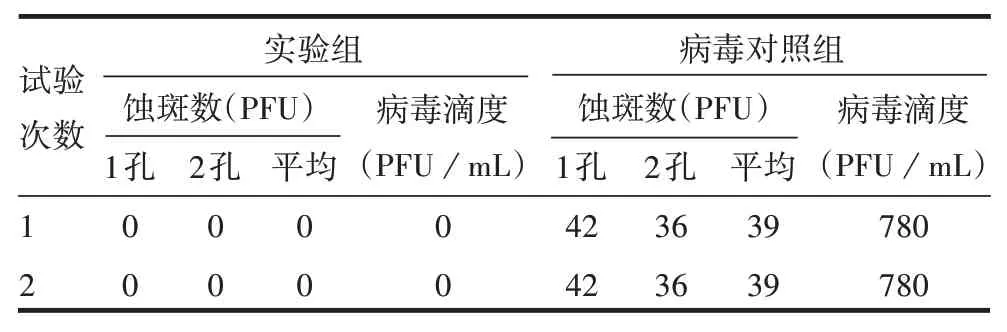
表1 鉴别试验结果Tab.1 Identification test results
3 讨论
本研究结果表明,采用重组gE糖蛋白与不同佐剂组合免疫家兔后制备的免疫血清均具有中和活性,其中重组gE糖蛋白与弗氏佐剂组合制备的血清中和效价最高,为1∶512,中和病毒能力可达240 000 PFU/mL。因此,重组gE 糖蛋白与弗氏佐剂的组合方式为最优组合方式。
目前在水痘减毒活疫苗及带状疱疹减毒活疫苗质量控制中,进行鉴别试验以及外源病毒因子检查时均需要中和样品中VZV,但目前国内尚无VZV 中和抗体标准品。国内各厂家进行鉴别试验或外源病毒因子检查时,通常采用自制免疫血清,免疫原为VZV。由于免疫原为病毒,而病毒需通过细胞制备,有外源病毒因子污染的可能,且纯度也不高,在外源病毒因子检查中可能出现假阴性,而采用高纯度蛋白进行免疫可避免以上问题。
综上所述,本研究采用高纯度gE 糖蛋白制备了高中和性免疫血清,该血清适用于水痘减毒活疫苗和带状疱疹减毒活疫苗日常生产中的质量控制,为质量控制提供了保障。
