硼烷化合物的合成:从小硼烷分子到多面体硼烷
2023-12-29王盈盈郗碧莹陈学年
荆 怡,王盈盈,王 凯,郗碧莹,陈学年
郑州大学 化学学院 绿色催化中心,河南 郑州 450001
硼和氢形成的一系列中性和阴阳离子化合物,通称为硼烷。由于B原子的缺电子特性,以及其2s和2p轨道之间的能级差较小易发生杂化,使得硼化合物具有多样的成键形式和丰富的化学反应性[1-2]。第一个硼烷化合物的合成可以追溯到1912年[3],并且此后的25年中,硼烷化学的先驱德国化学家Stock教授系统地合成并表征了一系列不稳定的硼烷化合物[4]。这类不稳定硼烷化合物的合成得益于真空线技术的出现,它起源于Stock的实验室,用于处理对水和空气敏感的硼烷化合物,并延续使用至今[4]。Stock[4]开创性地合成和分离了一系列中性硼烷化合物,包括乙硼烷(6)(B2H6)、丁硼烷(10)(B4H10)、戊硼烷(9)(B5H9)、戊硼烷(11)(B5H11)、己硼烷(10)(B6H10)和癸硼烷(14)(B10H14)。随后Lipscomb[5]对此类硼氢化合物的结构进行了系统总结。由于硼烷及其衍生物具有比碳氢化合物更高的燃烧热,20世纪50年代美国和苏联等国家试图利用硼烷(液体B5H9和固体B10H14)作为潜在的高能火箭燃料,并对其进行了系统的研究[6-7]。通过多年对硼化合物的研究,硼化学家逐渐对多面体硼烷化合物的合成和性质有了系统的认识。多面体硼烷由多个B原子组成,这类富硼化合物的骨架结构与碳氢化合物采用的链状或环状形式不同,常见的结构可分为三类,分别为闭式(closo)、巢式(nido)和蛛网式(arachno)(图1)[8]。这类化合物是适用于硼中子俘获疗法(boron neutron capture therapy, BNCT)技术的潜在硼药重要前体化合物[9]。
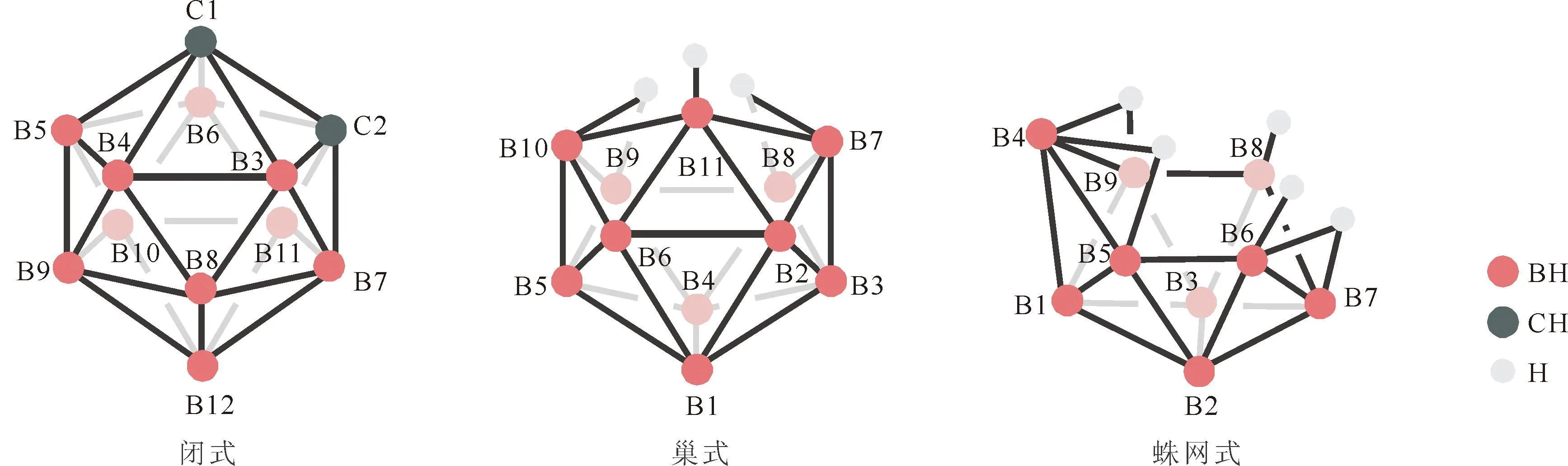
图1 多面体硼烷化合物常见的三种结构类型[8]Fig.1 Three types of common polyhedral borane structures[8]
近年来,BNCT的研究和应用在我国取得重要进展,基于加速器的BNCT中子源已经建成[10],因此,适用于BNCT的硼药研究和开发已成为研究热点。硼中子俘获疗法作为一种新型放射性二元治疗方案,利用10B载体选择性富集在肿瘤细胞中,随后通过超热中子束照射肿瘤部位进行治疗[11-14]。BNCT硼药的开发最早始于20世纪50年代,临床试验中使用的首批硼化合物包括硼酸(B(OH)3)、硼氢化钠(NaBH4)及其衍生物,虽然这类化合物具有易得和较低的细胞毒性特点,但由于缺乏选择性和热中子穿透能力有限限制了其治疗效果[15-17]。第二代硼药主要为两种,一种为芳基硼酸化合物的(L)-4-二羟基硼基苯丙氨酸(BPA),另一种为多面体硼烷阴离子的巯基十二硼烷二钠盐(Na2B12H12,BSH)。但是由于这两类化合物固有的性质,包括BPA的B含量低、水溶性差以及BSH没有肿瘤靶向性和负电荷阻碍细胞膜等缺点,推进了第三代硼药的开发。第三代硼药包括一些硼化核苷和硼化碳水化合物等[18-21]。多面体硼烷和高含硼量的碳硼烷化合物,可以作为BNCT硼药载体,对其进行修饰,从而改善或提高其在肿瘤细胞中的富集浓度、肿瘤细胞靶向性和停留时间[21-22]。本文以含一个B原子到十二个B原子的次序,简要综述硼烷化合物的合成方法、结构和11B NMR谱图表征,旨在为硼氢化合物及其衍生物的广泛应用特别是在开发应用于BNCT技术的新一代硼药前体的开发提供基础知识。
1 硼氢化合物和硼烷Lewis碱加合物(MBH4和L·BH3)的合成
1.1 NaBH4的合成
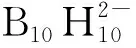
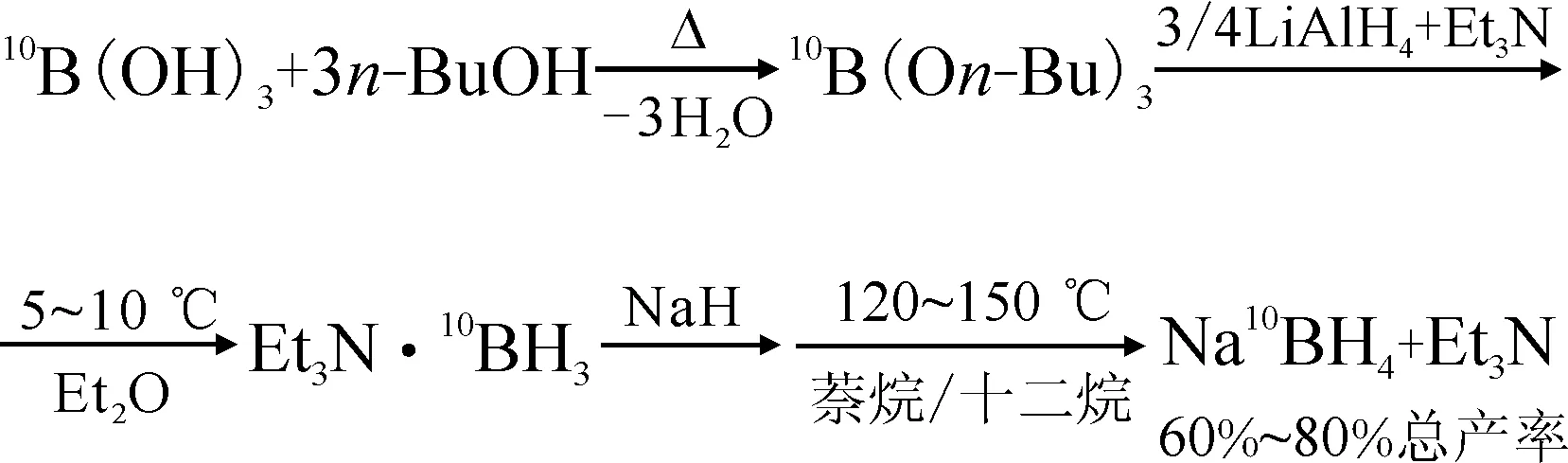
图2 合成Na10BH4[28]Fig.2 Synthesis of Na10BH4[28]
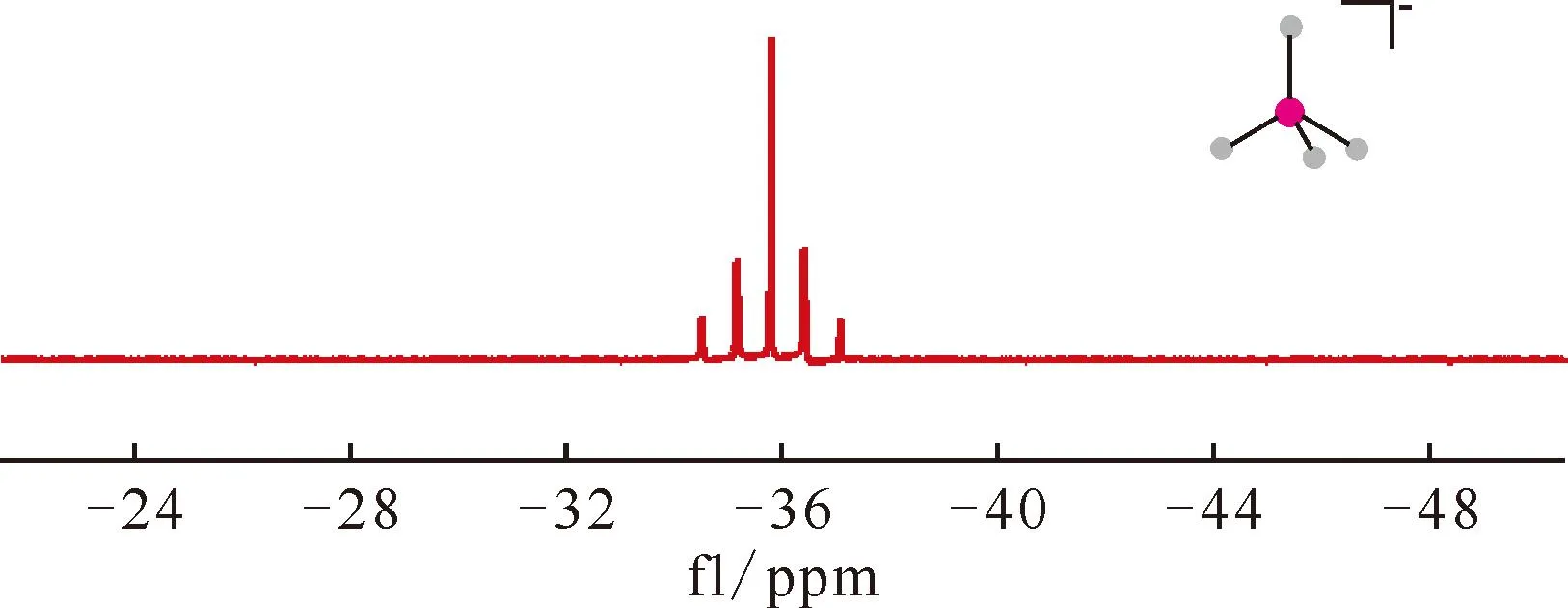
fl:化学位移(下同)图3 Na10BH4在二甲基亚砜(DMSO)-d6中的10B NMR谱图[28]Fig.3 10B NMR spectrum of Na10BH4 in DMSO-d6[28]
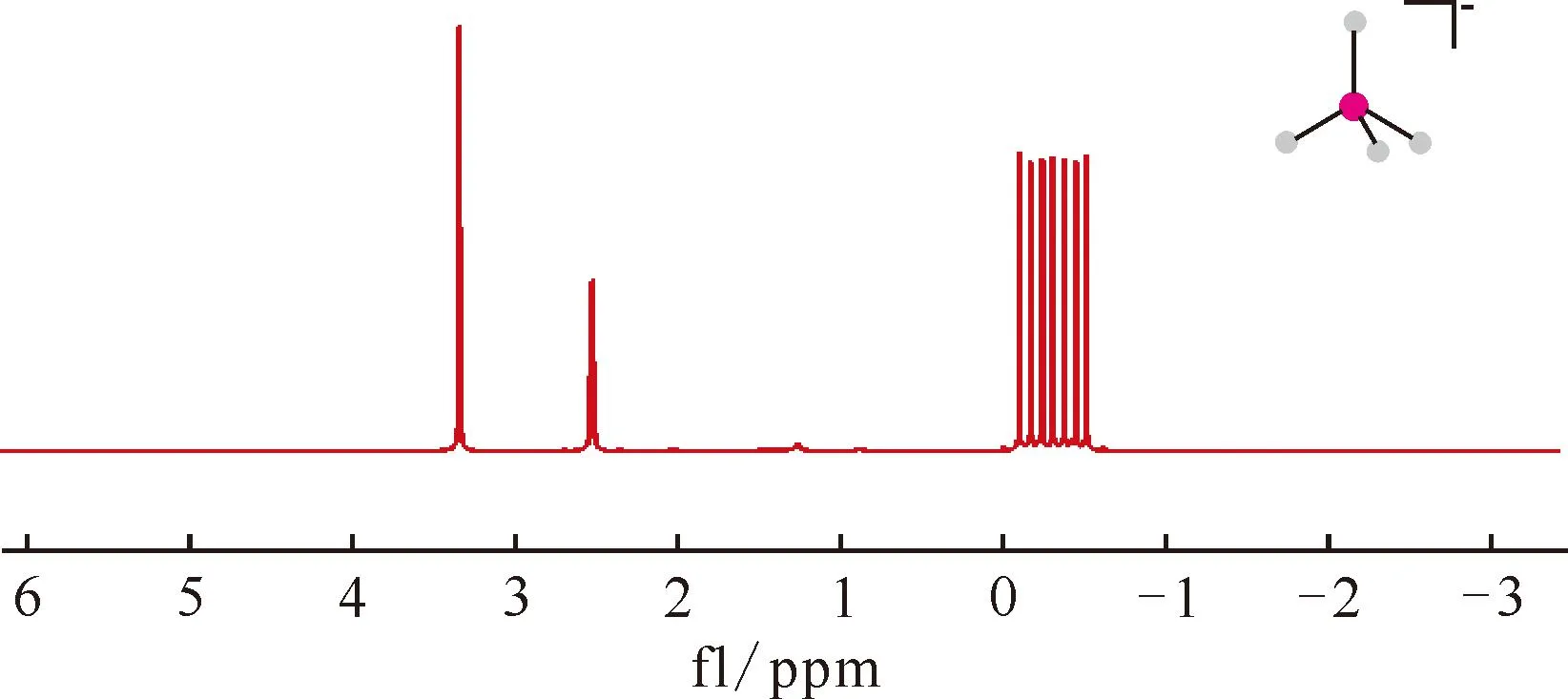
图4 Na10BH4在DMSO-d6中的1H NMR谱图[28]Fig.4 1H NMR spectrum of Na10BH4 in DMSO-d6[28]
1.2 硼烷Lewis碱加合物(L·BH3)的合成
BH3是基本的硼烷单元,由于三配位的B原子有一个空的2p轨道,所以不能以单体的形式存在,在非配位溶剂中以二聚体B2H6的形式存在。BH3也可以作为Lewis酸接受电子,从而与Lewis碱配位形成加合物(图5),其配位键的强弱与配位原子的给电子能力有关。BH3可与N-杂环卡宾(NHC)、膦和胺等具有强给电子能力的Lewis碱形成稳定硼烷加合物,也可以和四氢呋喃(THF)和二甲基硫醚(DMS)等具有弱给电子能力的Lewis碱形成不稳定硼烷加合物[29-32]。硼烷Lewis碱加合物的稳定性顺序为:NHC·BH3>硼烷膦配合物(phosphine·BH3)>硼烷胺配合物(amine·BH3)>DMS·BH3>THF·BH3[32]。硼烷加合物的实验室合成一般利用较强的Lewis碱与THF·BH3或DMS·BH3反应,取代弱配位的Lewis碱从而形成稳定的硼烷加合物,反应如式(1)[29,33]。而工业上一般使用NaBH4与铵盐或鏻盐反应制备,反应如式(2)[34-35]。IMe·BH3(IMe=1,3-二甲基咪唑-2-亚烯)、NH3·BH3、DMS·BH3和THF·BH3的11B NMR谱图见图6[29,36]。

图5 硼烷加合物的形成过程[32]Fig.5 Formation of borane adducts[32]
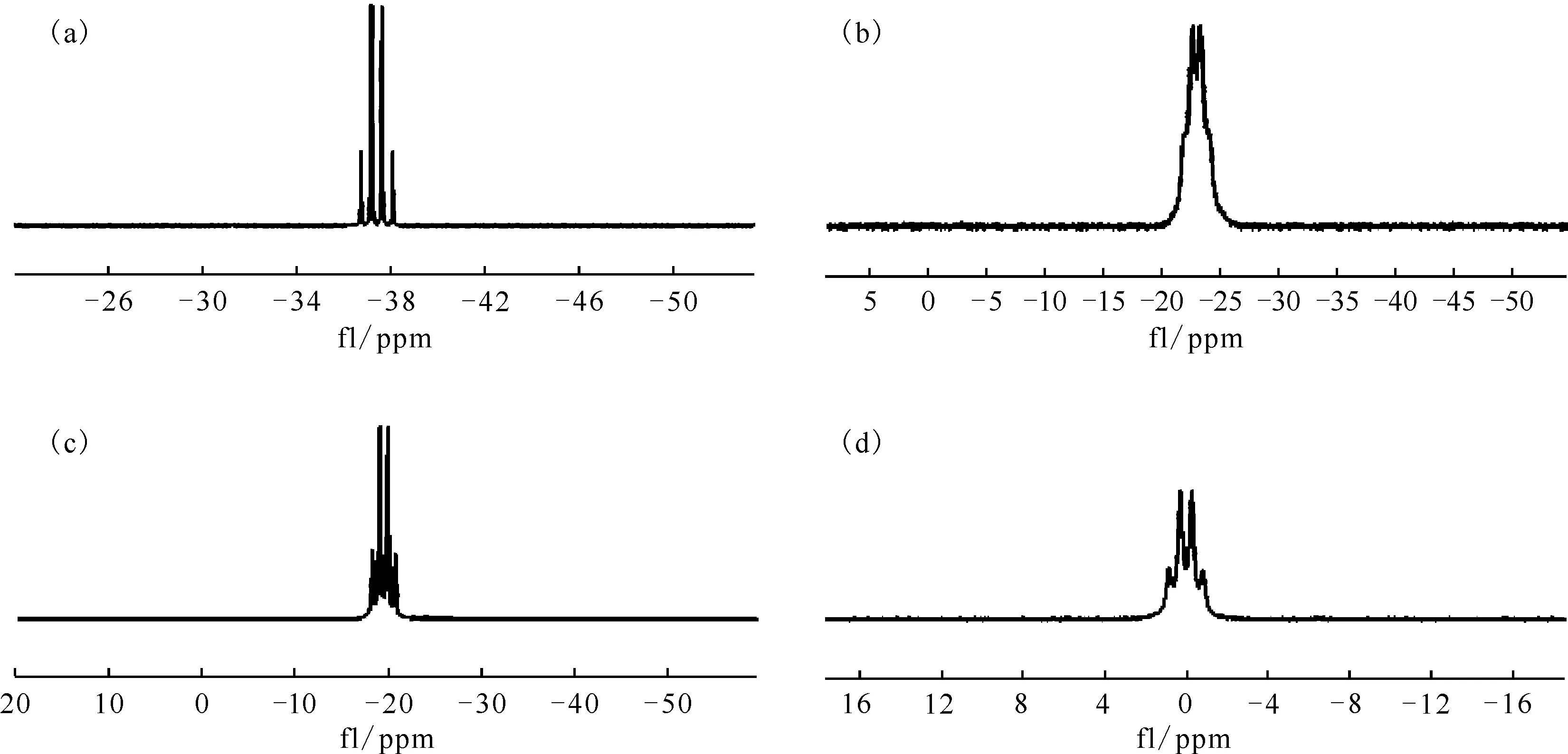
溶剂:(a)——CDCl3,(b)——DMSO,(c)——DMS,(d)——THF图6 IMe·BH3(a)、NH3·BH3(b)、DMS·BH3(c)和THF·BH3(d)的11B NMR谱图[29,36]Fig.6 11B NMR spectra of IMe·BH3(a), NH3·BH3(b), DMS·BH3(c) and THF·BH3(d)[29,36]
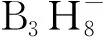

(1)

(2)
另一类重要的硼烷化合物是频哪醇硼烷(HBpin)和儿茶酚硼烷(HBcat)[41-42]。在这类硼烷化合物中没有BH3结构单元,B原子只与一个H原子键合。不同于一般的硼烷Lewis碱加合物,这些化合物中的B原子是三配位,分别和一个H原子和两个O原子键合(图7)。O原子和B原子之间的p-p反馈π键稳定了三配位B原子的结构。由于这类稳定的硼烷加合物具有易得、操作简单以及对空气和水不敏感等特点,近年来在有机硼化合物的合成研究中被广泛应用[32,43]。更重要的是其双联频哪醇硼酸酯(B2pin2)和双联邻苯二酚硼酸酯(B2cat2)衍生物常被广泛用于Suzuki偶联反应合成有机硼化合物[43]。最近刘超课题组报道了由市场可得的10B同位素的10BF3与Lewis碱加合物直接合成10B同位素的双联频哪醇硼酸酯(10B2pin2)的方法,为合成富硼的BNCT的硼药提供了新的路径[44]。
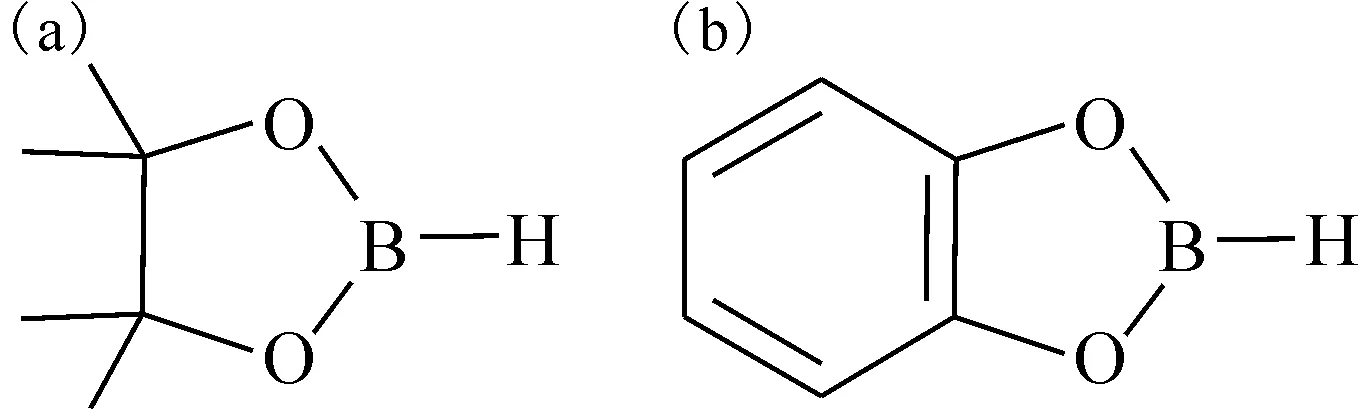
图7 频哪醇硼烷(a)和儿茶酚硼烷(b)分子结构[41-42]Fig.7 Molecular structures of HBpin(a) and HBcat(b)[41-42]
2 乙硼烷(6)(B2H6)的合成
B2H6在常温下为无色气体,对水和空气极其敏感,有剧毒。B2H6最早在1912年被Stock等[3]合成和表征,利用金属Mg与硼酸反应的产物水解后得到B4H10,随后B4H10分解成B2H6及其他硼烷化合物,反应如式(3—5)。1931年,Schlesinger和Burg[45]通过BCl3和H2在高压放电条件下合成B2H6,收率为50%,反应如式(6—7)。随后化学家开发了多种以NaBH4作为原料的合成方法[46-47],其中Freeguard和Long[48]报道利用NaBH4与I2在二乙二醇二甲醚(diglyme)中反应,可以生成98%纯度的B2H6,反应如式(8)。另一种常用的合成方法依赖于NaBH4与Et2O·BF3反应制备B2H6,此方法为简单的实验室制备方法[49],反应如式(9)。B2H6的11B NMR谱图见图8[50]。

图8 B2H6在C6H6中的11B NMR谱图[50]Fig.8 11B NMR spectrum of B2H6 in C6H6[50]

(3)

(4)

(5)

(6)

(7)

(8)

(9)
3 MB3H8与L·B3H7的合成以及相互转化
3.1 八氢丙硼酸盐的合成
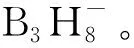

(10)

(11)

(12)

(13)

(14)
3.1.2碱金属硼氢化合物MBH4与硼烷反应 为避免使用对空气非常敏感的碱金属单质,可以利用碱金属硼氢化合物和硼烷反应合成MB3H8。1963年Gaines等[61]利用B2H6和NaBH4在diglyme作溶剂、100 ℃条件下合成NaB3H8,产率为63%,反应如式(15)。随后,Dewkett等[62]对NaBH4和Et2O·BF3反应条件进行优化,将反应体系升至100 ℃使得反应过程中生成的B2H6和NaBH4·BH3(NaB2H7)进一步转化为NaB3H8,反应如式(16)。此方法避免直接使用B2H6气体,产率为65%。2018年,本课题组利用MBH4与THF·BH3反应,在较温和条件下合成MB3H8(M=Li和Na),反应如式(17)[37]。由于KBH4在THF中的溶解度差,并且THF·BH3浓度低,因此KB3H8不能通过此方法合成。当DMS·BH3代替THF·BH3参与反应,1,4-二氧六环代替THF做溶剂时,该方法适用于所有碱金属盐MB3H8(M=Li、Na、K、Rb和Cs)的合成,反应如式(18)[38]。

(15)

(16)

(17)

(18)
3.1.3其他合成方法 除以上总结的两类合成碱金属盐MB3H8方法外,还有其他制备方法,如利用中性硼烷B4H10或B10H14的不对称裂解[63-64]、MBH4的热解脱氢聚合反应[65]、利用丙硼烷(7)与NaBH4或MNH2BH3反应(M=Li和Na)[66-67],以及利用NaBH4与I2、有机或无机卤化物反应等[57,68-69]。此外,本课题组[70]利用甲基硫二硼烷化合物K[BH3(CH3)SBH3]与DMS·BH3反应,也可以生成产率为86%的KB3H8,反应如式(19)。KB3H8的11B NMR谱图见图9[60]。
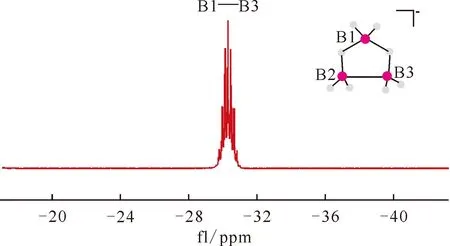
图9 KB3H8在DMSO中的11B NMR谱图[60]Fig.9 11B NMR spectrum of KB3H8 in DMSO[60]

(19)
3.2 丙硼烷(7)(L·B3H7)的合成
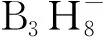
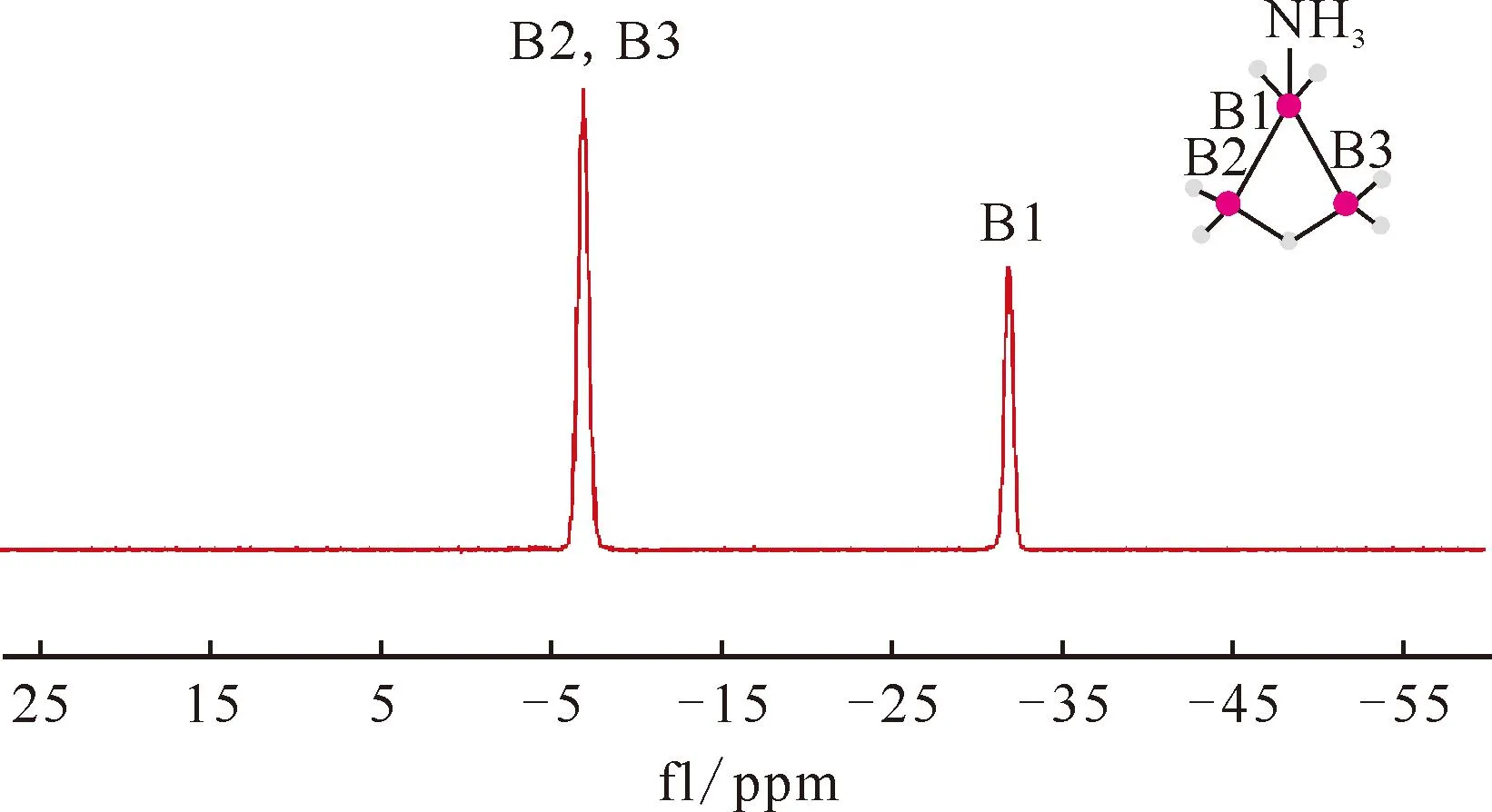
图10 NH3·B3H7在CH2Cl2中的11B NMR谱图[60]Fig.10 11B NMR spectrum of NH3·B3H7 in CH2Cl2[60]

(20)

(21)

(22)
(23)

(24)

(25)
4 四顶点多面体硼烷的合成
4.1 丁硼烷(10)(arachno-B4H10)的合成
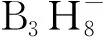
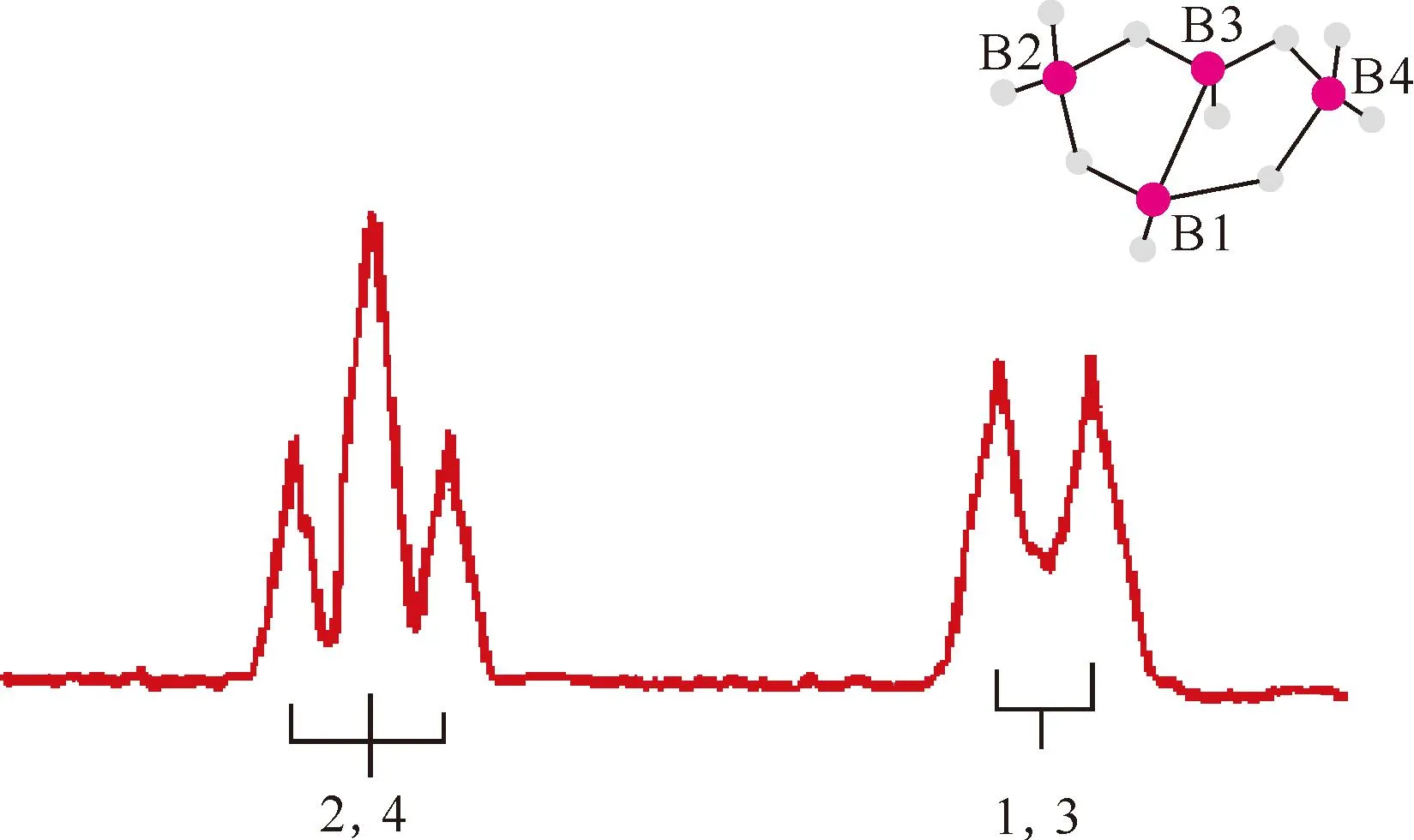
图11 B4H10的11B NMR谱图(32.1 MHz)[76]Fig.11 11B NMR spectrum(32.1 MHz) of B4H10[76]

(26)

(27)
(28)
(29)
(30)
4.2 九氢丁硼酸盐的合成
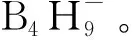
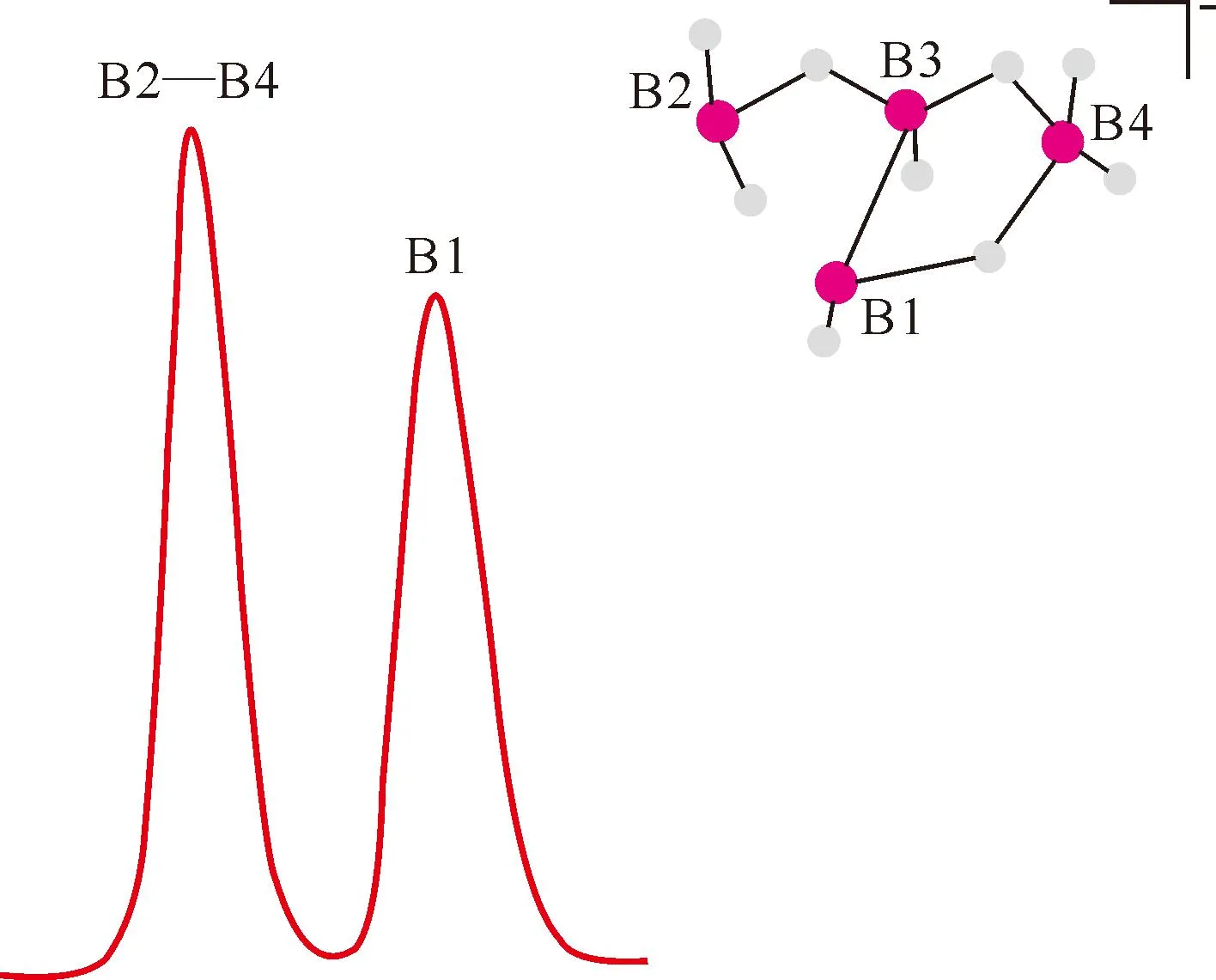
图12 40 ℃下[Ph3PCD3]B4H9在CD2Cl2中的11B NMR谱图[81]Fig.12 11B NMR spectrum of [Ph3PCD3]B4H9 in CD2Cl2 at 40 ℃[81]

(31)

(32)
5 五顶点多面体硼烷的合成
5.1 戊硼烷(9)(nido-B5H9)的合成
在中性低聚硼烷中B5H9的稳定性最好。1923年Stock等[83]首次报道B5H9,其商业制备可以利用B2H6热解[84],反应如式(33)。由于相对其他小硼烷分子其稳定性较好,所以可以延长热处理时间进行提纯。实验室可以利用n-Bu4NB3H7Br在100 ℃条件下热解的方法制备,反应如式(34)[85]。此外,还可以通过B4H10在醚类溶剂中裂解生成的B3H7,进而催化B4H10生成B5H9,反应如式(35)[86]。B5H9的11B NMR谱图见图13[76]。

图13 B5H9的11B NMR谱图 (32.1 MHz)[76]Fig.13 11B NMR spectrum(32.1 MHz) of B5H9[76]

(33)

(34)

(35)
5.2 八氢戊硼酸盐的合成
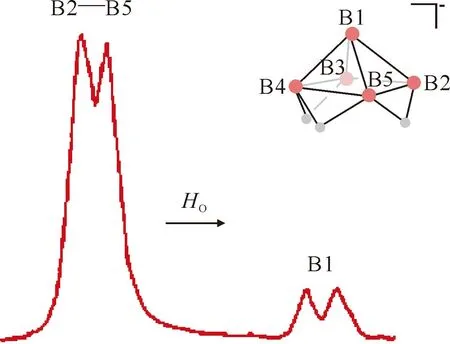
图14 LiB5H8在35 ℃下的11B NMR谱图[88]Fig.14 11B NMR spectrum of LiB5H8 at 35 ℃[88]

(36)
6 六顶点多面体硼烷的合成
6.1 己硼烷(10)(nido-B6H10)的合成
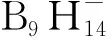
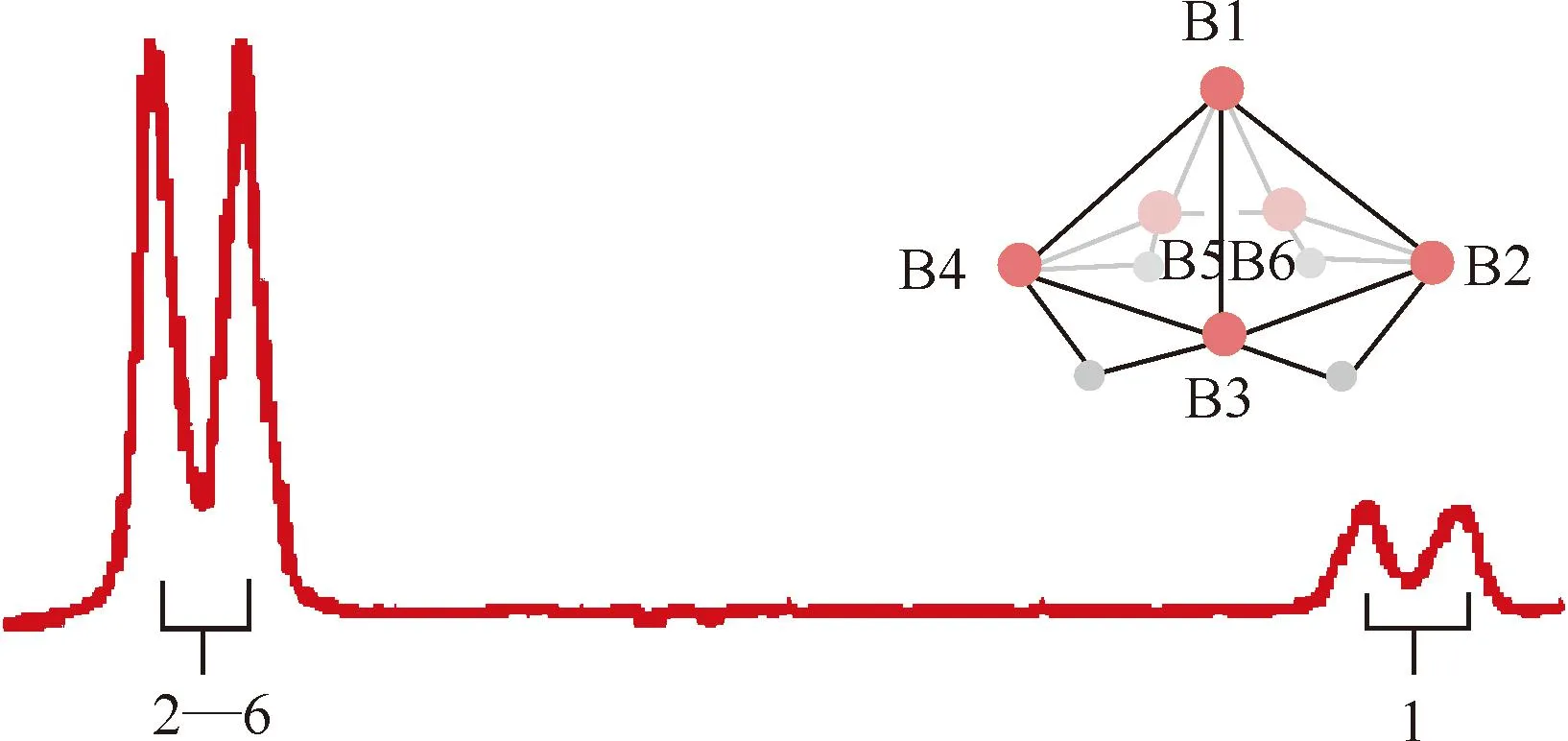
图15 B6H10的11B NMR谱图(32.1 MHz)[76]Fig.15 11B NMR spectrum(32.1 MHz) of B6H10[76]

(37)

(38)
6.2 六氢己硼酸盐的合成
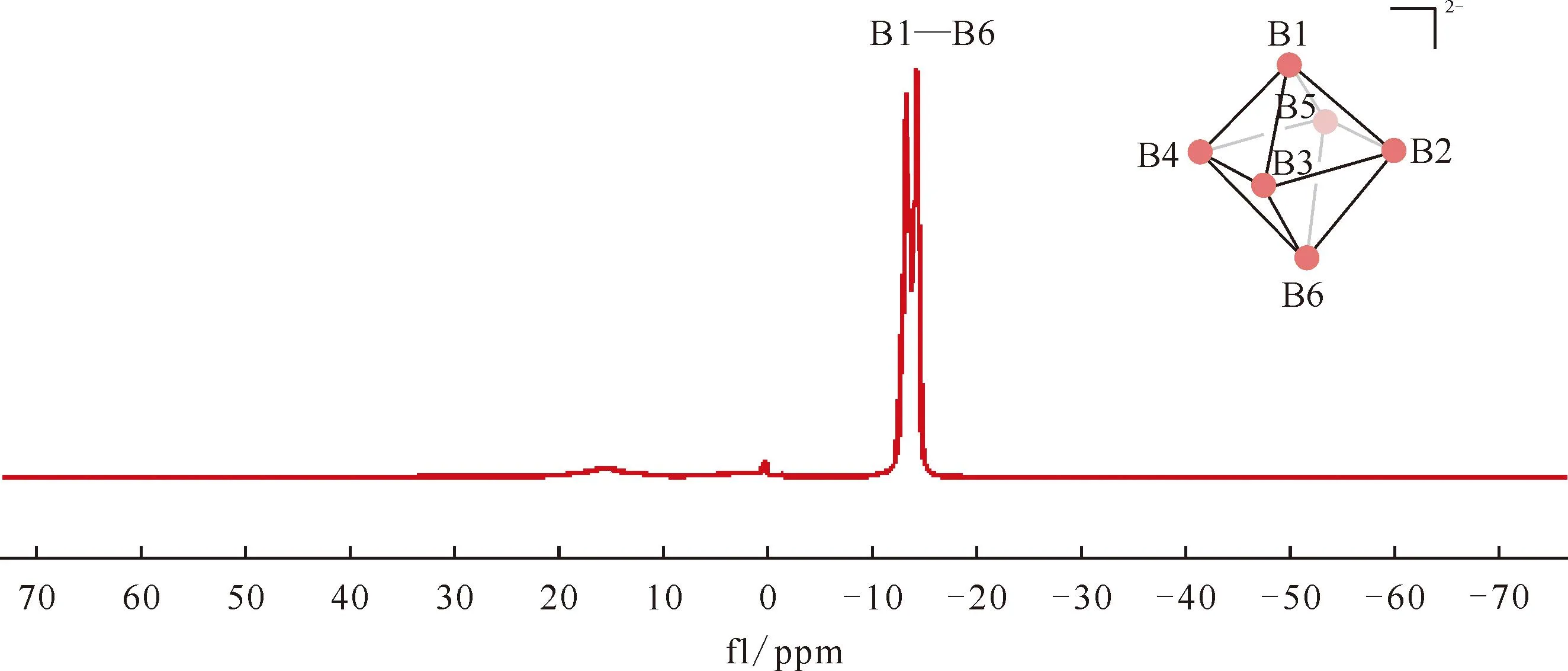
图16 Na2B6H6在D2O的11B NMR谱图[96]Fig.16 11B NMR spectrum of Na2B6H6 in D2O[96]

(39)

(40)
7 七顶点和八顶点多面体硼烷的合成
7.1 庚硼烷(11)(nido-B7H11)的合成
由于中性庚硼烷化合物极其不稳定,其合成和分离非常困难,目前还没有能够分离和表征的中性庚硼烷化合物单体[97-99]。但庚硼烷(11)(B7H11)可以通过KB7H12与HCl在乙醚中反应得到,但产物为乙醚的加合物Et2O·B7H11,反应如式(41)[99]。

(41)
7.2 辛硼烷(12)(nido-B8H12)的合成
1964年,Lipscomb课题组[100]首次报道辛硼烷(12)(B8H12),利用B2H6和B5H9在放电的条件下制备分离。1965年,Williams课题组[101]发现在B9H15的分解过程中会出现少量的B8H12,反应如式(42)。随后1968年,Schaeffer课题组[102]通过对B9H15分解的研究发现,在无溶剂条件下B9H15的快速分解可以方便地制备少量B8H12,而要进行大量制备时,需要戊烷作溶剂使B9H15进行快速分解,反应更容易控制并且产率较高。B8H12的11B NMR谱图见图17[76]。
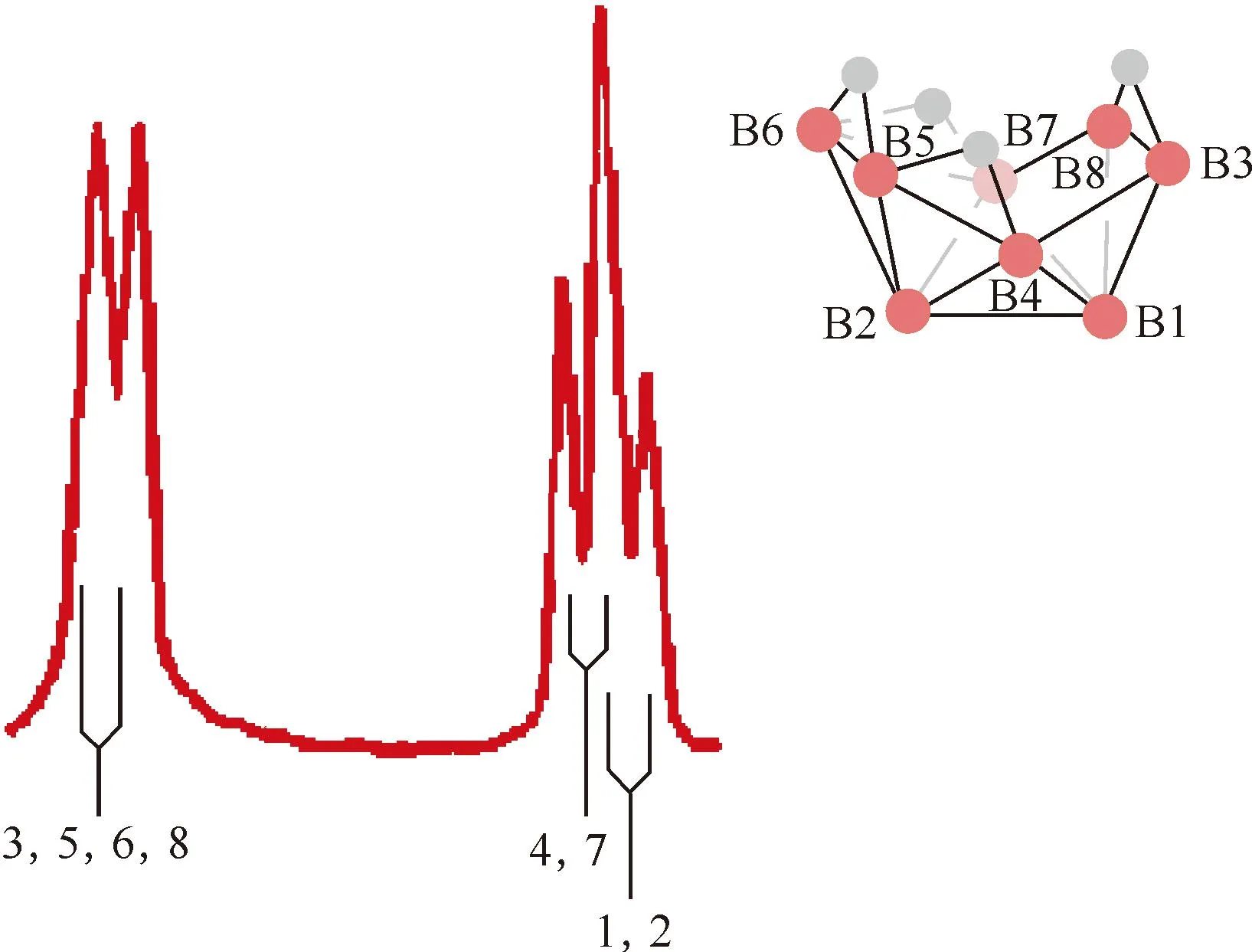
图17 B8H12的11B NMR谱图(70.6 MHz)[76]Fig.17 11B NMR spectrum(70.6 MHz) of B8H12[76]

(42)
7.3 七氢庚硼酸盐和八氢辛硼酸盐的合成


图18 [Ph4P]2B7H7在CD2Cl2中的11B NMR谱图[104]Fig.18 11B NMR spectrum of [Ph4P]2B7H7 in CD2Cl2[104]
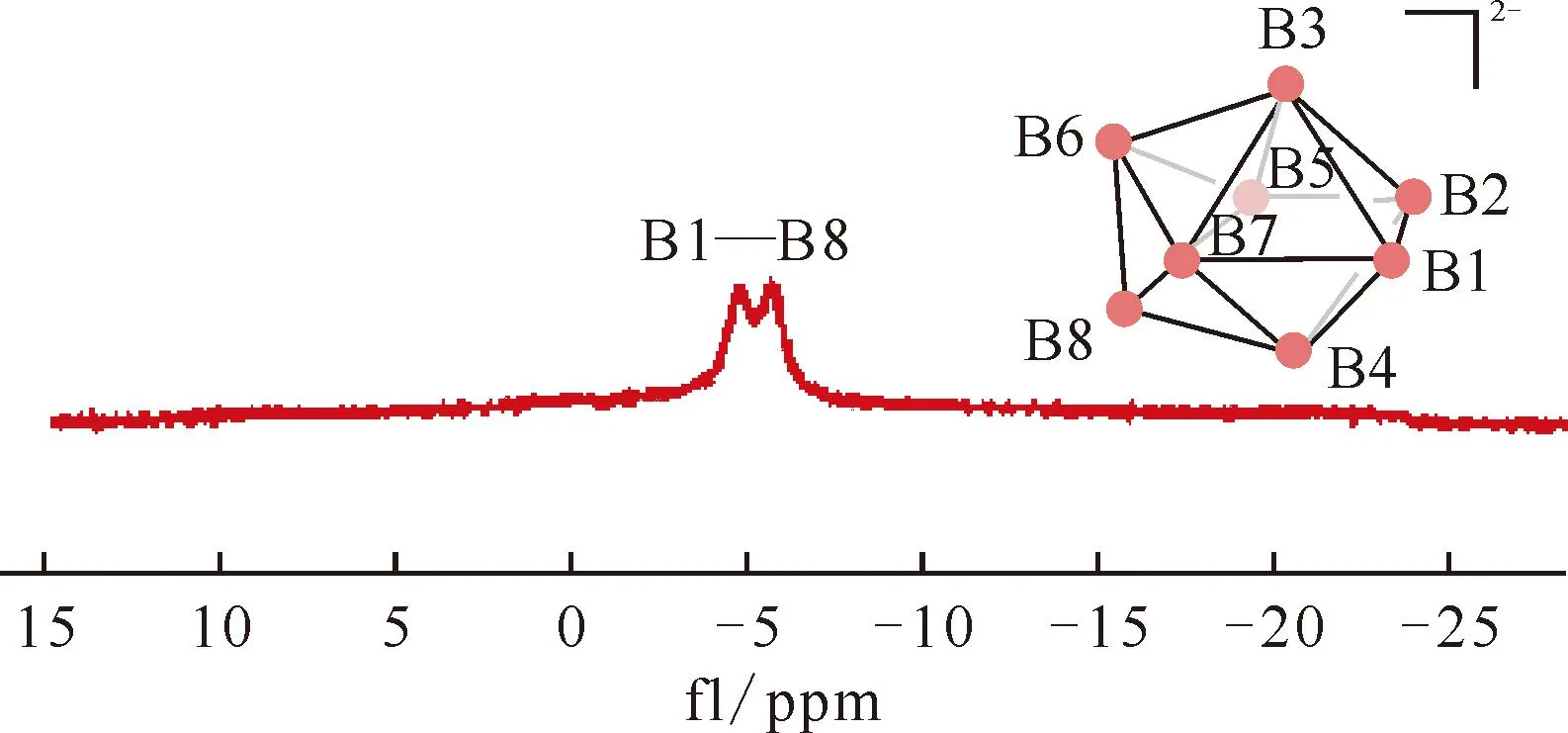
图19 [n-Bu4N]2B8H8在CD2Cl2中的11B NMR谱图[105]Fig.19 11B NMR spectrum of [n-Bu4N]2B8H8 in CD2Cl2[105]
7.4 八氢庚硼酸盐和九氢辛硼酸盐的合成
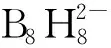
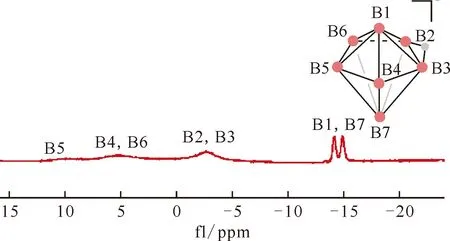
图20 [Ph4P]B7H8在CD2Cl2中的11B NMR谱图[104]Fig.20 11B NMR spectrum of [Ph4P]B7H8 in CD2Cl2[104]
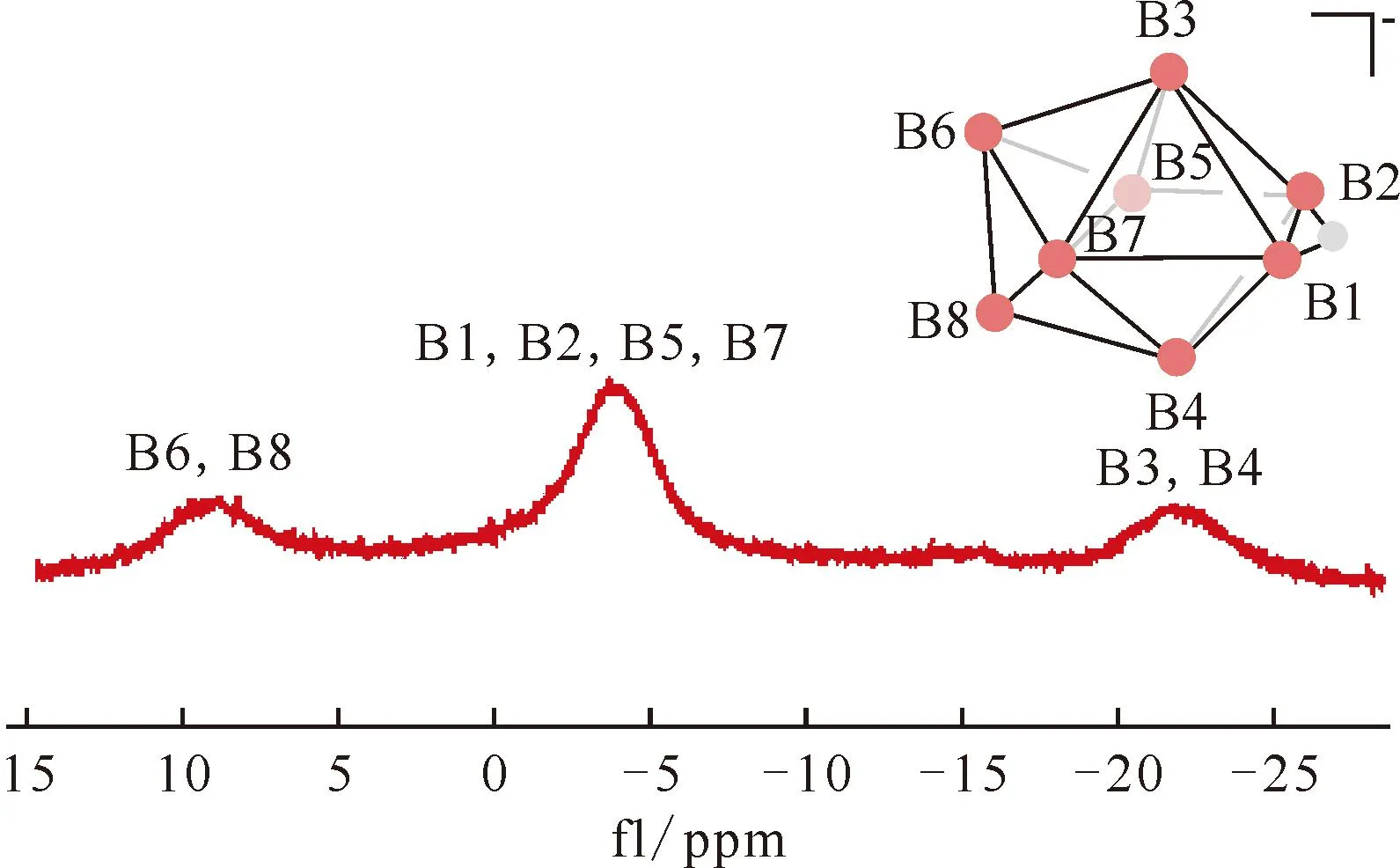
图21 [n-Bu4N]B8H9在CD2Cl2中的11B NMR谱图[105]Fig.21 11B NMR spectrum of [n-Bu4N]B8H9 in CD2Cl2[105]

(43)

(44)
8 九顶点多面体硼烷的合成
8.1 壬硼烷(15)(arachno-B9H15)的合成
1958年壬硼烷(15)(arachno-B9H15)被报道,但其为硼烷相互转化过程中极不稳定并且占比非常少的副产物[106]。由于B9H15的热稳定性低,并且处理方法苛刻,所以目前为止对B9H15的研究非常少。1958年,Kotlensky和Schaeffer[106]利用B2H6在放电条件下合成B9H15,但在产物中占比少于1.5%,反应如式(45)。1962年,Kratzer课题组[107]利用B5H9与(CH2)6N4的结晶表面反应,经过蒸馏和低温结晶后以13%的收率制备B9H15,反应如式(46)。随后1965年,Williams课题组[101]将液体的B5H9和气态的B2H6混合,在2.53 MPa条件下得到黄色固体产物B9H15,收率为70%,但是B9H15极不稳定会继续分解生成B8H12,反应如式(42)。n-B9H15的11B NMR谱图见图22[108]。

图22 n-B9H15的11B NMR谱图(70.6 MHz)[108]Fig.22 11B NMR spectrum(70.6 MHz) of n-B9H15[108]

(45)

(46)
8.2 十四氢壬硼酸盐的合成
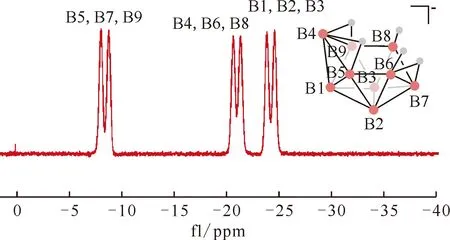
图23 Et4NB9H14在CH3CN中的11B NMR谱图[116]Fig.23 11B NMR spectrum of Et4NB9H14 in CH3CN[116]

(47)

(48)
8.3 九氢壬硼酸盐的合成
9 十顶点多面体硼烷的合成
9.1 癸硼烷(14)(nido-B10H14)的合成
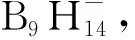
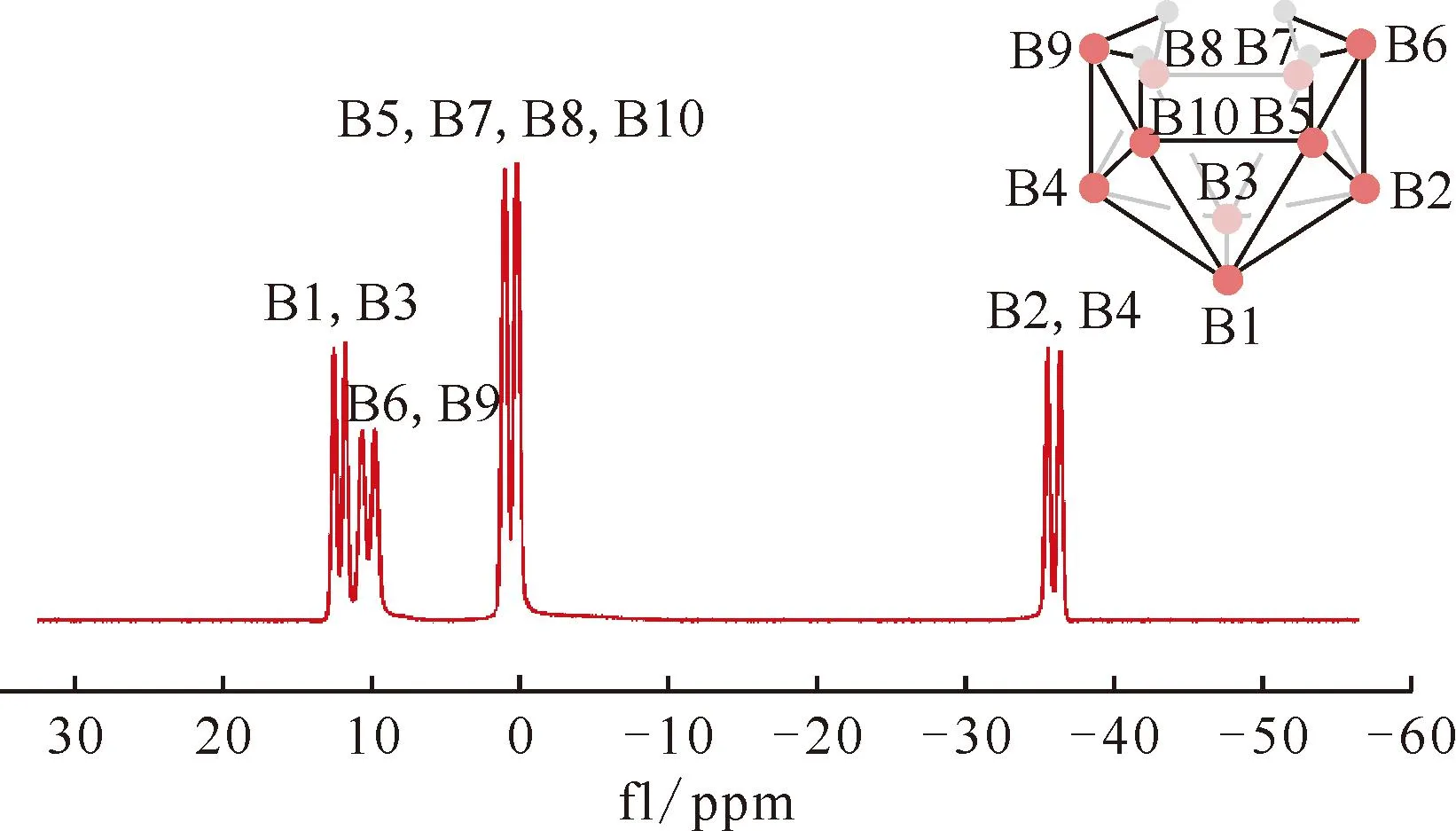
图25 B10H14在CHCl3中的11B NMR谱图[50]Fig.25 11B NMR spectrum of B10H14 in CHCl3[50]

(49)
(50)
9.2 十四氢癸硼酸盐的合成

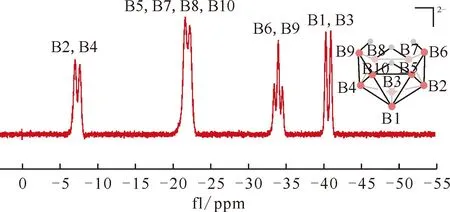
图26 Na2B10H14在DMSO中的11B NMR谱图[50]Fig.26 11B NMR spectrum of Na2B10H14 in DMSO[50]

(51)
9.3 十氢癸硼酸盐的合成

图27 Na2B10H10在DMSO中的11B NMR谱图[50]Fig.27 11B NMR spectrum of Na2B10H10 in DMSO[50]

(52)

(53)
10 十一顶点多面体硼烷的合成
十一顶点的硼氢化合物在多面体硼氢化合物中具有特殊的地位。它可以作为合成癸硼烷和碳硼烷以及杂原子硼烷的起始原料[27,135-137]。虽然十一顶点的硼氢化合物早在20世纪70年代已被合成,由于缺乏合适的合成方法,其研究和应用却远不及其他多面体硼氢化合物[136-137]。
10.1 十四氢十一硼酸盐的合成
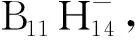

(54)

(55)


(56)
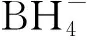
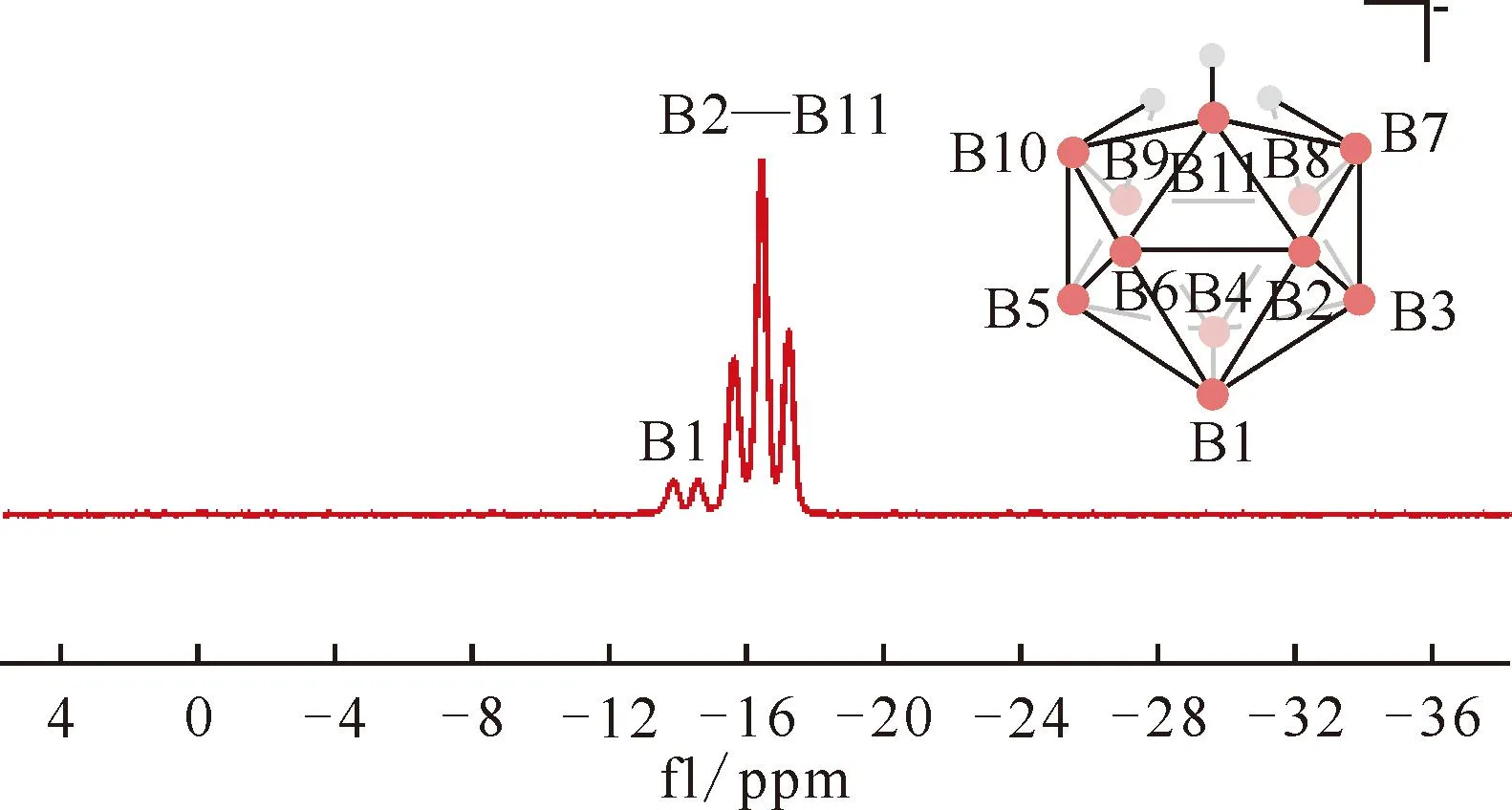
图28 NaB11H14在DMSO中的11B NMR谱图[142]Fig.28 11B NMR spectrum of NaB11H14 in DMSO[142]

(57)
10.2 十一硼烷(15)(nido-B11H15)的合成
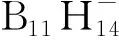

δ=-14.9(d, J=145 Hz)、-17.5(d, J=145 Hz) ppm图29 -40 ℃下B11H15在甲苯中的11B NMR谱图[144]Fig.29 11B NMR spectrum of B11H15 in toluene at -40 ℃[144]
(58)
10.3 十一氢十一硼酸盐的合成
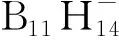
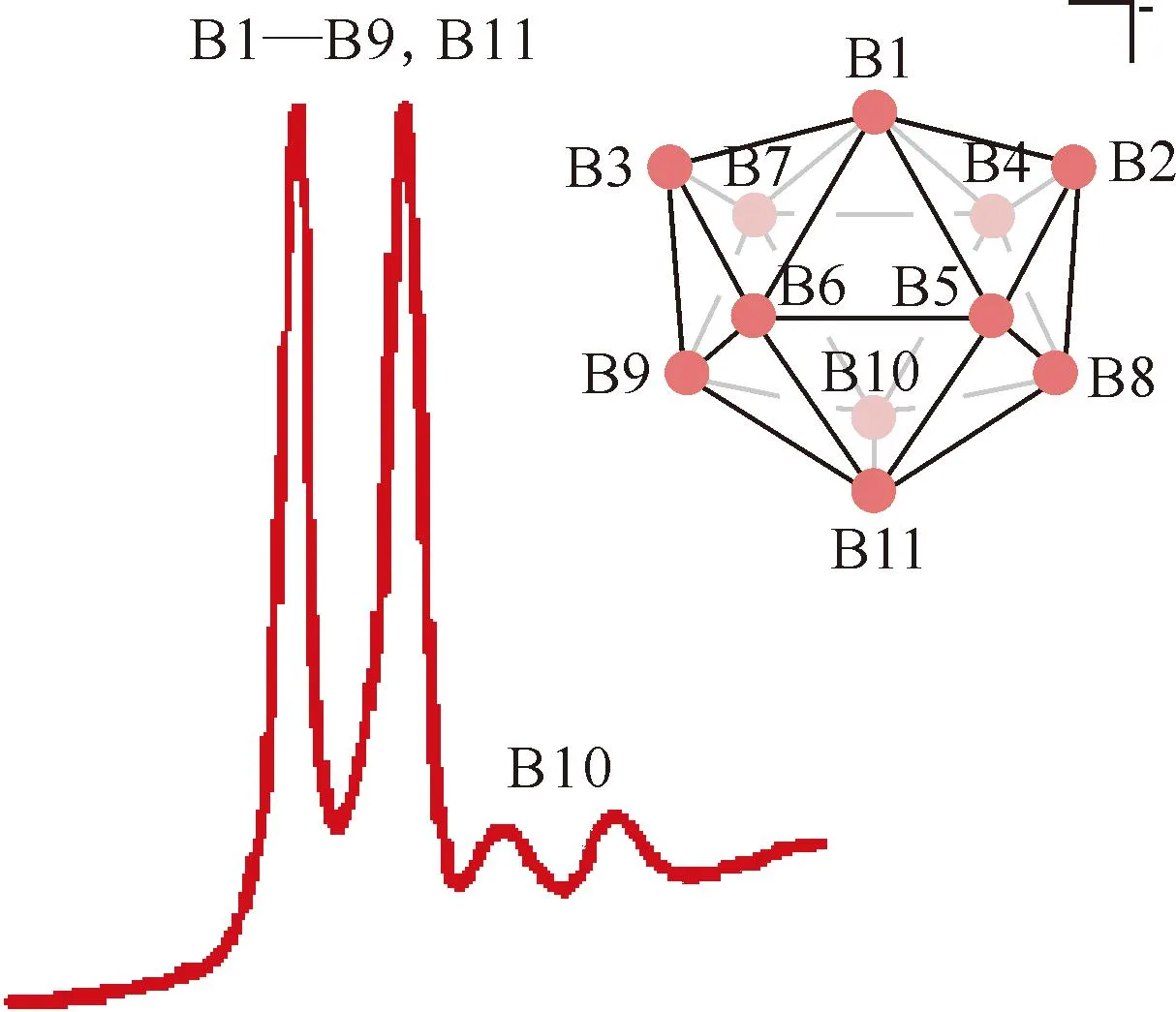
图30 [Cs(CH3)4N]B11H11在H2O中的11B NMR谱图[117]Fig.30 11B NMR spectrum of [Cs(CH3)4N]B11H11 in H2O[117]

(59)

(60)

(61)
11 十二顶点多面体硼烷十二氢十二硼酸盐的合成
11.1 L·BH3与硼烷反应

(62)

(63)

(64)
11.2 硼氢化合物与硼烷反应

(65)

(66)

(67)
11.3 硼氢化合物的热解
11.4 其他合成方法
除以上合成方法,利用NaBH4与有机卤化物或I2在diglyme中回流也可以生成收率为51%的Na2B12H12[159]。此外,将碱金属盐MBH4与碱金属氢化物或B2H6进行球磨,也可以得到M2B12H12[160-161]。2023年,本课题组[142]利用MB11H14(M=Na、K)分别与MB3H8(M=Na、K)在diglyme中加热,可以得到收率为80%的M2B12H12。Na2B12H12的11B NMR谱图见图31[142]。
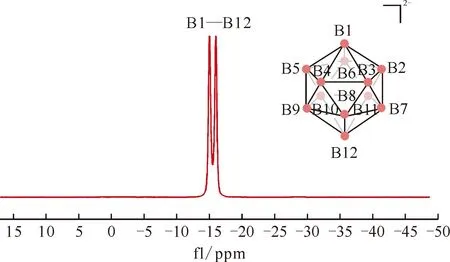
图31 Na2B12H12在DMSO中的11B NMR谱图[142]Fig.31 11B NMR spectrum of Na2B12H12 in DMSO[142]
与多面体硼氢化合物密切相关的是碳硼烷,这是一类包含B原子和C原子的团簇。对硼烷与炔的探索性研究,即在多面体硼烷的骨架中引入C原子,致使碳硼烷的诞生[162]。合成碳硼烷化合物需要制备多面体硼烷前体,所以合成路径常常需要多步[163-165]。虽然现有的碳硼烷已经商品化,但是价格昂贵,所以需要寻找更经济的合成路径。
12 十/十二顶点多面体碳硼烷的合成
12.1 十氢1-一碳十硼酸盐的合成


图32 阴离子的合成路径[175]Fig.32 Synthesis paths of preparation of the anion[175]
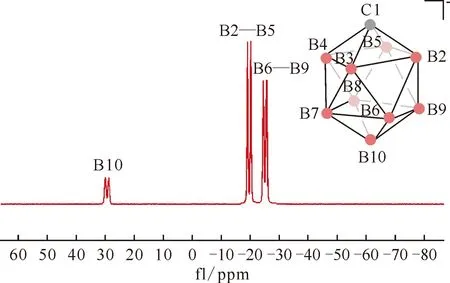
图33 NaCB9H10在DMSO中的11B NMR谱图[175]Fig.33 11B NMR spectrum of NaCB9H10 in DMSO[175]

(68)
12.2 十二氢一碳十二硼酸盐的合成
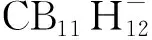
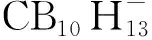

图34 阴离子的合成路径[181]Fig.34 Synthesis paths of preparation of the anion[181]
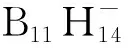
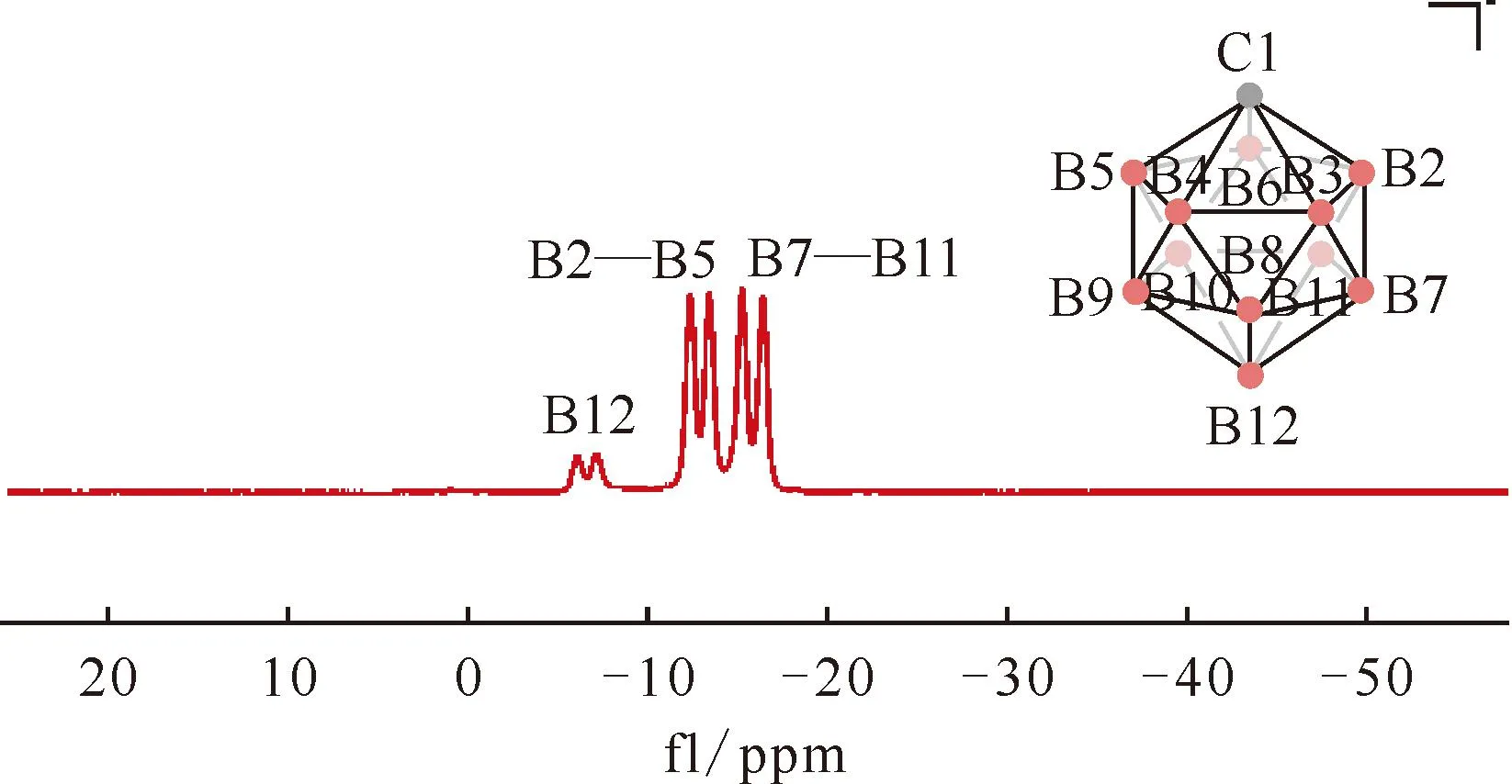
图35 NaCB11H12在DMSO中的11B NMR谱图[181]Fig.35 11B NMR spectrum of NaCB11H12 in DMSO[181]
12.3 1,2-二碳十二硼烷(12)(closo-1,2-C2B10H12)的合成
根据碳硼笼上两个碳原子的位置不同C2B10H12可以被分为三类:o-C2B10H12、m-C2B10H12和p-C2B10H12[165]。o-C2B10H12通过加热可以依次转化为m-C2B10H12和p-C2B10H12[182-183]。本文主要讨论o-C2B10H12的合成。
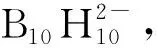
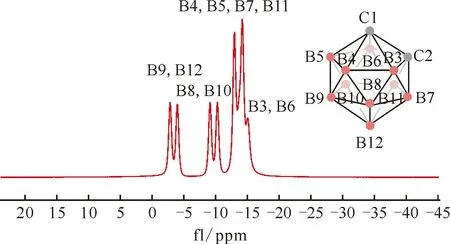
图36 C2B10H12在DMSO中的11B NMR谱图[50]Fig.36 11B NMR spectrum of C2B10H12 in DMSO[50]

(69)

(70)
(71)
图3、4、6、8、9、10、23、25、26、27、28、31、33、35和36为本组自测谱图,均与各图引用文献报道数据相符。
Na2B12H12作为BNCT硼药载体的前驱体,对其进行巯基修饰得到BSH[193]。BSH虽具有高含硼量、良好的水溶性以及低毒性,但是缺乏靶向性[21]。近年来发展的第三代BNCT硼药主要利用生物分子与硼化合物结合,对硼烷以及碳硼烷化合物进行修饰,将其结合到肿瘤细胞的各种靶向分子上,包括核苷、氨基酸、卟啉和抗体[21-22,194]。在过去的50年里,科研人员对BNCT硼药的研究投入了相当大的努力,尽管富硼化合物的种类繁多,但目前临床上使用的BNCT的药物只有BPA和BSH两种,并不能满足治疗效果限制了其在临床治疗上的发展,因此硼药的开发和临床应用仍有广阔的提升空间。
13 硼烷化合物的合成机理
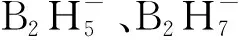
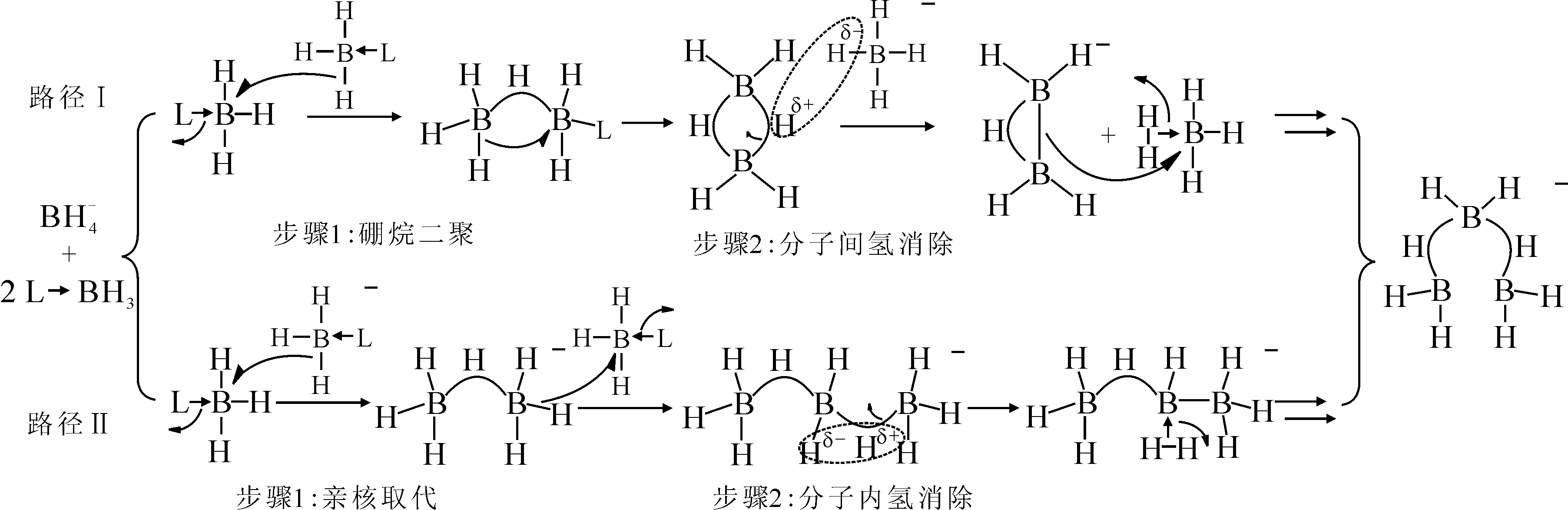
图37 硼氢化物与Lewis碱BH3加合物反应生成阴离子的一般机理[38]Fig.37 General mechanisms of formation of the anion from the reaction of borohydrides and BH3 adducts[38]
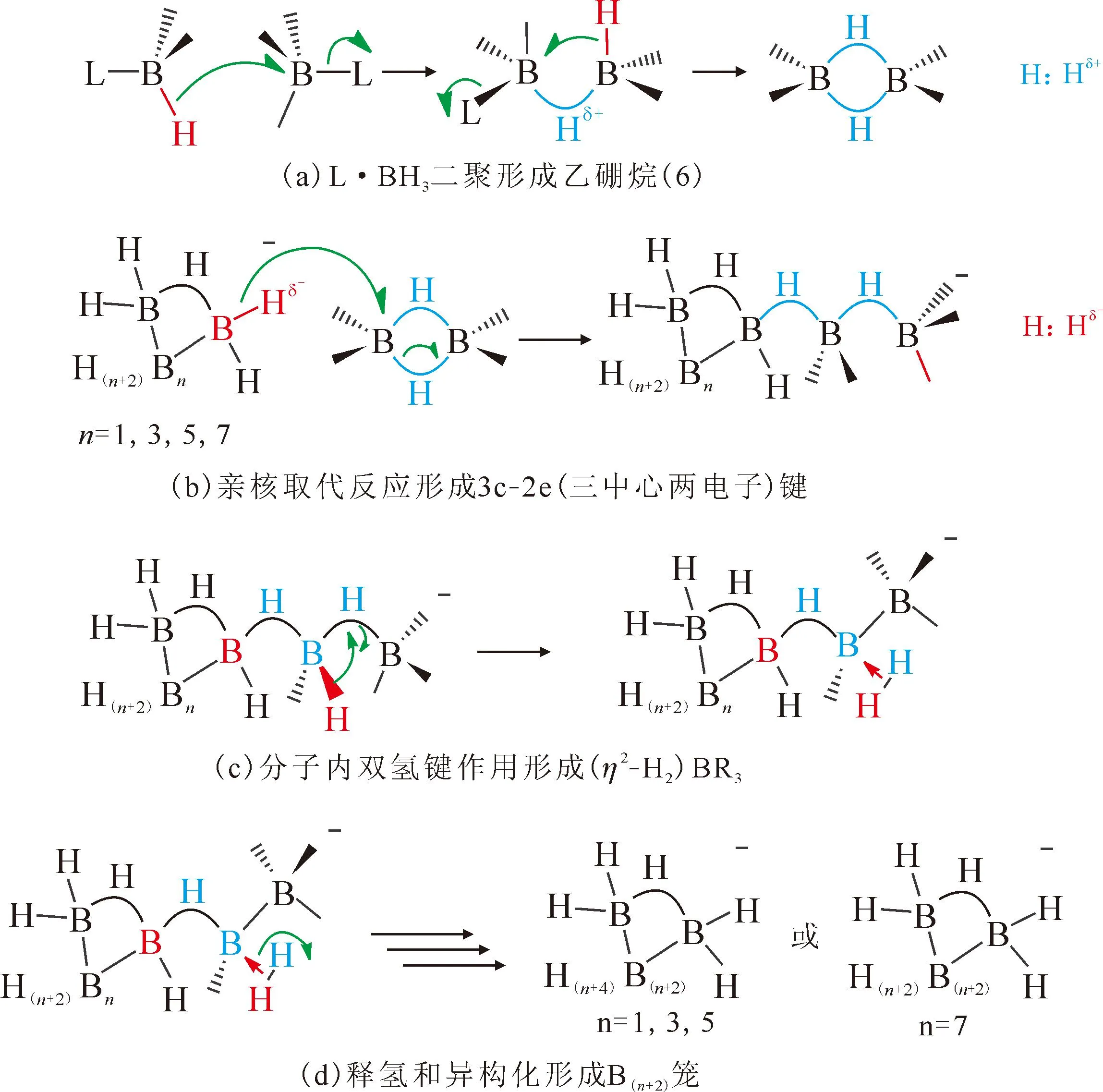
图38 小分子硼烷通过B-H键缩合反应生成多面体硼烷的一般机理[142]Fig.38 The general formation mechanism of polyhedral boranes from small boranes through the B-H bond condensation reaction[142]
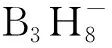
14 闭式硼烷热稳定性和水溶性讨论
15 总结与展望
硼烷是一类重要的含硼化合物,其中多面体硼烷化合物在化学、材料和医疗,尤其是BNCT等领域有重要的应用。但是其合成方法多数是在40多年前发展起来的,使用原料多为有毒易燃的小硼烷分子如B2H6,以及当时条件下易得的中间体如B5H9和B10H14。报道中的合成方法不易重复,有些报道相互矛盾,形成机理也尚未解释清楚,所以有必要对多面体硼烷化合物的合成路径和机理进行系统研究,从而发现简单高效的合成方法和现时更廉价易得的原料,从而实现规模化合成。因此,按照由小硼烷分子逐个到多面体硼烷的次序,结合本课题组最近的工作,对硼烷的合成方法进行了系统的总结,较详细地介绍了各类硼烷化合物的合成方法,同时提供了多面体硼烷的分子结构和特征11B NMR谱图。此外,通过调研硼烷化合物的研究方法,发现利用催化剂催化合成多面体硼烷类化合物并未被研究,未来可以尝试找到合适的催化剂体系选择性地合成多面体硼烷。希望本文对进一步研究硼烷化合物的合成和BNCT等领域的应用提供有用的信息。
