Cu-FeOx@AC 活化PMS 体系除藻效能与机制
2023-12-26陈昊天姜文超李玉平
陈昊天,向 平,姜文超,李玉平,周 元,王 凯
(重庆大学 环境与生态学院,重庆 400043)
水体富营养化易引发藻类爆发,威胁水环境质量和水生生物生存[1]。为应对以铜绿微囊藻为主的水华,可采取机械打捞、化学方法和生物工艺等,但这些方法有耗能高,效果差等问题[2,3]。近些年,以活化过一硫酸盐(PMS)为代表的高级氧化工艺(AOPs)由于处理效果好、适用范围广和污染小而被广泛研究[4]。过一硫酸盐可以通过光照、热活化,过渡金属活化等多种方法活化产生SO-4·、·OH 等氧化基团[5],其中过渡金属活化法因效益高,室温下即可反应,成本低廉[6]而备受关注。
当前,单过渡金属活化PMS 是过渡金属活化PMS 的主要手段,钴离子[7]、铁离子[8]、锰离子[9]、铜离子[10]都有良好的效果,但是均存在残留离子污染水环境,难以回收等问题。过渡金属氧化物催化PMS 活性的研究,主要集中在单金属氧化物,如FexOy、CuxOy[11]等;双金属氧化物相比于单金属氧化物,表面活性位点多且催化活性高。Wu 等[12]制得钴锰双金属氧化物CoFe2O4-x作为活化PMS 的催化剂;Xian 等[13]用制备出的催化剂CuO-Fe2O3活化过硫酸盐去除酸性橙7,并进行了材料表征和机理分析;Lyu 等[14]采用水热法制得了磁性材料CuO-Fe2O3-CuFe2O4用于活化过硫酸盐,反应2 h 后体系可去除75.5%的氧氟沙星。上述双金属氧化物材料均具有活化PMS 的良好效果,但易形成团聚结构,影响材料与外界的接触面积[15]。故考虑将双金属材料负载到具有较大比表面积的碳基物质上,例如活性炭、活性碳纤维,碳纳米管,以此增强材料性能。其中,活性炭廉价易得,吸附性能好,是催化剂载体的极佳选择[16]。
本研究采用水热法和高温烧结法制备复合催化剂Cu-FeOx@AC,并探究Cu-FeOx@AC 活化PMS 体系的除藻效能与机制。使用扫描电镜等表征手段,对材料的形貌、结构等进行探究;研究了不同条件下,Cu-FeOx@AC 活化PMS 体系的除藻率,并证明了双金属氧化物Cu-FeOx负载在活性炭上,催化性能更佳,为应对藻类爆发提供了新方法。
1 材料与方法
1.1 Cu-FeOx@AC 复合材料的制备
称取2.416 g Cu(NO3)2·3H2O 和8.080 g Fe(NO3)3·9H2O 置于100 mL 烧杯中,加入30 mL 超纯水,室温下搅拌至完全溶解,然后加入16.000 g NaOH 和40 mL 超纯水溶解,冷却后,添加不同质量AC 颗粒(20~50 目)搅拌3 h,见表1。将混合液体倒入水热反应釜,180 ℃下反应48 h,冷却后洗涤3 次至中性并干燥,再使用马弗炉,400 ℃煅烧4 h,得到目标材料Cu-FeOx@AC。

表1 复合材料Cu-FeOx@AC 中Fe(NO3)3·9H2O、Cu(NO3)2·3H2O 和AC 投加量Table 1 Dosage of Fe(NO3)3·9H2O, Cu(NO3)2·3H2O and AC in Cu-FeOx@AC
1.2 Cu-FeOx@AC 复合材料的表征
材料的成分通过X 射线衍射仪(XRD,PANalytical X’Pert PRO)分析。采用扫描电镜SEM(ZWISS Gemini 300,德国卡尔蔡司公司)观察材料形貌特征,材料表面微区的元素组成通过EDS 能谱仪(OXFORD Xplore,英国牛津仪器公司)分析。铁、铜相对含量通过ICP(美国赛默飞公司 iCAP PRO)测定。复合材料化学键的类别,使用FTIR(Thermo Scientific Nicolet iS20)在4 000~400 cm-1的范围内分析。通过X 射线光电子能谱(XPS,Thermo Scientific K-Alpha),了解反应前后材料所含元素的价态变化。
1.3 藻细胞降解实验和分析计算方法
以铜绿微囊藻为研究对象,用0.5 mol/L 的NaOH 和0.5 mol/L 的HCl 调节pH 至6,初始藻细胞密度为每升1.4×109个(OD680=0.14),PMS 初始质量浓度0.5 g/L,复合催化剂投加量0.2 g/L,反应90 min,搅拌藻液和Cu-FeOx@AC 催化剂至混合均匀并降解。藻细胞数量采用光学显微镜(Motic BA310)在血球计数板下计数。
2 结果与讨论
2.1 Cu-FeOx@AC 材料的表征
Cu-FeOx和Cu-FeOx@AC 复合材料的XRD 图谱,如图1 所示。Cu-FeOx在2θ 角为24.15°、33.16°、35.63°、40.86°、49.46°、54.07°、57.59°、62.44°和64.00°处有不同的衍射峰,与Fe2O3的标准图谱(JCPDS PDF# 80-2377)相吻合;在24.15°,33.16°,35.63°处的特征衍射峰,与CuO 的标准图谱(JCPDS PDF# 72-0269)一致。初步判断,形成的铜铁双金属氧化物Cu-FeOx,是Fe2O3和CuO 的复合物。复合材料的XRD 图谱相比于Cu-FeOx并无明显变化,表明Cu-FeOx负载在活性炭上,不会改变原有的晶型结构。
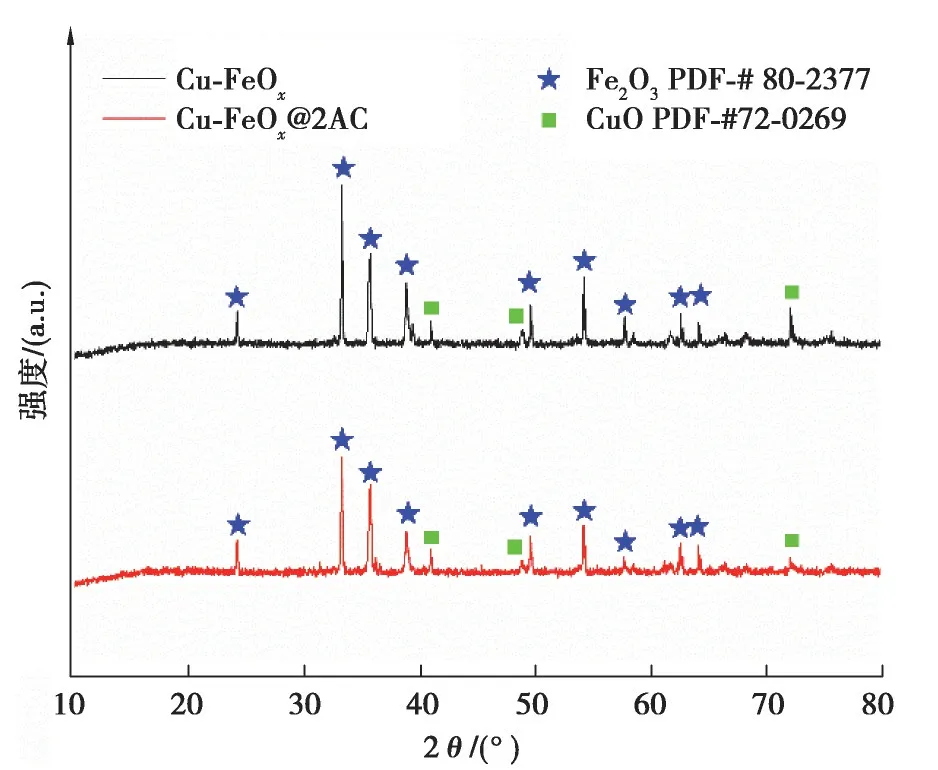
图1 Cu-FeOx和Cu-FeOx@AC 复合材料的XRD 图Fig. 1 XRD results of Cu-FeOx and Cu-FeOx@AC
采用SEM 对AC 单体、Cu-FeOx和Cu-FeOx@AC 复合材料表面形貌进行观察。通过图2(a)(b)观察到,活性炭表面粗糙不平,具有发达的孔隙结构,为Cu-FeOx在活性炭表面的负载提供了可能。从图2(c)(d)看出,Cu-FeOx单体由有棱边的盘状颗粒构成,每个盘状颗粒都由2 部分构成,具有多边形片状体,并负载着无序聚集的矩形小颗粒,有一定的团聚现象。从图2(e)(f)看出,Cu-FeOx负载到活性炭上之后,材料的团聚现象明显减少。使用EDS 分析Cu-FeOx@AC 复合材料表面微区的元素种类及含量,如图3 所示,可知复合材料基本由O、C、Fe、Cu 构成,其中Cu 原子约占20.14%,Fe 约占16.29%,O 约占41.00%,可计算出Cu-FeOx@AC 复合材料中Fe2O3:CuO 分子比约为2:5。
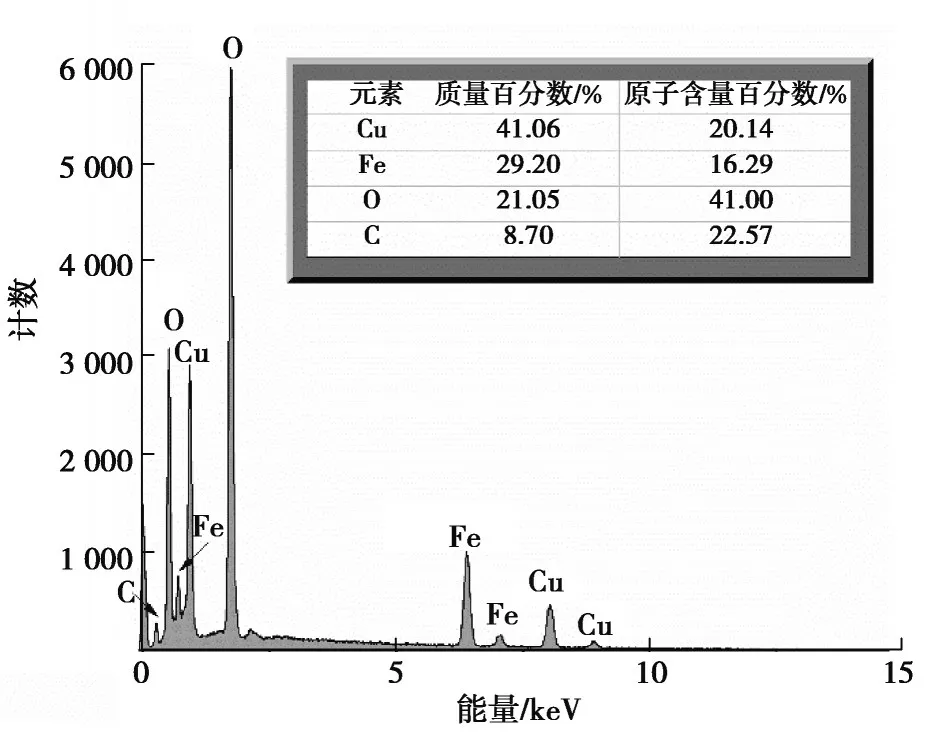
图3 Cu-FeOx@AC 复合材料的EDS 图Fig. 3 Energy dispersive spectrum of Cu-FeOx@AC
从图4 可知Cu-FeOx和Cu-FeOx@AC 复合材料的FTIR 表征结果。从局部放大图看出,在532 cm-1和450 cm-1附近的峰,可归因于Cu—O 键和Fe—O 的振动,结合前述SEM 与XRD 可知,证实了CuO 及Fe2O3的形成。活性炭负载Cu-FeOx后,3 450~3 400 cm-1之间出现了明显的吸收带,这可能是因为活性炭上面有丰富的氢氧官能团,官能团伸缩振动导致在红外光谱此区域上留下吸收谱带[18]。在1 626 cm-1处的特征峰,可能由于活性炭造成。活性炭表面的羧基有具有拉伸作用的使得图谱在1 450 cm-1附近出现了吸收峰。负载活性炭后,活性炭C—O 键拉伸,造成1 450~1 000 cm-1处的吸收带出现了明显下降,据推测是因为反应后的复合材料表面形成了Cu—O—C 键及Fe—O—C 键[19]。总的来看,对于Cu-FeOx和Cu-FeOx@AC复合材料来说,除了反应后的峰的强度发生了少量变化,峰位置改变不多,新的特征峰的出现也较少,说明Cu-FeOx@AC 复合材料产生的新官能团较少,具有一定的稳定性,可重复使用。
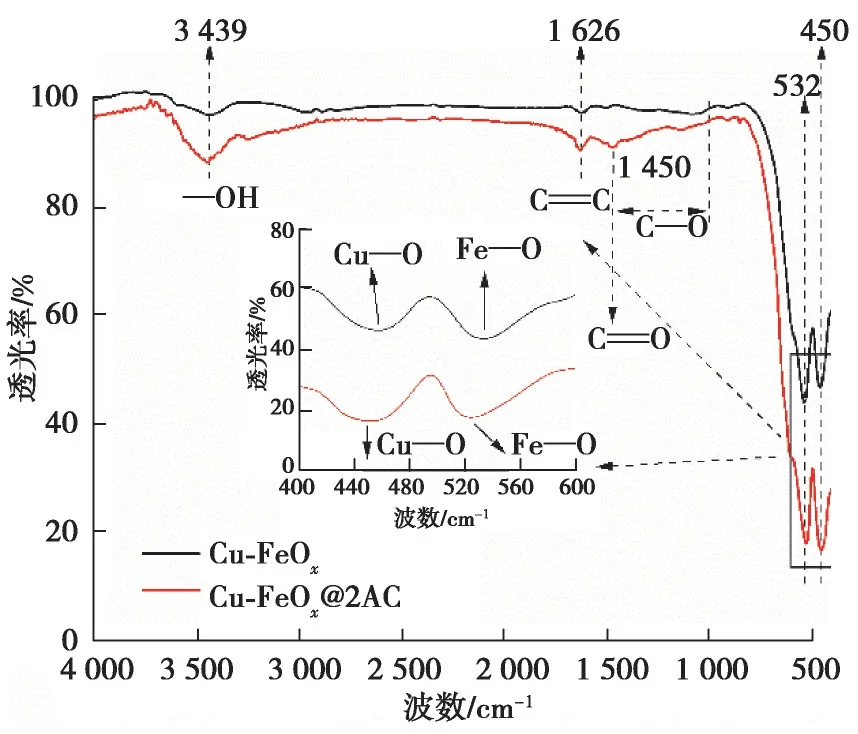
图4 Cu-FeOx和Cu-FeOx@AC 复合材料的FTIR 表征图Fig. 4 FTIR spectra of Cu-FeOx and Cu-FeOx@AC
2.2 Cu-FeOx@AC 负载比对除藻效能的影响
选取相同质量不同负载比的复合材料Cu-FeOx@1~4AC 进行除藻实验,如图5 所示。选取4 种不同负载比的Cu-FeOx@AC 材料进行了ICP 测试,测定了铁、铜元素在载体AC 上的负载量,如表2 所示。从图5可以看出,复合材料Cu-FeOx@1~3AC 的除藻率都可以稳定在60%及以上,但是Cu-FeOx@4AC 的除藻率不足50%,由此可以初步判断,对于Cu-FeOx@2~4AC 来说,随着AC 在复合材料中比重增加,除藻率依次下降,可能原因是过多的AC 将Cu-FeOx包裹起来,阻碍了Cu、Fe 元素进入体系中与PMS 反应。但是除藻率Cu-FeOx@1AC<Cu-FeOx@2AC,根据ICP 测试可知,Fe、Cu 元素负载量Cu-FeOx@1AC<Cu-FeOx@2AC,则AC 占比Cu-FeOx@1AC>Cu-FeOx@2AC,与上述推测相符。而除藻率Cu-FeOx@3AC<Cu-FeOx@1AC,据推测可能原因是随着Fe、Cu 元素负载量提高,参与反应的Fe3+、Cu2+增多,对除藻率上升的影响,比不上因AC 减少使得粒子团聚带来的不利影响,总体上使得体系除藻率下降。综合来看,复合材料Cu-FeOx@2AC 表现最佳,因此在后续的实验中,选择Cu-FeOx@2AC 复合催化剂。
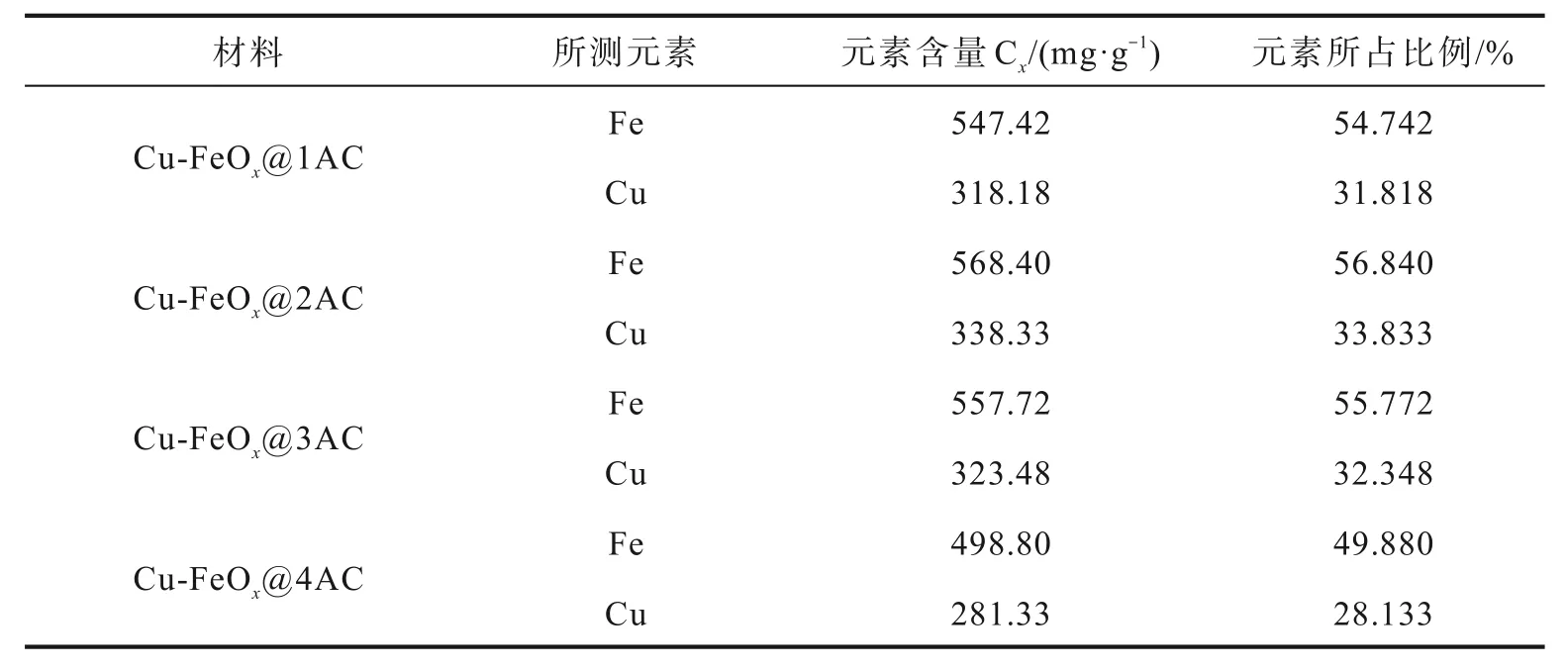
表2 铁、铜元素在AC 上的负载量Table 2 Capacities of Fe and Cu elements in activated carbon
2.3 初始PMS 质量浓度对除藻效能的影响
反应体系初始PMS 质量浓度,会影响除藻率[20-21]。如图6 所示,当PMS 为0.1 g/L 时,最终藻去除率为76.38%,可能原因是当反应体系中PMS 质量浓度处于很低的水平时,难以产生足够数量的自由基,参与目标污染物的链式反应。随着PMS 质量浓度的增加,体系除藻率也在逐步上升,当PMS 初始质量浓度为0.5 g/L时,铜绿微囊藻去除率可达97.25%。当PMS 质量浓度达到0.6 g/L 时,除藻率开始下降,可能原因是过多的PMS 与生成的自由基发生反应,消耗了可参与污染物降解反应的·OH,SO-4·,导致除藻效能变差(式(1)~(2))。在Li 等[20]的探究中也有相类似的情况。

图6 不同初始PMS 质量浓度对除藻效能的影响Fig. 6 Efficacy of different initial PMS concentrations on
2.4 初始pH 对除藻效能的影响
传统芬顿系统中,溶液pH 值是影响反应的重要参数之一[22-23]。为了探究pH 值对反应体系除藻效能的影响,设置5 个不同的pH 值(pH=3、5、6、8、10)进行实验。从图7 可以看出,在90 min 的反应时间内,藻去除率均可以达到95%以上,其中当pH=6 时,除藻率可达97.25%。传统芬顿系统特点之一是需要体系pH 值在3 附近,而发生铜绿微囊藻藻华的水体,pH 一般在7~9 之间[24]。
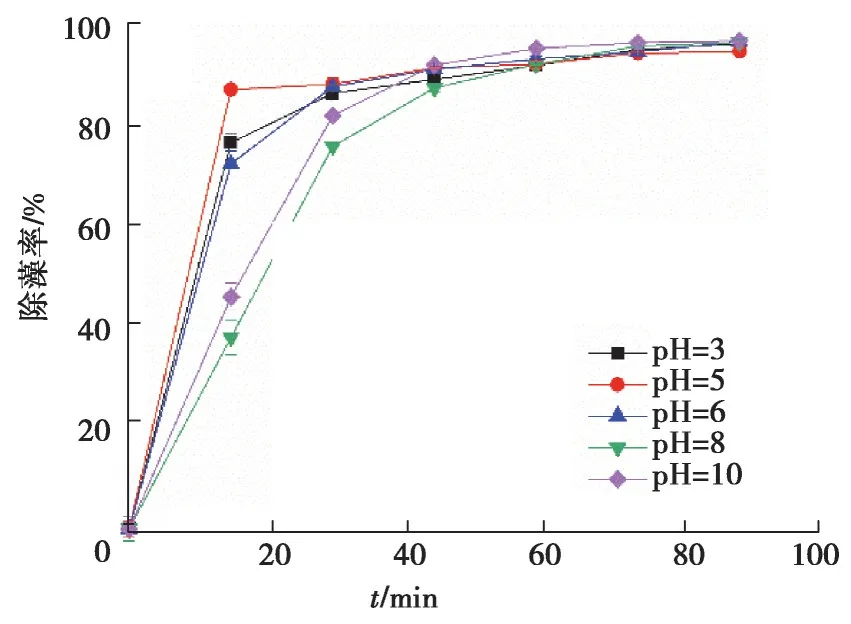
图7 不同初始pH 值对除藻效能的影响Fig. 7 Efficacy of different initial pH values on
因此,相比于传统芬顿系统,Cu-FeOx@AC 活化PMS 体系具有广泛的pH 适用范围,更加适合于处理含藻量高,pH 偏碱性的水体。
2.5 不同体系对除藻效能的影响
在不存在PMS 的条件下,采用AC、CuO 与Fe2O3单体,Cu-FeOx和复合材料Cu-FeOx@2AC 除藻,效果见图8。总体来看,3 种单体材料对铜绿微囊藻的吸附率都不高,均未达30%。AC 单体对藻的吸附率可达28.37%,但负载一定比例Cu-FeOx单体后,吸附藻率迅速下降到18.16%,可能原因是AC 表面负载了Cu-FeOx单体,使得AC 的吸附位点减少,削弱了材料对藻的吸附能力。

图8 不同催化剂对藻的吸附能力Fig. 8 Adsorption capacity of different catalysts for algae
在存在PMS 时,不同体系活化PMS 除藻的效果比较,如图9 所示。不投入复合催化剂时,单独的PMS 几乎对藻细胞的存在无显著影响,除藻率仅为9.12%。体系AC+PMS 除藻率可达42.07%,相较于PMS 单独存在的体系,除藻率提升了33%左右,根据前面的研究可归因于AC 对藻的吸附能力。然而,Cu-FeOx+PMS 体系除藻率仅为46.96%,相比AC+PMS 体系除藻率并无大的改进,且CuO 或Fe2O3+PMS 体系除藻率也不超过30%,表明3 种单体和Cu-FeOx都无法很好地活化PMS,参与和目标降解物的链式反应。研究Cu-FeOx@2AC+PMS体系可以发现,反应前15 min,除藻率迅速上升至66.56%,随后除藻率稳步提升。在90 min 的反应时间内,总除藻率可稳定在80%,相比于不添加AC 提高了31.72%,可能原因是新加入的AC 单体充当了Cu-FeOx催化剂的载体,减少了Cu-FeOx催化剂之间的团聚,增加了与溶液的接触面积,使得更多的Fe3+、Cu2+参加了活化PMS 这一过程。

图9 不同体系的除藻能力Fig. 9 Different systems’ algae removal capacity
2.6 Cu-FeOx@AC 复合材料重复利用性研究
取OD680=0.14 的藻液(初始藻细胞密度为每升1.4×109个)200 mL,调节pH 至6,加入0.5 g/L 的PMS,0.2 g/L 复合催化剂Cu-FeOx@2AC,每隔半小时取一次样。反应90 min 后,将收集的混合液在振荡器上混合均匀,用磁铁分离。用NaOH 和超纯水多次洗涤催化剂,使用高速离心机在5 000 r/min 的速度下离心回收催化剂。离心后,依次加入超纯水、无水乙醇各在离心机内清洗2 次。最后,把催化剂放入60 ℃真空干燥箱干燥,蒸干后以备下次使用。上述过程循环5 次,研究复合催化剂Cu-FeOx@2AC 的重复利用性。
如图10 所示,第1 次实验90 min 内,除藻率可达97.25%,铜绿微囊藻可以被去除绝大部分;第2 次循环使用后,除藻率仍有87.91%,相较于第一次实验仅下降9.34%,表明复合催化剂Cu-FeOx@2AC 具有良好的可回收利用性。从第3 次循环实验开始,铜绿微囊藻去除率的下降速度开始放缓,可能是催化剂Cu-FeOx@2AC表面吸附了一部分藻细胞及其降解产物,使催化剂表面形成了相对稳定的状态,溶出至反应体系中的Fe、Cu元素减少。最终,经过5 次循环实验,除藻率仍有61.54%。总体来看,复合催化剂Cu-FeOx@2AC 具有一定的重复利用性。

图10 复合催化剂的重复使用性研究Fig. 10 Reusability of composite catalyst
2.7 Cu-FeOx@AC 催化PMS 反应机理
传统过渡金属活化PMS 的反应机理,主要有基于·OH、SO-4·的自由基氧化反应理论,和基于空穴(h+)和单线态氧(1O2)的非自由基反应机理。为了详细探究Cu-FeOx@AC 活化PMS 体系的除藻机理,确定复合催化剂活化PMS 体系起主要作用的自由基,进行了淬灭实验。
如图11 所示,添加不同自由基淬灭剂,对比Cu-FeOx@AC 活化PMS 体系除藻率。甲醇是一种常用的·OH和SO-4·淬灭剂,反应常数k(·OH)≈9.7×108L(mol·s)-1、k(SO-4·)≈2.5×107L/(mol·s);而叔丁醇是常用的·OH 淬灭剂,其反应常数k(·OH)在3.8~7.6×108L/(mol·s)之间,但对SO-4·抑制作用差(k(SO-4·)≈4.0×105L/(mol·s))[25,26]。1O2是PMS 产生的重要非自由基反应产物之一[27],所以可选糠醇作为1O2的淬灭剂(k(·OH)≈1.5×1010L/(mol·s)、k(1O2)≈1.2×108L/(mol·s)),通过藻去除率的变化判断体系是否产生了1O2;通过苯醌抑制超氧自由基(·O-2),·O-2可能是由于Fe、Cu 元素在相关活化反应中产生的[28],如式(3)~(7)所示。通过投加EDTA-2Na(乙二胺四乙酸二钠),可确认体系是否存在具有氧化能力的空穴(h+)[29]。当投加4 mmol/L EDTA-2Na 后,体系的除藻率下降至49.66%,表明在复合催化剂活化PMS 体系除藻过程中,空穴氧化是一个重要的影响因素。但是当对苯醌为4 mmol/L 时,除藻率只有47.52%,表明在与目标污染物的降解反应中·O-2比空穴占主导作用。

图11 屏蔽剂对Cu-FeOx@AC/PMS 体系除藻率的影响Fig. 11 Effects of shielding agent on algae removal rate of Cu-FeOx@AC/PMS system
由表3 可知,·OH、SO-4·对除藻的贡献率加起来不超过30%,且体系起主要作用的是h+,·O-2等氧化基团,其次是·OH,1O2。这与图11 实验结果相吻合。
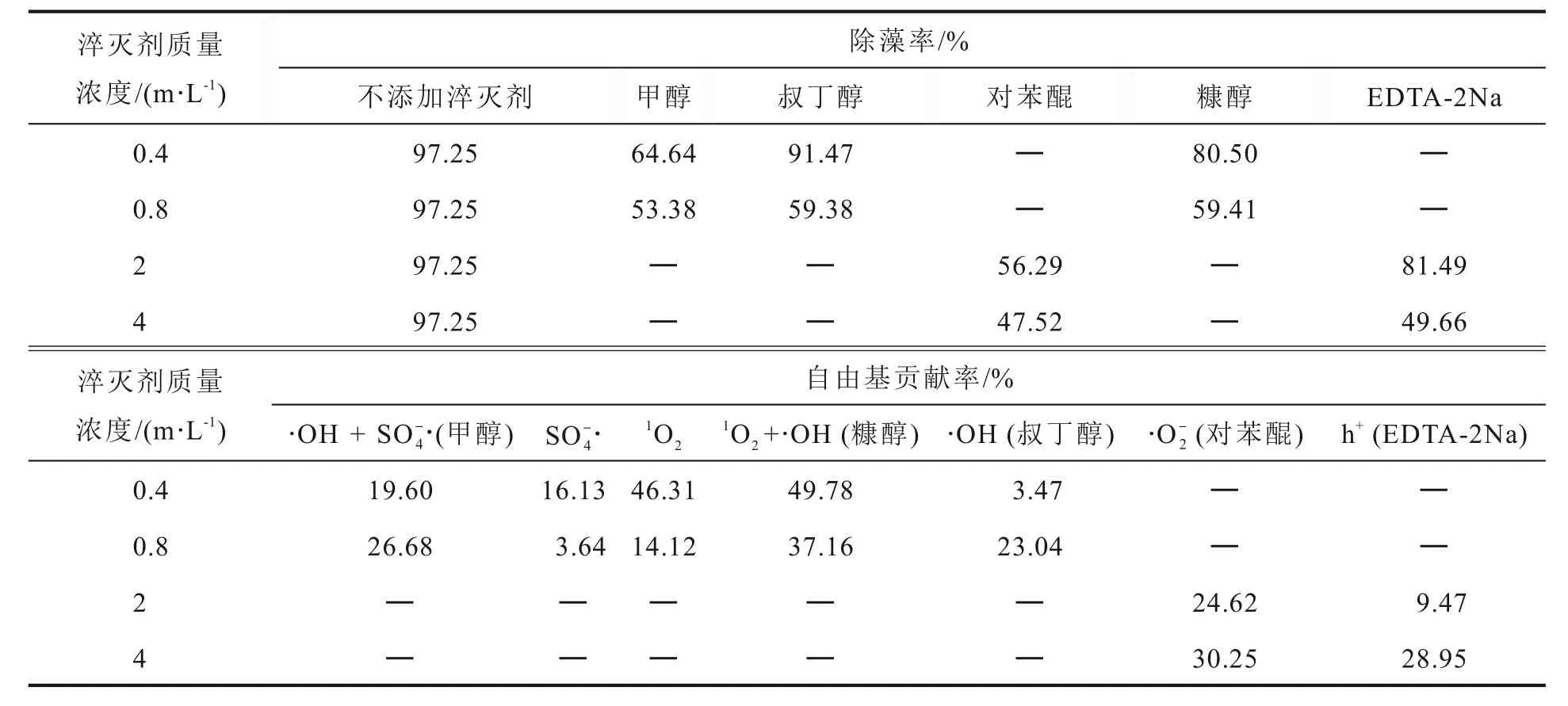
表3 屏蔽剂对除藻率的影响及相应自由基的贡献率Table 3 Effects of shielding agent on algae removal rate and contribution rate of radicals
用XPS 研究复合材料反应前后元素的价态变化,进一步探体系除藻机理。从图12(a)XPS 全谱图可知,复合材料Cu-FeOx@AC 主要由Cu、Fe、O、C 组成。对比反应前后,铜和铁的强度都有所下降,可能是复合催化剂在活化PMS 时,部分铜、锰离子溶出,促进了自由基SO-4·、·O-2和·OH 的产生,导致铁、铜离子含量均减少。
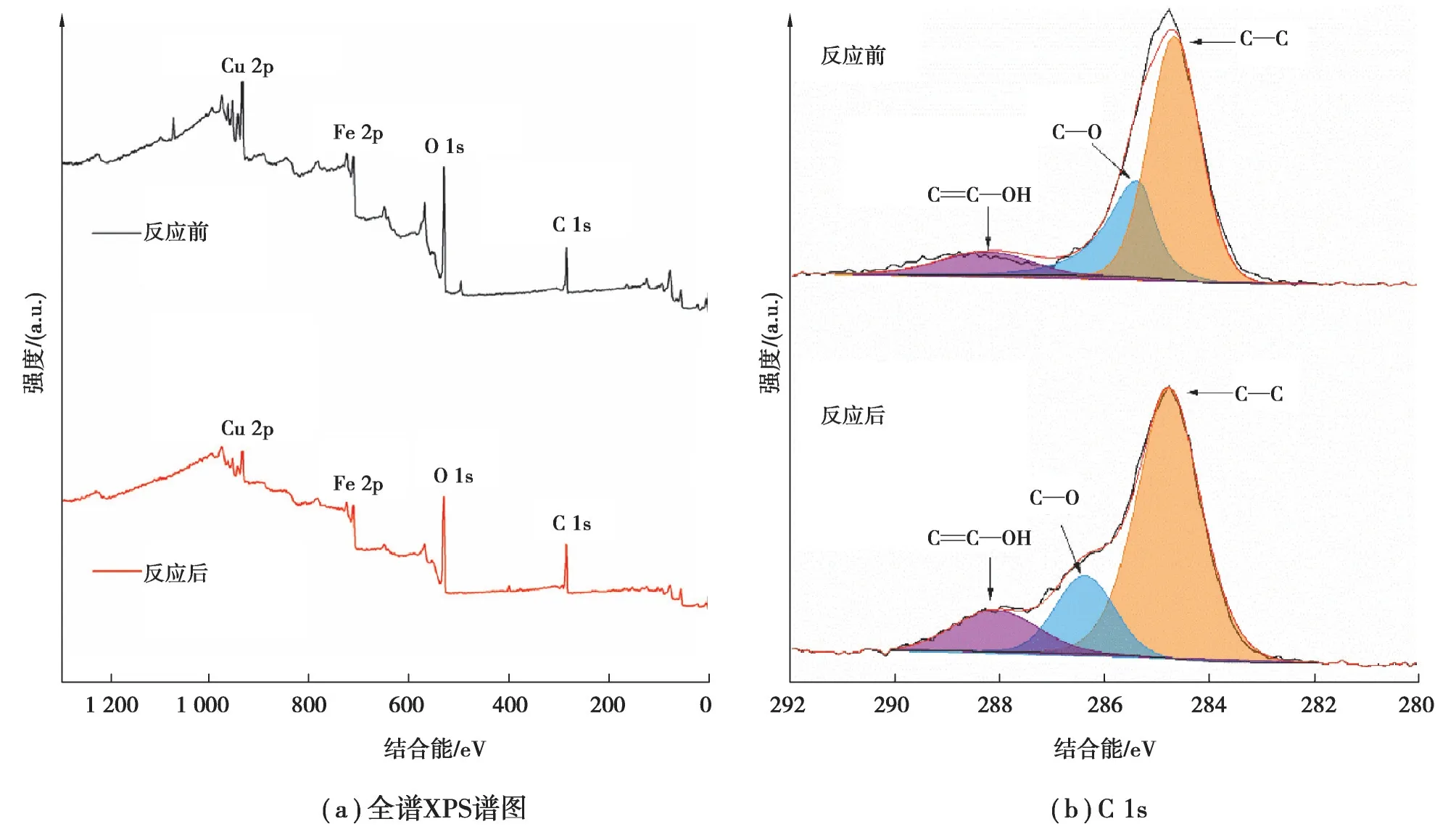
图12 反应前后Cu-FeOx@AC 的全谱XPS 谱图、C 1s、Cu 2p 和Fe 2p 高分辨图Fig. 12 XPS spectra of full spectrum (a), C 1s (b), Cu 2p (c) and Fe 2p (d) of Cu-FeOx@AC before and after the reaction
碳元素C 1s 高分辨XPS 图如12(b),C 1s 图谱主峰分为3 个峰,依次对应键(288.18 eV),键(286.38 eV),C—C 键(284.78 eV)。在复合材料催化PMS 活性后,的峰面积增加,明显左移,说明复合催化剂受到了氧化作用的影响,这个过程可能与催化PMS 产生·O-2、·OH 有关[30]。
从图12(c)中Cu 2p 的高分辨图看出,在反应前953.78 eV 和933.98 eV 两个主峰分别对应于Cu 2p1/2、Cu 2p3/2,941.78~944.08 eV 之间的双峰是卫星峰,可能对应的是Cu 2p3/2[31]。除藻反应后,(943.00±10.00) eV附近的卫星峰谱峰强度减小,代表Cu 2p3/2的主峰略微移动到结合能较高的地方,说明反应可能存在还原作用,复合催化剂表面存在Cu(Ⅱ)转变为Cu(Ⅰ)的情况,并连续发生铜元素之间的价态转换[26],见式(8)~(10)。
图12(d)是铁元素Fe 2p XPS 高分辨谱。在723.78 eV 和710.88 eV 处的峰分别是Fe 2p1/2和Fe 2p3/2原子轨道。分峰拟合后,可知Fe 元素存在Fe(Ⅱ)和Fe(Ⅲ),且在719.28、713.68 eV 处有Fe(Ⅲ)和Fe(Ⅱ)卫星峰存在。复合催化剂参与体系的反应后,709.78 eV 处的Fe(Ⅱ)峰向着结合能增大的方向偏移,说明体系存在Fe(Ⅱ)向Fe(Ⅲ)的转化,并且724.28eV 处的Fe(Ⅲ)峰面积减小,可能存在Fe(Ⅲ)向Fe(Ⅱ)转变[32],或铜铁之间存在电子相互转移,见式(11)~(13)。
总之,多种作用参与了铜绿微囊藻的降解,如图13 所示。复合材料不仅能吸附藻细胞,降低溶液含藻率,还可通过活化PMS 还原HSO-5,促进Fe(Ⅲ)与Fe(Ⅱ)、Cu(Ⅱ)与Cu(Ⅰ)的相互转变,克服了传统芬顿体系铁泥过多的局限[33],并产生多种氧化活性产物(h+,·O-2为主,·OH、SO-4·和1O2次之),实现藻细胞结构的破坏和去除。
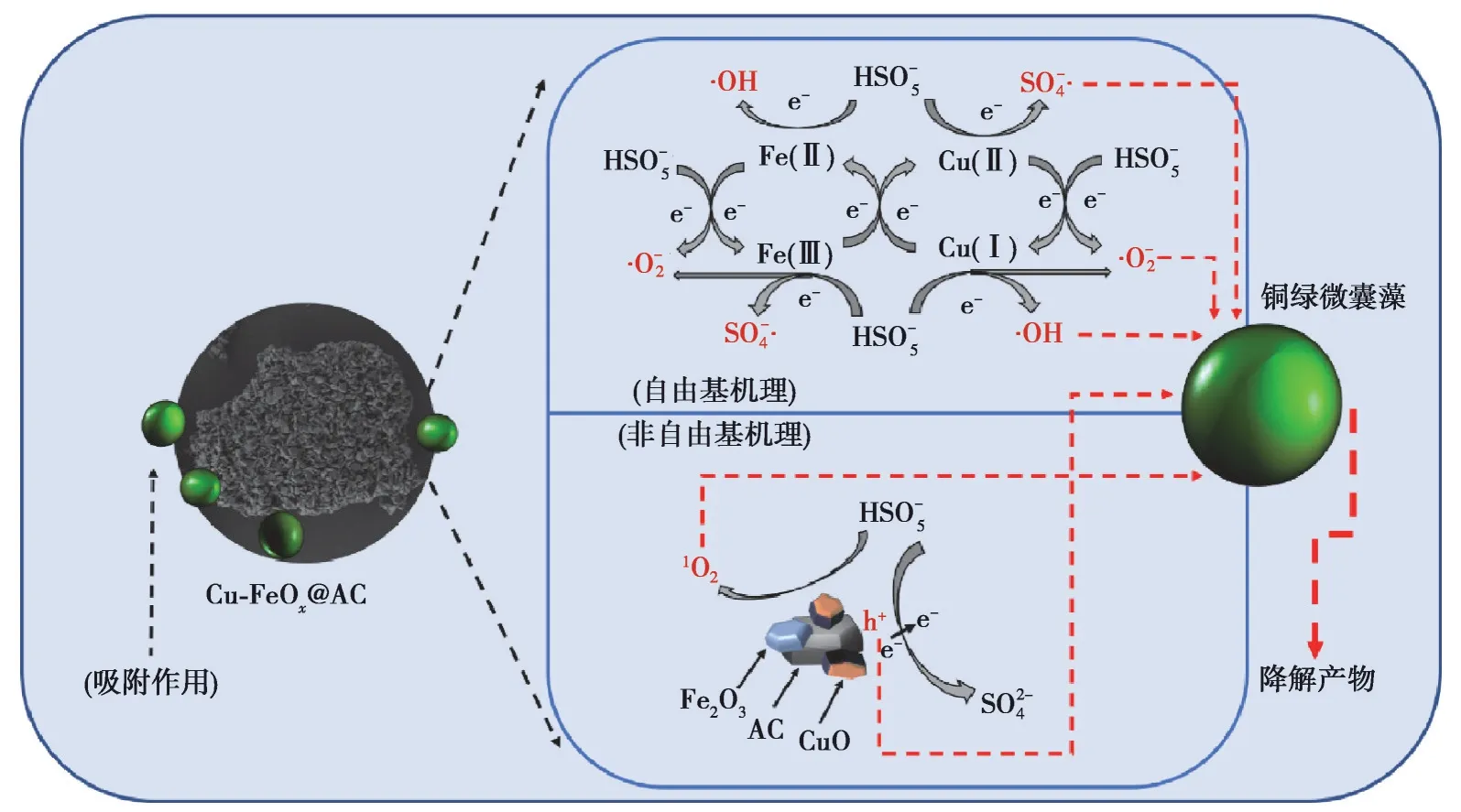
图13 AC 负载铁铜双金属氧化物活化PMS 体系除藻机理图Fig. 13 Algae removal mechanism of Cu-FeOx@AC/PMS system
3 结 论
1)采用水热法和高温煅烧法,成功制备铜铁双金属氧化物Cu-FeOx并使其负载在AC 表面,得到Cu-FeOx@AC 复合催化剂。通过多种表征,发现Cu-FeOx主要是CuO 和Fe2O3。
2)当初始pH=6,藻细胞密度为每升1.4×109个,使用催化剂0.5 g/L,PMS 0.2 g/L 时,降解90 min,体系对铜绿微囊藻的降解率可达97.25%。Cu-FeOx@AC 活化PMS 体系相较于Cu-FeOx和AC,除藻率都有明显提升。
3)通过不同体系下除藻效能对比,自由基淬灭实验和XPS 分析,对除藻机理进行了研究。结果表明,复合催化剂可以通过吸附一部分藻细胞降低其在溶液中的含量,还可活化PMS 还原HSO-5,促进Fe(Ⅲ)与Fe(Ⅱ)、Cu(Ⅱ)与Cu(Ⅰ)之间的相互转变,产生多种氧化基团(h+,·O-2为主,·OH、SO-4·和1O2为辅),实现藻细胞的破坏和去除。
